腰椎滑脱症患者常伴有顽固性腰痛,若合并椎间盘突出或椎管狭窄将会出现下肢放射性疼痛及间歇性跛行,严重影响患者的生活质量,保守治疗无效时需行脊柱融合术治疗[1-2]。近年来,随着脊柱内镜技术的发展和手术器械的不断更新,内镜下腰椎融合术已成为脊柱外科的重要技术,但该技术仍存在术中损伤出口神经根、椎间隙处理效率较低和融合率不高等不足[3-9]。针对这些问题,我院脊柱微创团队采用局部麻醉侧卧位内镜下腰椎椎间融合术(posterolateral endoseopic lumbar interbody fusion,PE-LIF)治疗腰椎滑脱症,并辅助麻醉监护镇静术(monitored anesthesia care),患者术中处于清醒状态,在手术操作对神经根稍有刺激时会发出自我报警,从而大大降低了神经根损伤风险,且术后可立即恢复进食、加快恢复,更加符合加速康复外科理念。此外,采用侧卧位可避免微创手术操作空间的限制及俯卧位导致腹内压升高、手术出血量增加的问题,并且有利于开放术侧椎间孔,还能够使硬膜囊因重力向手术对侧沉降,利于术中操作,提高手术安全性[10]。本研究回顾性分析了接受局部麻醉PE-LIF治疗的58例腰椎滑脱症患者的资料,通过临床数据及手术前后影像学的改变分析其临床疗效,以期为该病的治疗提供新手段。
1 资料和方法 1.1 病例资料回顾分析2020年1月至2022年1月在我科接受局部麻醉结合麻醉监护镇静下PE-LIF治疗的腰椎滑脱症患者资料。纳入研究的病例术前均行腰椎X线片、CT和MRI检查,且手术均由同一名医师完成。本研究通过遵义市播州区人民医院医学伦理委员会审批。
纳入标准:(1)根据影像学检查、体格检查和临床体征,具有腰背部疼痛伴神经症状或有间歇性跛行、单节段Ⅰ度腰椎滑脱症的患者;(2)合并腰椎不稳且腰椎过伸过屈侧位X线片示矢状面相邻椎体位移≥4 mm,和/或相邻椎体终板间的角度变化≥11°;(3)经保守治疗3个月以上无效;(4)主要观察指标齐全。
排除标准:(1)多节段(≥2个节段)腰椎滑脱;(2)合并需要矫正的脊柱侧凸和/或脊柱后凸畸形;(3)脊柱感染性疾病;(4)Ⅱ度及以上腰椎滑脱;(5)严重的腰椎管狭窄症,内镜手术无法双侧充分松解及减压;(6)脊柱肿瘤;(7)严重骨质疏松(T值<-2.5)。
1.2 麻醉方案及手术方法(1)麻醉方案:局部浸润麻醉+麻醉监护镇静术分为超前镇痛、镇静及局部麻醉浸润,椎间融合,以及置入螺钉3个阶段。患者摆好合适体位后,预先予咪达唑仑0.02~0.04 mg/kg静脉注射,待1~5 min后予舒芬太尼0.1~0.2 μg/kg静脉注射,随后再给予右美托咪定持续以0.2~0.7 μg/(kg·h)静脉泵注(未使用右美托咪定负荷剂量)。手术开始前,术区消毒铺巾后,予适量0.1%罗哌卡因+0.27%利多卡因混合液(含肾上腺素1∶200 000)进行局部浸润麻醉。当进行终板软骨处理时,再次予舒芬太尼0.1~0.2 μg/kg静脉注射加强镇痛。置入椎弓根螺钉时,适当追加舒芬太尼加强镇痛,待螺钉固定成功后停止静脉泵注右美托咪定。
(2)PE-LIF:采用聚醚醚酮材质的常规后路椎间融合器(Optima LT1)、钛合金长臂万向椎弓根钉,椎间植骨材料为神经减压所获取的自体骨。患者取侧卧位(症状侧在上方,双侧症状者选择影像学表现较严重的一侧入路),在C臂系统透视下定位手术节段双侧椎弓根、椎间隙及棘突中线体表投影点并标记,常规消毒铺巾,分别于双侧椎弓根置入导丝。根据患者体重以椎间隙体表投影处后正中线旁开8~13 cm为穿刺点,穿刺点局部予浸润麻醉,平行手术节段椎间隙用穿刺针定位于上关节突肩部,从皮肤至关节突关节逐层浸润麻醉。沿着穿刺针中心置入导丝,用逐级扩张管扩张工作通道软组织,放入工作通道,连接脊柱内镜系统。镜下用一次性等离子刀头清除软组织,显露至关节突关节,用内镜辅助可视环锯切除上下关节突、部分下椎板、部分上椎板及棘突基底部骨质,行椎管扩大成形术。骨质切除顺序:①上关节突肩部;②上关节突基底部(显露黄韧带起点);③下关节突肩部;④下关节突基底部(显露黄韧带止点);⑤同侧棘突基底部;⑥压低环锯切除对侧下关节突腹侧(如为单侧症状则不进行该步骤)。显露并切除黄韧带后,背侧减压范围可达硬膜囊及双侧神经根背侧,再用一次性等离子刀头、篮钳及髓核钳处理粘连组织,并进行神经根及硬膜囊粘连松解。松解完毕后放置更大直径半套管,旋转套管保护神经根及硬脊膜,切开椎间盘纤维环,并进行神经根及硬膜囊腹侧减压,腹侧减压范围达到对侧神经根。将半套管适当插入椎间隙,用镜下椎间盘铰刀处理椎间隙,彻底处理软骨终板、显露骨性终板。予椎间融合器试模确定椎间融合器大小,将自体骨骨粒及椎间融合器置入椎间隙,随后取出内镜及工作通道。沿导丝分别置入4枚椎弓根螺钉,根据腰椎生理曲度预弯连接棒,椎弓根安置连接棒后拧紧螺帽并行椎体提拉复位。
1.3 随访及评价指标记录手术时间、术中出血量、住院时间及手术相关并发症。术中出血量采用Gross循环血量线性方程计算。于术前、术后1个月、术后6个月、术后1年采用疼痛视觉模拟量表(visual analogue scale,VAS)评分和Oswestry功能障碍指数(Oswestry disability index,ODI)评价临床疗效。
在术前、术后1个月、术后6个月、术后1年门诊随访时拍摄腰椎X线片和腰椎CT。(1)手术节段椎间隙高度:侧位X线片上取滑脱椎体重叠部分中点处,下位椎体上终板与上位椎体下终板间的距离。(2)腰椎前凸角:侧位X线片上L1椎体上缘与S1椎体上缘延长线的夹角。(3)手术节段前凸角:侧位X线片上手术节段上位椎体下缘与下位椎体上缘的夹角。(4)植骨融合情况:在术后6个月、术后1年腰椎CT图像上,若手术节段上、下终板的桥接骨小梁穿过内植骨即判断为椎间植骨融合[11]。(5)椎弓根螺钉置钉准确率:通过术后1个月腰椎CT的三维重建图像,采用改良Gertzbein-Robbins椎弓根螺钉位置分类标准评估椎弓根螺钉置钉准确率[12]。A级为椎体或椎弓根皮质无破坏,B级为螺钉穿透皮质<2 mm,C级为螺钉穿透骨皮质≥2 mm但<4 mm,D级为螺钉穿透骨皮质≥4 mm但<6 mm,E级为螺钉穿透骨皮质≥6 mm。其中A级和B级被认为椎弓根螺钉位置临床可接受,C~E级被认为是不良置钉。椎弓根螺钉置钉优良率为A级和B级螺钉占置钉总数的比例。
1.4 统计学处理应用SPSS 21.0软件进行统计学分析。计量资料以x±s表示,手术前后评分的比较采用重复测量方差分析,两两比较采用Bonferroni检验。检验水准(α)为0.05。
2 结果 2.1 患者的一般资料共58例患者纳入本研究,男24例、女34例,年龄为37~82(53.1±14.5)岁;L3/4节段腰椎滑脱症患者4例(6.90%),L4/5节段34例(58.6%),L5/S1节段20例(34.5%);退变性滑脱36例,峡部裂性滑脱22例;伴有原发性高血压15例,冠状动脉粥样硬化性心脏病7例,糖尿病12例,高尿酸血症3例。58例患者均有不同程度的腰背痛和下肢放射痛,其中24例伴间歇性跛行。
2.2 临床疗效评价58例患者均顺利完成PE-LIF,均未更改麻醉方式、手术体位及手术方式,手术时间为130~190(160±30)min,术中出血量为52~120(63±15)mL,住院时间为6~15(9.3±3.5)d。58例患者均获得随访,随访时间为13~26(17.4±2.8)个月。PE-LIF术后1个月、术后6个月、术后1年,患者腰痛VAS评分、下肢痛VAS评分和ODI均较术前降低,手术节段椎间隙高度、腰椎前凸角、手术节段前凸角均较术前增大,差异均有统计学意义(均P<0.05,表 1)。术后6个月时,24例(41.38%)患者获得骨性融合;术后1年时,所有患者均获得骨性融合。典型病例资料见图 1。
|
|
表 1 腰椎滑脱症患者PE-LIF术后临床疗效和影像学评估 |
|
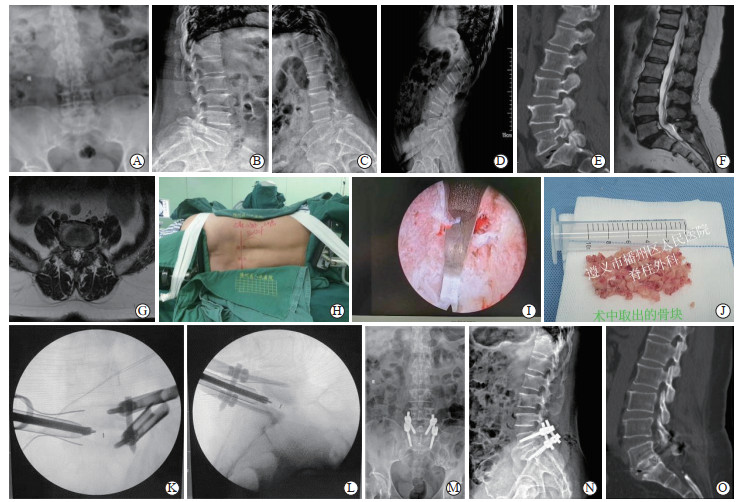
图 1 1例65岁女性L5椎体峡部裂型滑脱症患者的诊治资料 左侧为患侧和手术入路侧,在局部麻醉辅助麻醉监护镇静下行侧卧位内镜下腰椎椎间融合术.A:术前正位X线片;B:术前侧位X线片;C:术前过伸位X线片;D:术前过屈曲位X线片;E:术前腰椎计算机断层扫描提示L5椎体滑脱、峡部断裂;F:术前腰椎矢状面磁共振成像提示L5椎体滑脱;G:术前腰椎水平位磁共振成像提示L5/S1椎管狭窄;H:术前患者手术体位摆放;I:内镜下观察椎间隙处理完成后终板植骨床;J:术中用于椎间隙植骨切取所备的自体骨块;K、L:术中C臂系统透视下在半套管的保护下置入椎间融合器;M:术后3 d复查正位X线片提示L5椎体完全复位;N:术后3 d复查侧位X线片提示L5椎体完全复位;O:术后1年计算机断层扫描检查示L5/S1椎间已融合. |
2.3 置钉准确率评价
所有置钉中A级和B级螺钉分别为165枚(71.72%)、36枚(15.52%),C级和D级螺钉分别为24枚(10.34%)、7枚(3.02%),无E级螺钉,总体置钉优良率为86.64%(201/232)。
2.4 并发症发生情况术中放置椎间融合器试模时,2例患者出现一过性下肢放射痛,考虑为出口根侵扰所致,根据患者提示及时调整操作后缓解。术后即刻,2例患者出现下肢麻木,采用地塞米松、甘露醇等对症治疗,术后1周症状明显缓解。围手术期无肌力下降、脊柱感染、椎管内血肿形成等并发症发生。术后1年时,所有患者均获得骨性融合,未见椎间不融合及假关节形成等情况。随访期间所有患者均未发生椎间融合器移位/沉降、椎弓根螺钉松动或断钉断棒、脊柱感染、椎管内血肿等严重并发症。
3 讨论腰椎滑脱症是引起腰腿疼痛的重要原因之一,是脊柱外科常见疾病,经典的后路腰椎椎间融合术和改良的经椎间孔腰椎椎间融合术是治疗此类疾病的常用手术方式。但这些手术方式因存在对软组织损伤较严重、椎旁肌剥离广泛易造成脊柱后方结构破坏、术中长时间牵拉神经容易引起神经刺激等缺陷,导致部分患者在术后出现顽固性腰痛,影响患者满意度[13-14]。近年来,经皮脊柱内镜技术快速发展,从最初单纯用于治疗腰椎间盘突出症到内镜下腰椎融合技术的初步应用,涌现出一系列技术创新与改进[15-19]。本研究采用局部麻醉结合麻醉监护镇静下PE-LIF治疗腰椎滑脱症,获得满意的治疗效果。
常规的脊柱内镜下腰椎椎间融合术采用全身麻醉和俯卧位,其手术相关并发症较多[20],其中较为严重的是神经根损伤,由于镜下视野有限,对解剖结构区分不如肉眼所见。出口神经根损伤也常见报道,特别是在腰椎滑脱症患者,其椎体间位置变化导致出口神经根位置异常,术中损伤风险更高。2012年Osman[21]报道了脊柱内镜下腰椎椎间融合术并获得满意的近期临床效果,但该手术并发症的总发生率高达20%,其中最主要的并发症是出口神经根损伤;随后Jacquot和Gastambide[22]也报道了内镜辅助下腰椎椎间融合术,初步临床结果满意,然而术中出口神经根损伤的发生率为12.3%,总体并发症(包括融合器移位等)发生率高达36%。虽然有文献报道术中可通过电生理监测预警出口神经根损伤,但其准确率及灵敏度均不满意[23]。笔者认为,患者身体是最灵敏、准确的神经监测系统,全身麻醉下患者不能对神经刺激进行反馈,术中损伤神经时无法预警。本组患者采用局部麻醉辅助麻醉监护镇静,患者术中保持清醒,当手术器械刺激神经根时,患者会有下肢疼痛、麻木或电击感,可将这种异常感觉反馈给医师,为避免神经根损伤提供了高效、准确的预警;镜下减压结束后,医师在镜下观察神经根自主搏动的同时观察患者做直腿抬高动作时的神经根滑动情况,并与患者交流了解即刻感受,从而保证神经减压疗效。局部麻醉手术避免了全身麻醉气管插管及对全身基础情况的干扰,也使部分合并腹腔或胸腔积液等疾病而不能耐受全身麻醉和俯卧位手术的患者获得了治疗机会。
腰椎滑脱症主要发生于中老年人,常合并心肺功能不全等基础疾病。在麻醉镇静时,俯卧位易导致心肺受压,加上静脉止痛和镇静药物对呼吸的抑制作用,可引起呼吸功能障碍。文献报道合并心肺功能不全的老年患者长时间俯卧会出现呼吸功能障碍加重甚至死亡等严重并发症[24-25]。Kolcun等[26]曾尝试在俯卧位基础麻醉不进行气管插管的条件下对100例患者进行PE-LIF,虽未发生严重麻醉并发症,但研究指出这种手术方式对麻醉团队要求极高。
由于腹部压力与椎管内压力呈正相关,患者在俯卧位时腹内压增高,手术操作过程中椎管内的高压力使硬膜囊邻近的静脉丛怒张而更容易受到损伤,且损伤后也容易发生镜下出血,影响镜下手术操作。有学者在经皮经椎间孔入路内镜下髓核切除术治疗腰椎间盘突出症的研究中发现,俯卧位术中出血量为(53.72±16.80)mL,侧卧位术中出血量为(41.99±13.25)mL,差异有统计学意义(P<0.05)[27]。因此,本研究采取侧卧位使患者腹部松弛,腹压和椎管内压力相对较低,在一定程度上规避了上述问题。
Matsumoto等[28]认为侧卧位脊柱内镜手术有利于开放患者术侧椎间孔,并且在侧卧位时硬膜囊因重力作用向手术对侧下沉,有利于术中操作并提高手术安全性。本组病例的术后ODI、腰痛VAS评分及下肢痛VAS评分均较术前降低,患者的腰部功能和疼痛症状得到了改善,直至术后1年仍保持较为稳定的临床疗效。此外,X线片测量结果提示术后手术节段椎间隙高度较术前改善,并在术后1年仍维持稳定,术后1年达到骨性融合后未见明显塌陷;腰椎前凸角及手术节段前凸角也较术前增大,术后1年达到骨性融合后仍保持着较理想的角度,说明侧卧位手术不影响临床疗效。
临床症状改善与术中充分减压关系密切,侧卧位改变了减压视角,笔者建议减压范围和顺序如下:镜下环锯开窗减压时切除部分关节突关节及上下部分椎板,减压范围近远端可达到黄韧带起止点,头侧可至上位椎弓根下缘,外侧可至椎间孔外口,尾侧可至下位椎弓根上缘;通过压低工作套管可减压至双侧神经根及硬膜囊腹侧,对侧通过镜下环锯切除棘突基底部然后压低环锯或使用镜下动力系统切/磨除对侧下关节突腹侧,进行硬膜囊及神经根背侧减压;咬骨钳沿黄韧带背侧咬除上关节突内侧进行侧隐窝减压,从而实现对目标神经根背侧、腹侧及侧隐窝的全程松解减压。
本组病例术后腰痛症状轻,术后第1天即可在腰围或支具固定下下床活动,这与腰背部软组织损伤较轻有关。单节段PE-LIF的手术切口为4个长约1.5 cm切口及1个长约2 cm切口,通过逐级扩张导管建立工作通道来完成镜下减压、椎间融合器置入及椎弓根螺钉置入,不需要广泛剥离肌肉,不损伤后方韧带复合体。
本组病例术后1年均获得骨性融合,这与术中充分植骨及终板良好的植骨床有关。在处理终板的过程中,使用镜下绞刀切除软骨终板时前方可至前纵韧带并形成扇形区域,且镜下能够清晰观察到软骨终板被充分清除,达到了骨性终板“微渗血”的标准,有利于椎间植骨及椎间融合器置入。
本研究通过Gertzbein-Robbins椎弓根螺钉位置分类标准进行判断,发现椎弓根螺钉置钉大部分为A和B类(占86.64%),C和D类仅占13.36%,且C和D类主要是早期手术患者,考虑主要与前期侧卧位置钉经验不足有关。经皮椎弓根螺钉置入是侧卧位手术的难点,由于侧卧位置钉与常规俯卧位置钉手术习惯差别较大,尤其是下方置钉其角度与俯卧位手术的差距更大,需要术者有良好的三维空间概念。此外,该手术方式手术时间较长,随着手术量的增加,侧卧位置钉技术逐渐成熟,手术时间与俯卧位置钉的差距也会减小。导航技术、机器人等辅助置钉技术的应用可能有助于提高手术置钉的效率和准确率。
该手术技术学习曲线陡峭,要求术者有PE-LIF和脊柱内镜手术经验,笔者在数百例局部麻醉侧卧位脊柱内镜下单纯减压术及数十例全身麻醉俯卧位内镜下腰椎椎间融合术的经验基础上才开始尝试该技术。笔者认为该手术的关键之处在于保持镜下视野清晰,并重视“预止血”的概念,即在出现微小渗血或有小静脉阻挡视野时先进行止血处理后再切除椎间盘。此外,本团队在局部麻醉下对神经根松解完毕后,放置更大直径半套管并旋转套管保护神经根和硬脊膜,然后将半套管适当插入椎间隙同时使用骨锤敲击固定牢靠,助手单手扶稳半套管防止其移动或退出,再使用普通开放铰刀与刮刀逐级处理椎间隙,处理结束后连接脊柱内镜观察植骨床,与以往全程使用镜下铰刀处理椎间隙相比大大提高了椎间隙处理效率,缩短了手术时间。
综上所述,局部麻醉结合麻醉监护镇静下PE-LIF治疗腰椎滑脱症近期疗效可靠,椎间融合率较高,且相较于全身麻醉下俯卧位手术具有可降低神经根损伤风险、避免心肺功能受损、减少失血等优势。本研究是单中心回顾性研究,样本量较小,且未设对照组,随访时间较短,远期疗效需进一步观察,有待进一步开展多中心大样本前瞻性对照试验等更高循证证据等级的研究。
| [1] |
CHAN A K, SHARMA V, ROBINSON L C, et al. Summary of guidelines for the treatment of lumbar spondylolisthesis[J]. Neurosurg Clin N Am, 2019, 30(3): 353-364. DOI:10.1016/j.nec.2019.02.009 |
| [2] |
SEMBRANO J N, TOHMEH A, ISAACS R, et al. Two-year comparative outcomes of MIS lateral and MIS transforaminal interbody fusion in the treatment of degenerative spondylolisthesis: part Ⅰ: clinical findings[J]. Spine (Phila Pa 1976), 2016, 41(Suppl 8): S123-S132. DOI:10.1097/BRS.0000000000001471 |
| [3] |
BRUSKO G D, WANG M Y. Endoscopic lumbar interbody fusion[J]. Neurosurg Clin N Am, 2020, 31(1): 17-24. DOI:10.1016/j.nec.2019.08.002 |
| [4] |
AO S, ZHENG W, WU J, et al. Comparison of preliminary clinical outcomes between percutaneous endoscopic and minimally invasive transforaminal lumbar interbody fusion for lumbar degenerative diseases in a tertiary hospital: is percutaneous endoscopic procedure superior to MIS-TLIF? A prospective cohort study[J]. Int J Surg, 2020, 76: 136-143. DOI:10.1016/j.ijsu.2020.02.043 |
| [5] |
WU J, LIU H, AO S, et al. Percutaneous endoscopic lumbar interbody fusion: technical note and preliminary clinical experience with 2-year follow-up[J]. Biomed Res Int, 2018, 2018: 5806037. DOI:10.1155/2018/5806037 |
| [6] |
YANG J, LIU C, HAI Y, et al. Percutaneous endoscopic transforaminal lumbar interbody fusion for the treatment of lumbar spinal stenosis: preliminary report of seven cases with 12-month follow-up[J]. Biomed Res Int, 2019, 2019: 3091459. DOI:10.1155/2019/3091459 |
| [7] |
YIN P, GAO H, ZHOU L, et al. Enhanced recovery after an innovative percutaneous endoscopic transforaminal lumbar interbody fusion for the treatment of lumbar spinal stenosis: a prospective observational study[J]. Pain Res Manag, 2021, 2021: 7921662. DOI:10.1155/2021/7921662 |
| [8] |
YIN P, ZHANG Y, PAN A, et al. The feasibility for a novel minimally invasive surgery-percutaneous endoscopic transforaminal lumbar interbody fusion (PE-TLIF) for the treatment of lumbar degenerative diseases: a cadaveric experiment[J]. J Orthop Surg Res, 2020, 15(1): 387. DOI:10.1186/s13018-020-01930-0 |
| [9] |
JIN M, ZHANG J, SHAO H, et al. Percutaneous transforaminal endoscopic lumbar interbody fusion for degenerative lumbar diseases: a consecutive case series with mean 2-year follow-up[J]. Pain Physician, 2020, 23(2): 165-174. |
| [10] |
KOLCUN J P G, BRUSKO G D, WANG M Y. Endoscopic transforaminal lumbar interbody fusion without general anesthesia: technical innovations and outcomes[J]. Ann Transl Med, 2019, 7(Suppl 5): S167. DOI:10.21037/atm.2019.07.92 |
| [11] |
中国康复医学会脊柱脊髓损伤专业委员会脊柱微创学组, 中国康复医学会脊柱脊髓专业委员会腰椎研究学组. 脊柱内镜辅助下腰椎椎体间融合术应用的中国专家共识[J]. 中华医学杂志, 2023, 103(5): 329-335. DOI:10.3760/cma.j.cn112137-20220817-01749 |
| [12] |
GERTZBEIN S D, ROBBINS S E. Accuracy of pedicular screw placement in vivo[J]. Spine (Phila Pa 1976), 1990, 15(1): 11-14. DOI:10.1097/00007632-199001000-00004 |
| [13] |
杨善智, 易红蕾, 许俊杰, 等. 极外侧腰椎间融合术治疗轻度腰椎滑脱症[J]. 中国矫形外科杂志, 2020, 28(9): 774-779. DOI:10.3977/j.issn.1005-8478.2020.09.02 |
| [14] |
PRICE J P, DAWSON J M, SCHWENDER J D, et al. Clinical and radiologic comparison of minimally invasive surgery with traditional open transforaminal lumbar interbody fusion: a review of 452 patients from a single center[J]. Clin Spine Surg, 2018, 31(2): E121-E126. DOI:10.1097/BSD.0000000000000581 |
| [15] |
SHEN J. Fully endoscopic lumbar laminectomy and transforaminal lumbar interbody fusion under local anesthesia with conscious sedation: a case series[J]. World Neurosurg, 2019, 127: e745-e750. DOI:10.1016/j.wneu.2019.03.257 |
| [16] |
PARK M K, PARK S A, SON S K, et al. Clinical and radiological outcomes of unilateral biportal endoscopic lumbar interbody fusion (ULIF) compared with conventional posterior lumbar interbody fusion (PLIF): 1-year follow-up[J]. Neurosurg Rev, 2019, 42(3): 753-761. DOI:10.1007/s10143-019-01114-3 |
| [17] |
AHN Y, YOUN M S, HEO D H. Endoscopic transforaminal lumbar interbody fusion: a comprehensive review[J]. Expert Rev Med Devices, 2019, 16(5): 373-380. DOI:10.1080/17434440.2019.1610388 |
| [18] |
YOUN M S, SHIN J K, GOH T S, et al. Full endoscopic lumbar interbody fusion (FELIF): technical note[J]. Eur Spine J, 2018, 27(8): 1949-1955. DOI:10.1007/s00586-018-5521-4 |
| [19] |
KAMSON S. Full-endoscopic lumbar fusion outcomes in patients with minimal deformities: a retrospective study of data collected between 2011 and 2015[J]. Pain Phys, 2019, 22(1): 75-88. DOI:10.36076/ppj/2019.22.75 |
| [20] |
HEO D H, LEE D C, KIM H S, et al. Clinical results and complications of endoscopic lumbar interbody fusion for lumbar degenerative disease: a meta-analysis[J]. World Neurosurg, 2021, 145: 396-404. DOI:10.1016/j.wneu.2020.10.033 |
| [21] |
OSMAN S G. Endoscopic transforaminal decompression, interbody fusion, and percutaneous pedicle screw implantation of the lumbar spine: a case series report[J]. Int J Spine Surg, 2012, 6: 157-166. DOI:10.1016/j.ijsp.2012.04.001 |
| [22] |
JACQUOT F, GASTAMBIDE D. Percutaneous endoscopic transforaminal lumbar interbody fusion: is it worth it?[J]. Int Orthop, 2013, 37(8): 1507-1510. DOI:10.1007/s00264-013-1905-6 |
| [23] |
YANG X, WANG L, YANG Q, et al. Neurological safety of endoscopic transforaminal lumbar interbody fusion: a magnetic resonance neurography study[J]. Spine (Phila Pa 1976), 2023, 48(5): 344-349. DOI:10.1097/BRS.0000000000004496 |
| [24] |
KIM J H, KIM S, YU T, et al. Sudden arrhythmia in the prone position during spinal surgery: a case report[J]. Medicine (Baltimore), 2022, 101(33): e30137. DOI:10.1097/MD.0000000000030137 |
| [25] |
AHMED JONAYED S, ALAM M S, AL MAMUN CHOUDHURY A, et al. Efficacy, safety, and reliability of surgery on the lumbar spine under general versus spinal anesthesia—an analysis of 64 cases[J]. J Clin Orthop Trauma, 2021, 16: 176-181. DOI:10.1016/j.jcot.2020.12.032 |
| [26] |
KOLCUN J P G, BRUSKO G D, BASIL G W, et al. Endoscopic transforaminal lumbar interbody fusion without general anesthesia: operative and clinical outcomes in 100 consecutive patients with a minimum 1-year follow-up[J]. Neurosurg Focus, 2019, 46(4): E14. DOI:10.3171/2018.12.FOCUS18701 |
| [27] |
项宇峰. 侧卧位与俯卧位下经椎间孔入路经皮内窥镜下腰椎椎间盘切除术治疗腰椎椎间盘突出症[J]. 脊柱外科杂志, 2022, 20(2): 98-102. DOI:10.3969/j.issn.1672-2957.2022.02.006 |
| [28] |
MATSUMOTO M, HASEGAWA T, ITO M, et al. Incidence of complications associated with spinal endoscopic surgery: nationwide survey in 2007 by the Committee on Spinal Endoscopic Surgical Skill Qualification of Japanese Orthopaedic Association[J]. J Orthop Sci, 2010, 15(1): 92-96. DOI:10.1007/s00776-009-1428-6 |
 2024, Vol. 45
2024, Vol. 45


