A型主动脉夹层(type A aortic dissection,AAD)是心血管急症,往往需要急诊开放手术治疗,由于AAD手术操作步骤复杂、手术时间长,还需要低温体外循环,对凝血功能影响破坏较大,止血是手术难点之一[1]。包裹止血是经典的止血方法,能够有效解决缝合针孔渗血等问题,但AAD患者施行全弓置换手术时因四分叉人工血管分支多,包裹耗时长,增加了手术时间和术中出血量,影响手术效果[2]。为进一步提高手术疗效,减少出血,缩短手术时间,本研究在AAD全弓置换手术中设计了一种预置心包包裹止血法,现将手术方法和治疗效果报告如下。
1 资料和方法 1.1 研究对象回顾性分析2021年1月至11月我院收治的35例经CT血管造影诊断为AAD并采用预置心包包裹法行主动脉全弓置换术患者(预置心包组)的临床资料,以同期传统方法行全弓置换术的35例AAD患者为对照。所有患者术前完善心脏超声、凝血功能和其他常规手术检查项目,手术由2位主刀医师随机完成,术后监护室内每日行血常规及肝肾功能检查,术后第一日行凝血功能检查。排除标准:同期行冠状动脉搭桥手术或采用David手术等其他根部处理方式的夹层手术患者。本研究通过中国人民解放军南部战区总医院伦理委员会审批(NZLLKZ2023010)。
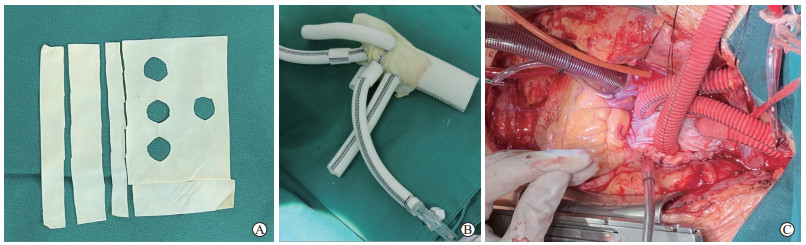
1.2 手术方法及术后管理预置包裹组患者的手术由两组医师同时进行,一组缝合四分叉人工血管预置包裹心包,将10.0 cm×10.5 cm国产牛心包补片裁剪成宽为0.5、1.0、1.5 cm的牛心包条(图 1A),分别用于包裹主动脉远端吻合口、主动脉内近端吻合口、主动脉外近端吻合口,剩余牛心包按四分叉人工血管分支血管排列方式开孔后套入几个分支内,使用4-0聚丙乙烯(prolen)线对牛心包和分支血管起始部缝合,将四分支人工血管10 mm直径分支端剪下2段2 cm长血管,分别套在2个8 mm分支血管上,预包裹备用(图 1B)。另一组同时进行手术操作。游离血管开胸建立体外循环,采用股动脉、右侧腋动脉和左颈总动脉3根管道灌注。温度降至32 ℃时阻闭主动脉,切开升主动脉,直接冠状动脉冷灌组氨酸-色氨酸-同戊二酸溶液(商品名:康斯特)。心脏停跳后切开升主动脉并探查。如行Bentall术则使用带瓣管道连续或间断缝合主动脉瓣环和人工瓣膜,人工血管开孔后与冠状动脉开口直接吻合。如行升主动脉置换,则在冠状动脉开口上方1.0 cm处横断主动脉根部,内衬心包外垫血管片和心包固定根部,固定完成后将外垫心包与横断的升主动脉远端后壁连续包裹缝合,缝合后留线备用。当鼻咽温度降至26 ℃,阻闭无名动脉近端及左颈总动脉、左锁骨下动脉,停下半身体循环行选择性双侧顺行脑灌注。松开主动脉阻闭钳,暴露主动脉弓部,选用合适覆膜术中支架送至降主动脉内释放,行四分叉人工血管与支架近端吻合,前壁吻合口加外垫心包,最后吻合主动脉根部,根部吻合完成后,使用后壁与心包包裹备用缝线完成根部包裹。排除左心气体后开放升主动脉,后依次行人工血管分支与左锁骨下动脉、无名动脉、左颈总动脉吻合,如无活动出血将外套10 mm人工血管下拉覆盖吻合口(图 1C)。最后将预置包裹心包与剩余主动脉外膜连续缝合,并与右心耳做分流。操作完成后停体外循环止血并关胸。对照组除不缝合预置包裹心包外,其余手术方法同预置包裹组,根据术后出血情况决定是否包裹。
|
图 1 牛心包剪裁示意图(A)、预包裹示意图(B)及预包裹术中照片(C) |
手术后患者进入ICU监护,给予呼吸机辅助呼吸,监测桡动脉有创动脉血压、中心静脉压,根据血压、心率和一般情况使用血管活性药物,应用头孢类抗生素抗感染。患者苏醒后逐渐减少呼吸辅助条件,患者肌力可、自主呼吸良好后拔除气管插管。
1.3 观察指标对比分析预置包裹组与对照组术中主动脉根部处理方式、手术时间、体外循环时间、心脏停搏时间、术中红细胞使用量,以及两组的术后早期凝血功能(术后1 d血小板计数、凝血酶原时间,纤维蛋白原浓度、K时间、最大血块强度)和术后恢复情况(术后24 h引流量、再次开胸止血情况、机械通气时间、血液净化治疗情况、入住ICU时间)。
1.4 统计学处理应用SPSS 17.0软件进行数据分析,符合正态分布的计量资料以x±s表示,组间比较采用t检验;非正态分布的计量资料以中位数(下四分位数,上四分位数)表示,组间比较采用非参数秩和检验;计数资料以例数和百分数表示,组间比较采用χ2检验。检验水准(α)为0.05。
2 结果 2.1 一般资料比较两组患者的一般临床资料及术前血小板计数和凝血功能差异均无统计学意义(P均>0.05),见表 1。
|
|
表 1 两组A型主动脉夹层患者术前一般情况及凝血功能比较 |
2.2 术中情况比较
两组AAD患者均完成手术操作,两组间主动脉根部处理方式、心脏停搏时间的差异均无统计学意义(P均>0.05)。与对照组比较,预置包裹组的体外循环时间、手术时间较短,术中红细胞使用量较少(P均<0.05)。见表 2。
|
|
表 2 两组A型主动脉夹层患者术中情况分析 |
2.3 术后早期凝血功能及术后恢复指标比较
预置包裹组患者术后1 d血小板计数、纤维蛋白原浓度、最大血块强度均高于对照组,凝血酶原时间、K时间均短于对照组(P均<0.05)。预置包裹组患者术后24 h引流量少于对照组(P<0.05),但两组患者术后机械通气时间、再次开胸止血、入住ICU时间及血液净化治疗差异均无统计学意义(P均>0.05)。见表 3。
|
|
表 3 两组A型主动脉夹层患者术后早期凝血功能及术后恢复情况比较 |
3 讨论
一般认为AAD患者伴有弓部破口、弓部动脉瘤、弓部环周型剥离、左颈总动脉夹层累及、马方综合征等情况时需要施行全弓置换术,大部分全弓置换手术需要使用四分叉人工血管[3],导致吻合口增多并涉及脑保护、脑灌注方式,增加了手术操作的复杂性且体外循环和手术时间延长,影响凝血功能和术后止血[2, 4-5]。对任何AAD患者,全弓置换术后外科止血均不容轻视,而当患者术前有使用抗凝治疗或抗血小板治疗时,术后止血挑战极大[6]。
为了解决止血问题,有学者提出根部人工血管翻转法,即在主动脉根部吻合时将人工血管翻转插入左心室流出道内进行吻合,吻合完成后将人工血管翻转拉出心脏再进行远端操作[7-8];还有学者对远端和近端吻合口使用外膜翻转法固定,然后再进行吻合,他们认为外膜翻转能更好地封闭假腔,减少出血[9-10]。包裹止血是大血管外科经典的止血方法,大部分处理困难的外科出血几乎都能够通过包裹止血解决[4, 11]。包裹止血可以针对局部出血点,使用心包或血管片小范围包裹,也可以针对吻合口进行环周包裹,还可以对全部主动脉术野或者扩大术野包裹[12]。Chen等[13]报道,对于高龄和术前凝血功能异常的AAD患者,横断主动脉后先封闭横窦,心脏复跳后使用心包覆盖前壁包裹止血,可取得满意的临床效果。而全主动脉术野包裹止血可能存在包裹腔压力过大压迫真腔导致血流梗阻,为了避免这种危害,有学者提出在包裹止血基础上加用包裹腔和右心房系统分流的方法,最常见的分流部位是主动脉根部和右心耳,也有学者报道与上腔静脉侧壁、无名静脉进行分流[14-17]。
虽然上述包裹方法能够部分解决外科性出血问题,但包裹和分流等操作要求具备较高的缝合技巧,尤其是主动脉根部后壁等部位包裹难度大、时间长、术中出血量大[18]。本研究设计的预置心包包裹法AAD全弓置换术由两组医师同时进行,一组常规开胸操作,另一组同时在无菌操作台进行预置心包包裹的手术操作,节省体外循环和手术时间。将10.0 cm×10.5 cm国产牛心包补片裁剪成宽0.5 cm的牛心包条用于主动脉远端吻合口,裁剪成宽1.0 cm用于主动脉内近端吻合口,裁剪成宽1.5 cm用于主动脉外近端吻合口,能翻转后与四分叉人工血管上的预置心包包裹。使用预置包裹准备好的四分叉人工血管与主动脉近远端进行吻合。在主动脉吻合口方面,远端吻合口不横断主动脉,按四分叉人工血管、心包条、主动脉壁和术中支架血管的顺序连续缝合,后壁缝合后在前壁主动脉外留置心包条用以翻转包裹。对升主动脉置换患者根部使用内衬心包外垫血管片和心包条的“三明治”方法制作近端底座,完成底座后先包裹后壁,然后进行四分支人工血管与底座吻合,待根部吻合全部完成后再包裹前壁,整个流程由后至前,暴露充分,可操作性强。对有凝血功能异常倾向的患者可以做包裹腔与右心耳分流。根据笔者操作经验,吻合操作完成后只需要1~2根缝线就能完成全部包裹止血操作,往往包裹止血缝合完成时体外循环复温也刚好完成。
在本研究中,两组患者的一般临床资料及术前凝血功能指标无明显差异,主动脉根部处理方式及心脏停搏时间无明显差异(P均>0.05)。与对照组相比,预置心包包裹组术中红细胞使用量、体外循环时间及手术时间较少,术后早期凝血功能较好,术后24 h引流量较少(P均<0.05)。这一结果表明了预置心包包裹法是AAD全弓置换手术患者术后止血的一个好方法,在本组患者中未见因止血困难导致严重并发症和死亡的病例,该方法操作制式化、标准流程化,在减少术中出血及缩短心脏停搏时间及手术时间上的优势能够让年轻的心血管外科医师有信心进行相关手术操作。
该方法目前仍有一定的的局限性,预置心包包裹本质上增加了纵隔内异物存留量,甚至部分患者术后包裹腔内有积液存留,存在发热可能;此外,该方法在本中心初步展开,目前的病例数量仍相对较少,需进一步扩大研究病例数,延长随访时间,观察远期临床效果。
| [1] |
DHIR A, TEMPE D K. Anemia and patient blood management in cardiac surgery-literature review and current evidence[J]. J Cardiothorac Vasc Anesth, 2018, 32(6): 2726-2742. DOI:10.1053/j.jvca.2017.11.043 |
| [2] |
LIU Y, HAN L, LI J, et al. Consumption coagulopathy in acute aortic dissection: principles of management[J]. J Cardiothorac Surg, 2017, 12(1): 50. DOI:10.1186/s13019-017-0613-5 |
| [3] |
WONG R H L, HO J Y K, UNDERWOOD M J. Complex reoperative thoracic aortic surgery: tactics and techniques[M]//TINTOIU I C, URSULESCU A, ELEFTERIADES J A, et al. New approaches to aortic diseases from valve to abdominal bifurcation. Amsterdam: Elsevier, 2018: 515-528.
|
| [4] |
GALEA J, MANCHÉ A. Method of hemorrhage control from the aorta after repair of a dissected aortic aneurysm[J]. Ann Thorac Surg, 2017, 103(3): e299-e300. DOI:10.1016/j.athoracsur.2016.08.105 |
| [5] |
LIU J, SUN L L, WANG J, et al. The relationship between fibrinogen and in-hospital mortality in patients with type A acute aortic dissection[J]. Am J Emerg Med, 2018, 36(5): 741-744. DOI:10.1016/j.ajem.2017.10.001 |
| [6] |
GUAN X, LI J, GONG M, et al. The hemostatic disturbance in patients with acute aortic dissection: a prospective observational study[J]. Medicine, 2016, 95(36): e4710. DOI:10.1097/MD.0000000000004710 |
| [7] |
INOUE Y, MINATOYA K, ITONAGA T, et al. Utility of proximal stepwise technique for acute aortic dissection involving the aortic root[J]. Ann Thorac Surg, 2016, 101(5): e183-e185. DOI:10.1016/j.athoracsur.2015.11.050 |
| [8] |
TOOLE J M, STROUD M R, IKONOMIDIS J S. Salvage periaortic pericardial baffle equalizes mortality in bleeding patients undergoing aortic surgery[J]. J Thorac Cardiovasc Surg, 2014, 148(1): 151-155. DOI:10.1016/j.jtcvs.2013.08.008 |
| [9] |
TANAKA K, MORIOKA K, LI W, et al. Adventitial inversion technique without the aid of biologic glue or Teflon buttress for acute type A aortic dissection[J]. Eur J Cardiothorac Surg, 2005, 28(6): 864-869. DOI:10.1016/j.ejcts.2005.08.029 |
| [10] |
ODA T, MINATOYA K, SASAKI H, et al. Adventitial inversion technique for type A aortic dissection distal anastomosis[J]. J Thorac Cardiovasc Surg, 2016, 151(5): 1340-1345. DOI:10.1016/j.jtcvs.2016.01.018 |
| [11] |
HU X, WANG Z, REN Z, et al. Simplified total aortic arch replacement with an in situ stent graft fenestration technique for acute type A aortic dissection[J]. J Vasc Surg, 2017, 66(3): 711-717. DOI:10.1016/j.jvs.2017.01.030 |
| [12] |
SUN B C, DICKINSON T A, TESDAHL E A, et al. The unintended consequences of over-reducing cardiopulmonary bypass circuit prime volume[J]. Ann Thorac Surg, 2017, 103(6): 1842-1848. DOI:10.1016/j.athoracsur.2016.09.099 |
| [13] |
CHEN L W, WU X J, DAI X F. Transverse pericardial sinus closure in acute type A aortic dissection operation[J]. Ann Thorac Surg, 2017, 104(4): e351-e353. DOI:10.1016/j.athoracsur.2017.06.035 |
| [14] |
GOLDSTONE A B, CHIKWE J, STELZER P. Modified cabrol shunt to treat left ventricular rupture[J]. Ann Thorac Surg, 2010, 89(1): 313-314. DOI:10.1016/j.athoracsur.2009.04.075 |
| [15] |
ELEFTERIADES J A, YOUSSEF S, ROUSOU L, et al. Novel valved graft modification of cabrol fistula for bleeding after aortic root surgery[J]. Ann Thorac Surg, 2012, 94(5): 1741-1743. DOI:10.1016/j.athoracsur.2012.05.114 |
| [16] |
HOOVER E L, HSU H K, ERGIN A, et al. Left-to-right shunts in control of bleeding following surgery for aneurysms of the ascending aorta[J]. Chest, 1987, 91(6): 844-849. DOI:10.1378/chest.91.6.844 |
| [17] |
SAKAKIBARA Y, KOSHIJI T, HAGIO K, et al. Novel wrapping technique with insertion of fat tissue for hemostasis in aortic surgery[J]. Ann Thorac Surg, 2010, 89(3): 992-993. DOI:10.1016/j.athoracsur.2009.05.066 |
| [18] |
ISHII H, ENDO H, TSUCHIYA H, et al. Enhanced hemostasis with a sealant consisting of hydrofit and surgicel[J]. J Card Surg, 2017, 32(9): 576-578. DOI:10.1111/jocs.13202 |
 2023, Vol. 44
2023, Vol. 44


