抑郁症是一种长期心情低落导致的精神类疾病,据WHO预测,到2030年抑郁症将成为全球首要的疾病负担[1]。目前临床上多以神经递质再摄取抑制剂如5-羟色胺进行抗抑郁治疗,同时给予患者相应的心理疏导,但部分抑郁症患者对此类药物的敏感性较低,长期服用不仅会加重患者对药物的依赖性,还会造成性功能障碍等不良反应[2]。加之目前市面上治疗抑郁症的药物大多是化学药物,寻找安全、低毒的天然药物十分必要。
黄芪多糖(Astragalus polysaccharide,APS)是中药黄芪干燥根茎经提取得到的大分子多糖,是黄芪的主要活性成分。研究证明APS具有抗抑郁的作用[3],但其作用机制尚不清楚。氧化应激参与了抑郁的发生、发展,核因子E2相关因子2(nuclear factor erythroid 2-related factor 2,Nrf2)的抗氧化作用已得到证实[4]。在正常生理状态下,Nrf2在细胞质内且处于抑制状态,但当其被有毒、有害物质激活转位进入细胞核后会与抗氧化反应元件(antioxidant response element,ARE)结合,形成Nrf2-ARE信号通路发挥作用[5]。Nrf2信号通路是机体重要的氧化调节通路,研究表明大量可对Nrf2信号通路发挥调节作用的天然产物具有显著的抗抑郁功效[6]。APS是否通过Nrf2信号通路改善抑郁症状及APS调控Nrf2信号通路后血清氧化指标变化的相关研究较少,本研究以此为出发点,探讨APS抗抑郁的作用机制。
1 材料和方法 1.1 动物、药品、试剂与仪器36只8周龄雄性BALB/c小鼠,体重18~20 g,由厦门大学实验动物中心提供,实验动物使用许可证号为SYXK(闽)2018-0009,动物实验获得厦门大学实验动物伦理委员会审批。小鼠饲养于湿度40%~50%、温度(24.0±1.0)℃的通气笼系统。
APS购于上海江莱生物科技有限公司(货号JL210102003),溶于超纯水中配成400 mg/kg的溶液;氟西汀购于中国食品药品检定研究院(批号100513-201602),溶于0.9%生理盐水中配成1 mg/mL的注射液;丙二醛检测试剂盒、超氧化物歧化酶(superoxide dismutase,SOD)检测试剂盒和谷胱甘肽过氧化物酶(glutathione peroxidase,GSH-Px)检测试剂盒均购于上海江莱生物科技有限公司(货号分别为JL20282、JL1227、JL49904);超氧阴离子(O2·)检测试剂盒、羟自由基(·OH)检测试剂盒均购于北京索莱宝生物科技有限公司(货号分别为20210127、20201231);Nrf2抗体、β-肌动蛋白抗体购于英国Abcam公司(货号分别为ab31163、GR265013-1)。168-1130型全自动酶标仪购于美国Bio-Rad公司。
1.2 慢性轻度不可预见性应激(chronic unpredictablemild stress,CUMS)抑郁模型小鼠的构建参照文献[7]的方法对小鼠进行单笼饲养,并给予每天6种刺激方式(固定在塑料管内、鼠笼倾斜、不筑巢、拥挤环境、明暗颠倒、白噪声)中的任意2种进行刺激。每天的2种刺激方式为随机选取,同一刺激方式不同时出现,各刺激方式按随机原则分布于各应激周期。给予小鼠上述刺激4周建立CUMS抑郁模型,采用行为学实验评价造模是否成功。
1.3 动物分组及处理36只小鼠随机分成4组:正常对照组、CUMS抑郁模型组(CUMS组)、CUMS抑郁模型+氟西汀干预组(CUMS+F组)和CUMS抑郁模型+APS干预组(CUMS+APS组),每组9只。造模成功后,CUMS+F组小鼠每天给予氟西汀10 mg/kg腹腔注射,同时给予灌胃刺激;CUMS+APS组小鼠每天给予APS 400 mg/kg灌胃(结合预实验结果和文献[8]确定灌胃剂量),同时给予注射针刺激;正常对照组和CUMS组小鼠给予等体积超纯水灌胃和注射针刺激。各组均连续干预4周,然后通过行为学实验观察小鼠抑郁状态的改善情况。
1.4 行为学实验 1.4.1 蔗糖偏好实验将小鼠置于有2个饮水瓶的鼠笼中适应24 h,其中一瓶装1%蔗糖水,另一瓶装普通水,12 h后互换2个饮水瓶的位置。实验开始后小鼠禁食过夜,8 h后测量2个饮水瓶液体消耗体积。计算公式:蔗糖偏好率(%)=V蔗糖溶液/(V蔗糖溶液+V普通水)×100%
1.4.2 高架十字迷宫实验将小鼠从中央格面向闭合臂放入高架迷宫,用ANY-maze动物行为分析系统记录5 min内小鼠进入开放臂的次数和在开放臂停留的时间。每只小鼠实验结束后在实验平台喷洒75%乙醇,以消除其运动痕迹对后面测试的影响。
1.4.3 旷场实验将小鼠放置于尺寸为90 cm×90 cm×30 cm的木箱中5 min,用ANY-maze动物行为分析系统记录小鼠在测试时间内跨越方块的次数。每只小鼠实验结束后在实验平台喷洒75%乙醇,以消除其运动痕迹对后面测试的影响。
1.4.4 悬尾实验将小鼠放置在悬尾实验平台上6 min,用ANY-maze动物行为分析系统记录小鼠在后4 min测试时间内的不动时间。
1.5 小鼠血清与脑海马组织标本采集小鼠药物干预4周后眼眶取血,将血液静置2 h后600×g离心10 min,收集上层血清于-80 ℃冰箱保存。处死小鼠取出海马组织,置于-80 ℃冰箱保存。
1.6 小鼠血清氧化指标检测采用ELISA检测试剂盒测定小鼠血清丙二醛、SOD、GSH-Px、O2·和·OH水平,操作严格按照试剂盒说明书进行。
1.7 蛋白质印迹法检测小鼠海马组织中Nrf2蛋白的表达每组随机选取6只小鼠的海马组织置于匀浆器中球状部位,用干净的剪刀将组织块剪碎,加入1 mL单去污剂裂解液(含苯甲基磺酰氟)于匀浆器中匀浆,然后在4 ℃下2 400×g离心5 min,蛋白质上清液使用BCA试剂盒测定浓度,采用10% SDS-PAGE分离蛋白质并转移至PVDF膜。在室温下用5%脱脂牛奶封闭1 h,加入Nrf2抗体(稀释比例为1∶500)和β-肌动蛋白抗体(稀释比例为1∶5 000),4 ℃孵育过夜。次日用TBST冲洗3次后加入二抗孵育2 h,然后加化学发光液观察。使用ImageJ软件分析条带的相对灰度。
1.8 统计学处理应用SPSS 20.0软件进行统计学分析。因正常对照组有1只小鼠行为学实验数据与其他8只偏离较大,故予以剔除,为保证统计一致性,每组实际只统计8只小鼠的行为学实验和血清氧化指标结果。计量资料以x±s表示,任意两组间比较采用独立样本t检验。检验水准(α)为0.05。
2 结果 2.1 各组小鼠行为学实验结果比较与正常对照组比较,CUMS组小鼠悬尾实验不动时间延长,蔗糖偏好率、旷场实验穿越次数、高架十字迷宫实验开放臂进入次数和停留时间均下降,差异均有统计学意义(P均<0.01)。与CUMS组比较,CUMS+F组和CUMS+APS组小鼠悬尾实验不动时间缩短,蔗糖偏好率、旷场实验穿越次数、高架十字迷宫实验开放臂进入次数和停留时间均增加,差异均有统计学意义(P<0.05,P<0.01)。见表 1。
|
|
表 1 各组小鼠行为学实验结果比较 |
2.2 各组小鼠血清氧化指标比较
与正常对照组比较,CUMS组小鼠血清丙二醛含量升高(P<0.01),而血清SOD、GSH-Px、O2·、·OH含量均下降,差异均有统计学意义(P<0.05,P<0.01)。与CUMS组比较,CUMS+F组和CUMS+APS组小鼠血清丙二醛含量下降,而血清SOD、GSH-Px、O2·、·OH含量均升高,差异均有统计学意义(P<0.05,P<0.01)。见表 2。
|
|
表 2 各组小鼠血清氧化指标比较 |
2.3 各组小鼠海马组织Nrf2表达水平比较
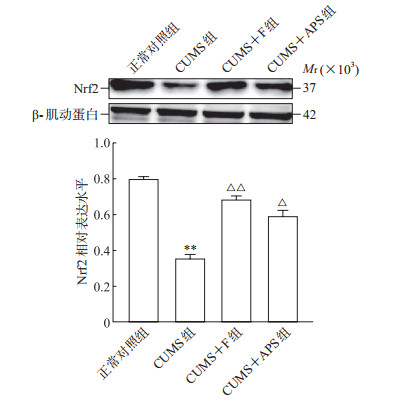
与正常对照组比较,CUMS组小鼠海马组织中Nrf2蛋白表达水平下降(P<0.01)。与CUMS组比较,CUMS+F组和CUMS+APS组小鼠海马组织中Nrf2蛋白表达水平均升高,差异均有统计学意义(P<0.05,P<0.01)。见图 1。
|
图 1 各组小鼠海马组织中Nrf2蛋白表达水平比较 **P<0.01与正常对照组比较;△P<0.05,△△P<0.01与CUMS组比较.n=6, x±s.Nrf2:核因子E2相关因子2;CUMS:慢性轻度不可预见性应激;F:氟西汀;APS:黄芪多糖. |
3 讨论
研究发现抑郁样行为的发生与海马组织损伤、炎症反应和氧化应激等病理性改变有关[9],而Nrf2蛋白是一个重要的调控抗氧化酶系的转录因子[10-11]。本研究结果显示,与正常对照组比较,CUMS组小鼠海马组织中Nrf2蛋白表达水平下降,可能的原因为CUMS程序性刺激引起小鼠体内氧化应激水平升高,过强的氧化应激负反馈性抑制了Nrf2表达,影响了Nrf2由细胞质向细胞核移位,使其活性受到抑制,表达减少[12]。经APS干预后,CUMS+APS组小鼠海马组织中Nrf2蛋白表达水平较CUMS组升高。
目前常使用动物模型进行抑郁症的相关分子机制研究,CUMS是一种被广泛认可的抑郁症动物模型,具有良好的外观效应、预测性和建构效度,模型构建成功与否可通过行为学实验评价,如通过糖水偏好实验检测快感的缺失情况来判断抑郁状态、通过旷场实验检测动物的探究能力、通过强迫游泳实验检测抑郁类行为等。本研究行为学实验结果表明CUMS抑郁模型构建成功,且经APS干预后小鼠悬尾实验不动时间缩短,蔗糖偏好率、旷场实验穿越次数、高架十字迷宫实验开放臂进入次数和停留时间均增加。以上结果说明APS可对抑郁症起到治疗作用,且可能与Nrf2通路有关。中医学认为抑郁症属于郁证的范畴,其发病主要与气机失调有关[13]。APS是常见的补气中药,这也在一定程度上为APS治疗抑郁症提供了理论基础。
氧化应激是指体内氧化与抗氧化失衡的状态,机体内许多疾病的发生、发展与氧化应激具有一定的相关性。当机体受到有害刺激时会导致体内高活性的自由基如活性氧、丙二醛等产生过多,一旦超出SOD、GSH-Px等抗氧化酶系统的清除能力就会造成氧化应激损伤[14]。当小鼠受到CUMS程序性刺激时,小鼠机体表现出氧化应激异常增强,本研究也观察到与正常对照组比较,CUMS组小鼠血清丙二醛含量升高,而血清SOD、GSH-Px表达下降,表明机体发生抑郁后氧化应激反应进一步增强,同时也说明氧化应激增强能够诱导抑郁症的发生和发展。给予APS干预后,与CUMS组比较,CUMS+APS组小鼠血清丙二醛含量下降,而血清SOD、GSH-Px表达升高,提示APS可能通过抑制机体的氧化应激反应改善CUMS抑郁模型小鼠的抑郁状态。但本研究中O2·、·OH含量不升反降,可能原因是本次造模成功后并没有继续使用CUMS程序性刺激,而轻度抑郁症在一定时间内能够自我修复,本研究为造模成功后经过4周才测量O2·、·OH含量,在此过程中CUMS组小鼠通过自我修复使其体内O2·、·OH含量呈上升趋势;正常对照组由于未受到相应刺激,其体内维持动态平衡,从而造成模型组O2·、·OH含量低于正常对照组。这是本研究的一个不足之处,后续将继续完善。
本研究选择氟西汀作为阳性对照药,不仅因为氟西汀是临床治疗抑郁症的首选药物,而且有研究发现,氟西汀可改善脑卒中后抑郁大鼠的学习记忆能力,认为其机制可能与脑内丙二醛水平降低、SOD水平增加,从而改善氧化应激有关[15]。我们前期研究发现,低剂量(每天5 mg/kg)氟西汀联合重复经颅磁刺激能够改善CUMS小鼠的抑郁状态,提示在不改变治疗效果的前提下降低化学药物的使用剂量能够缓解其带来的不良反应,但前期研究并未探讨其作用机制[16]。本实验中给予氟西汀治疗后,CUMS抑郁模型小鼠的血清氧化指标明显改善,表明氟西汀在一定程度上也能够改善机体的氧化应激,从而对抑郁症起到治疗作用。
综上所述,APS能够缩短CUMS抑郁模型小鼠悬尾实验不动时间,增加蔗糖偏好、旷场实验穿越次数及高架十字迷宫实验开放臂进入次数和停留时间,从而改善抑郁状态,其作用可能是通过调节海马组织Nrf2通路和血清氧化指标实现的。
| [1] |
MALHI G S, MANN J J. Depression[J]. Lancet, 2018, 392(10161): 2299-2312. DOI:10.1016/S0140-6736(18)31948-2 |
| [2] |
ROTHMORE J. Antidepressant-induced sexual dysfunction[J]. Med J Aust, 2020, 212(7): 329-334. DOI:10.5694/mja2.50522 |
| [3] |
刘佳蕾, 王宇亮, 赵宏, 等. 百合多糖与黄芪多糖联用对慢性应激小鼠抑郁行为的影响及机制[J]. 中国实验方剂学杂志, 2022, 28(5): 62-70. DOI:10.13422/j.cnki.syfjx.20220539 |
| [4] |
董渠龙, 王华, 侯海燕, 等. Nrf2-ARE信号通路功能的研究进展[J]. 国际妇产科学杂志, 2015, 42(4): 425-428. |
| [5] |
吕容. 褶纹冠蚌JNK介导Nrf2-ARE通路调控抗氧化基因研究[D]. 南昌: 南昌大学, 2020.
|
| [6] |
MAES M, FIŠAR Z, MEDINA M, et al. New drug targets in depression: inflammatory, cell-mediated immune, oxidative and nitrosative stress, mitochondrial, antioxidant, and neuroprogressive pathways. And new drug candidates-Nrf2 activators and GSK-3 inhibitors[J]. Inflammopharmacology, 2012, 20(3): 127-150. DOI:10.1007/s10787-011-0111-7 |
| [7] |
WANG J, QIAO J, ZHANG Y, et al. Desvenlafaxine prevents white matter injury and improves the decreased phosphorylation of the rate-limiting enzyme of cholesterol synthesis in a chronic mouse model of depression[J]. J Neurochem, 2014, 131: 229-238. DOI:10.1111/jnc.12792 |
| [8] |
李承德. 黄芪多糖的抗抑郁作用及其机制的实验研究[D]. 济南: 山东中医药大学, 2018.
|
| [9] |
ZHANG J C, YAO W, HASHIMOTO K. Brain-derived neurotrophic factor (BDNF)-TrkB signaling in inflammation-related depression and potential therapeutic targets[J]. Curr Neuropharmacol, 2016, 14(7): 721-731. DOI:10.2174/1570159x14666160119094646 |
| [10] |
SHAW P, CHATTOPADHYAY A. Nrf2-ARE signaling in cellular protection: mechanism of action and the regulatory mechanisms[J]. J Cell Physiol, 2020, 235(4): 3119-3130. DOI:10.1002/jcp.29219 |
| [11] |
王磊, 任冠宇, 许成, 等. 核因子E2相关因子2在2型糖尿病膀胱功能障碍小鼠发病中的作用机制[J]. 海军军医大学学报, 2022, 43(10): 1155-1162. WANG L, REN G Y, XU C, et al. Role of nuclear factor erythroid derived 2-like 2 in pathogenesis of bladder dysfunction in type 2 diabetic mice[J]. Acad J Naval Med Univ, 2022, 43(10): 1155-1162. DOI:10.16781/j.CN31-2187/R.20220128 |
| [12] |
芦笛, 惠旭东, 赵琳, 等. 姜黄素激活Nrf2/ARE信号通路对产后抑郁症大鼠氧化应激损伤的影响[J]. 中国优生与遗传杂志, 2023, 31(3): 508-512. DOI:10.13404/j.cnki.cjbhh.2023.03.005 |
| [13] |
程洪燕, 武成. 81例抑郁症患者中医证候特征的临床调查[J]. 天津中医药大学学报, 2010, 29(3): 129-131. |
| [14] |
王珑, 王实涛. 抑郁症氧化应激发病机制及针刺治疗研究进展[J]. 针灸临床杂志, 2017, 33(11): 76-80. DOI:10.3969/j.issn.1005-0779.2017.11.021 |
| [15] |
方玲, 马婉. 氟西汀对脑卒中后抑郁大鼠学习记忆能力和氧化应激反应的影响[J]. 中国老年学杂志, 2018, 38(22): 5545-5547. DOI:10.3969/j.issn.1005-9202.2018.22.066 |
| [16] |
袁前发, 何珏, 徐志忠, 等. 重复经颅磁刺激联合低剂量氟西汀对CUMS抑郁小鼠的影响[J]. 中国应用生理学杂志, 2021, 37(6): 650-653. DOI:10.12047/j.cjap.6070.2021.035 |
 2023, Vol. 44
2023, Vol. 44


