2. 海军军医大学(第二军医大学)海军医学系卫生毒理学教研室, 上海 200433
2. Department of Health Toxicology, Faculty of Naval Medicine, Naval Medical University (Second Military Medical University), Shanghai, 200433, China
现代战争条件下,战创伤导致的不可控出血仍然是战创伤相关死亡的首要因素,出血死亡人数约占战场总死亡人数的50%~80%[1]。既往研究显示,90%的战创伤死亡发生在伤员被送到野战救治机构之前的战术环境中[2],伤后0.5 h内得到急救、1 h内得到救治可使伤员死亡率降低66.3%[3]。美军战术作战伤员救护(tactical combat casualty care,TCCC)指南从第1版开始就一直把止血作为战创伤救治的首要核心技术。
传统的绷带、止血纱布、止血粉等止血材料已难以满足现代战创伤急救的需求。膨胀止血材料主要指遇水后可迅速膨胀,能机械压迫创面达到止血目的的高分子材料。常见的膨胀止血材料包括聚乙烯醇(polyvinyl alcohol,PVA)、聚醚酯-氨基甲酸乙酯(polyether ester-ethyl carbamate,PEEC)、聚乙烯乙酸、聚氨酯等。目前,膨胀止血材料已广泛用于鼻腔填充止血,取得了良好的临床治疗效果,具有止血确实、头痛和头胀闷感轻的优点[4]。膨胀止血材料在战创伤急救中的应用仍处于早期探索阶段,本研究拟探索PVA和PEEC的体外物理性能及其在典型战创伤模型中的止血效能。
1 材料和方法 1.1 主要材料PVA(建德市康华医疗器械有限公司)、PEEC(荷兰Polyganics BV公司)、无菌纱布、生理盐水、EDTA抗凝兔血、游标卡尺(德力西集团有限公司)、平板测力计(SL-10N型,东莞市三量精密量仪有限公司)、普通教学尺子(得力办公用品有限公司)、精密电子天秤(BSA224S-CW,德国Sartorius公司)、注射器、秒表、电子显微镜(BX43F,日本Olympus公司)、载玻片、盖玻片、甲醛水溶液(上海国药集团化学试剂有限公司)、戊巴比妥钠(上海国药集团化学试剂有限公司)、夹子、塑料薄板、实验动物手术器械等。
1.2 实验动物及分组清洁级成年雄性SD大鼠购于上海市计划生育科学研究所实验动物经营部[动物生产许可证号:SCXK(沪)2018-0006],饲养于温度为22~24 ℃、湿度为55%~65%,每12 h昼夜光照循环的屏障环境动物房内,分笼饲养,自由饮食。适应性饲养1周后,将18只成年雄性SD大鼠(体重200~250 g)随机分为PVA组、PEEC组和无菌纱布组,每组6只。普通级雄性新西兰兔购于上海甲干生物科技有限公司[动物生产许可证号:SCXK(沪)2020-0006],饲养于温度21~25 ℃,湿度为45%~65%,每12 h昼夜光照循环的普通级动物房内,单笼饲养,自由饮食。适应性饲养1周后,将18只成年雄性兔(体重3~4 kg)随机分为PVA组、PEEC组和无菌纱布组,每组6只。实验操作严格按照海军军医大学(第二军医大学)第一附属医院实验动物管理条例和实验动物伦理要求执行。
1.3 体外物理性能评价制备生理盐水、抗凝兔血及生理盐水与抗凝兔血1∶1混合液;将相同体积的PVA和PEEC分别放置在以上3种模拟体液中,记录膨胀止血材料完全膨胀所需时间和膨胀后体积、重量变化情况;用平板测力计测量膨胀止血材料体积被压缩一半时所需压强。
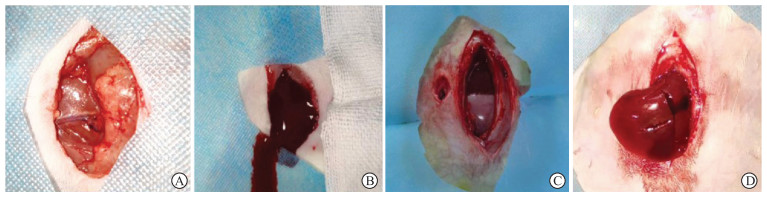
1.4 股动静脉损伤出血模型制备及观察指标麻醉大鼠后,于右后肢内侧划开皮肤找到股动脉股静脉并剪断,构建股动静脉损伤出血模型(图 1A、1B)[5];将相同体积的PVA、PEEC和无菌纱布置于出血部位后迅速缝合(保证手术伤口大小、位置一致)。术后1 h剪开伤口,取出止血材料,观察材料取出时的粘连程度和取出难易程度;观察评估取出止血材料后1 min的出血量;用吸引器吸取术野出血及血块,采用称重法计算术后1 h总出血量;取止血材料周边肌肉组织做病理切片行H-E染色,观察止血材料周边肌肉组织中炎症细胞浸润情况。重新置入新的止血材料,24 h后观察记录取出止血材料的粘连程度、取出难易程度、取出止血材料后1 min的出血量、24 h总出血量,并取止血材料周边肌肉组织做病理切片行H-E染色。
|
图 1 股动静脉损伤和肝损伤出血模型 Fig 1 Bleeding models of femoral arteriovenous injury and liver injury A: Exposure of rat femoral artery and vein; B: Femoral arteriovenous injury model of rats; C: Skin incision of rabbit liver injury model; D: Liver X-shaped incision of rabbit liver injury model. |
1.5 肝损伤出血模型制备及观察指标
将兔麻醉后打开腹腔,暴露左中叶肝脏,用手术刀片于肝脏做3 cm×3 cm“ X ”形创口后快速缝合,用穿孔器在兔腹壁做穿孔模拟贯通伤和盲管伤入口,构建肝损伤出血模型(图 1C、1D)[5-6];从腹壁穿孔填塞相同体积的PVA、PEEC和无菌纱布(保证手术伤口大小、位置一致)。术后1 h剪开伤口,取出止血材料,观察材料取出时的粘连程度和取出难易程度;用吸引器吸取术野出血及血块,计算术后1 h总出血量,观察评估取出止血材料后1 min的出血量。重新置入新的止血材料,24 h后观察记录取出止血材料的粘连程度、取出难易程度、取出止血材料后1 min的出血量、24 h总出血量。
1.6 指标判定标准及计算方法体积变化系数=止血材料膨胀后体积/止血材料膨胀前体积;体积变化速率=(止血材料膨胀后体积-止血材料膨胀前体积)/(止血材料膨胀前体积×止血材料完全膨胀所需时间);重量变化系数=止血材料膨胀后重量/止血材料膨胀前重量。粘连百分比=止血材料同周围组织紧密贴合在一起的面积/止血材料的表面积;粘连程度评分标准:无粘连计0分,粘连0~30%计1分,粘连31%~60%计2分,粘连>60%计3分。取出难易程度标准:0分,轻松取出,可一次性将止血材料同周围组织进行分离,且分离后不对周围组织造成二次伤害;1分,花费少量精力可取出,需轻柔仔细地分离止血材料和周围组织,分离后对周围组织产生轻微二次伤害;2分,花费大量精力可取出,需多次、逐步清理粘连在组织上的止血材料,且分离后对周围组织产生一定的二次伤害;3分,无法完全取出,止血材料粘连在周围组织上、部分被降解,无法通过钳夹将止血材料从组织上进行分离。总出血量=止血材料吸附的血+吸引器吸出的血+凝固的血块。
1.7 统计学处理采用SPSS 18.0软件进行统计学分析。符合正态分布且方差齐的计量资料以x±s表示,组间比较采用t检验。取出止血材料时粘连程度评分及取出难易程度评分为各组得分的平均数。检验水准(α)为0.05。
2 结果 2.1 膨胀止血材料的体外物理性能评价由图 2可见,PVA在生理盐水、抗凝兔血及生理盐水与抗凝兔血1∶1混合液中的体积变化系数均大于PEEC(P均<0.001),重量变化系数均小于PEEC(P均<0.01),体积变化速率均大于PEEC(P均<0.01);PVA在生理盐水和抗凝兔血中体积压缩一半时所需压强均低于PEEC(P均<0.05),PVA与PEEC在生理盐水与抗凝兔血1∶1混合液中体积压缩一半时所需压强的差异无统计学意义(P>0.05)。

|
图 2 2种膨胀止血材料的体外物理性能比较 Fig 2 Physical properties of 2 swelling hemostatic materials in vitro A-D: Normal saline; E-H: Anticoagulant rabbit blood; I-L: 1∶1 mixture of anticoagulant rabbit blood and normal saline. n=6, x±s. PVA: Polyvinyl alcohol; PEEC: Polyether ester-ethyl carbamate; PIHVR: Pressure intensity after half volume reduction. |
2.2 膨胀止血材料在股动静脉损伤出血模型中的止血效能和安全性评估
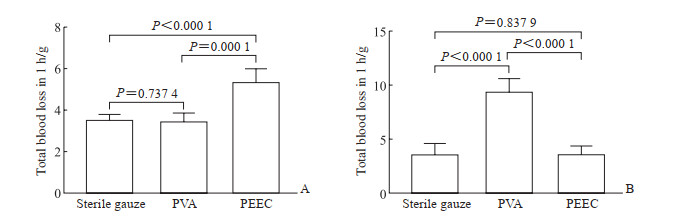
术后1 h,无菌纱布组、PVA组、PEEC组取出止血材料时粘连程度评分分别为2、0、1分,取出难易程度评分分别为1、0、1分。无菌纱布组和PVA组术后1 h总出血量均低于PEEC组(P均<0.01,图 3A);取出止血材料后1 min内,无菌纱布组2只大鼠可见少量出血(0.41 mL和0.98 mL),PVA组和PEEC组均未见活动性出血。
|
图 3 3种止血材料在动物创伤模型中的止血效果比较 Fig 3 Comparison of hemostatic effect of 3 hemostatic materials in animal trauma models A: Bleeding model of rat femoral arteriovenous injury; B: Bleeding model of rabbit liver injury. n=6, x±s. PVA: Polyvinyl alcohol; PEEC: Polyether ester-ethyl carbamate. |
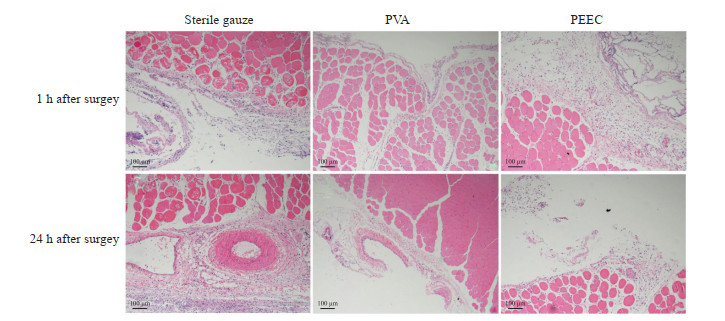
术后24 h,无菌纱布组取出止血材料时粘连程度评分为3分,取出难易程度评分为2分;PVA组取出止血材料时粘连程度及取出难易程度评分均为0分;PEEC组止血材料大部分被分解,取出难易程度评分为3分。无菌纱布组和PVA组术后24 h总出血量差异无统计学意义[(2.90±0.14)g vs(2.87±0.24)g,P>0.05],PEEC组仅见少量出血,无法计算出血量;取出止血材料后1 min各组均未见活动性出血。PVA组的肌肉组织周边炎症细胞浸润少于无菌纱布组和PEEC组(图 4)。
|
图 4 大鼠股动静脉损伤出血模型中止血材料周边肌肉组织H-E染色 Fig 4 H-E staining of muscle tissue around hemostatic materials in rat femoral arteriovenous injury model H-E: Hematoxylin-eosin staining; PVA: Polyvinyl alcohol; PEEC: Polyether ester-ethyl carbamate. |
2.3 膨胀止血材料在肝损伤出血模型中的止血效能和安全性评估
术后1 h,无菌纱布组、PVA组、PEEC组取出止血材料时粘连程度评分分别为2、0、1分,取出难易程度评分分别为1、0、1分。PVA组术后1 h总出血量大于无菌纱布组和PEEC组(P<0.01,图 3B);取出止血材料后1 min,无菌纱布组有3只新西兰兔见少量出血(0.05 mL、0.03 mL和0.10 mL),PVA组和PEEC组均未见活动性出血。
术后24 h,无菌纱布组取出止血材料时粘连程度评分为3分,取出难易程度评分为2分;PVA组取出止血材料时粘连程度及取出难易程度评分均为0分;PEEC大部分被分解,取出难易程度评分为3分。PVA组24 h总出血量高于无菌纱布组[(14.43±0.72)g vs(5.08±0.24)g,P<0.01],PEEC组仅见少量出血,无法计算出血量;取出止血材料1 min后,3个观察组均未见活动性出血。
3 讨论出血是导致战创伤死亡的最主要因素[7],在抵达医疗救治机构之前及时有效地控制急性大出血可以挽救90%伤员的生命[8]。分析2001-2011年美军在伊拉克军事行动中的伤员送达医疗救治机构前创伤相关死亡因素时发现,躯干出血占所有出血死亡的67.3%、交界性出血占19.2%、四肢出血占13.5%,其中胸腔出血占躯干出血的36%、腹腔出血占躯干出血的64%[9]。美军TCCC指南推荐在抵达医疗救治机构前应用止血带控制四肢出血和交界性出血[10];对于止血带无法控制的躯干出血和部分交界性出血,推荐应用止血敷料控制出血[11]。由于在抵达医疗救治机构之前无法开展确切手术止血,体腔内出血和交界性出血的战创伤急救仍面临着巨大的困难和挑战[9]。
止血敷料一直是战创伤救治领域研究的重点,理想的止血敷料应满足以下要求:(1)2 min内止住严重的动静脉出血;(2)无不良反应;(3)不引起疼痛和热损伤;(4)对医护人员无任何风险;(5)随取随用,不需或仅需简单培训;(6)轻便耐用;(7)灵活应对复杂伤口并且容易去除残留物;(8)在极端环境中作用稳定,使用方便;(9)弥补止血带在控制交界性出血中的缺陷;(10)保质期长;(11)价格低廉;(12)可生物降解[12]。尽管目前仍没有一种敷料能满足以上所有要求,但针对伤口与伤情特点设计的特定敷料与止血系统为战创伤急救止血提供了支持和选择。美军基于沸石类止血材料开发了能够显著提高大面积出血和严重创伤者生存率的止血敷料QuickClot[13],并在此基础上推出产热量较少、组织热损伤较轻的速效止血海绵(QuickClot-Advanced Clotting Sponge)产品[14]。基于高岭土类止血材料开发的战伤纱布(QuickClot Combat Gauze)具有携带方便、操作简单、容易储存的优点,已入选2008年美军“十大顶尖陆军装备”,列装美军及多个北约国家的军队[15]。应用壳聚糖类止血材料相继开发的HemCon Gauze、HemCon Chito Flex、Celox Granules、Celox Gauze、HemCon Chito Gauze等产品不但可以活化凝血因子和血小板,促进凝血过程,还可通过改变细胞膜通透性来干扰细菌和真菌代谢,起到抗菌、抑菌作用[16]。将壳聚糖和纤维素压制成圆片状结构并装入注射器中开发的适用于狭窄伤道止血的Xstat[17],对交界区止血的成功率高达90%,可持续止血40 h,但若放置时间超过40 h可造成横纹肌溶解[18]。应用海藻酸盐类止血材料开发的Modified Rapid Deployment Heostat和Rapid Deployment Heostat止血敷料,具有无毒、高吸水性、良好的生物相容性、高透氧性、可生物降解吸收等特性[16]。
我军在战救止血敷料开发领域也取得了丰硕成果,如壳聚糖止血海绵、聚丙烯酸树脂止血敷料、多功能液体止血敷料、多聚糖止血颗粒、沸石止血敷料等的止血效果显著[19]。其中,以沸石为主要成分的速效止血粉“血盾”已正式列装[20]。
尽管上述止血敷料取得了不错的战救止血效果,但仍难以满足现代战争条件下战伤急救的需求。压迫止血是外科手术中常见的止血方法,指压法也是战创伤急救止血的基本技能。膨胀止血材料通过吸收包括血液在内的体液使自身体积膨大,同时受限于创伤局部的有限空间,形成创伤局部高压环境,发挥压迫止血的作用。膨胀止血材料体外性能评价实验发现,PVA充分吸收体液后体积变化系数和速率优于PEEC,PEEC充分吸收体液后重量变化系数大于PVA,PEEC在生理盐水和抗凝兔血中体积被压缩一半时所需压强大于PVA。这表明PVA材料的膨胀性能优于PEEC,而PEEC的液体吸收能力和抗压能力更强。
在大鼠股动静脉损伤出血模型和兔肝损伤出血模型中,尽管PVA和PEEC 2种材料在术后1 h总出血量上存在一定差异,但均可有效控制股动静脉和肝脏出血。由于PEEC是一种可吸收材料,其在动物模型中的粘连程度评分和取出难易程度评分均大于PVA;尤其是在术后24 h,大部分PEEC已被吸收降解,无法取出。同时,由于PEEC被吸收降解,无法计算术后24 h总出血量,无法比较两组间术后24 h总出血量的差异。此外,PEEC和PVA在股动静脉损伤出血模型和肝损伤出血模型中止血效能相似;PVA基本不会与组织发生粘连,容易去除;PEEC与组织粘连严重,但可被吸收降解,无需取出。本研究中粘连程度评分和取出难易程度评分均采用半定量方法进行评估,在一定程度上受研究者主观判断影响,对研究结果的客观性可能造成一定影响。值得一提的是,PEEC需保存在4 ℃的低温环境中,这在某种程度上限制了其在战伤急救中的推广应用。此外,在股动静脉损伤出血模型中,PVA引起的肌肉组织周边炎症反应低于无菌纱布组和PEEC组,显示出了较好的组织耐受性。本研究构建的肝损伤出血模型创面较小,所需膨胀止血材料较少,未对腹腔脏器、循环和呼吸稳定性造成影响。在严重腹腔脏器损伤出血需大量膨胀止血材料压迫止血时,还需充分考虑膨胀止血材料体积膨大后对腹腔脏器造成的不良损伤和对呼吸循环稳定性的影响,这一点在今后的研究中进一步探讨明确。
本研究创造性地探索鼻用膨胀止血材料PVA和PEEC在战创伤急救中的应用价值,研究发现PVA和PEEC均可通过吸收包括血液在内的体液使自身体积膨大控制股动静脉损伤出血和肝损伤出血,为战伤救治新装备的研发提供了新的选择。
| [1] |
DEVLIN J J, KIRCHER S, KOZEN B G, et al. Comparison of ChitoFlex®, CELOXTM, and QuikClot® in control of hemorrhage[J]. J Emerg Med, 2011, 41(3): 237-245. DOI:10.1016/j.jemermed.2009.02.017 |
| [2] |
李丽娟, 刁天喜. 外军卫勤研究系列讲座(63) 美军战术战伤救治理念的发展与启示[J]. 人民军医, 2013, 56(3): 280-282. |
| [3] |
蒋建新, 李磊. 战伤创伤救治新进展与展望[J]. 解放军医学杂志, 2010, 35(7): 781-784. |
| [4] |
何平. 三种鼻腔填塞物在老年鼻出血患者中的应用[J]. 西部医学, 2011, 23(8): 1522-1523. DOI:10.3969/j.issn.1672-3511.2011.08.051 |
| [5] |
吴伟萍, 彭承宏, 韩宝三, 等. 羧甲基壳聚糖在大鼠创伤出血模型的止血效果的观察[J]. 外科理论与实践, 2010, 15(3): 240-244. DOI:10.16139/j.1007-9610.2010.03.039 |
| [6] |
林振华, 侯丽, 董传俊, 等. 胶原蛋白止血海绵在猪肝脏出血模型中止血效果研究[J]. 中国医疗设备, 2018, 33(11): 7-9. DOI:10.3969/j.issn.1674-1633.2018.11.002 |
| [7] |
STRAUSS R, MENCHETTI I, PERRIER L, et al. Evaluating the Tactical Combat Casualty Care principles in civilian and military settings: systematic review, knowledge gap analysis and recommendations for future research[J]. Trauma Surg Acute Care Open, 2021, 6(1): e000773. DOI:10.1136/tsaco-2021-000773 |
| [8] |
HOENCAMP R, VERMETTEN E, TAN E C, et al. Systematic review of the prevalence and characteristics of battle casualties from NATO coalition forces in Iraq and Afghanistan[J]. Injury, 2014, 45(7): 1028-1034. DOI:10.1016/j.injury.2014.02.012 |
| [9] |
EASTRIDGE B J, MABRY R L, SEGUIN P, et al. Death on the battlefield (2001-2011): implications for the future of combat casualty care[J]. J Trauma Acute Care Surg, 2012, 73(6 Suppl 5): S431-S437. DOI:10.1097/TA.0b013e3182755dcc |
| [10] |
SHACKELFORD S A, BUTLER F K, KRAGH J F, et al. Optimizing the use of limb tourniquets in tactical combat casualty care: TCCC guidelines change 14-02[J]. J Spec Oper Med, 2015, 15(1): 17-31. DOI:10.55460/tdtk-rin8 |
| [11] |
BRADLEY M, NEALEIGH M, OH J S, et al. Combat casualty care and lessons learned from the past 100 years of war[J]. Curr Probl Surg, 2017, 54(6): 315-351. DOI:10.1067/j.cpsurg.2017.02.004 |
| [12] |
胡传忠, 梁向党, 刘申. 战创伤院前急救止血敷料研究进展[J]. 医疗卫生装备, 2017, 38(12): 106-109, 145. DOI:10.7687/j.issn1003-8868.2017.12.106 |
| [13] |
BUTLER F K, HOLCOMB J B, GIEBNER S D, et al. Tactical combat casualty care 2007: evolving concepts and battlefield experience[J]. Mil Med, 2007, 172(Suppl_1): 1-19. DOI:10.7205/MILMED.172.Supplement_1.1 |
| [14] |
GEGEL B, BURGERT J, GASKO J, et al. The effects of QuikClot combat gauze and movement on hemorrhage control in a porcine model[J]. Mil Med, 2012, 177(12): 1543-1547. DOI:10.7205/MILMED-D-12-00165 |
| [15] |
张宜, 张梦, 刘学会, 等. 美军高岭土止血材料的研究进展[J]. 华南国防医学杂志, 2014, 28(12): 1275-1277. DOI:10.3969/j.issn.1009-2595.2014.12.042 |
| [16] |
陈艺, 贾柯瑶, 邓蓉, 等. 战创伤止血材料的研究进展[J]. 东南国防医药, 2022, 24(4): 397-402. DOI:10.3969/j.issn.1672-271x.2022.04.013 |
| [17] |
QIN H, YANG L, LIU D, et al. Efficacy of a temporary hemostatic device in a swine model of closed, lethal liver injury[J]. Mil Med, 2020, 185(5-6): e742-e747. DOI:10.1093/milmed/usz372 |
| [18] |
WARRINER Z, LAM L, MATSUSHIMA K, et al. Initial evaluation of the efficacy and safety of in-hospital expandable hemostatic minisponge use in penetrating trauma[J]. J Trauma Acute Care Surg, 2019, 86(3): 424-430. DOI:10.1097/TA.0000000000002091 |
| [19] |
史跃, 朱卉琪, 张琦, 等. 创伤急救止血贴的研制及应用研究[J]. 东南国防医药, 2019, 21(2): 219-221. DOI:10.3969/j.issn.1672-271X.2019.02.027 |
| [20] |
张平, 肖南, 张治纲, 等. 战创伤止血敷料的现状及展望[J]. 创伤外科杂志, 2009, 11(4): 378-380. DOI:10.3969/j.issn.1009-4237.2009.04.033 |
 2023, Vol. 44
2023, Vol. 44


