痛风是高尿酸血症引起的一种代谢性疾病。长期的高尿酸血症会导致尿酸盐结晶在组织、关节等处沉积,引发痛风等症状[1],当尿酸炎结晶在关节腔中析出并沉淀时会引发强烈的炎症反应,表现为红、肿、热、痛,即痛风性关节炎。目前临床上对于痛风患者的抗炎治疗主要是服用非甾体抗炎药吲哚美辛,但是吲哚美辛常伴随胃肠道反应、肝肾毒性等不良反应[2]。近年来中药在痛风的治疗中引起了广泛关注[3-5],中药治疗痛风疗效显著,不良反应轻微,适合长期服用[5-6]。然而中药成分复杂,各成分的作用效果和作用机制不明确,这是限制中药发展的主要原因[6-7]。明确中药物质基础,并进一步以现代药理学方法、化学生物学方法确定药效成分、阐明中药药理作用及其作用机制是促进中药全球化的必经之路。
虎杖为蓼科植物虎杖(Polygonum cuspidatum Sieb.et Zucc)的干燥根茎和根,具有利湿退黄、清热解毒、散瘀止痛、止咳化痰等功效[8-9]。现代中医常用虎杖复方制剂如虎杖痛风颗粒治疗急性痛风性关节炎,临床效果良好[10]。虎杖化学成分复杂,主要成分为二苯乙烯类和蒽醌类,其中白藜芦醇、虎杖苷和大黄素为其主要成分,且细胞实验表明此3种单体可降低人巨噬细胞中炎症因子的表达水平[11],但未在动物模型上证实其抗炎效果。本研究通过建立痛风性关节炎大鼠模型考察虎杖3种主要化合物单体的抗炎活性,初步明确虎杖抗痛风作用的效果和作用机制。
1 材料和方法 1.1 实验动物6~8周龄雄性SD大鼠72只[上海斯莱克实验动物有限责任公司,合格证号:20180006012428,动物生产许可证号:SCXK(沪)2018-0006],于相对湿度50%左右、室温下饲养,光照时间∶黑暗时间=1∶1,自由饮食水。
1.2 仪器与试剂自动脱水机(Asp300)、包埋机(HistoCore Arcadia)、切片机(RM2235)购自德国Leica公司,光学显微镜(BX 43)、电子图像采集和成像系统(Cellsence Entry)购自日本Olympus公司。
吲哚美辛(上海源叶生物科技有限公司,批号为Y01S7C20288,HPLC检测纯度≥99%);虎杖苷、白藜芦醇和大黄素均购于上海笛柏生物科技有限公司,批号分别为M10GS147767、R19T12S138196和T17O11F127680,纯度均≥95%;尿酸钠(monosodium urate,MSU)购于德国Sigma公司,批号为102177471;生理盐水(山东齐都药业有限公司,批号为11B19090702);TNF-α、IL-6、IL-10 ELISA检测试剂盒(美国ThermoFisher Scientific公司,货号分别为BMS607-3、88-50625-22、88-50629-22);戊巴比妥钠(上海玉研科学仪器有限公司,批号为201803152)。
1.3 实验分组72只大鼠适应性饲养1周后,按体重随机分为12组,分别为空白对照组、模型组、阳性对照组及虎杖3种化合物单体(虎杖苷、白藜芦醇、大黄素)低、中、高剂量组,每组6只。
1.4 痛风性关节炎大鼠模型的建立及给药空白对照组、模型组大鼠予生理盐水,阳性对照组予吲哚美辛10 mL/kg,虎杖苷低、中、高剂量组分别予虎杖苷125、250、500 mg/kg,白藜芦醇低、中、高剂量组分别予白藜芦醇125、250、500 mg/kg,大黄素低、中、高剂量组分别给予大黄素125、250、500 mg/kg,各组大鼠均连续灌胃给药14 d。所有药物均混悬于0.5%羧甲基纤维素钠(国药控股股份有限公司,批号为20180823)溶液中。给药第12天时,空白对照组大鼠注射0.2 mL生理盐水,其他11组大鼠于右后足趾关节分别注射MSU溶液(1.250 g MSU结晶加入50 mL生理盐水)0.2 mL以建立痛风性关节炎大鼠模型。建模后继续给药2 d,第15天时(建模后第3天)取血和右后足趾关节组织进行检测。
1.5 大鼠足趾肿胀的测量分别于注射MSU溶液后0、4、12、24、48 h时用测径器测定大鼠右后足趾的厚度。炎症肿胀程度用厚度差表示,即实时大鼠右后足趾的厚度减去注射后0 h大鼠右后足趾的厚度。
1.6 大鼠右后足趾关节组织病理学分析建模后第3天各组大鼠均腹腔注射2%的戊巴比妥钠(2 mL/kg)进行麻醉,从腹主动脉取血后处死并进行解剖。取大鼠右后足趾关节组织(含肌肉)进行组织病理学检查,以评价关节的充血、水肿和炎症等病变情况。趾关节组织在10%中性甲醛溶液中固定后进行脱钙、取材修块、常规脱水、石蜡包埋、切片(厚4~5 μm)、H-E染色,封片,光学显微镜下观察。用电子图像采集和成像系统进行图片摄像记录。根据大鼠趾关节的关节腔、肌肉和滑膜组织的病理变化,选择炎症反应及结晶体沉积为形态学观察半定量指标,以评价虎杖不同化合物单体对大鼠痛风性炎症的影响。
炎症反应的诊断标准:(1)轻微,仅少量炎症细胞浸润或炎性渗出;(2)轻度,多量或多灶性的炎症细胞浸润,伴有炎性渗出,水肿、淤血,有时可见组织细胞的坏死;(3)中度,大量炎症细胞浸润、组织坏死,血管反应如微静脉淤血、出血、水肿,大量炎性分泌物渗出等;(4)重度,关节、滑膜及肌肉的弥漫性炎症反应,组织坏死或化脓明显,肉芽组织形成;(5)严重,正常的组织结构已基本被破坏,镜下几乎全部是炎症细胞、坏死化脓的组织及肉芽组织。结晶体沉积的诊断标准:(1)轻微,偶见单个小结晶体沉积;(2)轻度,多个小结晶体形成灶性沉积;(3)中度,多灶性的结晶体沉积;(4)重度,大面积或弥漫性的结晶体沉积。
1.7 大鼠血清TNF-α、IL-6和IL-10水平的检测采用ELISA试剂盒分别检测各组大鼠血清中TNF-α、IL-6和IL-10的水平。所有操作均严格按照试剂盒说明书进行。
1.8 统计学处理采用SPSS 22.0软件进行统计学分析。符合正态分布且方差齐性的计量资料以x±s表示,组间比较采用单因素方差分析,多重比较采用最小显著性差异法;方差不齐时采用非参数检验,两两比较采用Nemenyi法。检验水准(α)为0.05。
2 结果 2.1 虎杖3种化合物单体对痛风性关节炎模型大鼠足趾肿胀的影响造模后4~48 h各组大鼠的关节肿胀程度均高于空白对照组(P均<0.05)。除空白对照组外,其余11组大鼠的关节肿胀程度均随着时间的推移先升高后降低,造模后48 h时仍高于造模0 h(P均<0.01)。造模后4 h虎杖苷低剂量组、虎杖苷中剂量组、白藜芦醇高剂量组、大黄素高剂量组大鼠的关节肿胀程度均低于模型组(P均<0.05),造模后12 h阳性对照组及大黄素3个剂量组均低于模型组(P均<0.05),造模后48 h阳性对照组、白藜芦醇低剂量组、白藜芦醇高剂量组、虎杖苷3个剂量组和大黄素3个剂量组均低于模型组(P均<0.05)。见表 1。
|
|
表 1 建模后痛风性关节炎大鼠右后足趾的肿胀程度 Tab 1 Swelling degree of right hind toe of rats with gouty arthritis after modeling |
2.2 虎杖3种化合物单体对痛风性关节炎模型大鼠足趾关节组织病理学的影响
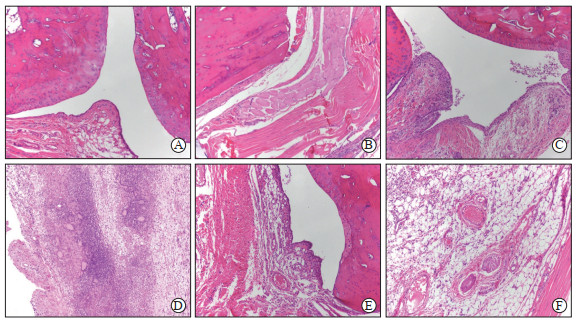
与空白对照组(图 1A、1B)比较,模型组大鼠(图 1C、1D)的关节出现中度到严重的炎症反应,包括关节腔的炎性分泌物渗出、滑膜和肌肉的炎症反应(如细胞浸润、坏死或化脓)、血管反应(如微静脉淤血、出血、水肿、肉芽组织形成)等,关节内还可见嗜碱性结晶体沉积,表明痛风性关节炎大鼠模型建模成功。与模型组比较,给予吲哚美辛干预的阳性对照组大鼠(图 1E、1F)的滑膜和肌肉炎症反应减轻,关节腔分泌物减少,结晶体沉积减少。给予虎杖苷、白藜芦醇和大黄素干预后,大鼠关节部位仍可见以炎症反应及结晶体沉积为主的病理变化,但均较模型组减轻(图 2)。
|
图 1 痛风性关节炎大鼠模型右后足趾关节组织的病理学变化 Fig 1 Pathological changes of right posterior toe joint tissue in gouty arthritis rats A: Blank control group, normal joint cavity and synovial tissue; B: Blank control group, normal joint adjacent muscle tissue; C: Model group, increased inflammatory secretions in the joint cavity; D: Model group, severe inflammation and crystals in the joint; E: Positive control group, mild synovial inflammation; F: Positive control group, mild inflammation in the muscle tissue. Hematoxylin-eosin staining (100×). |

|
图 2 虎杖3种化合物单体对痛风性关节炎模型大鼠右后足趾关节组织病理学变化的影响 Fig 2 Effects of 3 different monomers of Polygonum cuspidatum on pathological changes of right posterior toe joint tissues of gouty arthritis rats A: A small amount of inflammatory secretion (arrow) in the joint cavity in the high-dose (500 mg/kg) polydatin group; B: Mild synovial and muscular inflammation in the high-dose polydatin group; C: Mild crystals (arrow) in the high-dose polydatin group; D: Normal joint cavity in the medium-dose (250 mg/kg) resveratrol group; E: Mild synovial and muscular inflammation in the medium-dose resveratrol group; F: Mild crystals (arrow) in the high-dose (500 mg/kg) resveratrol group; G: Normal joint cavity with a small amount of serous joint fluid (arrow) in the medium-dose (250 mg/kg) emodin group; H: Mild synovial and muscular inflammation in the medium-dose emodin group; I: Minimal crystals (arrow) in the high-dose (500 mg/kg) emodin group. Hematoxylin-eosin staining (100×). |
各组大鼠炎症反应及结晶体沉积的发生情况及严重程度见图 3。与模型组相比,白藜芦醇低、中剂量组发生炎症反应的大鼠数量各减少1只,白藜芦醇高剂量组、虎杖苷3个剂量组及大黄素3个剂量组发生炎症反应的大鼠数量均未减少。与模型组比较,虎杖苷低剂量组、虎杖苷高剂量组、白藜芦醇3个剂量组及大黄素3个剂量组大鼠炎症反应的病变程度均减轻,但减轻程度未见剂量相关性(图 3A)。白藜芦醇3个剂量组及大黄素3个剂量组发生结晶体沉积的大鼠数量均明显减少,其中白藜芦醇中剂量组及大黄素中剂量组均有1只发生结晶体沉积,而虎杖苷3个剂量组中仅低剂量组发生结晶体沉积的大鼠数量较模型组减少1只;与模型组比较,虎杖苷、白藜芦醇及大黄素3个剂量组大鼠的结晶体沉积严重程度均有不同程度的减轻(图 3B)。

|
图 3 虎杖3种化合物单体对痛风性关节炎模型大鼠右后足趾关节病理变化严重程度的影响 Fig 3 Effects of 3 compound monomers of Polygonum cuspidatum on pathological severity of right posterior toe joint in gouty arthritis rats A: Severity grade of inflammation; B: Severity grade of crystals deposited. The low-, medium-and high-dose groups of the 3 compound monomers were given corresponding drugs 125, 250 and 500 mg/kg, respectively. N=6. |
2.3 虎杖3种化合物单体对痛风性关节炎模型大鼠血清细胞因子水平的影响
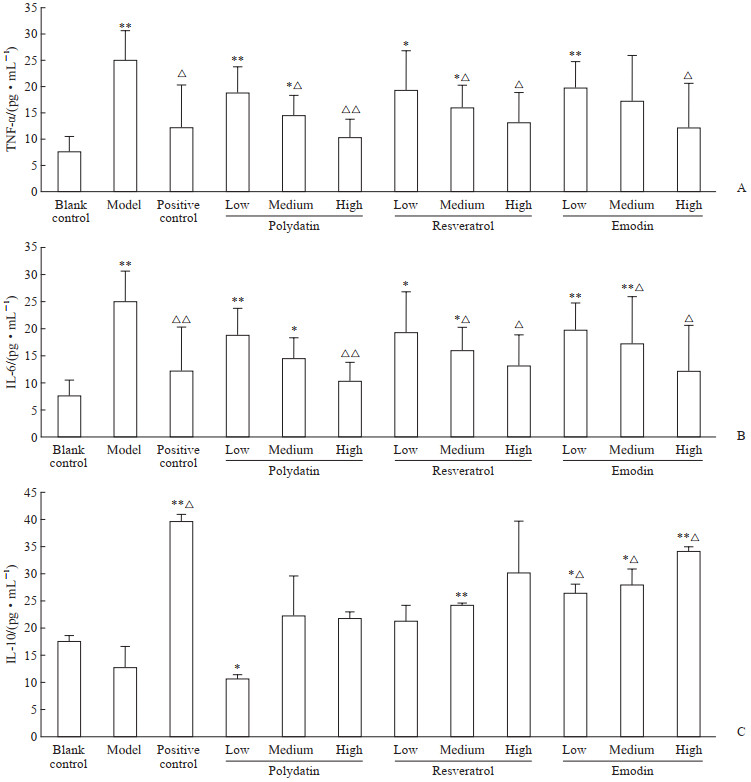
阳性对照组、虎杖苷中剂量组、虎杖苷高剂量组、白藜芦醇中剂量组、白藜芦醇高剂量组、大黄素高剂量组大鼠血清中TNF-α水平均较模型组降低(P均<0.05,图 4A)。与模型组比较,阳性对照组、虎杖苷高剂量组、白藜芦醇中剂量组、白藜芦醇高剂量组、大黄素中剂量组、大黄素高剂量组大鼠血清中IL-6水平均降低(P均<0.05,图 4B)。与空白对照组比较,虎杖苷低剂量组大鼠血清中IL-10的水平降低(P<0.05),阳性对照组、白藜芦醇中剂量组及大黄素3个剂量组大鼠血清中IL-10的水平均升高(P均<0.05);与模型组比较,阳性对照组及大黄素3个剂量组大鼠血清中IL-10的水平均升高(P均<0.05)。见图 4C。结果表明,虎杖中的虎杖苷、白藜芦醇和大黄素均对痛风性关节炎模型大鼠具有抗炎作用,但3种化合物单体对不同炎症因子的影响不同。
|
图 4 虎杖3种化合物单体对痛风性关节炎模型大鼠血清中TNF-α(A)、IL-6(B)、IL-10(C)水平的影响 Fig 4 Effects of 3 compound monomers of Polygonum cuspidatum on serum TNF-α (A), IL-6 (B) and IL-10 (C) levels of gouty arthritis rats The low-, medium-and high-dose groups of the 3 compound onomers were given corresponding drugs 125, 250 and 500 mg/kg, respectively. *P < 0.05, **P < 0.01 vs blank control group; △P < 0.05, △△P < 0.01 vs model group. n=6, x±s; TNF-α: Tumor necrosis factor-α; IL: Interleukin. |
3 讨论
随着全球经济生活水平的提高,人们的饮食结构逐渐发生改变,高蛋白和高嘌呤食物的大量摄取使痛风的发病率在各个国家都呈逐年上升趋势[12-13]。我国幅员辽阔,边境线绵长,湿热地区、高原高寒地区的人们极易患痛风,研究治疗痛风的药物和深入探讨痛风的发病机制具有极为重要的社会意义。
痛风的治疗方法包含2个方面,其一是控制体内血尿酸水平,其二是抗炎[14]。有研究者发现,虎杖苷处理后痛风模型大鼠血清肌酐、尿素氮、IL-1β、IL-6及肾组织丙二醛等水平均降低,而肾组织超氧化物歧化酶和谷胱甘肽水平升高,说明虎杖苷具有抗炎作用和抗氧化应激作用[15]。已有多项研究报道显示,虎杖总提取物或其单个生物活性成分有降低血尿酸水平的作用。侯建平等[16]发现虎杖提取物可降低高尿酸血症模型动物血尿酸水平和抑制黄嘌呤氧化酶活性,改善痛风性关节炎的病理变化。李相成[17]、Kong等[18]通过体外实验发现,虎杖提取物对黄嘌呤氧化酶具有抑制作用。Shi等[19]发现,白藜芦醇及其结构类似物通过调节高尿酸血症小鼠的肾脏有机离子受体发挥促尿酸排泄和肾脏保护作用。Chen等[20]发现,白藜芦醇可以改善MSU诱导的痛风性关节炎小鼠的足趾肿胀情况,降低酵母多糖和奥替拉西钾诱导的高尿酸小鼠的血尿酸水平。
也有研究显示虎杖总提取物具有抗炎作用。Chainy等[21]发现,白藜芦醇通过抑制TNF进而抑制NF-κB通路的激活,达到抗炎作用。Ghanim等[22]在正常大鼠中发现虎杖提取物能够抑制NF-κB的结合等途径,降低血浆中TNF-α、IL-6、IL-1β等的浓度,进而抑制氧化和炎症反应。Zhang等[23]和黎颖等[24]分别发现,虎杖苷可以抑制四氯化碳诱导肝损伤小鼠模型及体外缺血再灌注损伤大鼠模型的肾小管上皮细胞中NF-κB的表达以及炎症因子IL-1β和TNF-α的水平。Kumar等[25]发现,大黄素抑制人血管内皮细胞中TNF诱导的NF-κB激活,进而有效治疗各种炎症性疾病。Li等[26]在RAW264.7巨噬细胞中也发现,大黄素能够抑制NF-κB的活性及TNF-α的表达。
本研究发现,高剂量的虎杖苷、白藜芦醇、大黄素均能够降低痛风性关节炎大鼠血清中TNF-α、IL-6水平,但仅大黄素能升高IL-10的水平。这表明虎杖苷、白藜芦醇和大黄素具有抗炎作用。病理结果显示,给予虎杖苷、白藜芦醇及大黄素后,虎杖苷低剂量组、虎杖苷高剂量组、白藜芦醇3个剂量组及大黄素3个剂量组大鼠炎症反应的病变程度均较模型组减轻,其中白藜芦醇低、中剂量组发生关节炎症反应的大鼠数量也各减少1只。与模型组相比,虎杖苷、白藜芦醇及大黄素3个剂量组大鼠的结晶体沉积严重程度均有不同程度的减轻,其中虎杖苷低剂量组、白藜芦醇3个剂量组及大黄素3个剂量组发生结晶体沉积的大鼠数量均减少。
研究表明高尿酸血症引起的痛风性关节炎与尿酸钠微晶体在关节周围组织沉积有关[27-28]。本研究显示虎杖3种化合物单体,尤其是白藜芦醇及大黄素可降低痛风性关节炎模型大鼠关节内结晶体的沉积,可能降低关节炎症反应的发生,对关节炎有一定程度的改善作用。
| [1] |
尹相林, 姚嵩坡, 李兴洲, 沈萍, 展秀君, 张淑红, 等. 痛风和高尿酸血症发病的危险因素[J]. 中国老年学杂志, 2020, 40: 2041-2044. |
| [2] |
中华医学会内分泌学分会. 中国高尿酸血症与痛风诊疗指南(2019)[J]. 中华内分泌代谢杂志, 2020, 36: 1-13. DOI:10.3760/cma.j.issn.1000-6699.2020.01.001 |
| [3] |
郑启艳, 孙鲁英, 赵庆, 张笑笑, 王娅辉, 金化男, 等. 补肾泄浊法对比别嘌醇治疗痛风性肾病疗效及安全性的Meta分析[J]. 中国全科医学, 2019, 22: 947-953. DOI:10.12114/j.issn.1007-9572.2018.00.259 |
| [4] |
黄继勇, 谢冠群, 张艳, 陈凯, 李霄鹏, 范永升. 范永升运用"痛随利减"理论治疗急性痛风经验[J]. 中华中医药杂志, 2020, 35: 235-237. |
| [5] |
孙宇洁, 付书璠, 李慧, 郭锦晨. 近30年中医药治疗痛风临床用药规律数据挖掘研究[J]. 中药药理与临床, 2020, 36: 208-213. |
| [6] |
史亚夫, 姚雪莲, 黄小方, 关志宇, 朱继孝. 痛风的分子机制与中药治疗研究进展[J]. 中药新药与临床药理, 2018, 29: 673-678. |
| [7] |
魏蔼玲, 袁明昊, 刘娟汝, 刘红梅, 叶强, 刘雨诗, 等. 中药在痛风疾病中的应用及其作用机制研究进展[J]. 中国实验方剂学杂志, 2020, 26: 225-234. |
| [8] |
谢招虎, 解静, 李兆福, 段姮妃, 段荔, 王特. 虎杖治疗痛风的作用机制及临床应用研究进展[J]. 辽宁中医杂志, 2019, 46: 1111-1113. |
| [9] |
李姣姣, 于猛, 高源, 张涛, 贾红梅, 张宏武, 等. 基于谱效关系的中药虎杖抗炎活性成分探讨[J]. 中国实验方剂学杂志, 2019, 25: 208-213. |
| [10] |
张明, 朱周, 王一飞. 虎杖痛风颗粒治疗急性痛风性关节炎临床观察[J]. 上海中医药杂志, 2008, 42: 16-18. |
| [11] |
左卫平, 蔡昱, 刘文英, 汪冬庚. 虎杖化学成分研究[J]. 中国药学杂志, 2020, 55: 189-193. |
| [12] |
MATTIUZZI C, LIPPI G. Recent updates on worldwide gout epidemiology[J]. Clin Rheumatol, 2020, 39: 1061-1063. DOI:10.1007/s10067-019-04868-9 |
| [13] |
PATHMANATHAN K, ROBINSON P C, HILL C L, KEEN H I. The prevalence of gout and hyperuricaemia in Australia: an updated systematic review[J]. Semin Arthritis Rheum, 2021, 51: 121-128. DOI:10.1016/j.semarthrit.2020.12.001 |
| [14] |
王昱, 邓雪蓉, 张卓莉. 2020年美国风湿病学会痛风治疗指南[J]. 中华风湿病学杂志, 2020, 24: 862-864. DOI:10.3760/cma.j.c141217-20200612-00251 |
| [15] |
VAN DURME C M, WECHALEKAR M D, BUCHBINDER R, SCHLESINGER N, VAN DER HEIJDE D, LANDEWÉ R B. Non-steroidal anti-inflammatory drugs for acute gout[J/OL]. Cochrane Database Syst Rev, 2014(9): CD010120. DOI: 10.1002/14651858.CD010120.pub2.
|
| [16] |
侯建平, 王亚军, 严亚峰, 王斌, 孟建国. 虎杖提取物抗动物高尿酸血症的实验研究[J]. 西部中医药, 2012, 25: 21-24. |
| [17] |
李相成. 基于黄嘌呤氧化酶靶点虎杖抗高尿酸血症物质基础研究[D]. 青岛: 青岛大学, 2015.
|
| [18] |
KONG L D, CAI Y, HUANG W W, CHENG C H, TAN R X. Inhibition of xanthine oxidase by some Chinese medicinal plants used to treat gout[J]. J Ethnopharmacol, 2000, 73: 199-207. DOI:10.1016/S0378-8741(00)00305-6 |
| [19] |
SHI Y W, WANG C P, WANG X, ZHANG Y L, LIU L, WANG R W, et al. Uricosuric and nephroprotective properties of Ramulus Mori ethanol extract in hyperuricemic mice[J]. J Ethnopharmacol, 2012, 143: 896-904. DOI:10.1016/j.jep.2012.08.023 |
| [20] |
CHEN H, ZHENG S, WANG Y, ZHU H, LIU Q, XUE Y, et al. The effect of resveratrol on the recurrent attacks of gouty arthritis[J]. Clin Rheumatol, 2016, 35: 1189-1195. DOI:10.1007/s10067-014-2836-3 |
| [21] |
CHAINY G B, MANNA S K, CHATURVEDI M M, AGGARWAL B B. Anethole blocks both early and late cellular responses transduced by tumor necrosis factor: effect on NF-kappaB, AP-1, JNK, MAPKK and apoptosis[J]. Oncogene, 2000, 19: 2943-2950. DOI:10.1038/sj.onc.1203614 |
| [22] |
GHANIM H, SIA C L, ABUAYSHEH S, KORZENIEWSKI K, PATNAIK P, MARUMGANTI A, et al. An antiinflammatory and reactive oxygen species suppressive effects of an extract of Polygonum cuspidatum containing resveratrol [J/OL]. J Clin Endocrinol Metab, 2010, 95: E1-E8. DOI: 10.1210/jc.2010-0482.
|
| [23] |
ZHANG H, YU C H, JIANG Y P, PENG C, HE K, TANG J Y, et al. Protective effects of polydatin from Polygonum cuspidatum against carbon tetrachloride-induced liver injury in mice[J/OL]. PLoS One, 2012, 7: e46574. DOI: 10.1371/journal.pone.0046574.
|
| [24] |
黎颖, 熊维建, 杨敬, 钟锦, 郑劲, 张玲, 等. 虎杖苷对NRK-52E细胞缺血再灌注损伤时TLR-4表达的抑制作用[J]. 中国中药杂志, 2014, 39: 3157-3161. |
| [25] |
KUMAR A, DHAWAN S, AGGARWAL B B. Emodin (3-methyl-1, 6, 8-trihydroxyanthraquinone) inhibits TNF-induced NF-κB activation, IκB degradation, and expression of cell surface adhesion proteins in human vascular endothelial cells[J]. Oncogene, 1998, 17: 913-918. DOI:10.1038/sj.onc.1201998 |
| [26] |
LI H L, CHEN H L, LI H, ZHANG K L, HEN X Y, WANG X W, et al. Regulatory effects of emodin on NF-κBactivation and inflammatory cytokine expression in RAW 264.7 macrophages[J]. Int J Mol Med, 2005, 16: 41-47. |
| [27] |
陈新华, 王洪峰, 王维正, 尚蕊, 王朝辉. 痛风性关节炎中医外治法的研究进展[J]. 中国老年学杂志, 2019, 39: 730-733. DOI:10.3969/j.issn.1005-9202.2019.03.070 |
| [28] |
赵正奇, 叶超, 王泽然, 叶新苗. 叶新苗针药结合治疗痛风性关节炎经验[J]. 中华中医药杂志, 2019, 34: 1537-1539. |
 2022, Vol. 43
2022, Vol. 43


