2. 海军军医大学(第二军医大学)第二附属医院健康管理科,上海 200003
2. Department of Health Management, The Second Affiliated Hospital of Naval Medical University (Second Military Medical University), Shanghai 200003, China
类风湿关节炎(rheumatoid arthritis,RA)是一种慢性自身免疫性疾病,我国RA发病率约为0.3%,其病理特点是关节血管翳的形成、滑膜炎及邻近骨侵蚀,并最终导致关节畸形和功能丧失[1-2]。目前,RA的发病机制尚未完全阐明,临床上用于治疗RA的药物主要包括改善病情抗风湿药(disease modifying antirheumatic drug,DMARD)、糖皮质激素、生物靶向药物、非甾体抗炎药等。然而,DMARD、糖皮质激素等药物具有骨髓抑制、诱发或加重感染、增加肿瘤风险等严重不良反应且部分患者对药物表现出低反应性,致使患者依从性较差、治疗效果不佳[3];生物靶向药物不但费用昂贵,而且存在用药禁忌或风险,如慢性肝炎、结核、肿瘤等患者使用生物制剂会导致原有病情加重甚至复发;非甾体抗炎药虽然止痛效果好,但不能从根本上改善病情。中药如雷公藤、白芍总苷等在治疗风湿免疫性疾病中已经得到广泛的应用且疗效显著,在RA的治疗中也发挥了关键的作用[4-5],值得进一步研究。
现代中医理论认为RA属于“痹症”,既与自身正气不足有关也与“风”“寒”“湿”“瘀”等邪气侵袭有关,中药方剂可通过抑制患者疾病进展以防止关节畸形[6-7]。甘草附子汤出自《伤寒论》,由甘草、附子、白术、桂枝组成。甘草具有抗炎及调节免疫作用,早在《神农本草经》中就有记载它具有缓急止痛、清热解毒功能[8]。附子是毛茛科植物乌头的子根,具有强心、抗炎、阵痛、增强免疫功能等药理作用[9]。白术作为常用中药,可调节免疫系统,同时具有抗炎、保肝、调节胃肠功能的作用[10]。桂枝可止烦出汗,疏邪散风,其汤类方可治疗RA引起的“痹症”,滋阴和阳, 调和营卫[11]。现代药理学对甘草附子汤中单药的作用研究已取得一定的进展[12-13],但每味中药里均有多种有效成分且其对应的靶点复杂,甘草附子汤用于治疗RA的作用靶点及其作用机制尚不明确。
网络药理学可构建中药-活性成分-疾病靶点网络,进而预测药物治疗疾病的作用机制[14]。本文基于网络药理学联合分子对接的分析方法,从分子水平分析甘草附子汤的活性成分、靶点以及与RA之间的相互作用,初步揭示甘草附子汤治疗RA的作用机制。
1 材料和方法 1.1 药材成分靶点的筛选利用中药系统药理学数据库与分析平台(Traditional Chinese Medicine Systems Pharmacology Database and Analysis Platform,TCMSP;http://tcmspw.com/tcmsp.php),根据口服中药在人体内的吸收、分布、代谢和消除(absorption,distribution,metabolism,and elimination,ADME)参数,以口服生物利用度(oral bioavailability,OB)≥30%和类药性(drug like,DL)≥0.18为筛选条件,分别筛选甘草附子汤中4味药材(甘草、附子、桂枝、白术)的活性成分及其对应靶点,并应用UniProt数据库(https://www.uniprot.org/)将所得靶点转换成对应基因名。
1.2 RA相关靶点基因的筛选利用基因表达汇编(Gene Expression Omnibus,GEO)数据库收集RA滑膜相关的基因表达谱,获得的芯片编号为GSE55235,首先对数据进行主成分分析及聚类分析,随后筛选基因芯片数据并归一化处理,通过R语言GPL96平台将探针转换成基因名称。筛选差异表达基因,以校正P<0.05且|log2FC|≥1[FC为差异倍数(fold change)]作为差异表达基因的筛选标准。使用在线工具jvenn(http://jvenn.toulouse.inra.fr/app/index.html)对甘草附子汤和RA的靶点取交集,得到甘草附子汤有效成分治疗RA的潜在靶基因[15]。
1.3 甘草附子汤的中药-活性成分-疾病靶点网络构建将甘草附子汤治疗RA的靶点及其对应的有效活性成分和中药成分导入生物信息网络可视化分析软件Cytoscape 3.7.1,制作甘草附子汤的中药-活性成分-疾病靶点网络图,利用软件中的Network Analyzer插件分析网络节点度值(degree),并筛选出重要的中药活性成分。
1.4 蛋白质-蛋白质相互作用(protein-protein interaction,PPI)网络构建将甘草附子汤治疗RA的潜在靶点输入STRING数据库中,选择“multiple proteins”“Homo sapiens”进行检索。最低相互作用得分设定为0.4,并隐藏与其他蛋白无相互作用的节点,得到PPI网络后导入Cytoscape 3.7.1软件,根据节点度值筛选出重要的蛋白靶点。
1.5 基因本体(GeneOntology,GO)和京都基因与基因组百科全书(Kyoto Encyclopedia of Genes and Genomes,KEGG)通路富集分析使用Metascape数据(http://metascape.org/)库对1.2节中筛选得到的交集基因进行GO和KEGG信号通路富集分析,限定物种为“人”,以P<0.01为筛选条件,对富集结果按照P值由小到大排序,使用生物信息学在线工具(http://www.bioinformatics.com.cn/)绘制富集柱状图及气泡图。
1.6 分子对接选取PPI网络中度值排名前4位的靶点作为受体。从PubChem数据库(https://pubchem.ncbi.nlm.nih.gov/)下载对应活性成分2D结构的文件,利用ChemBio3D软件进行优化,将其转化为3D结构。在RCSB PDB数据库(https://www.rcsb.org/)下载核心靶点蛋白3D结构pdb格式文件,运用PyMOL软件移除靶蛋白中的配体和非蛋白分子(如水分子),再保存为pdb后缀的文件。将准备好的配体和受体分子导入AutoDockTools-1.5.6软件进行分子对接,随后利用PyMOL软件对分子对接结果进行可视化。
2 结果 2.1 甘草附子汤活性成分及潜在靶点通过TCMSP数据库筛选,以OB≥30%和DL≥0.18为条件,得到甘草活性成分92个、附子活性成分21个、白术活性成分7个、桂枝活性成分7个,去重后得到有效活性成分125个。根据上述活性成分,通过TCMSP平台获得相应的作用靶点,其中白术作用靶点23个,桂枝作用靶点51个,附子作用靶点30个,甘草作用靶点227个,去重后得到236个作用靶点。
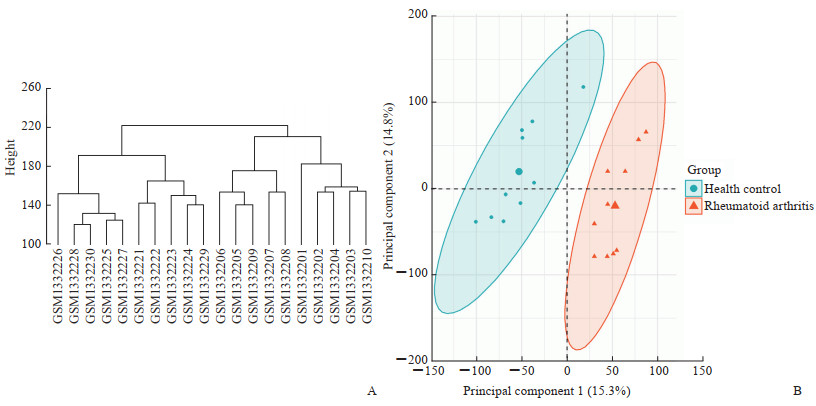
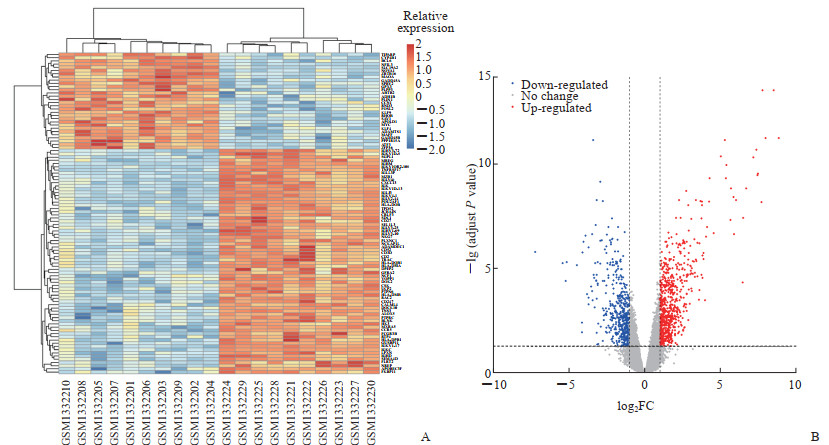
2.2 甘草附子汤治疗RA的潜在作用靶点预测GSE55235芯片内包含10名健康人和10例RA患者的关节滑膜组织的基因表达情况,聚类分析和主成分分析可将健康对照组和RA组间样本区分开且组内差异较小(图 1),以校正P<0.05为筛选条件、|log2FC|≥1为筛选标准,获得RA组与健康对照组的差异表达基因1 141个,其中上调基因678个、下调基因463个,通过热图及火山图呈现(图 2)。通过在线工具jvenn将药物靶点(236个)与差异表达基因(1 141个)取交集,得到甘草附子汤治疗RA的潜在靶点44个。
|
图 1 类风湿关节炎患者与健康对照者基因表达的聚类分析(A)和主成分分析(B)结果 Fig 1 Results of cluster analysis (A) and principal component analysis (B) of gene expression in patients with rheumatoid arthritis and healthy controls |
|
图 2 类风湿关节炎患者与健康对照者差异表达基因的热图(A)及火山图(B) Fig 2 Heat map (A) and volcano plot (B) of differentially expressed genes in patients with rheumatoid arthritis and healthy controls FC: Fold change. |
2.3 中药-活性成分-疾病靶点网络
中药-活性成分-疾病靶点网络包含143个节点,包括药材节点4个、甘草附子汤治疗RA的潜在靶点44个、潜在靶点所对应的活性化合物节点95个,组成了478条相互作用关系的网络(图 3)。经网络拓扑结构分析,度值排名前5位的活性成分是槲皮素(quercetin,MOL000098)、山萘酚(kaempferol,MOL000422)、7-甲氧基-2-甲基异黄酮(7-methoxy-2-methyl isoflavone,MOL003896)、柚皮素(naringenin,MOL004328)、芒柄花素(formononetin,MOL000392),度值分别为31、13、10、9、9。这5种化学成分可能是甘草附子汤发挥治疗作用的关键活性成分。

|
图 3 甘草附子汤治疗类风湿关节炎的中药-活性成分-疾病靶点分析 Fig 3 Network of traditional Chinese medicine-active ingredient-disease target of Gancao Fuzi decoction treating rheumatoid arthritis he blue arrows present Chinese medicinal materials. Active drug ingredients are labeled in orange. Disease targets are labeled in yellow. The lines link the Chinese medicinal materials and the active ingredients, the active ingredients and the disease targets, and they show the relevance separately. |
2.4 PPI网络的构建及筛选关键基因
由图 4可见,PPI网络有39个节点,平均节点度值为11.3。PPI网络分析结果显示基质金属蛋白酶(matrix metalloproteinase,MMP)9、C-X-C基序趋化因子配体8(C-X-C motif chemokine 8,CXCL8)、过氧化物酶体增殖物激活受体γ(peroxisome proliferative activated receptor γ,PPARγ)、表皮生长因子受体(epidermal growth factor receptor,EGFR)可能为甘草附子汤治疗RA的关键靶点。

|
图 4 甘草附子汤治疗类风湿关节炎靶点的蛋白质-蛋白质相互作用网络图 Fig 4 Protein-protein interaction network of Gancao Fuzi decoction treating rheumatoid arthritis Nodes represent proteins. The lines between nodes represent the interactions between proteins. The darker the color of the node, the greater the interaction degree between the proteins. |
2.5 GO富集分析结果
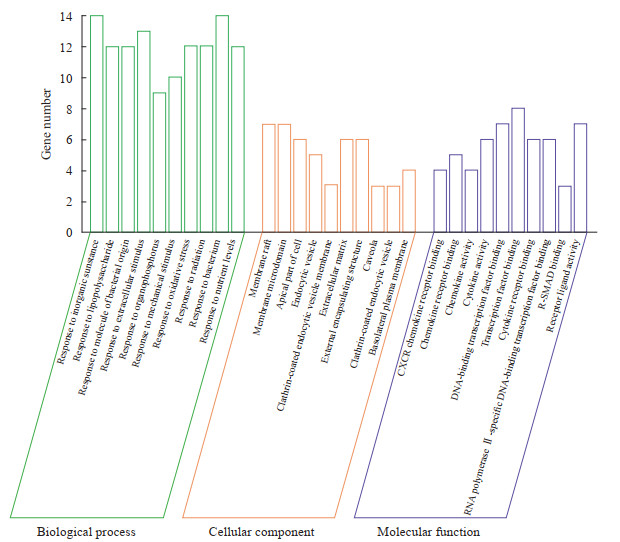
对44个交集关键基因进行GO功能分析,结果显示在甘草附子汤治疗RA的作用机制中主要包括对无机物、脂多糖、细菌来源分子、细胞外刺激、有机磷、机械刺激、氧化应激、放射线、细菌、营养水平的反应等生物过程,细胞组分主要涉及膜筏、膜微区、顶端细胞、内吞膜泡、网格蛋白包被的内吞囊泡膜、细胞外基质、外部封装结构、(胞膜)小窝、网格蛋白包被的内吞囊泡、基底外侧质膜,分子功能主要涉及CXCR趋化因子受体结合、趋化因子受体结合、趋化因子活性、细胞因子活性、DNA结合转录因子结合、转录因子结合、细胞因子受体结合、RNA聚合酶Ⅱ特异性DNA结合转录因子结合、受体相关的SMAD(receptor-associated SMAD,R-SMAD)结合、受体配体活性等,见图 5。
|
图 5 甘草附子汤治疗类风湿关节炎靶点基因的基因本体富集分析 Fig 5 Gene Ontology enrichment analysis of target genes in treatment of rheumatoid arthritis by Gancao Fuzi decoction R-SMAD: Receptor-associated SMAD. |
2.6 KEGG通路富集分析
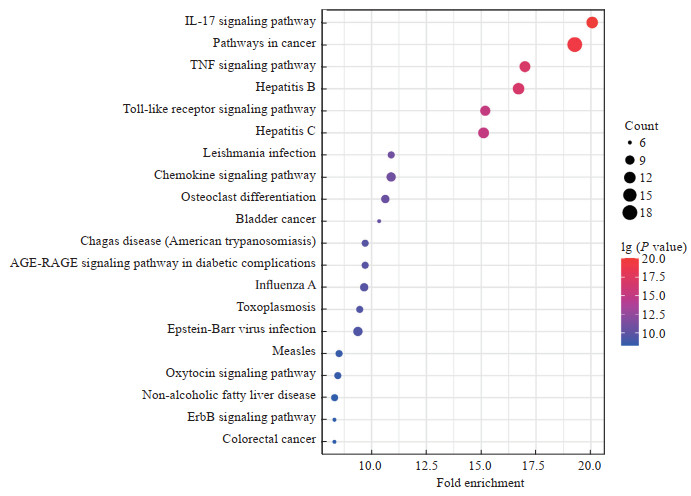
通过Metascape数据库对甘草附子汤治疗RA的靶点基因进行KEGG通路富集分析。选取KEGG富集显著性统计前20条通路绘制气泡图(图 6),其主要调节的通路包括IL-17信号通路、癌症通路、TNF信号通路、乙型肝炎、Toll样受体(Toll-like receptor,TLR)信号通路、丙型肝炎、利什曼病、趋化因子信号通路、破骨细胞分化等,推测甘草附子汤主要通过这些途径起到治疗RA的作用。
|
图 6 甘草附子汤治疗类风湿关节炎靶点基因的KEGG通路富集分析 Fig 6 KEGG pathway enrichment analysis of target genes in treatment of rheumatoid arthritis by Gancao Fuzi decoction IL-17: Interleukin 17; TNF: Tumor necrosis factor; AGE: Advanced glycation end products; RAGE: Receptor for advanced glycation end products; ErbB: Epidermal growth factor receptor. |
2.7 分子对接
图 3显示槲皮素为预测靶点最多的活性成分,4种核心靶点均为槲皮素所对应的靶点,选择MMP9(PDB ID:1GKD)、CXCL8(PDB ID:1ICW)、PPARγ(PDB ID:1FM6)、EGFR(PDB ID:1IVO)与槲皮素分别作为分子对接的受体和配体。检索到槲皮素的PubChem CID为5280343,下载其2D结构并转化为3D结构。见图 7,分子对接结果显示槲皮素能稳定地对接到受体蛋白结构活性口袋中,槲皮素与MMP9、CXCL8、PPARγ、EGFR 4种核心靶点的最低结合能分别为33.858、25.916、36.784、30.022 KJ/mol。槲皮素配体小分子与受体蛋白MMP9形成氢键的氨基酸残基为Asn38、Arg51,与CXCL8相结合形成氢键的氨基酸残基为Gln8、Glu48,与PPARγ相结合的氨基酸残基为Arg288、Glu295、Ser289、Leu228,与EGFR相结合的位点为Met769、Thr766、Asp831。甘草附子汤的核心化学成分槲皮素与受体4种核心靶点均可形成结构稳定、结合活性较高的构象。

|
图 7 槲皮素与MMP9(A)、CXCL8(B)、PPARγ(C)、EGFR(D)相互作用的分子对接示意图 Fig 7 Molecular docking diagram of quercetin interacting with MMP9 (A), CXCL8 (B), PPARγ (C) and EGFR (D) MMP9: Matrix metalloproteinase 9; CXCL8: C-X-C motif chemokine ligand 8; PPARγ: Peroxisome proliferator activated receptor γ; EGFR: Epidermal growth factor receptor. |
3 讨论
《伤寒论》中记载“风湿相搏,骨节疼烦,掣痛不得屈伸,近之则痛剧,汗出短气,小便不利,恶风不欲去衣,或身微肿者,甘草附子汤主之。”其药物配比为甘草二两(炙),附子二枚(炮,去皮,破),白术二两,桂枝四两(去皮)。《医方考》中记载“附子之热,可以散寒湿;桂枝之辛,可以解风湿;甘草健脾,则湿不生;白术燥脾,则湿有制。是方也,以桂、附之辛热而治湿,犹之潦了之地,得太阳曝之,不终朝而湿去,亦治湿之一道也”。中医认为甘草附子汤中的药物成分能相互配伍、疏通经络并除湿驱寒,使风湿之症内外分解。此外,临床研究也证实甘草附子汤能够降低RA患者红细胞沉降率,降低血清中的类风湿因子及TNF-α等炎症因子水平,改善临床症状并缓解疾病进展[16-17]。
本研究通过对甘草附子汤的分析,构建了中药-活性成分-作用靶点网络。网络分析显示95种有效成分与RA相关,并根据度值将槲皮素、山萘酚、7-甲氧基-2-甲基异黄酮、柚皮素、芒柄花素等5种成分纳为主要的活性成分。研究发现甘草附子汤的主要成分以黄酮类化合物为主,其中槲皮素能够通过调节TLR4/髓样分化因子88(myeloid differentiation factor 88,MyD88)/NF-κB信号通路减轻炎症[18],提高T细胞对癌症细胞的杀伤活性,同时抑制程序性死亡受体1(programmed death 1,PD-1)/程序性死亡受体1配体(programmed death-ligand 1,PD-L1)相互作用[19],具有一定的抗炎、抗氧化作用[20-22]。山萘酚可降低IL-5、IL-13、粒细胞-巨噬细胞集落刺激因子(granulocyte-macrophage colony-stimulating factor,GM-CSF)水平,有效减轻炎症,同时能够促进成骨细胞分化及矿化[23-24]。柚皮素可减轻RA症状、降低血清中相关炎症因子水平,具有一定的抗癌作用,可降低MMP2和MMP9的活性,抑制癌细胞的迁移[25-26];芒柄花素具有调节免疫的作用,能预防小鼠自身免疫性肝炎,激活沉默信息调节因子1(silence information regulator 1,SIRT1)/核因子E2相关因子2(nuclear factor E2-related factor 2,Nrf2)信号通路,抑制促炎细胞因子的表达[27-28]。
通过对44个交集基因进行分析,结果显示MMP9、CXCL8、PPARγ和EGFR为甘草附子汤作用于RA的关键基因。MMP称为基质素,是锌家族和依赖性肽链内切酶,包括层粘连蛋白、胶原和纤连蛋白等成分。MMP9是MMP家族的重要成员,对白细胞迁移等过程起重要作用[29],并可直接降解软骨中的重要成分如纤维胶原蛋白Ⅰ、纤维胶原蛋白Ⅱ和蛋白多糖[30],同时MMP9可以促进成纤维细胞迁移、炎症细胞浸润并导致骨软骨的破坏[31-34],在RA的进展中发挥重要作用。RA患者血浆中MMP9升高且与患者关节侵蚀破坏的情况及全身炎症密切相关[35]。CXCL8(IL-8)是一种趋化因子,可募集中性粒细胞、嗜碱性粒细胞和T细胞,RA患者滑膜和软骨细胞中CXCL8水平升高,可导致白细胞募集并加重炎症[36]。PPARγ属于核激素受体超家族,可调节多种细胞功能,包括脂肪生成、脂质生物合成、能量消耗和储存、炎症和分化,并能够通过NF-κB促进炎症[37-38]。EGFR是表皮生长因子(epidermal growth factor,EGF)的受体,可与EGF、TGF-α、双向调节素(amphiregulin,AREG)、上皮细胞有丝分裂蛋白(epithelial mitogen,EPGN)等多种配体相结合并发挥多种生物学功能,促进RA的进展[39]。由此可见,甘草附子汤可能通过调控RA患者的MMP9、CXCL8、PPARγ、EGFR等关键潜在靶点对免疫系统、全身炎症情况及骨侵蚀进行调节,以缓解RA病情。
通过Metascape对交集基因进行GO和KEGG富集分析,发现甘草附子汤治疗RA的分子功能主要集中于炎症及免疫的调节,包括CXCR趋化因子受体结合、趋化因子活性、细胞因子活性、DNA结合转录因子结合、细胞因子受体结合等。KEGG通路富集分析显示基因靶点涉及多条与RA密切相关的信号通路,如IL-17信号通路、TNF信号通路、破骨细胞分化通路、TLR信号通路等,有大量靶点富集在炎症相关的信号通路。大量研究证实,RA患者外周血和关节组织中IL-17A水平升高[40-41],IL-17通路具有促进炎症、血管生成和破骨细胞生成等生物学功能[42]。此外,IL-17和TNF-α之间可通过协同作用刺激促炎因子产生,如IL-1β、IL-6、IL-8、前列腺素E2(prostaglandin E2,PGE2)和MMP,在RA早期促进疾病进展[2-3, 43-44]。TNF可通过血管内皮细胞在局部组织中引起炎症反应,同时它能上调细胞表面黏附分子在内皮细胞中的表达,进而募集白细胞、促进炎症反应,临床实验证明了TNF抑制剂对炎症性疾病的治疗潜力[45-46]。RA的骨质破坏核心在于骨吸收过度和骨骼重建不足,抑制破骨细胞的分化可减轻骨质破坏[47]。从分子对接结果可知,甘草附子汤中主要的活性化合物槲皮素可通过氢键与甘草附子汤的关键靶点MMP9、CXCL8、PPARγ、EGFR结合并发挥作用,在分子层面上验证了甘草附子汤的作用机制。
综上所述,本研究运用网络药理学结合分子对接的研究方法,从甘草附子汤主要的活性成分入手分析其在RA治疗中可能的作用机制,构建中药-活性成分-疾病靶点网络、PPI网络、进行GO富集分析和KEGG通路富集分析,研究结果提示甘草附子汤的主要活性成分槲皮素、山萘酚、7-甲氧基-2-甲基异黄酮、柚皮素、芒柄花素等可能通过MMP9、CXCL8、PPARγ、EGFR等靶点调节炎症反应、抑制破骨细胞过度活化而治疗RA。
| [1] |
RANA A K, LI Y, DANG Q J, YANG F. Monocytes in rheumatoid arthritis: circulating precursors of macrophages and osteoclasts and, their heterogeneity and plasticity role in RA pathogenesis[J]. Int Immunopharmacol, 2018, 65: 348-359. DOI:10.1016/j.intimp.2018.10.016 |
| [2] |
GIANNINI D, ANTONUCCI M, PETRELLI F, BILIA S, ALUNNO A, PUXEDDU I. One year in review 2020:pathogenesis of rheumatoid arthritis[J]. Clin Exp Rheumatol, 2020, 38: 387-397. |
| [3] |
CONIGLIARO P, TRIGGIANESE P, DE MARTINO E, FONTI G L, CHIMENTI M S, SUNZINI F, et al. Challenges in the treatment of rheumatoid arthritis[J]. Autoimmun Rev, 2019, 18: 706-713. DOI:10.1016/j.autrev.2019.05.007 |
| [4] |
王会敏, 王萌. 治疗类风湿性关节炎的中药纳米制剂研究进展[J]. 中国中药杂志, 2019, 44: 3908-3916. |
| [5] |
ZHANG L Y, CAO Z Y, YANG Y Y, TAN X Y, MAO J C, SU L. Traditional Chinese medicine on treating active rheumatoid arthritis: a protocol for systematic review and meta-analysis[J/OL]. Medicine (Baltimore), 2020, 99: e20642. DOI: 10.1097/MD.0000000000020642.
|
| [6] |
LÜ S, WANG Q S, LI G Y, SUN S, GUO Y Y, KUANG H X. The treatment of rheumatoid arthritis using Chinese medicinal plants: from pharmacology to potential molecular mechanisms[J]. J Ethnopharmacol, 2015, 176: 177-206. DOI:10.1016/j.jep.2015.10.010 |
| [7] |
LI X Z, ZHANG S N. Herbal compounds for rheumatoid arthritis: literatures review and cheminformatics prediction[J]. Phytother Res, 2020, 34: 51-66. DOI:10.1002/ptr.6509 |
| [8] |
李葆林, 麻景梅, 田宇柔, 张铁军, 牛丽颖. 甘草中新发现化学成分和药理作用的研究进展[J]. 中草药, 2021, 52: 2438-2448. |
| [9] |
熊秋韵, 李梦婷, 缪璐琳, 易进海, 谢晓芳, 彭成. 附子不同炮制品抗炎、镇痛和提高免疫功能作用的比较研究[J]. 中药药理与临床, 2017, 33: 123-127. |
| [10] |
左军, 张金龙, 胡晓阳. 白术化学成分及现代药理作用研究进展[J]. 辽宁中医药大学学报, 2021, 23: 6-9. |
| [11] |
陈倩雯, 何奕坤, 沈佳莹, 杨光辉. 桂枝汤类方治疗类风湿关节炎的研究进展[J]. 风湿病与关节炎, 2021, 10: 58-62. |
| [12] |
邓桃妹, 彭灿, 彭代银, 俞年军, 陈卫东, 王雷. 甘草化学成分和药理作用研究进展及质量标志物的探讨[J]. 中国中药杂志, 2021, 46: 2660-2676. |
| [13] |
要晓静. 甘草附子汤化学成分分析[D]. 长春: 吉林大学, 2013.
|
| [14] |
PERRETTI M, LEROY X, BLAND E J, MONTERO-MELENDEZ T. Resolution pharmacology: opportunities for therapeutic innovation in inflammation[J]. Trends Pharmacol Sci, 2015, 36: 737-755. DOI:10.1016/j.tips.2015.07.007 |
| [15] |
BARDOU P, MARIETTE J, ESCUDIÉ F, DJEMIEL C, KLOPP C. Jvenn: an interactive Venn diagram viewer[J/OL]. BMC Bioinformatics, 2014, 15: 293. DOI: 10.1186/1471-2105-15-293.
|
| [16] |
曹江山, 庄贺, 侯王君, 邓传超, 孙素平. 甘草附子汤治疗类风湿关节炎34例临床观察[J]. 中医药导报, 2013, 19: 35-37. |
| [17] |
冯亚兵. 甘草附子汤治疗风湿病及对抗环瓜氨酸肽抗体和类风湿因子的影响研究[J]. 亚太传统医药, 2018, 14: 191-192. |
| [18] |
ZHAO B J, ZHANG Q, LIANG X C, XIE J, SUN Q. Quercetin reduces inflammation in a rat model of diabetic peripheral neuropathy by regulating the TLR4/MyD88/NF-κB signalling pathway[J/OL]. Eur J Pharmacol, 2021, 912: 174607. DOI: 10.1016/j.ejphar.2021.174607.
|
| [19] |
JING L, LIN J R, YANG Y, TAO L, LI Y Y, LIU Z X, et al. Quercetin inhibiting the PD-1/PD-L1 interaction for immune-enhancing cancer chemopreventive agent[J]. Phytother Res, 2021, 35: 6441-6451. |
| [20] |
D'ANDREA G. Quercetin: a flavonol with multifaceted therapeutic applications?[J]. Fitoterapia, 2015, 106: 256-271. |
| [21] |
UTHRA C, SHRIVASTAVA S, JASWAL A, SINHA N, RESHI M S, SHUKLA S. Therapeutic potential of quercetin against acrylamide induced toxicity in rats[J]. Biomedecine Pharmacother, 2017, 86: 705-714. |
| [22] |
ZHU Q, LIU M X, HE Y X, YANG B. Quercetin protect cigarette smoke extracts induced inflammation and apoptosis in RPE cells[J]. Artif Cells Nanomed Biotechnol, 2019, 47: 2010-2015. |
| [23] |
MOLITORISOVA M, SUTOVSKA M, KAZIMIEROVA I, BARBORIKOVA J, JOSKOVA M, NOVAKOVA E, et al. The anti-asthmatic potential of flavonol kaempferol in an experimental model of allergic airway inflammation[J/OL]. Eur J Pharmacol, 2021, 891: 173698. DOI: 10.1016/j.ejphar.2020.173698.
|
| [24] |
KIM I R, KIM S E, BAEK H S, KIM B J, KIM C H, CHUNG I K, et al. The role of kaempferol-induced autophagy on differentiation and mineralization of osteoblastic MC3T3-E1 cells[J/OL]. BMC Complement Altern Med, 2016, 16: 333. DOI: 10.1186/s12906-016-1320-9.
|
| [25] |
ZHU L P, WANG J, WEI T T, GAO J, HE H, CHANG X Y, et al. Effects of naringenin on inflammation in complete freund's adjuvant-induced arthritis by regulating Bax/Bcl-2 balance[J]. Inflammation, 2015, 38: 245-251. |
| [26] |
SHI X Y, LUO X P, CHEN T, GUO W, LIANG C J, TANG S H, et al. Naringenin inhibits migration, invasion, induces apoptosis in human lung cancer cells and arrests tumour progression in vitro[J]. J Cell Mol Med, 2021, 25: 2563-2571. |
| [27] |
LIU G W, ZHAO W X, BAI J M, CUI J J, LIANG H W, LU B P. Formononetin protects against concanavalin-A-induced autoimmune hepatitis in mice through its anti-apoptotic and anti-inflammatory properties[J]. Biochem Cell Biol, 2021, 99: 231-240. |
| [28] |
HUANG J J, CHEN X F, XIE A H. Formononetin ameliorates IL-13-induced inflammation and mucus formation in human nasal epithelial cells by activating the SIRT1/Nrf2 signaling pathway[J/OL]. Mol Med Rep, 2021, 24: 832. DOI: 10.3892/mmr.2021.12472.
|
| [29] |
VANDOOREN J, VAN DEN STEEN P E, OPDENAKKER G. Biochemistry and molecular biology of gelatinase B or matrix metalloproteinase-9 (MMP-9): the next decade[J]. Crit Rev Biochem Mol Biol, 2013, 48: 222-272. |
| [30] |
LI J X, LONG Y, GUO R, REN K B, LU Z Z, LI M, et al. Shield and sword nano-soldiers ameliorate rheumatoid arthritis by multi-stage manipulation of neutrophils[J]. J Control Release, 2021, 335: 38-48. |
| [31] |
LEY K, LAUDANNA C, CYBULSKY M I, NOURSHARGH S. Getting to the site of inflammation: the leukocyte adhesion cascade updated[J]. Nat Rev Immunol, 2007, 7: 678-689. |
| [32] |
CHARNI-BEN TABASSI N, DESMARAIS S, BAY-JENSEN A C, DELAISSÉ J M, PERCIVAL M D, GARNERO P. The type Ⅱ collagen fragments Helix-Ⅱ and CTX-Ⅱ reveal different enzymatic pathways of human cartilage collagen degradation[J]. Osteoarthritis Cartilage, 2008, 16: 1183-1191. |
| [33] |
HUBER L C, DISTLER O, TARNER I, GAY R E, GAY S, PAP T. Synovial fibroblasts: key players in rheumatoid arthritis[J]. Rheumatology (Oxford), 2006, 45: 669-675. |
| [34] |
NOSS E H, BRENNER M B. The role and therapeutic implications of fibroblast-like synoviocytes in inflammation and cartilage erosion in rheumatoid arthritis[J]. Immunol Rev, 2008, 223: 252-270. |
| [35] |
AHRENS D, KOCH A E, POPE R M, STEIN-PICARELLA M, NIEDBALA M J. Expression of matrix metalloproteinase 9 (96-kD gelatinase B) in human rheumatoid arthritis[J]. Arthritis Rheum, 1996, 39: 1576-1587. |
| [36] |
PATTERSON A M, GARDNER L, SHAW J, DAVID G, LOREAU E, AGUILAR L, et al. Induction of a CXCL8 binding site on endothelial syndecan-3 in rheumatoid synovium[J]. Arthritis Rheum, 2005, 52: 2331-2342. |
| [37] |
DESVERGNE B, WAHLI W. Peroxisome proliferator-activated receptors: nuclear control of metabolism[J]. Endocr Rev, 1999, 20: 649-688. |
| [38] |
DEBRIL M B, RENAUD J P, FAJAS L, AUWERX J. The pleiotropic functions of peroxisome proliferator-activated receptor gamma[J]. J Mol Med (Berl), 2001, 79: 30-47. |
| [39] |
YUAN F L, LI X, LU W G, SUN J M, JIANG D L, XU R S. Epidermal growth factor receptor (EGFR) as a therapeutic target in rheumatoid arthritis[J]. Clin Rheumatol, 2013, 32: 289-292. |
| [40] |
GULLICK N J, ABOZAID H S, JAYARAJ D M, EVANS H G, SCOTT D L, CHOY E H, et al. Enhanced and persistent levels of interleukin (IL)-17+ CD4+ T cells and serum IL-17 in patients with early inflammatory arthritis[J]. Clin Exp Immunol, 2013, 174: 292-301. |
| [41] |
KIRKHAM B W, LASSERE M N, EDMONDS J P, JUHASZ K M, BIRD P A, LEE C S, et al. Synovial membrane cytokine expression is predictive of joint damage progression in rheumatoid arthritis: a two-year prospective study (the DAMAGE study cohort)[J]. Arthritis Rheum, 2006, 54: 1122-1131. |
| [42] |
ZWICKY P, UNGER S, BECHER B. Targeting interleukin-17 in chronic inflammatory disease: a clinical perspective[J/OL]. J Exp Med, 2020, 217: e20191123. DOI: 10.1084/jem.20191123.
|
| [43] |
VAN HAMBURG J P, ASMAWIDJAJA P S, DAVELAAR N, MUS A M, COLIN E M, HAZES J M, et al. Th17 cells, but not Th1 cells, from patients with early rheumatoid arthritis are potent inducers of matrix metalloproteinases and proinflammatory cytokines upon synovial fibroblast interaction, including autocrine interleukin-17A production[J]. Arthritis Rheum, 2011, 63: 73-83. |
| [44] |
PAULISSEN S M, VAN HAMBURG J P, DAVELAAR N, ASMAWIDJAJA P S, HAZES J M, LUBBERTS E. Synovial fibroblasts directly induce Th17 pathogenicity via the cyclooxygenase/prostaglandin E2 pathway, independent of IL-23[J]. J Immunol, 2013, 191: 1364-1372. |
| [45] |
BRADLEY J R. TNF-mediated inflammatory disease[J]. J Pathol, 2008, 214: 149-160. |
| [46] |
MONACO C, NANCHAHAL J, TAYLOR P, FELDMANN M. Anti-TNF therapy: past, present and future[J]. Int Immunol, 2015, 27: 55-62. |
| [47] |
YAO Y, CAI X Y, REN F J, YE Y Q, WANG F M, ZHENG C H, et al. The macrophage-osteoclast axis in osteoimmunity and osteo-related diseases[J/OL]. Front Immunol, 2021, 12: 664871. DOI: 10.3389/fimmu.2021.664871.
|
 2022, Vol. 43
2022, Vol. 43


