创伤性颈内动脉海绵窦瘘(traumatic carotid cavernous fistula,TCCF)多继发于头部外伤颅底骨折后,颈内动脉海绵窦段或其分支损伤、撕裂,直接与海绵窦形成异常的动静脉交通,是颈内动脉主干直接向海绵窦供血的高流量瘘(Barrow分型为A型)[1]。TCCF可导致海绵窦内的压力增高,从而引起一系列相关症状,包括搏动性耳鸣、颅内杂音、眼部症状,或因皮层静脉逆流而发生脑内血肿。由于海绵窦区解剖结构的复杂性,TCCF通常采用血管内介入治疗策略,包括可解脱球囊、弹簧圈、液体栓塞剂、覆膜支架或几种材料联合应用对瘘口进行栓塞[2-4]。本研究通过回顾性分析我院脑血管病中心2009年1月至2020年6月采用Onyx联合弹簧圈栓塞治疗的TCCF患者资料,探讨该治疗方法的安全性及有效性。
1 资料和方法 1.1 研究对象与纳入标准回顾性分析2009年1月至2020年6月我院脑血管病中心收治的TCCF患者资料。纳入标准:(1)数字减影血管造影(digital subtraction angiography,DSA)提示颈内动脉直接与海绵窦相交通,明确诊断为Barrow A型TCCF;(2)患者接受Onyx胶联合弹簧圈栓塞治疗;(3)患者随访资料完整。本研究通过我院伦理委员会审批。
1.2 治疗方法所有患者手术均在全身麻醉下进行。常规行DSA,明确瘘口位置及引流静脉情况,必要时行压颈试验明确瘘口远端边界及患侧大脑半球的血流代偿情况。
动脉入路:6 F导引导管沿导丝经右侧股动脉输送至患侧颈内动脉。选择适当规格的球囊输送至瘘口处,双微导管在微导丝引导下通过瘘口超选至海绵窦内分别进行弹簧圈栓塞及注射Onyx胶操作。首先进行弹簧圈栓塞,根据造影结果选择合适大小的弹簧圈进行栓塞,其间反复造影明确瘘口情况,当瘘口血流量显著减小后再行Onyx胶栓塞。路图下充盈球囊,通过微导管或导引导管造影证实球囊完全覆盖瘘口。空白路图下缓慢注入Onyx-18胶或Onyx-34胶,采用注胶-反流-等待-注胶的方法进行栓塞。在注射Onyx胶过程中,反复充、泄球囊并通过导管造影确认瘘口是否完全闭塞。
静脉入路:8 F导引导管沿导丝经右侧股静脉输送至患侧颈内静脉,双微导管在微导丝导引下经岩下窦超选至海绵窦内。同时选取适当规格球囊经右侧股动脉输送至患侧颈内动脉海绵窦段瘘口处。同法先经微导管填圈,再以动脉内球囊保护下经另一微导管注射Onyx胶,反复造影确认瘘口闭塞情况。
1.3 围术期管理及随访方案术后严密监测患者生命体征,控制术后血压波动,观察患者症状有无减轻或消失,针对眼部症状对症处理,如球结膜水肿、充血等。针对TCCF导致的颅神经麻痹症状用营养神经药物促进症状缓解。所有患者术后均接受临床和影像学随访,术后3~6个月复查DSA。根据DSA结果制订进一步治疗方案。
1.4 统计学处理应用SPSS 22.0软件进行数据分析。呈正态分布的计量资料以x±s表示,呈偏态分布的计量资料以中位数(范围)表示,计数资料以例数和百分数表示。
2 结果 2.1 患者基线资料共50例TCCF患者入组,其中男27例(54%)、女23例(46%),年龄为17~78岁,平均年龄为(45±15)岁,首发症状距头颅外伤时间为1.0(0.5~4.0)个月。28例(56%)患者合并搏动性耳鸣或颅内杂音,20例(40%)患者表现为眼静脉压力升高(包括突眼、眼球胀痛或球结膜充血红肿),11例(22%)患者有不同程度的视力下降(3例患者入院时已失明),11例(22%)患者眼球活动受限,8例(16%)患者出现视物重影,5例(10%)患者眼睑下垂,4例(8%)患者合并头痛。
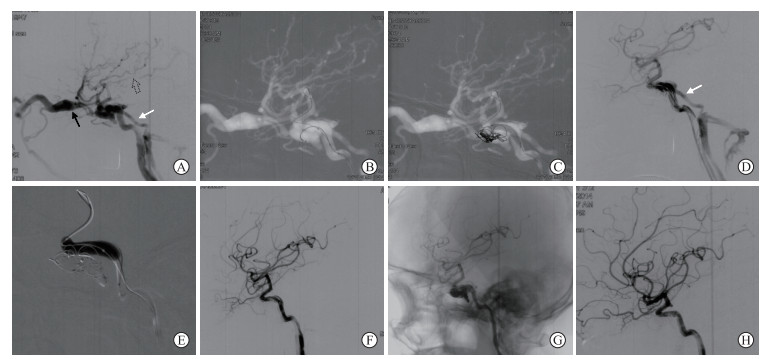
2.2 手术治疗情况50例TCCF患者中42例(84%)经动脉入路栓塞,5例(10%)经动、静脉联合入路栓塞(图 1),3例(6%)经动脉入路栓塞困难后改经静脉入路栓塞。50例患者中共21例(42%)使用动脉内球囊栓塞。
|
图 1 1例左侧创伤性颈内动脉海绵窦瘘造影图像 男,47岁,车祸致创伤性颈内动脉海绵窦瘘.A:左侧颈内动脉造影提示颈内动脉海绵窦瘘,经眼上静脉-面静脉、岩下窦-颈内静脉引流,同时伴有皮质静脉逆流,创伤性颈内动脉海绵窦瘘呈“全偷流”,瘘口远端颈内动脉未见显影(黑色实线箭头所示为眼上静脉,白色实线箭头所示为岩下窦,空心虚线箭头所示为皮质静脉);B,C:微导管经瘘口超选至海绵窦内,将Hyperglide 4/20球囊置入颈内动脉备用(B),并行弹簧圈栓塞(C);D:弹簧圈栓塞后造影提示瘘口血流量明显减小,远端颈内动脉显影,残余瘘口通过岩下窦-颈内静脉引流(白色实线箭头所示为岩下窦);E:球囊保护下注射Onyx胶进行栓塞;F,G:术后造影提示瘘口完全闭塞(F),未减影图像显示Oynx胶铸型和弹簧圈形态(G);H:术后6个月复查造影提示瘘口消失,未见复发. |
2.3 影像学检查结果
栓塞术后即刻造影显示46例(92%)患者瘘口消失,未见异常引流;4例(8%)瘘口少量残留。
2.4 围手术期临床结果术后患者的眼部红肿、颅内杂音及耳鸣等症状均明显好转或消失,但3例入院前已完全失明的患者视力无明显恢复。出院时合并眼肌麻痹的患者中有5例症状完全缓解,6例症状部分缓解。2例(4%)患者发生围手术期并发症,其中1例患者术后出现右侧肢体偏瘫,术前压颈试验提示前、后交通代偿不佳,考虑为术中球囊闭塞时间较长导致的缺血相关并发症,予抗血小板聚集及营养神经治疗后右侧肌力部分恢复;另1例患者术后次日突发失明,考虑造影剂脑病,予对症处置后2 d视力恢复。
2.5 随访结果50例患者术后均接受临床及影像学随访,随访时间为4(2~9)个月。随访期间3例失明患者视力均未恢复,1例遗留眼肌麻痹症状,余患者症状均消失。随访期间无患者出现缺血症状。影像学随访提示50例患者瘘口均完全消失,患侧颈内动脉及远端血管通畅,未见颈内动脉狭窄及闭塞。
3 讨论介入栓塞是目前TCCF的首选治疗方案,有多种栓塞材料可供选择[5-6]。TCCF治疗的目的是通过封闭瘘口减轻海绵窦及相关引流静脉内压力和颈内动脉盗血,从而缓解症状[7]。早期的TCCF介入干预方式是利用可解脱球囊(BALT,法国)进行栓塞,其因操作简便、价格低廉,曾一度成为TCCF的首选治疗方法[8-9],但存在术中球囊提前解脱栓塞颈内动脉或球囊泄露导致瘘口复发等缺陷[6, 10-11]。单纯裸圈或水凝胶修饰弹簧圈栓塞也曾用于TCCF治疗[12],但由于海绵窦容积较大,应用弹簧圈栓塞手术费用高昂,且大量弹簧圈栓塞后易出现占位效应。此外,弹簧圈压缩可导致TCCF复发或假性动脉瘤形成[13],且对于瘘口较大的TCCF,栓塞过程中弹簧圈易凸入颈内动脉,增加颈内动脉闭塞风险。支架辅助弹簧圈栓塞可有效解决弹簧圈凸入供血动脉的问题[14],但围手术期抗血小板聚集治疗不适用于部分急性期出血风险较高的外伤患者,并可能减慢术后瘘口部位的血栓形成而导致TCCF复发[15]。血流导向装置在治疗颅内动脉瘤方面取得了良好效果[16],因其能够达到重建动脉管壁的目的,因而也有使用血流导向装置进行直接型颈内动脉海绵窦瘘的栓塞治疗的个案报道[17]。但血流导向装置治疗同样存在增加出血风险的问题,且治疗费用昂贵。
液态栓塞材料治疗TCCF有其独特优势。液态栓塞材料主要有2种,一种是黏性无机组织胶NBCA(Glubran,美国),被广泛用于颅内动静脉畸形和动静脉瘘的栓塞治疗[18]。但NBCA黏滞度较低,在TCCF瘘口血流量较大的情况下操控性较差,且该胶具有一定黏性,存在粘管或粘连辅助球囊的风险。另一种是非黏性栓塞材料Onyx胶(EV3,美国),它是乙烯-乙烯醇共聚物溶解于无水DMSO并加入钽粉作为显影剂的一种材料。当Onyx胶注入血管内,由于DMSO被血液稀释,乙烯-乙烯醇共聚物固化析出,与钽粉形成血管铸型而达到栓塞效果。Onyx胶在理论上不存在粘管的风险,且栓塞过程为乙烯-乙烯醇共聚物析出固化,其操作及栓塞方向相对可控。本团队曾报道一组在球囊保护下单纯使用Onyx胶栓塞颈内动脉海绵窦瘘的病例[19],其安全性和有效性已经得到证实,但这些病例瘘口均相对较小。对于瘘口较大的TCCF,单纯Onyx胶栓塞可能难以闭塞瘘口。使用弹簧圈联合Onyx胶栓塞较其他栓塞材料具有以下优势:(1)首先进行弹簧圈栓塞,即使是疏松栓塞,仍可大大降低瘘口血流量,使后续液态栓塞材料Onyx胶栓塞更为可控;(2)弹簧圈为Onyx胶建立了网状基础,液态的Onyx胶与弹簧圈形成钢筋混凝土结构,在瘘口形成塞子,封堵牢靠不易复发;(3)弹簧圈无需致密栓塞,节省手术费用的同时减少了占位效应的发生;(4)与单纯使用Onyx胶相比,弹簧圈的使用使Onyx胶的注射时间明显缩短,从缩短了动脉保护球囊的阻断时间,减少了颈内动脉缺血事件的发生。既往对Onyx胶联合弹簧圈栓塞治疗TCCF的报道较少,Ramalingaiah等[20]报道了21例Onyx胶联合弹簧圈栓塞治疗直接型颈内动脉海绵窦瘘的疗效及随访结果,90.5%(19/21)的患者术中瘘口完全栓塞,其中1例患者大脑中动脉栓塞,均未遗留神经功能缺损,术后6个月随访无瘘口复发患者。Zhang等[2]回顾了16例Onyx胶联合弹簧圈治疗的TCCF患者,均在保持颈内动脉通畅的同时完全栓塞病变,术后2个月所有患者症状均得到缓解,平均随访32.6个月后未见神经功能恶化。本研究中除3例入院已出现失明的患者外,其余患者随访时症状均消失。
因TCCF为直接型动静脉瘘,且外伤后瘘口较大,瘘口流量较大。介入干预通常经动脉入路进行栓塞,当瘘口较小或多发小瘘口时超选困难,或已经过动脉入路栓塞后复发,可以通过静脉入路到达瘘口部位进行栓塞[21]。部分患者造影时岩下窦不显影,可通过闭塞开通到达瘘口部位。有研究认为岩下窦不显影时成功开通的概率为30%~50%[22-23],一旦岩下窦无法超选,可通过岩上窦、面静脉、角静脉、翼状窦和眼上静脉进行超选。也有报道采用外科操作暴露[22, 24]或超声引导下直接穿刺面部静脉[25]进入病变。
为最大程度避免栓塞并发症,可提前在颈内动脉瘘口置入保护球囊备用[5]。需要注意的是,使用球囊保护需行全面的血管评估,必要时行压颈实验或球囊闭塞试验以明确患者的患侧大脑半球血流代偿情况。对于术前已出现TCCF盗血相关大脑半球缺血症状或前、后交通动脉代偿较差的患者,需适当缩短单次球囊闭塞保护的时间或不使用球囊保护,以防止发生缺血并发症。本组病例中有1例患者术前评估前、后交通动脉代偿较差,虽已缩短球囊充盈时间但仍发生了缺血事件,值得注意。
综上所述,Onyx胶联合弹簧圈栓塞治疗TCCF安全、有效,是治疗TCCF的理想方式之一,但仍需更长期的随访和多中心大样本的研究进一步证实。
| [1] |
ELLIS J A, GOLDSTEIN H, CONNOLLY E S Jr, MEYERS P M. Carotid-cavernous fistulas[J/OL]. Neurosurg Focus, 2012, 32: E9. DOI: 10.3171/2012.2.FOCUS1223.
|
| [2] |
ZHANG X, GUO W, SHEN R, SUN J P, YIN J, CHEN X Z, et al. Combined use of Onyx and coils for transarterial balloon-assisted embolization of traumatic carotid-cavernous fistulas: a report of 16 cases with 17 fistulas[J]. J Neurointerventional Surg, 2016, 8: 1264-1267. DOI:10.1136/neurintsurg-2015-012107 |
| [3] |
ERTL L, BRÜCKMANN H, PATZIG M, FESL G. Endovascular therapy of direct dural carotid cavernous fistulas-a therapy assessment study including long-term follow-up patient interviews[J/OL]. PLoS One, 2019, 14: e0223488. DOI: 10.1371/journal.pone.0223488.
|
| [4] |
李生, 李宝民, 张远征, 姜金利, 王君, 曹向宇, 等. 创伤性颈内动脉海绵窦瘘的介入治疗[J]. 中国医学影像学杂志, 2007, 15: 354-357. DOI:10.3969/j.issn.1005-5185.2007.05.011 |
| [5] |
GONZALEZ L F, CHALOUHI N, TJOUMAKARIS S, JABBOUR P, DUMONT A S, ROSENWASSER R H. Treatment of carotid-cavernous fistulas using intraarterial balloon assistance: case series and technical note[J/OL]. Neurosurg Focus, 2012, 32: E14. DOI: 10.3171/2012.2.Focus1213.
|
| [6] |
GEMMETE J J, ANSARI S A, GANDHI D M. Endovascular techniques for treatment of carotid-cavernous fistula[J]. J Neuroophthalmol, 2009, 29: 62-71. DOI:10.1097/WNO.0b013e3181989fc0 |
| [7] |
YU Y, HUANG Q, XU Y, HONG B, ZHAO W, DENG B, et al. Use of Onyx for transarterial balloon-assisted embolization of traumatic carotid cavernous fistulas: a report of 23 cases[J]. AJNR Am J Neuroradiol, 2012, 33: 1305-1309. DOI:10.3174/ajnr.A2977 |
| [8] |
NIU Y, CHEN T, TANG J, JIANG Z, ZHU G, CHEN Z. Detachable balloon embolization as the preferred treatment option for traumatic carotid-cavernous sinus fistula?[J]. Interv Neuroradiol, 2020, 26: 90-98. DOI:10.1177/1591019919871849 |
| [9] |
KIRSCH M, HENKES H, LIEBIG T, WEBER W, ESSER J, GOLIK S, et al. Endovascular management of dural carotid-cavernous sinus fistulas in 141 patients[J]. Neuroradiology, 2006, 48: 486-490. DOI:10.1007/s00234-006-0089-9 |
| [10] |
XU X Q, LIU S, ZU Q Q, ZHAO L B, XIA J G, ZHOU C G, et al. Follow-up of 58 traumatic carotid-cavernous fistulas after endovascular detachable-balloon embolization at a single center[J]. J Clin Neurol, 2013, 9: 83-90. DOI:10.3988/jcn.2013.9.2.83 |
| [11] |
LEWIS A I, TOMSICK T A, TEW J M. Management of 100 consecutive direct carotid-cavernous fistulas: results of treatment with detachable balloons[J]. Neurosurgery, 1995, 36: 239-244. DOI:10.1227/00006123-199502000-00001 |
| [12] |
WANG Z G, DING X, ZHANG J Q, QU C C, WANG C W, HUANG D Z, et al. HydroCoil occlusion for treatment of traumatic carotid-cavernous fistula: preliminary experience[J]. Eur J Radiol, 2009, 71: 456-460. DOI:10.1016/j.ejrad.2008.06.009 |
| [13] |
LUO C B, TENG M M, CHANG F C, LIN C J, GUO W Y, CHANG C Y. Transarterial detachable coil embolization of direct carotid-cavernous fistula: immediate and long-term outcomes[J]. J Chin Med Assoc, 2013, 76: 31-36. DOI:10.1016/j.jcma.2012.09.007 |
| [14] |
EDDLEMAN C S, SURDELL D, MILLER J, SHAIBANI A, BENDOK B R. Endovascular management of a ruptured cavernous carotid artery aneurysm associated with a carotid cavernous fistula with an intracranial self-expanding microstent and hydrogel-coated coil embolization: case report and review of the literature[J]. Surg Neurol, 2007, 68: 562-567. DOI:10.1016/j.surneu.2006.10.074 |
| [15] |
MORÓN F E, KLUCZNIK R P, MAWAD M E, STROTHER C M. Endovascular treatment of high-flow carotid cavernous fistulas by stent-assisted coil placement[J]. AJNR Am J Neuroradiol, 2005, 26: 1399-1404. |
| [16] |
PRADEEP N, NOTTINGHAM R, KAM A, GANDHI D, RAZACK N. Treatment of post-traumatic carotid-cavernous fistulas using pipeline embolization device assistance[J/OL]. J Neurointerv Surg, 2016, 8: e40. DOI: 10.1136/neurintsurg-2015-011786.rep.
|
| [17] |
YOON N K, AWAD A W, GEE J M, TAUSSKY P. Ruptured persistent trigeminal artery causing direct cavernous sinus fistula treated with pipeline embolization and minimal coiling[J/OL]. World Neurosurg, 2018, 109: 471-475. e1. DOI: 10.1016/j.wneu.2017.10.017.
|
| [18] |
LIU H M, HUANG Y C, WANG Y H. Embolization of cerebral arteriovenous malformations with n-butyl-2-cyanoacrylate[J]. J Formos Med Assoc, 2000, 99: 906-913. |
| [19] |
YU Y, LI Q, HUANG Q H, ZHANG Y W, FANG Y B, XU Y, et al. Embolization of direct carotid cavernous fistula with Onyx and coils under transarterial balloon protection[J]. Cardiovasc Interv Radiol, 2014, 37: 679-685. DOI:10.1007/s00270-013-0732-x |
| [20] |
RAMALINGAIAH A H, PRASAD C, SABHARWAL P S, SAINI J, PANDEY P. Transarterial treatment of direct carotico-cavernous fistulas with coils and Onyx[J]. Neuroradiology, 2013, 55: 1213-1220. DOI:10.1007/s00234-013-1224-z |
| [21] |
HALBACH V V, HIGASHIDA R T, HIESHIMA G B, HARDIN C W, YANG P J. Transvenous embolization of direct carotid cavernous fistulas[J]. AJNR Am J Neuroradiol, 1988, 9: 741-747. |
| [22] |
QUIÑONES D, DUCKWILER G, GOBIN P Y, GOLDBERG R A, VIÑUELA F. Embolization of dural cavernous fistulas via superior ophthalmic vein approach[J]. AJNR Am J Neuroradiol, 1997, 18: 921-928. |
| [23] |
KLISCH J, HUPPERTZ H J, SPETZGER U, HETZEL A, SEEGER W, SCHUMACHER M. Transvenous treatment of carotid cavernous and dural arteriovenous fistulae: results for 31 patients and review of the literature[J]. Neurosurgery, 2003, 53: 836-857. DOI:10.1227/01.NEU.0000083551.26295.AB |
| [24] |
BERLIS A, KLISCH J, SPETZGER U, FAIST M, SCHUMACHER M. Carotid cavernous fistula: embolization via a bilateral superior ophthalmic vein approach[J]. AJNR Am J Neuroradiol, 2002, 23: 1736-1738. |
| [25] |
BERKMEN T, TROFFKIN N A, WAKHLOO A K. Transvenous sonographically guided percutaneous access for treatment of an indirect carotid cavernous fistula[J]. AJNR Am J Neuroradiol, 2003, 24: 1548-1551. |
 2021, Vol. 42
2021, Vol. 42


