气管插管是麻醉医师对全身麻醉状态下的患者进行气道管理的重要手段。尽管气管插管技术和设备有了很大改进,但困难气管插管导致的围手术期并发症和伤残的发生率依然较高,特别是未预知的困难气管插管[1-2]。目前评估困难气管插管的方法包括Mallampati分级、LEMON(Look externally, Evaluate the 3-3-2 rule, Mallampati, Obstruction, and Neck mobility)法评分、Wilson评分及辅助CT、MRI、超声检查等,过程复杂且阳性评估值不高,均存在一定局限性[3-5]。近年有报道称人工智能面部图像分析能够预测困难气管插管[6-7],但研究者们多关注智能算法和智能模型辨识率的提高,在困难气管插管相关的具体面部特征方面鲜有探究。本研究通过对拟接受全身麻醉下颅颌面手术且行气管插管的患者不同极限姿势的面部图像、人口学资料及其可视喉镜暴露声门真实结果进行采集、分析,探索面部特征指标与可视喉镜暴露声门困难的相关性,并归纳相关的阳性评估指标。
1 资料和方法 1.1 研究对象选择2020年8月至10月在上海交通大学医学院附属第九人民医院拟接受全身麻醉下颅颌面手术且行气管插管的患者537例作为研究对象。入选标准:全身麻醉下行颅颌面手术且需气管插管患者;美国麻醉医师学会(American Society of Anesthesiologists,ASA)分级Ⅰ~Ⅱ级。排除标准:聋哑患者或听力交流能力缺陷者;语言不通,母语非中文者;患有精神或中枢神经系统疾病者;昏迷或意识障碍者;重大创伤者;不能根据指令规范摆动作者;未行气管插管者;无法进行可视喉镜检查者;过去3个月内参与过其他相关临床研究者。本研究获得上海交通大学医学院附属第九人民医院伦理委员会批准,并在美国临床试验数据库(ClinicalTrials)注册(注册编号为NCT04458220)。
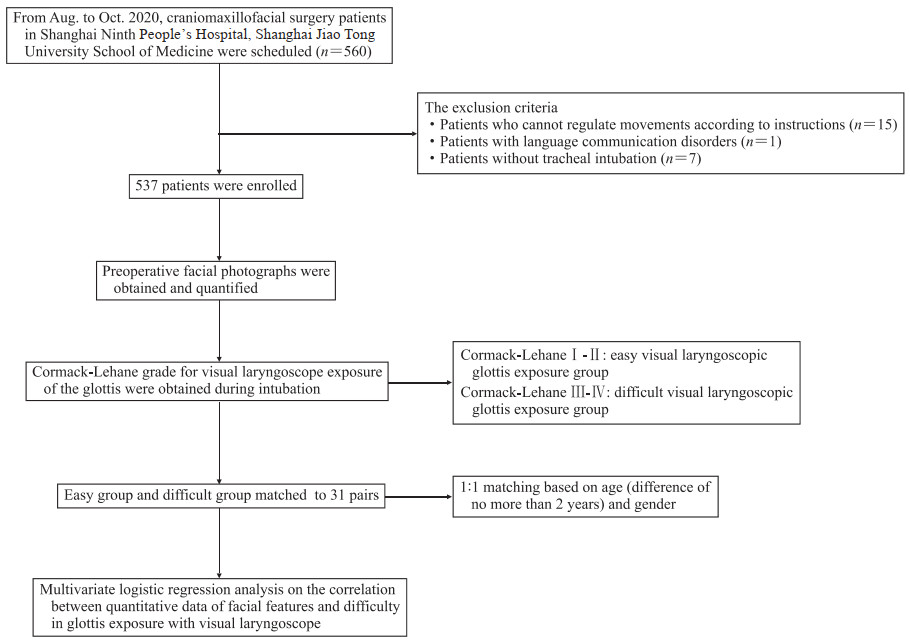
1.2 研究方法由研究者以标准格式于手术麻醉前收集患者基本信息,包括身高、体重、年龄、性别、BMI等。在气管插管诱导前对患者面部正面中立位照、张口伸舌照和仰头照进行采集,然后由具有5年以上临床经验的麻醉医师用统一规格可视喉镜实施气管插管。采用“嗅花位”暴露声门,由统计者记录插管时可视喉镜暴露声门的Cormack-Lehane(C-L)等级,研究者不干预麻醉医师采取的可视喉镜暴露声门困难气管插管的解决方案(使用环状软骨压迫、套囊充气、弯钳等)。研究者根据可视喉镜暴露下声门的C-L等级将患者分为可视喉镜暴露声门容易组(C-L等级Ⅰ~Ⅱ级)和可视喉镜暴露声门困难组(C-L等级Ⅲ~Ⅳ级)。对可视喉镜暴露声门困难者基于年龄(差异不大于2岁)和性别与可视喉镜暴露声门容易者进行1∶1匹配。研究筛选流程见图 1。
|
图 1 研究筛选流程图 Fig 1 Research flow chart |
1.3 面部特征信息采集及定量化
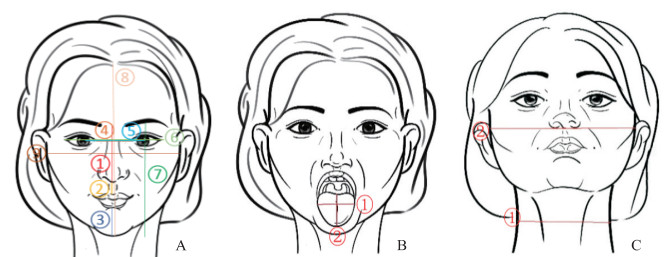
对患者不同姿势的面部照片(图 2)分别测量如下指标并进行定量化分析。正面中立位照:眉心至鼻尖距离、鼻尖至上唇红缘距离、下唇红缘至下颏距离、内眦点宽度、瞳孔间宽度、外眦点宽度、眉毛至下颏垂直距离,并以额骨鳞部体表冠状面顶点处至下颏距离(垂直指标)或面部最宽处宽度(宽度指标)作为参考,计算各指标占参考指标的比例。正面张口伸舌照:舌最宽处宽度,并以舌伸出长度(舌根与口腔交界)作为参考,计算指标在参考指标中所占比例,舌伸不出来者不记录该部分数据并记为伸舌受限。正面仰头照:颈部最宽处宽度,并以面部最宽处宽度作为参考,计算指标占参考指标的比例。
|
图 2 接受颅颌面手术且行气管插管患者3种姿势的面部图像示意图 Fig 2 Schematic diagram of facial images of 3 postures in patients undergoing craniomaxillofacial surgery and tracheal intubation A: Frontal neutral position (①: Distance from brow to nasal tip; ②: Distance from nasal tip to upper vermillion border; ③: Distance from lower vermillion border to chin; ④: Distance between inner canthi; ⑤: Distance between pupils; ⑥: Distance between outer canthi; ⑦: Vertical distance from brow to chin; ⑧: Distance from the apex of the coronal surface of the frontal scale to the chin; ⑨: Width of the widest parts of the face). B: Frontal mouth opening with tongue extending position (①: Width of the widest parts of the tongue; ②: Length of tongue extension). C: Head-up position (①: Width of the widest parts of the neck; ②: Width of the widest parts of the face). |
1.4 统计学处理
计算预期可视喉镜暴露声门困难组与可视喉镜暴露声门容易组患者的面部特征点距离差值的标准差,假设Ⅰ类错误概率α=0.05、1-β=0.90,本研究采集的31对样本能够发现可视喉镜暴露声门困难组与可视喉镜暴露声门容易组之间差值大于0.6个标准差的评估指标,能够满足统计学和临床实际需求。
应用Digimizer软件对患者面部照片进行测量,数据导入SPSS 15.0软件进行统计学分析。计量资料以x±s表示,组间比较采用配对样本t检验;计数资料以例数和百分数表示,组间比较采用Pearson χ2检验(是否伸舌受限)。采用配对设计的logistic回归评估面部特征与可视喉镜暴露声门困难的相关性。检验水准(α)为0.05。
2 结果 2.1 基本情况本研究收集到2020年8月至10月在上海交通大学医学院附属第九人民医院进行颅颌面外科手术且需全身麻醉气管插管的可视喉镜暴露声门困难的患者31例,并根据年龄和性别1∶1匹配可视喉镜暴露声门容易患者31例。31对患者年龄15~75岁,每组男19例(61.3%)、女12例(38.7%)。可视喉镜暴露声门困难组年龄为(49.29±17.47)岁,可视喉镜暴露声门容易组年龄为(49.23±17.47)岁;可视喉镜暴露声门困难组BMI为(22.18±3.55)kg/m2,可视喉镜暴露声门容易组BMI为(23.33±3.06)kg/m2,两组BMI差异无统计学意义(t=-1.805,P=0.081)。
2.2 面部特征测量结果患者面部特征测量结果如表 1所示,可视喉镜暴露声门容易组、困难组眉心至鼻尖距离占额骨鳞部体表冠状面顶点处至下颏距离比例分别为0.283 0±0.024 5、0.309 6±0.039 8,两组比较差异有统计学意义(P=0.002);可视喉镜暴露声门容易组中有2例(6.5%,2/31)患者舌头无法伸出,可视喉镜暴露声门困难组有12例(38.7%,12/31),两组比较差异有统计学意义(P=0.002)。其余面部特征指标在两组间差异均无统计学意义(P均>0.05)。
|
|
表 1 接受颅颌面手术且行气管插管患者面部特征测量结果 Tab 1 Measurement results of facial features of patients undergoing craniomaxillofacial surgery and tracheal intubation |
2.3 多因素logistic回归分析
对于定量数据,定义logistic回归自变量的一个单位为0.01(1%)。将BMI、眉心至鼻尖距离占额骨鳞部体表冠状面顶点处至下颏距离比例和伸舌受限同时纳入logistic回归模型,结果(表 2)显示眉心至鼻尖距离占额骨鳞部体表冠状面顶点处至下颏距离比例与可视喉镜暴露声门困难的发生有关(OR=1.25,95% CI 1.02~1.53,P=0.033),表明可视喉镜暴露声门困难的患者更容易存在眉心至鼻尖距离占比增大的面部特征。
|
|
表 2 面部特征量化指标与可视喉镜暴露声门困难相关性的多因素logistic回归分析 Tab 2 Multivariate logistic regression analysis on the correlation between quantitative indexes of facial features and difficult visual laryngoscopic glottic exposure |
3 讨论
困难气道导致的麻醉伤残甚至死亡事件呈上升趋势[8],困难气道管理指南特别强调了困难气道早期识别和预警的重要性[9]。使用床旁检查来预测困难气管插管被认为是现代麻醉学气道管理的常用手段,已被纳入困难气道算法[10],然而,在临床实践中,所有容易执行的检查系统的表现都不尽如人意,灵敏度仅为20%~62%[11]。影像学方法虽然比床旁检查更加准确,但辐射和成本等问题限制了其在临床的广泛推广[5]。临床实践中,麻醉医师在预测困难气道时可能会受一些主观因素影响,包括患者的体态和面部外观、自身的经验等,不同的医师评估气道条件的侧重点也不一样,目前的评估检查方法过于依赖医师自身经验,而未能建立起一套稳定的评估体系。近年来人工智能飞速发展,尤其在图像识别诊断疾病方面的发展最为成熟[12],使得将头颈部床旁测试转化为图像后结合人工智能人脸识别算法建立一套稳定的困难气道评估体系成为可能[6-7]。
虽然临床医师评估困难气道会观察患者面部外观及头颈部发育状态,但目前有关面部特征与困难气道相关性的研究仍较少。建立人工智能识别困难气道模型的过程需要大量的样本及人力、物力,因此在模型构筑前,有必要基于较小的样本明确面部特征与困难气道的相关性,为构建基于面部识别的困难气道评估模型提供支持。本团队拟开展“人工智能人脸特征识别困难气道”的大型临床研究项目(ClinicalTrials注册编号NCT04458220),考虑人工智能学习建模样本量较大,先以4 000例样本为基数进行训练学习建模。本研究是在该大型研究样本的收集过程中对初步筛选的62例患者进行的一个小样本可行性研究,以探索患者面部特征与困难气道的相关性。在本研究中,我们发现眉心至鼻尖距离占额骨鳞部体表冠状面顶点处至下颏距离比例与可视喉镜暴露声门困难的发生有关,眉心至鼻尖距离的占比越大,可视喉镜暴露声门困难的可能性越大。这可能是因为在可视喉镜暴露声门困难组和容易组患者下颌、上颌长短基本一致的情况下,在某一个人身上看,一个人的额骨鳞部体表冠状面顶点处至下颏距离是不变的,而随着眉心至鼻尖的距离占额骨鳞部体表冠状面顶点处至下颏距离比例的增大,其下颌所占额骨鳞部体表冠状面顶点处至下颏距离比例相对缩短。在Connor和Segal[6]构建的基于白种男性患者的面部图像识别困难气管插管机器学习模型中,发现眉心至鼻尖的距离与下颏长度比例增大与困难气管插管的发生显著相关。这提示眉心至鼻尖距离占比是面部特征识别困难气道相关的关键因素。
目前,下颌后缩已被明确是喉镜暴露声门困难的重要危险因素[4]。本研究以下唇红缘至下颏距离占额骨鳞部体表冠状面顶点处至下颏距离比例衡量下颌是否后缩,本研究并未发现下唇红缘至下颏距离所占额骨鳞部体表冠状面顶点处至下颏距离比例在两组间的差异有统计学意义。这可能由于二维图像不能展示头的三维立体结构,因此在捕捉下颌缩短的信息方面有所欠缺,也可能是因为小下颌患者的样本量少,统计效能不够。
本研究存在一定局限性。首先,本研究为“人工智能人脸特征识别困难气道”项目的一个小样本可行性研究,旨在确定面部特征与困难气道的相关性,挖掘未知的与困难气道相关的特征,而非探索困难气道发生的独立危险因素,因此未考虑将既往研究发现的影响可视喉镜暴露声门困难的危险因素如Mallampati分级及甲颏间距、张口度等解剖结构[13]相关因素纳为混杂因素。视频喉镜下困难气道的发生率较低(3%~4%)[14],本中心可视喉镜下的困难气道也仅在6%左右,在本研究的发表周期内,我们根据纳入、排除标准仅采集到目前的样本数,故从统计角度也无法纳入较多因素进行logistic回归校正。其次,本研究定量化的面部特征或定量化方式可能远远达不到囊括足够丰富的面部特征信息。
综上所述,本研究证实面部存在与可视喉镜暴露声门困难相关的特征,眉心至鼻尖距离占额骨鳞部体表冠状面顶点处至下颏距离比例与可视喉镜暴露声门困难的发生有关。可视喉镜暴露声门困难气道患者仍存在一些我们未知的面容特征信息,相信未来基于人工智能的面部扫描分析技术和三维人脸识别技术能够挖掘更强大的相关面部信息用于困难气道预警。
| [1] |
APFELBAUM J L, HAGBERG C A, CAPLAN R A, BLITT C D, CONNIS R T, NICKINOVICH D G, et al. Practice guidelines for management of the difficult airway: an updated report by the American Society of Anesthesiologists Task Force on Management of the Difficult Airway[J]. Anesthesiology, 2013, 118: 251-270. DOI:10.1097/ALN.0b013e31827773b2 |
| [2] |
XU Z P, MA W H, HESTER D L, JIANG Y D. Anticipated and unanticipated difficult airway management[J]. Curr Opin Anaesthesiol, 2018, 31: 96-103. DOI:10.1097/ACO.0000000000000540 |
| [3] |
ROTH D, PACE N L, LEE A, HOVHANNISYAN K, WARENITS A M, ARRICH J, et al. Airway physical examination tests for detection of difficult airway management in apparently normal adult patients[J/CD]. Cochrane Database Syst Rev, 2018, 5: CD008874.
|
| [4] |
DETSKY M E, JIVRAJ N, ADHIKARI N K, FRIEDRICH J O, PINTO R, SIMEL D L, et al. Will this patient be difficult to intubate?[J]. JAMA, 2019, 321: 493-503. DOI:10.1001/jama.2018.21413 |
| [5] |
JI C, NI Q, CHEN W. Diagnostic accuracy of radiology (CT, X-ray, US) for predicting difficult intubation in adults: a meta-analysis[J]. J Clin Anesth, 2018, 45: 79-87. DOI:10.1016/j.jclinane.2017.12.023 |
| [6] |
CONNOR C W, SEGAL S. Accurate classification of difficult intubation by computerized facial analysis[J]. Anesth Analg, 2011, 112: 84-93. DOI:10.1213/ANE.0b013e31820098d6 |
| [7] |
CUENDET G L, SCHOETTKER P, YüCE A, SORCI M, GAO H, PERRUCHOUD C, et al. Facial image analysis for fully automatic prediction of difficult endotracheal intubation[J]. IEEE Trans Biomed Eng, 2016, 63: 328-339. DOI:10.1109/TBME.2015.2457032 |
| [8] |
JOFFE A M, AZIZ M F, POSNER K L, DUGGAN L V, MINCER S L, DOMINO K B. Management of difficult tracheal intubation: a closed claims analysis[J]. Anesthesiology, 2019, 131: 818-829. DOI:10.1097/ALN.0000000000002815 |
| [9] |
FRERK C, MITCHELL V S, MCNARRY A F, MENDONCA C, BHAGRATH R, PATEL A, et al. Difficult Airway Society 2015 guidelines for management of unanticipated difficult intubation in adults[J]. Br J Anaesth, 2015, 115: 827-848. |
| [10] |
American Society of Anesthesiologists Task Force on Management of the Difficult Airway. Practice guidelines for management of the difficult airway: an updated report by the American Society of Anesthesiologists Task Force on Management of the Difficult Airway[J]. Anesthesiology, 2003, 98: 1269-1277. DOI:10.1097/00000542-200305000-00032 |
| [11] |
YENTIS S M. Predicting difficult intubation: worthwhile exercise or pointless ritual?[J]. Anaesthesia, 2002, 57: 105-109. DOI:10.1046/j.0003-2409.2001.02515.x |
| [12] |
LUO H, XU G, LI C, HE L, LUO L, WANG Z, et al. Real-time artificial intelligence for detection of upper gastrointestinal cancer by endoscopy: a multicentre, case-control, diagnostic study[J]. Lancet Oncol, 2019, 20: 1645-1654. DOI:10.1016/S1470-2045(19)30637-0 |
| [13] |
AMANITI A, PAPAKONSTANTINOU P, GKINAS D, DALAKAKIS I, PAPAPOSTOLOU E, NIKOPOULOU A, et al. Comparison of laryngoscopic views between C-MACTM and conventional laryngoscopy in patients with multiple preoperative prognostic criteria of difficult intubation. An observational cross-sectional study[J/OL]. Medicina (Kaunas), 2019, 55: 760. DOI: 10.3390/medicina55120760.
|
| [14] |
AZIZ M F, HEALY D, KHETERNAL S, FU R F, DILLMAN D, BRAMBRINK A M. Routine clinical practice effectiveness of the Glidescope in difficult airway management: an analysis of 2, 004 Glidescope intubations, complications, and failures from two institutions[J]. Anesthesiology, 2011, 114: 34-41. DOI:10.1097/ALN.0b013e3182023eb7 |
 2021, Vol. 42
2021, Vol. 42


