2. 湖南中医药大学第一附属医院针灸推拿康复科, 长沙 410007
2. Department of Acupuncture and Massage Rehabilitation, the First Hospital of Hunan University of Chinese Medicine, Changsha 410007, Hunan, China
胃癌是一种常见的消化系统恶性肿瘤,对人类的健康造成较大威胁。《2018年全球癌症统计数据》显示,胃癌的发病率居全球癌症发病率的第5位,达到了5.7%;死亡率居全球癌症的第3位,达到了8.2%[1]。一般认为胃癌的好发年龄为50~70岁,但随着社会及饮食习惯的改变,青年胃癌患者(18~44岁)的发病率也呈现上升趋势[2-4]。有数据显示,2006-2017年我国15~49岁年龄组胃癌发病率呈上升趋势,由5.90/10万增高至7.56/10万[4]。
胃癌恶性程度高,发展迅速,早期漏诊、误诊率高,因而常常预后不佳[5-6],对胃癌患者预后影响因素进行研究有助于临床治疗策略的制定与实施。目前临床上主要根据美国癌症联合委员会(American Joint Committee on Cancer,AJCC)TNM分期系统第7、8版[7]对肿瘤患者进行疾病分期,分期的结果用于指导患者的治疗及生存期预测。但此分期系统仅关注肿瘤侵犯的深度、淋巴结转移个数及有无远处转移的情况,有研究表明年龄、性别、肿瘤大小、原发肿瘤部位和血管浸润等也可能会影响患者预后[8]。
经典的Cox回归模型通常用于疾病生存分析的研究,在Cox回归分析中生存结局的终点为二分类:感兴趣的结局事件和删失。但在现实世界中,研究对象在出现研究人员感兴趣的结局事件的同时,还会出现其他结局事件,这些结局事件可能阻挡研究人员感兴趣结局事件的出现或降低其出现的概率,形成“竞争”关系,这样的事件被定义为竞争事件。若忽略竞争事件直接进行经典Cox回归,将使结果产生偏差,竞争事件比例>10%采用传统方法可造成严重偏倚,而<10%可能出现假阳性或假阴性[8-9]。采用Fine-Gray竞争风险模型进行生存分析,可将生存数据的终点分为多类,把竞争事件与研究人员感兴趣的结局事件分开,消除竞争事件对预后研究带来的影响,是更为有效的生存分析模型[10]。
监测、流行病学和最终结果(Surveillance,Epidemiology,and End Results;SEER)数据库是美国权威的癌症统计数据库。该数据库记录了美国上百万例恶性肿瘤患者的人口统计数据,包括患者的个人信息、原发灶位置、肿瘤大小、肿瘤编码、部分治疗信息、生存期、死亡原因等,是极为难得的肿瘤人群大数据。本研究基于SEER数据库中的胃癌大数据进行研究,弥补了一般临床研究中样本量较小的缺点,使用比Cox回归模型更加精确的Fine-Gray竞争风险模型系统分析青年胃癌患者的预后因素,并构建列线图预后评价模型,为青年胃癌患者的预后预测提供更准确的参考。
1 资料和方法 1.1 研究资料通过SEER数据库客户端SEER*Stat 8.3.8收集胃癌病例资料,使用SEER 18 Regs Custom Data(with additional treatment fields)和Nov 2018 Sub(1975-2016 Varying)数据模块。纳入标准:(1)肿瘤原发部位为胃;(2)确诊年龄为18~44岁[2];(3)确诊依据为病理诊断提示阳性;(4)随访有效、随访资料完整且生存时间>0 d;(5)确诊年份为2004-2015年。排除标准:(1)资料来源于尸体解剖或死亡报告;(2)生存时间未知的病例;(3)非原发肿瘤。
1.2 研究指标以癌症特异性生存(cancer-specific survival,CSS)率为关注点,在数据库中筛选出可能与CSS相关的临床指标,包括年龄、种族、性别、原发肿瘤部位、病理类型、肿瘤分级、原发灶手术、区域淋巴结手术、T分期、N分期、M分期、原发肿瘤数目、放射治疗情况、化学治疗情况。其中T分期、N分期、M分期依据AJCC TNM分期第6版者均转换成第7版的TNM分期进行分析。
1.3 统计学处理应用R 4.0.3软件进行统计学分析,采用的工具包有caret、rms、foreign、survival、survivalROC、mstate等。计数资料以例数和百分数进行统计描述,采用χ2检验进行训练集与验证集组间的均衡性检验;根据数据库中记录的患者死亡原因,将非肿瘤原因死亡的患者进行独立分类,最终将患者分为存活、死于胃癌、死于非胃癌3类,采用竞争风险模型的生存曲线估计青年胃癌患者的CSS率。使用Fine-Gray竞争风险模型进行单因素和多因素分析,对单因素分析中差异有统计学意义的指标进行多因素分析,寻找青年胃癌患者CSS的独立影响因素,并建立预后模型,绘制列线图。使用ROC曲线和校准曲线验证模型的预测效果。检验水准(α)为0.05。
2 结果 2.1 训练集与验证集在临床预测模型研究所需样本量的估计中,参考胃癌5年生存率41.00%[11],依据文献中临床预测模型样本量计算公式[12],计算得胃癌5年临床预测模型所需的最小样本量约为474例。根据纳入与排除标准在SEER数据库中检索到4 298例青年胃癌病例数据,排除各临床指标及生存数据不明确或缺失的病例后得到2 673例,使用R 4.0.3软件将2 673例病例按照约7∶3的比例随机分成训练集(1 873例)与验证集(800例)。训练集数据用于预后预测模型的建立,验证集数据用于预后预测模型的验证。
2.2 训练集与验证集组间均衡性检验训练集与验证集患者的各项临床指标比较差异均无统计学意义(P均>0.05,表 1),说明训练集与验证集患者各项指标分布情况相同,在训练集中得到的统计模型可以在验证集中进行验证。
|
|
表 1 训练集与验证集青年胃癌患者各指标的描述与比较 Tab 1 Description and comparison of each variable of young gastric cancer patients in training set and validation set |
2.3 青年胃癌患者CSS的影响因素分析
训练集数据中Fine-Gray竞争风险模型多因素分析结果显示,肿瘤分级、T分期、N分期、M分期、原发灶手术情况、区域淋巴结手术情况、放化疗情况是青年胃癌患者CSS的影响因素(P均<0.05)。见表 2。
|
|
表 2 青年胃癌患者CSS影响因素的Fine-Gray竞争风险模型分析 Tab 2 Fine-Gray competitive risk model analysis of influencing factors of CSS in young patients with gastric cancer |
2.4 青年胃癌患者CSS率
将患者分为存活、死于胃癌、死于非胃癌3类,采用Fine-Gray竞争风险模型中的生存曲线模块,得出在各影响因素作用下,训练集中青年胃癌患者的1、3和5年累积CSS率分别为54.56%、29.70%和23.96%。
2.5 青年胃癌患者CSS影响因素的列线图构建基于对训练集数据进行Fine-Gray竞争风险模型多因素分析的结果,将肿瘤分级、T分期、N分期、M分期、原发灶手术情况、区域淋巴结手术情况、放化疗情况7个变量纳入青年胃癌患者CSS的预后模型,绘制预后评价模型列线图(图 1),根据患者个体情况,将各因素的得分相加即可预测青年胃癌患者1、3、5年的CSS率。

|
图 1 青年胃癌患者CSS率预测模型的列线图 Fig 1 Nomogram of CSS rate prediction model in young patients with gastric cancer CSS: Cancer-specific survival. |
2.6 列线图预测模型的验证
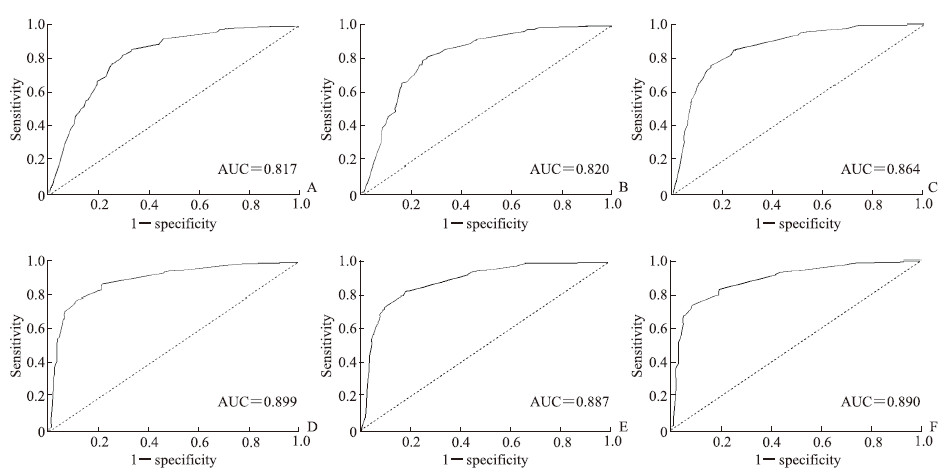
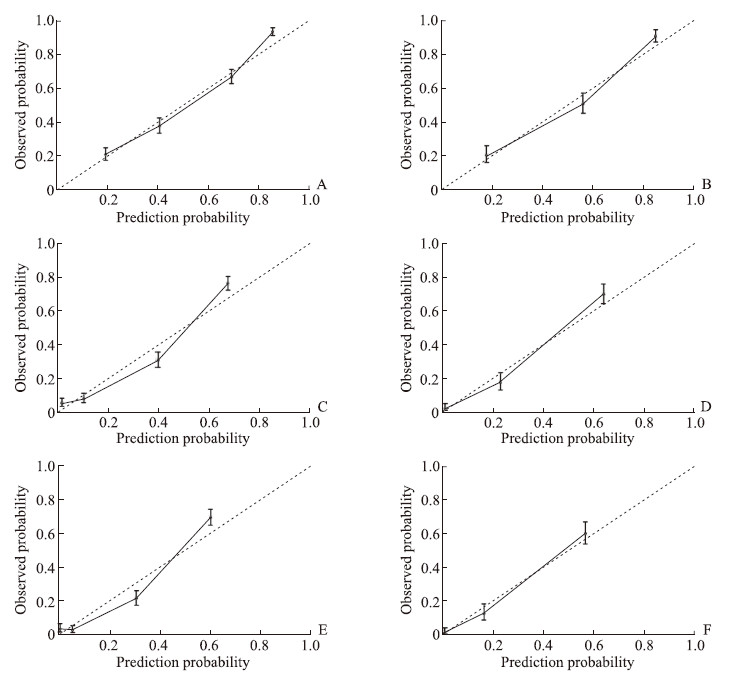
使用训练集与验证集数据从区分度、校准度2个方面对构建的列线图模型进行评价。区分度是指模型通过设置一定的风险界值正确区分未来发病风险高、低不同的人群的能力,校准度是指模型预测未来某个体发生结局事件概率的准确性的能力。通过绘制ROC曲线、计算AUC值评价模型区分度,AUC值越接近于1说明模型的区分度越好,一般来说AUC值>0.7说明模型的区分度较好。图 2为列线图模型预测青年胃癌患者1、3、5年CSS率的ROC曲线,在训练集中预测1、3、5年CSS率的AUC值分别为0.817、0.864、0.887,在验证集中分别为0.820、0.899、0.890,说明该列线图模型的区分度较好。使用校准图评价模型的校准度,校准图中的纵坐标为实际概率、横坐标为预测概率,对角线为参考线,折线为预测概率与实际概率对应后的拟合线。若预测概率接近实际概率,折线会接近参考线甚至与参考线重合。由图 3可见,1、3、5年CSS率的预测概率与实际概率非常接近,说明该列线图模型的校准度较好。
|
图 2 青年胃癌患者CSS率预测模型列线图区分度评价的ROC曲线分析 Fig 2 ROC curve analyses of differentiation evaluation of nomogram of CSS rate prediction model in young patients with gastric cancer A: ROC curve of 1-year CSS rate in the training set; B: ROC curve of 1-year CSS rate in the validation set; C: ROC curve of 3-year CSS rate in the training set; D: ROC curve of 3-year CSS rate in the validation set; E: ROC curve of 5-year CSS rate in the training set; F: ROC curve of 5-year CSS rate in the validation set. CSS: Cancer-specific survival; ROC: Receiver operating characteristic; AUC: Area under curve. |
|
图 3 青年胃癌患者CSS率预测模型列线图的校准度评价曲线 Fig 3 Calibration evaluation curve of nomogram of CSS rate prediction model in young patients with gastric cancer A: Calibration curve of 1-year CSS rate in the training set; B: Calibration curve of 1-year CSS rate in the validation set; C: Calibration curve of 3-year CSS rate in the training set; D: Calibration curve of 3-year CSS rate in the validation set; E: Calibration curve of 5-year CSS rate in the training set; F: Calibration curve of 5-year CSS rate in the validation set. CSS: Cancer-specific survival. |
3 讨论
近年来,青年人胃癌的发病率呈明显上升趋势[4-5, 13],对于青年胃癌患者来说,在确诊后更加希望了解预后情况。有研究表明,胃癌的预后可能与患者的年龄、性别、临床因素、肿瘤特征等多种因素相关[14-15],而目前临床常用的TNM分期系统只包含肿瘤的部分特征指标,并不全面,因此需构建一个综合的预后预测模型,给患者和临床医师提供个体化预测工具,为后续治疗方案的制订提供可靠参考。
本研究是基于SEER数据库的大数据研究,样本量达2 673例,统计学效能强,弥补了一般临床研究样本量小的缺点,具有较高的临床参考价值。本研究以CSS为终点进行预后分析,根据预后影响因素研究的结果构建列线图,并对列线图进行ROC曲线、校准曲线验证,结果显示构建的列线图对青年胃癌患者的预后有良好的预测效果。
经多因素Fine-Gray竞争风险模型分析,与青年胃癌患者预后有关的因素有肿瘤分级、T分期、N分期、M分期、原发灶手术情况、区域淋巴结手术情况和放化疗情况,其中肿瘤分级、T分期、N分期、M分期是预后危险因素,与临床一贯认知相符[16-20]。原发灶手术、区域淋巴结手术、放化疗情况是青年胃癌患者预后的保护因素,说明进行原发灶手术、区域淋巴结手术、放化疗的患者预后较好,这也与既往研究结果[6, 19, 21-23]一致。
与青年胃癌患者预后无关的因素有年龄、性别、种族、原发肿瘤部位、原发肿瘤数目、病理类型、转移灶手术情况。部分研究显示年龄是预后危险因素,在全年龄段患者中随着年龄的增长预后变差[6, 21-22, 24]。还有研究认为单原发肿瘤患者较多原发肿瘤患者预后更差[6]。在本研究中,可能由于研究对象为18~44岁患者,在这个年龄段内的患者身体素质没有太大差异,因此年龄在多因素分析中未成为预后的影响因素。关于原发肿瘤数目与预后的关系目前研究较少,肿瘤数目与预后关系到底如何还需进一步研究。
本研究有以下缺点:(1)SEER数据库作为一个经典的肿瘤数据库,其数据量大、涵盖肿瘤种类多,但其收集的数据绝大多数为临床指标,不包含实验室检查、影像学检查等指标,因此本研究构建的列线图预测模型也仅纳入了患者的临床指标。(2)SEER数据库中部分临床指标存在缺失值。(3)部分患者未进行手术治疗,因此无法得到其病理分期结果,本研究中使用的TNM分期为其临床分期的结果。这些都可能导致本研究构建的预后预测模型准确度受到影响。
综上所述,本研究利用SEER数据库中的临床大数据建立的青年胃癌患者CSS率预测列线图模型可有效评估患者预后,能作为临床治疗决策的重要参考工具。但由于SEER数据库本身的缺点,如指标不够丰富、某些数据存在缺失值、未手术患者的临床TNM分期准确度有待提高等,未来仍需要更多的临床研究进一步验证。
| [1] |
BRAY F, FERLAY J, SOERJOMATARAM I, SIEGEL R L, TORRE L A, JEMAL A. Global cancer statistics 2018:GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin, 2018, 68: 394-424. DOI:10.3322/caac.21492 |
| [2] |
朱建平. 世卫组织: 44岁以下为青年[J]. 健康博览, 2013(6): 13. |
| [3] |
季加孚. 我国胃癌防治研究三十年回顾[J]. 中国肿瘤临床, 2013, 40: 1345-1351. DOI:10.3969/j.issn.1000-8179.20131950 |
| [4] |
王静雷, 杨一兵, 耿云霞, 石文惠, 高欣, 马吉祥. 1990-2017年中国胃癌发病、患病及死亡状况趋势分析[J]. 中国慢性病预防与控制, 2020, 28: 321-325. |
| [5] |
李燕, 陆海林, 曹婷华, 段之佩, 黄维贤. 青年胃癌危险因素的调查分析[J]. 中国医药指南, 2016, 14: 14-15, 17. |
| [6] |
侯松林, 谢兴江, 彭强, 周国俊, 李利发, 周何, 等. 基于SEER数据库的胃癌肝转移预后因素分析与预后模型构建[J]. 中国普通外科杂志, 2020, 29: 1212-1223. DOI:10.7659/j.issn.1005-6947.2020.10.008 |
| [7] |
陈洛海, 周志伟, 陈洁. 美国癌症联合委员会(AJCC)第8版胃肠胰神经内分泌肿瘤分期解读及评价[J]. 中华胃肠外科杂志, 2017, 20: 972-976. DOI:10.3760/cma.j.issn.1671-0274.2017.09.003 |
| [8] |
WANG W, SUN X W, LI C F, LV L, LI Y F, CHEN Y B, et al. Comparison of the 6th and 7th editions of the UICC TNM staging system for gastric cancer: results of a Chinese single-institution study of 1, 503 patients[J]. Ann Surg Oncol, 2011, 18: 1060-1067. DOI:10.1245/s10434-010-1424-2 |
| [9] |
李海彬, 李霞, 王安心, 陶丽新, 刘龙, 陈斯鹏, 等. 竞争风险模型及其在Stata软件实现[J]. 中国卫生统计, 2016, 33: 889-891, 895. |
| [10] |
聂志强, 欧艳秋, 曲艳吉, 袁海云, 刘小清. 临床生存数据新视角: 竞争风险模型[J]. 中华流行病学杂志, 2017, 38: 1127-1131. DOI:10.3760/cma.j.issn.0254-6450.2017.08.026 |
| [11] |
杨建强. 影响胃癌术后5年生存率的因素分析[D]. 重庆: 重庆医科大学, 2020.
|
| [12] |
RILEY R D, ENSOR J, SNELL K I E, HARRELL F E, MARTIN G P, REITSMA J B, et al. Calculating the sample size required for developing a clinical prediction model[J/OL]. BMJ Clin Res Ed, 2020, 368: m441. DOI: 10.1136/bmj.m441.
|
| [13] |
王茂勋, 侯宏霖, 韩博涵, 郭娟, 韩黎丽, 陈小兵. 青年胃癌的临床病理特点及预后分析[J]. 河南医学研究, 2019, 28: 396-399. DOI:10.3969/j.issn.1004-437X.2019.03.004 |
| [14] |
WANG Z, XU J, SHI Z, SHEN X, LUO T, BI J, et al. Clinicopathologic characteristics and prognostic of gastric cancer in young patients[J]. Scand J Gastroenterol, 2016, 51: 1043-1049. DOI:10.1080/00365521.2016.1180707 |
| [15] |
SANTORO R, CARBONI F, LEPIANE P, ETTORRE G M, SANTORO E. Clinicopathological features and prognosis of gastric cancer in young European adults[J]. Br J Surg, 2007, 94: 737-742. DOI:10.1002/bjs.5600 |
| [16] |
金芝祥. 基于SEER数据分析术后辅助放化疗对进展期胃癌的预后影响[D]. 大连: 大连医科大学, 2019.
|
| [17] |
寇梦瑛, 王朝阳, 俸敏, 张相国, 王教成, 张群功, 等. 老年与中青年胃癌临床病理特征和预后影响因素的差异[J]. 广东医学, 2015, 36: 2691-2695. |
| [18] |
王学闽. 影响进展期胃癌预后和门静脉后淋巴结转移的相关因素分析[J/CD]. 临床医药文献电子杂志, 2020, 7: 64, 66.
|
| [19] |
谢怡, 叶劲松. 早期胃癌临床病理特征与淋巴结转移的关系及其对预后的影响[J]. 中国现代普通外科进展, 2020, 23: 866-869. |
| [20] |
王浩, 周岩冰, 牛兆建, 陈栋, 王东升, 吕亮, 等. 早期胃癌预后及复发转移因素分析[J]. 中华普通外科杂志, 2015, 30: 639-642. DOI:10.3760/cma.j.issn.1007-631X.2015.08.016 |
| [21] |
王贵娟, 李建彬. 胃癌辅助放疗研究现状与进展[J]. 中华肿瘤防治杂志, 2020, 27: 915-920. |
| [22] |
周宁, 杨咏强, 张力元, 田野. 中国胃癌术后辅助放疗的科学性与必要性[J]. 中华医学杂志, 2018, 98: 1629-1632. DOI:10.3760/cma.j.issn.0376-2491.2018.20.023 |
| [23] |
LIU W, DONG Z, HU R, WANG C. Association of vascular endothelial growth factor (VEGF) gene polymorphisms with gastric cancer and its development, prognosis, and survival[J/OL]. Technol Cancer Res Treat, 2018, 17: 1533034617753810. DOI: 10.1177/1533034617753810.
|
| [24] |
张晓杰, 赵东兵. 初诊胃癌肝转移患者预后模型的建立及风险分层[J/CD]. 消化肿瘤杂志(电子版), 2020, 12: 269-274.
|
 2021, Vol. 42
2021, Vol. 42


