2019年12月初,武汉发现多例原因不明肺炎患者,随后在1例来自武汉华南海鲜批发市场患者的支气管肺泡灌洗液样本中,利用宏基因组测序技术(metagenomic next-generation sequencing,mNGS)证明病原体是一种新型冠状病毒[1]。起初国内称其为2019新型冠状病毒,所致疾病称为新型冠状病毒肺炎。2020年2月11日国际病毒分类委员会(International Committee on Taxonomy of Viruses,ICTV)将病毒命名为严重急性呼吸综合征冠状病毒2(severe acute respiratory syndrome coronavirus 2,SARS-CoV-2)。这是继严重急性呼吸综合征冠状病毒(severe acute respiratory syndrome coronavirus,SARS-CoV)和中东呼吸综合征冠状病毒(Middle East respiratory syndrome coronavirus,MERS-CoV)之后,近年来发现的、冠状病毒科中能够感染人的第7种冠状病毒。WHO于2020年1月30日(当地时间)将此次SARS-CoV-2引起的新型冠状病毒肺炎疫情列为国际关注的突发公共卫生事件(Public Health Emergency of International Concern,PHEIC),并于近日将SARS-CoV-2引起的新型冠状病毒肺炎命名为coronavirus disease 2019(COVID-19)。截至2020年2月12日24时,国家卫生健康委员会官方网站数据显示COVID-19累计确诊病例达59 804例,死亡1 367例[2],并传播至全球20多个国家。我国已将COVID-19纳入《中华人民共和国传染病防治法》规定的乙类传染病,并按照甲类传染病采取预防和控制措施。本文就SARS-CoV-2的病原学特点及COVID-19的诊断、预防和治疗等进行讨论。
1 SARS-CoV-2病原学冠状病毒属于套式病毒目(Nidovirales)冠状病毒科(Coronaviridae)冠状病毒属(Coronavirus),是一类有包膜的单股正链RNA病毒[3]。基因组全长为30 kb,依次由5′-端非编码区、非结构蛋白开放阅读框(open reading frame,ORF)1a/b编码区、编码刺突糖蛋白(spike protein,S蛋白)的S区、编码包膜蛋白(envelope protein,E蛋白)的E区、编码膜蛋白(membrane protein,M蛋白)的M区、编码核衣壳蛋白(nucleocapsid protein,N蛋白)的N区及3′-端非编码区组成。其中,非结构蛋白ORF1a/b区编码的聚蛋白可被病毒的3C样蛋白酶(3C-like protease,3CLpro)和木瓜样蛋白酶(papain-like protease,PLpro)切割,形成病毒RNA依赖的RNA聚合酶(RNA-dependent RNA polymerase,RdRp)和解螺旋酶(helicase,Hel)等(图 1),指导病毒基因组复制、转录和翻译[4-5]。结构蛋白S可特异性地与宿主细胞的受体结合,是病毒入侵宿主易感细胞的关键蛋白[6]。M蛋白和E蛋白参与病毒包膜的形成,而N蛋白则参与病毒的装配[5](图 2)。

|
图 1 冠状病毒基因组结构及其编码蛋白 Fig 1 Genomic structure and its coded proteins of coronavirus A: SARS-CoV; B: MERS-CoV. SARS-CoV: Severe acute respiratory syndrome coronavirus; MERS-CoV: Middle East respiratory syndrome coronavirus; ORF1a/b: Open reading frame 1a/b; PLpro: Papain-like protease; 3CLpro: 3C-like protease; RdRp: RNAdependent RNA polymerase; Hel: Helicase; S: Spike protein; E: Envelope protein; M: Membrane protein; N: Nucleocapsid protein |
|
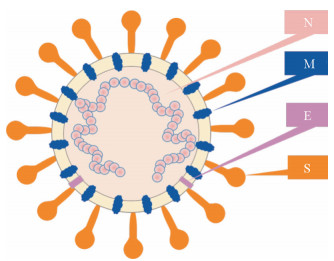
图 2 SARS-CoV-2结构蛋白 Fig 2 Structural proteins of SARS-CoV-2 SARS-CoV-2: Severe acute respiratory syndrome coronavirus 2; N: Nucleocapsid protein; M: Membrane protein; E: Envelope protein; S: Spike protein |
根据冠状病毒基因组结构和系统发生学分析,冠状病毒科可分为α、β、γ和δ 4个属,α和β属的冠状病毒一般感染哺乳类动物和人,γ和δ属的冠状病毒主要感染鸟类。此次SARS-CoV-2为β属的新型冠状病毒,为圆形或椭圆形,直径约60~140 nm,电镜下呈皇冠样形状[7]。除SARS-CoV-2外,尚有6种可感染人类的冠状病毒:人冠状病毒229E(human coronavirus 229E,HCoV-229E)、人冠状病毒OC43(human coronavirus OC43,HCoV-OC43)、人冠状病毒NL63(human coronavirus NL63,HCoV-NL63)、人冠状病毒HKU1(human coronavirus HKU1,HCoV-HKU1)、SARS-CoV和MERS-CoV。蛋白序列分析发现,SARS-CoV-2与SARS-CoV的7个保守的非结构蛋白氨基酸的相似度为94.6%,提示两者属于同一种类[8]。SARS-CoV-2基因组与蝙蝠SARS样冠状病毒(BatCoV RaTG13)的同源性达96%,推测蝙蝠可能是SARS-CoV-2的自然宿主[8-9]。采用β-CoV基因组中一个互补回文序列进行溯源分析,结果也证实SARS-CoV-2可能源自中华菊头蝠(Rhinolophus)[10]。
冠状病毒对热和紫外线较敏感,-80 ℃可保存数年,56 ℃下30 min可被灭活(实验室灭活SARS-CoV-2的最常用方法),75%乙醇、过氧乙酸和含氯消毒剂(氯己定除外)均能够有效灭活SARS-CoV-2[11]。
2 SARS-CoV-2致病性冠状病毒可引起人呼吸道感染或动物肠道感染,病毒侵染宿主细胞的过程需要宿主细胞膜表面受体的参与。冠状病毒表面的S蛋白可识别受体并与之结合,随后通过网格蛋白介导的内吞途径(clathrin-mediated endocytosis)侵入宿主细胞[12]。不同冠状病毒可利用不同的细胞受体来完成入侵,如HCoV-229E的受体是氨肽酶N(aminopeptidase N,也称CD13)[13],SARS-CoV的受体是血管紧张素转化酶2(angiotensin converting enzyme 2,ACE2)[14],而MERS-CoV的受体是二肽基肽酶4(dipeptidyl peptidase 4,DPP4,也称CD26)[15-16]。已有研究证明,氨肽酶N和DPP4均不是SARS-CoV-2的受体,而ACE2可作为其受体[8]。
HCoV-229E、HCoV-OC43、HCoV-NL63和HCoV-HKU1致病性较低,一般仅引起轻微的呼吸道症状。SARS-CoV和MERS-CoV则可分别引起严重急性呼吸综合征和中东呼吸综合征,曾暴发流行,症状重、病死率较高[17-19]。人群对SARS-CoV-2普遍易感,潜伏期一般为1~14 d,多为3~7 d;传染源主要是COVID-19患者,无症状感染者也可能成为传染源[11, 20-21];传播途径主要为呼吸道飞沫传播,接触沾染有病毒飞沫的物品也可被感染[11],此外,研究表明COVID-19患者粪便中可检出SARS-CoV-2核酸,提示SARS-CoV-2有可能通过粪-口途径经消化道传播[22]。
SARS-CoV-2引起的COVID-19主要表现为发热、干咳和乏力等症状,少数患者可伴有流涕、咽痛和腹泻,部分患者可出现呼吸困难,严重者可快速进展为急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)、出凝血功能障碍和脓毒症休克等[20-21]。从现有的治疗病例来看,轻型患者仅表现为低热、轻微乏力等,可无肺炎表现。多数患者预后良好,少数患者病情危重,老年人和有慢性基础疾病者预后较差[11]。
3 COVID-19检测诊断随着SARS-CoV-2的分离培养与基因组测序成功,目前确诊主要依靠qRT-PCR法检测SARS-CoV-2核酸基因。呼吸道标本或血液标本中SARS-CoV-2核酸阳性或病毒基因测序与已知的新型冠状病毒高度同源,可作为SARS-CoV-2感染的确诊标准[11]。采用胶体金技术和酶联免疫技术建立的IgM和IgG抗体检测试剂及SARS-CoV-2抗原检测试剂也已研发成功,目前不仅可作为科研试剂,也已用于辅助诊断。
4 COVID-19预防控制传染性疾病预防与控制的基本原则为消除传染源、切断传播途径和保护易感人群。疑似患者和确诊患者应与其他人群隔离,早期控制传染源,防止疫情迅速蔓延。SARS-CoV-2主要通过呼吸道飞沫传播和接触传播,采取必要的个人防护措施有助于控制疫情扩散。疫苗是保护易感人群的有效措施。在特异预防方面,目前尚无针对SARS-CoV-2的疫苗上市或临床试用,但数家国内外科研机构和企业正在采用诸如mRNA纳米疫苗技术、重组或灭活疫苗技术和DNA疫苗技术等多种途径进行SARS-CoV-2疫苗研发。
5 COVID-19临床治疗 5.1 对症及支持疗法目前对COVID-19患者主要采取对症治疗与支持疗法,包括治疗基础疾病、缓解症状,对内脏器官进行有效保护与支持治疗,积极防治并发症,必要时进行呼吸支持。临床上需注意维持患者的水和电解质平衡,维持内环境稳定,可根据患者呼吸困难程度和胸部影像学进展情况酌情短期内使用糖皮质激素[11]。
5.2 抗病毒治疗目前临床上尚无特异的抗SARS-CoV-2药物,较为高效的研究策略是“老药新用”,即在已批准上市的临床药物中筛选具有抗SARS-CoV-2潜能的药物[23]。美国吉利德(Gilead)公司用于治疗埃博拉病毒(Ebola virus)感染的在研药物瑞德西韦(remdesivir,GS-5734)是一种核苷类似物前药,能够抑制病毒RdRp从而发挥抗病毒作用[24],体外和动物模型中均已证实低剂量的瑞德西韦对SARS-CoV和MERS-CoV具有良好的抑制作用[25]。瑞德西韦具有完整的药物动力学实验结果和良好的安全性,可能是当前抗SARS-CoV-2感染肺炎最有希望的药物之一。最新研究表明瑞德西韦和氯喹在体外对SARS-CoV-2具有良好的抑制作用[26]。目前,在中日友好医院牵头下,瑞德西韦治疗COVID-19的Ⅲ期临床试验已于2020年2月5日正式在武汉市金银潭医院启动,其疗效正在等待严格的临床双盲试验验证。但是从治疗患者角度出发,可能采取“同情用药”的方式在患者中使用。
此外,根据《新型冠状病毒感染的肺炎诊疗方案(试行第五版)》,还可试用α-干扰素雾化吸入和洛匹那韦/利托那韦,或加用利巴韦林静脉注射[11]。
5.3 中医药治疗COVID-19属于中医疫病范畴,病因为感受疫戾之气,可根据初期(寒湿郁肺)、中期(疫毒闭肺)、重症期(内闭外脱)和恢复期(肺脾气虚)[11],对不同人群进行辨证论治。
迄今,在国家临床试验注册中心已登记了至少54项预防性、观察性和干预性药物研究,涉及多种中药和西药,如连花清瘟胶囊、氯喹和达芦那韦/考比司他等。
6 小结PHEIC的处置从来都不仅仅是医学问题,此次COVID-19的暴发流行再次证明生物安全是人类自身安全的重要组成部分。蝙蝠只是SARS-CoV-2的自然宿主,从自然宿主蝙蝠到人还应该有1~2个野生动物中间宿主,不善待野生动物就可能会受到大自然的惩罚。目前,COVID-19感染病例总数仍在增加,进一步消除传染源、切断传播途径、保护易感人群和实现早发现、早隔离、早治疗,有赖于临床医疗、公共卫生和基础研究专业人员形成合力,坚持把科研论文写在抗疫战场上,把科技成果应用到抗疫实践中,才能切实为疫情防控提供有力支撑。
志谢 本文由本人博士研究生朱耐伟协助整理,特此志谢。
| [1] |
WU F, ZHAO S, YU B, CHEN Y M, WANG W, SONG Z G, et al. A new coronavirus associated with human respiratory disease in China[D]. Nature, 2020. doi: 10.1038/s41586-020-2008-3.
|
| [2] |
中华人民共和国国家卫生健康委员会卫生应急办公室. 2020年2月12日新型冠状病毒感染的肺炎疫情情况[EB/OL]. (2020-02-13)[2020-02-13]. http://www.nhc.gov.cn/yjb/s7860/202002/26fb16805f024382bff1de80c918368f.shtml.
|
| [3] |
戚中田. 医学微生物学[M]. 3版. 北京: 科学出版社, 2014: 267-270.
|
| [4] |
VAN BOHEEMEN S, DE GRAAF M, LAUBER C, BESTEBROER T M, RAJ V S, ZAKI A M, et al. Genomic characterization of a newly discovered coronavirus associated with acute respiratory distress syndrome in humans[D]. mBio, 2012, 3. pii: e00473-12. doi: 10.1128/mBio.00473-12.
|
| [5] |
ZUMLA A, CHAN J F W, AZHAR E I, HUI D S, YUEN K Y. Coronaviruses-drug discovery and therapeutic options[J]. Nat Rev Drug Discov, 2016, 15: 327-347. DOI:10.1038/nrd.2015.37 |
| [6] |
MILLET J K, WHITTAKER G R. Host cell entry of Middle East respiratory syndrome coronavirus after twostep, furin-mediated activation of the spike protein[J]. Proc Natl Acad Sci USA, 2014, 111: 15214-15219. DOI:10.1073/pnas.1407087111 |
| [7] |
ZHU N, ZHANG D, WANG W, LI X, YANG B, SONG J, et al. A novel coronavirus from patients with pneumonia in China, 2019[D]. N Engl J Med, 2020. doi: 10.1056/NEJMoa2001017.
|
| [8] |
ZHOU P, YANG X L, WANG X G, HU B, ZHANG L, ZHANG W, et al. A pneumonia outbreak associated with a new coronavirus of probable bat origin[D]. Nature, 2020. doi: 10.1038/s41586-020-2012-7.
|
| [9] |
PARASKEVIS D, KOSTAKI E G, MAGIORKINIS G, PANAYIOTAKOPOULOS G, SOURVINOS G, TSIODRAS S. Full-genome evolutionary a nalysis of the novel corona virus (2019-nCoV) rejects the hypothesis of emergence as a result of a recent recombination event[D]. Infect Genet Evol, 2020, 79: 104212. doi: 10.1016/j.meegid.2020.104212.
|
| [10] |
陈嘉源, 施劲松, 丘栋安, 刘畅, 李鑫, 赵强, 等.武汉2019冠状病毒基因组的生物信息学分析[D].中国生物信息学杂志, 2020.(2020-01-21)[2020-02-07]. http://kns.cnki.net/KCMS/detail/23.1513.Q.20200120.0839.002.html.
|
| [11] |
国家卫生健康委员会, 国家中医药管理局.新型冠状病毒感染的肺炎诊疗方案(试行第五版)[S/OL]. (2020-02-04)[2020-02-07]. http://www.gov.cn/zhengce/zhengceku/2020-02/05/5474791/files/de44557832ad4be1929091dcbcfca891.pdf.
|
| [12] |
WANG H, YANG P, LIU K T, GUO F, ZHANG Y, ZHANG G, et al. SARS coronavirus entry into host cells through a novel clathrin- and caveolae-independent endocytic pathway[J]. Cell Res, 2008, 18: 290-301. DOI:10.1038/cr.2008.15 |
| [13] |
YEAGER C L, ASHMUN R A, WILLIAMS R K, CARDELLICHIO C B, SHAPIRO L H, LOOK A T, et al. Human aminopeptidase N is a receptor for human coronavirus 229E[J]. Nature, 1992, 357: 420-422. DOI:10.1038/357420a0 |
| [14] |
KUBA K, IMAI Y, RAO S, GAO H, GUO F, GUAN B, et al. A crucial role of angiotensin converting enzyme 2(ACE2) in SARS coronavirus-induced lung injury[J]. Nat Med, 2005, 11: 875-879. DOI:10.1038/nm1267 |
| [15] |
LU G, HU Y, WANG Q, QI J, GAO F, LI Y, et al. Molecular basis of binding between novel human coronavirus MERS-CoV and its receptor CD26[J]. Nature, 2013, 500: 227-231. DOI:10.1038/nature12328 |
| [16] |
WANG N, SHI X, JIANG L, ZHANG S, WANG D, TONG P, et al. Structure of MERS-CoV spike receptorbinding domain complexed with human receptor DPP4[J]. Cell Res, 2013, 23: 986-993. DOI:10.1038/cr.2013.92 |
| [17] |
闻玉梅. 冠状病毒的致病性及防控[J]. 微生物与感染, 2020, 15: 5-12. |
| [18] |
瞿涤, 陆路, 姜世勃. 中东呼吸综合征冠状病毒及其疫苗和特异性药物的研发[J]. 微生物与感染, 2015, 10: 200-207. |
| [19] |
YIN Y, WUNDERINK R G. MERS, SARS and other coronaviruses as causes of pneumonia[J]. Respirology, 2018, 23: 130-137. |
| [20] |
CHEN N, ZHOU M, DONG X, QU J, GONG F, HAN Y, et al. Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptive study[D]. Lancet, 2020. pii: S0140-6736(20)30211-7. doi: 10.1016/S0140-6736(20)30211-7.
|
| [21] |
CHANG D, LIN M, WEI L, XIE L, ZHU G, DELA CRUZ C S, et al. Epidemiologic and clinical characteristics of novel coronavirus infections involving 13 patients outside Wuhan, China[D]. JAMA, 2020. doi: 10.1001/jama.2020.1623.
|
| [22] |
HOLSHUE M L, DEBOLT C, LINDQUIST S, LOFY K H, WIESMAN J, BRUCE H, et al. First case of 2019 novel coronavirus in the United States[D]. New Engl J Med, 2020. doi: 10.1056/NEJMoa2001191.
|
| [23] |
LI G, DE CLERCQ E. Therapeutic options for the 2019 novel coronavirus (2019-nCoV)[D]. Nat Rev Drug Discov, 2020. (2020-02-10)[2020-02-13]. https://www.nature.com/articles/d41573-020-00016-0.
|
| [24] |
MULANGU S, DODD L E, DAVEY R T Jr, TSHIANI MBAYA O, PROSCHAN M, MUKADI D, et al. A randomized, controlled trial of Ebola virus disease therapeutics[J]. New Engl J Med, 2019, 381: 2293-2303. DOI:10.1056/NEJMoa1910993 |
| [25] |
SHEAHAN T P, SIMS A C, GRAHAM R L, MENACHERY V D, GRALINSKI L E, CASE J B, et al. Broad-spectrum antiviral GS-5734 inhibits both epidemic and zoonotic coronaviruses[D]. Sci Transl Med, 2017, 9. pii: eaal3653. doi: 10.1126/scitranslmed.aal3653.
|
| [26] |
WANG M, CAO R, ZHANG L, YANG X, LIU J, XU M, et al. Remdesivir and chloroquine effectively inhibit the recently emerged novel coronavirus (2019-nCoV) in vitro[D]. Cell Res, 2020. doi: 10.1038/s41422-020-0282-0.
|
 2020, Vol. 41
2020, Vol. 41


