随着产前超声检查的普及,胎儿期肾积水的检出率大大提高[1],如今已成为胎儿检出率第一的泌尿系统畸形。导致胎儿肾积水最常见的原因是肾盂输尿管连接部梗阻(ureteropelvic junction obstruction,UPJO),早期诊断能够使一部分严重梗阻的患儿尽早接受手术治疗,解除梗阻、缓解肾内压力,避免患肾功能进一步受损。离断式肾盂成形术是目前公认的治疗UPJO的手术方式,无论是开放、腹腔镜、后腹腔镜还是机器人手术,其手术成功率均超过90%[2-4],尽管如此,仍有5%~10%的患者术后因再次梗阻导致积水进一步增大或出现发作性腹痛等并发症需接受再次手术[5-7]。本研究回顾分析了2015年1月至2017年12月我科收治的因肾盂成形术后再梗阻而接受手术的UPJO患儿资料,总结归纳再梗阻的原因及发病特点,以期对减少肾盂成形术后再梗阻起到一定提示作用。
1 资料和方法 1.1 一般资料选取2015年1月至2017年12月我科收治的肾盂成形术后需再次手术的UPJO患儿共36例。纳入标准:患儿因UPJO已接受过1次肾盂成形手术;患儿术后出现肾积水较手术前进行性增大,或出现反复泌尿系感染和(或)患侧腰腹部疼痛、严重尿液外渗等并发症,考虑系再梗阻导致。排除标准:首次术后即明确存在患侧输尿管下端狭窄,计划行二期再植手术;合并同侧膀胱输尿管反流;患肾功能基本丧失需接受肾切除术;术后出现双J管引流不畅或滑脱等短期内并发症,需要重新置管。
36例患儿中,男30例、女6例,左侧27例、右侧9例。首次手术中位年龄为0.50岁(20 d~8.28岁);首次手术方式:腹腔镜肾盂成形术7例,开放离断式肾盂成形术24例,一期行肾造瘘术、二期行开放离断式肾盂成形术5例;首次手术原因:单纯分肾功能(differencial renal function, DRF)受损或进行性下降28例,间歇性患侧腰腹部疼痛伴积水增大6例,肾积水伴泌尿系感染2例;首次术后诊断:肾盂输尿管连接部单纯性狭窄34例,输尿管息肉1例,肾盂输尿管连接部狭窄伴高位输尿管开口1例;首次手术医院:我院8例,外院28例。
15例再梗阻患儿中表现为动态复查泌尿系B超提示术后(如前次手术留置双J管,则为拔管后)患侧肾积水进行性增大,患儿无不适主诉。9例术后出现不同程度的患侧腰腹部疼痛,严重者伴有呕吐,术后首次疼痛发作最早出现于拔除双J管当天,最晚于术后50个月,其中1例患儿拔除双J管后出现腹痛伴尿外渗。3例患儿首次术中留置肾造瘘管,术后夹闭造瘘管发现积水进行性增大,且经造瘘管注入造影剂提示肾盂扩张、输尿管不显影。9例患儿术后出现反复泌尿系感染伴积水不降或增大,其中1例合并真菌感染。
1.2 治疗方式36例患儿中,2例术中发现肾盏颈闭锁而行肾盏颈成形+输尿管肾下盏吻合术,其余34例均接受开放离断式肾盂成形术。再次接受肾盂成形术的时间距首次手术中位间隔为7.68个月,最短为术后4.3个月,最长于首次术后5.58年。
1.3 随访所有患儿再次手术时均留置双J管1根,术后4~8周来院拔除双J管,此后规律复查超声,术后6个月复查肾动态显像。随访截至2019年2月,术后中位随访时间为28(15~49)个月。以患侧无腰腹部疼痛发作伴肾积水增大、无反复泌尿系感染,超声检查提示患侧肾盂分离较术前减小表明手术成功。
1.4 统计学处理应用SPSS 19.0软件进行统计学分析。计数资料以例数和百分数表示;计量资料以中位数(范围)描述,采用Wilcoxon符号秩检验。检验水准(α)为0.05。
2 结果根据再次手术术中所见,分析肾盂成形术后造成梗阻的原因,吻合口水肿增厚、周围粘连与纤维化瘢痕形成导致再梗阻的比例最高(26例,72.22%),其次是吻合口旁或肾盂壁息肉(5例,13.89%)及高位输尿管开口(5例,13.89%)。比较少见输尿管原因包括首次手术遗漏迷走血管压迫输尿管(3例,8.33%)、吻合口远端输尿管狭窄(2例, 5.56%)和首次手术将肾下盏颈闭合(2例,5.56%)。有7例患儿同时存在2种梗阻原因。
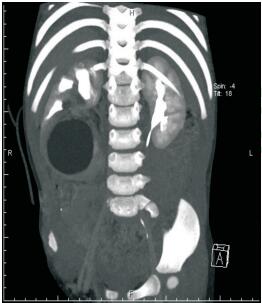
3例迷走血管压迫输尿管及2例肾下盏颈闭锁(图 1)造成再梗阻的患儿,首次手术均采用开放肾盂成形术。2例首次手术未发现吻合口远端输尿管存在狭窄段患儿,首次手术均采用开放肾盂成形术+肾造瘘术,且术中未留置双J管。
|
图 1 计算机断层扫描检查提示右肾下盏盏颈闭锁导致局限性肾积水增大 |
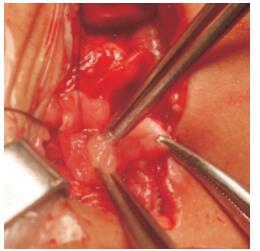
共有18例患儿于再次手术前留置肾造瘘管引流,1例留置双J管,1例同时留置双J管及肾造瘘管。19例再次手术前带肾造瘘管作为外引流患儿中,4例再梗阻原因为吻合口旁或肾盂壁息肉(图 2),术前带管时间分别为68、113、138、176 d。17例术前未造瘘患儿中,仅1例再梗阻系息肉导致。所有由息肉导致再梗阻的患儿,首次手术造成UPJO的原因均非息肉所致。
|
图 2 再手术见吻合口旁肾盂壁息肉 |
随访至2019年2月,36例患儿中34例无再诉患侧腰腹部疼痛,无反复上尿路感染发生。1例肾下盏颈闭锁患儿术后复查超声提示积水进行性增大,并且经上盏造瘘管造影提示下盏及输尿管未显影,遂于术后8个月再次行肾盏颈成形+输尿管肾下盏吻合术,术后诊断:上、下盏间及输尿管肾盏颈吻合口均再次闭锁。1例吻合口瘢痕形成患儿术后30个月再次出现患侧腰腹部疼痛伴呕吐,同时超声检查显示肾积水明显增加,第3次行肾盂成形术,提示前次吻合口再次瘢痕性狭窄。上述2例患儿第3次术后随访37个月和20个月,无再次梗阻表现。患儿再手术术前中位DRF为26.82%(4.36%~46.45%),再手术术后中位DRF为33.97%(19.50%~44.02%),再手术后患儿DRF较术前提高,差异有统计学意义(P=0.001)。
3 讨论Anderson和Hynes[8]于1949年首次报道了离断肾盂输尿管连接部的手术方式,目前Anderson-Hynes离断式肾盂成形术已成为治疗各种输尿管腔内外因素引起的UPJO的标准术式,其具有术后再狭窄发生率低的优势。经过数十年的发展,腹腔镜、后腹腔镜、机器人辅助下的肾盂成形术相继开展,各个中心手术技术日趋成熟。即便如此,术后5%~10%的再狭窄发生率[5-7]仍然是一个无法回避的问题。随着产前诊断的普及和规范化,越来越多的肾积水在胎内即被检出,肾积水患儿手术的年龄也越来越小[9-10]。如何避免再梗阻的发生及二次手术对患者,尤其是小年龄患儿的伤害,是每个泌尿外科医师需要思考的问题。
肾盂成形术后再梗阻最常见的原因为吻合口周围粘连、纤维化瘢痕性形成或水肿增厚引起的再狭窄,该原因在本组患儿中占72.22%(26/36)。尿外渗被认为是引起吻合口周围粘连的重要原因之一[11]。渗出的尿液导致吻合口周围组织产生无菌性炎症和组织纤维化,从而进一步加重吻合口的梗阻。对于术后留置肾外引流管的患儿,如出现尿外渗,通常的做法是延长引流时间直至无尿液引流出。当患儿出现发热、腹胀、呕吐等急性梗阻表现时,处理尿外渗及尿液囊肿需要更积极的手段,包括重新置入双J管、经皮肾穿刺造瘘等。本组1例患侧腰腹部疼痛合并尿外渗的患儿于症状出现当日先行肾穿刺造瘘术,后经造影检查提示吻合口梗阻,再次行肾盂成形术。
如果说吻合口粘连、瘢痕尚不能完全避免,更值得引起重视的是一些首次手术时如加以注意可避免再手术的情况。例如首次手术仅解除了肾盂输尿管连接部狭窄,而遗漏了压迫肾下极或输尿管的迷走血管,或遗漏了肾盂输尿管连接部远端输尿管仍有狭窄的情况。Asensio等[12]在其研究中也指出,迷走血管压迫在再手术原因中占重要地位且影响预后。本组再手术患儿中,所有合并迷走血管和吻合口远端狭窄的患儿首次手术均采用开放肾盂成形术的方式。开放小切口肾盂成形术在儿童是非常成熟的手术方式,由于儿童的组织游离度大,手术操作时可将肾盂输尿管连接部提到体外操作,为小切口手术创造了条件,但一味地追求小切口可能带来术野显露不足的问题。这提示在采用开放肾盂成形术时,应注意是否合并迷走血管压迫。部分患儿除肾盂输尿管连接部外,下段输尿管仍有狭窄,肾盂成形时应保证在肾盂与输尿管最宽敞处吻合。虽然无管化因其能减轻患者负担且不增加术后狭窄的风险被越来越多地采用[13-14],但在术中试插双J管或向输尿管远端注水以保证远端通畅性仍有其必要性。
此外,在首次手术的操作方面,需要术者留意的是未将输尿管吻合在肾盂最低点而造成高位输尿管引起再梗阻,或过度裁剪肾盂以至于缝合时将下盏颈闭合的情况。在肾外型肾盂较大的患儿中,开放小切口手术可能无法保证吻合口位于肾盂最低点,从而导致高位输尿管的发生。本组5例吻合口位置偏高的患儿,4例首次手术时采用了开放肾盂成形术的方式。术中适当延长切口充分暴露或是采用腹腔镜下或机器人肾盂成形术可以避免上述情况的发生。过度裁剪肾盂是造成肾盏颈闭锁的主要原因,表现为局限的肾盏严重扩张,这种扩张和整个肾盂及其他肾盏的扩张程度完全不相符。该类病例往往在首次手术时将肾盂过度裁剪,再次手术时则没有可供缝合的肾盂,此时要考虑肾盏输尿管吻合术,同时要保证各个肾盏之间相通。这提示我们在首次手术时,即便是较大的肾外型肾盂,最好也先通过牵引线悬吊,在靠近输尿管处的肾盂剪开小口,探查清楚各个肾盏开口位置后再做裁剪。部分患者肾下盏的出口位置很低,在距离肾盂输尿管连接处较远的位置做裁剪很容易误伤,术中如果没有留意,术后肾盏出口缝合闭锁,将会造成局部积水的明显增大。
吻合口及吻合口旁息肉形成在既往文献中少有提及,我们认为引起再梗阻的息肉可能与留置肾造瘘管有关。本组5例术后证实为息肉引起再梗阻的患儿,首次手术中发现造成UPJO的原因均非息肉,而其中4例均于首次肾盂成形术中同时留置肾造瘘管,造瘘管留置中位时间为125.5 d,最短68 d,提示医源性息肉的生长和造瘘管的刺激有关且生长迅速。医源性息肉病理结构与原发性息肉相同,但从大体标本上看,与原发性息肉多见细条状不同,医源性息肉多为宽基底。在处理医源性息肉时,注意要将息肉生长的黏膜组织一并切除,以减小息肉复发的可能性[15]。医源性息肉的实际发生概率可能更高,有些送检标本镜下见到息肉的组织学改变,但在大体上我们并未看到息肉,这些可能是息肉的早期状态。因此,在首次肾盂成形术时如需留置肾造瘘管,建议将造瘘管头端尽量远离吻合口;如术后因再梗阻行肾穿刺造瘘术,也建议尽量缩短带管时间,这样也许可减少息肉发生的概率。
肾盂成形术后再梗阻在儿童患者中最常用的处理手段是再次行肾盂成形术,开放手术效果明确,成功率接近100%。腹腔镜[2, 16-17]或机器人[6, 12, 18]辅助再次肾盂成形术也有78%~100%的成功率。在部分排除息肉、迷走血管压迫等原因的单纯再狭窄患者中,内镜下治疗也有一定疗效[19-20]。尽管如此,避免再梗阻的发生仍然是摆在术者面前的主要课题。大多数情况下,肾盂成形术后吻合口再狭窄与手术技术不一定有关,但上述遗漏诊断或误将肾盏颈闭合的情况,在首次手术时如多加注意完全可以避免。
综上所述,吻合口狭窄是肾盂成形术后再手术的最主要原因。但更值得注意的是一些少见、在首次手术中可避免的情况,如迷走血管压迫、合并吻合口远端输尿管狭窄、输尿管高位开口及肾盏颈闭锁。息肉引起的再梗阻可能与二次术前留置肾造瘘管有关,因此尽量缩短带管时间,造瘘管头端尽量远离吻合口或许可减少医源性息肉的发生。
| [1] |
LIU D B, ARMSTRONG W R 3rd, MAIZELS M. Hydronephrosis:prenatal and postnatal evaluation and management[J]. Clin Perinatol, 2014, 41: 661-678. DOI:10.1016/j.clp.2014.05.013 |
| [2] |
ABDEL-KARIM A M, FAHMY A, MOUSSA A, RASHAD H, ELBADRY M, BADAWY H, et al. Laparoscopic pyeloplasty versus open pyeloplasty for recurrent ureteropelvic junction obstruction in children[J/OL]. J Pediatr Urol, 2016, 12: 401.e1-401.e6. doi: 10.1016/j.jpurol.2016.06.010.
|
| [3] |
MINNILLO B J, CRUZ J A, SAYAO R H, PASSEROTTI C C, HOUCK C S, MEIER P M, et al. Long-term experience and outcomes of robotic assisted laparoscopic pyeloplasty in children and young adults[J]. J Urol, 2011, 185: 1455-1460. DOI:10.1016/j.juro.2010.11.056 |
| [4] |
李凌, 高小峰, 王林辉, 刘敏, 彭泳涵, 叶华茂, 等. 机器人辅助腹腔镜与输尿管软镜杂交手术治疗肾盂输尿管连接部梗阻合并肾结石[J]. 第二军医大学学报, 2015, 36: 212-215. LI L, GAO X F, WANG L H, LIU M, PENG Y H, YE H M, et al. Concomitant hybrid robotic-assistant laparoscopic pyeloplasty and flexible ureteroscopy for ureteropelvic junction obstruction combined with renal stones[J]. Acad J Sec Mil Med Univ, 2015, 36: 212-215. |
| [5] |
HELMY T E, SARHAN O M, HAFEZ A T, ELSHERBINY M T, DAWABA M E, GHALI A M. Surgical management of failed pyeloplasty in children:single-center experience[J]. J Pediatr Urol, 2009, 5: 87-89. DOI:10.1016/j.jpurol.2008.09.001 |
| [6] |
JACOBSON D L, SHANNON R, JOHNSON E K, GONG E M, LIU D B, FLINK C C, et al. Robot-assisted laparoscopic reoperative repair for failed pyeloplasty in children:an updated series[J]. J Urol, 2019, 201: 1005-1011. DOI:10.1016/j.juro.2018.10.021 |
| [7] |
SWEARINGEN R, AMBANI S, FAERBER G J, BLOOM D A, WOLF J S Jr. Definitive management of failure after pyeloplasty[J]. J Endourol, 2016, 30(Suppl 1): S23-S27. |
| [8] |
ANDERSON J C, HYNES W. Retrocaval ureter; a case diagnosed pre-operatively and treated successfully by a plastic operation[J]. Br J Urol, 1949, 21: 209-214. DOI:10.1111/j.1464-410X.1949.tb10773.x |
| [9] |
KAWAL T, SRINIVASAN A K, SHRIVASTAVA D, CHU D I, VAN BATAVIA J, WEISS D, et al. Pediatric robotic-assisted laparoscopic pyeloplasty: does age matter?[J/OL]. J Pediatr Urol, 2018, 14: 540.e1-540.e6. doi: 10.1016/j.jpurol.2018.04.023.
|
| [10] |
BAEK M, SILAY M S, AU J K, HUANG G O, ELIZONDO R A, PUTTMANN K T, et al. Does the use of 5 mm instruments affect the outcomes of robotassisted laparoscopic pyeloplasty in smaller working spaces? A comparative analysis of infants and older children[J/OL]. J Pediatr Urol, 2018, 14: 537.e1-537.e6. doi: 10.1016/j.jpurol.2018.06.010.
|
| [11] |
OZAYAR A, MORGAN M S, FRIEDLANDER J I, SAUMUR M, KRISHAN G, GAHAN J C, et al. Prompt management of anastomotic leak or acute obstruction after minimally invasive pyeloplasty with percutaneous nephrostomy preserves outcomes[J]. J Urol, 2014, 192: 1716-1719. DOI:10.1016/j.juro.2014.06.041 |
| [12] |
ASENSIO M, GANDER R, ROYO G F, LLORET J. Failed pyeloplasty in children: is robot-assisted laparoscopic reoperative repair feasible?[J/OL]. J Pediatr Urol, 2015, 11: 69.e1-6. doi: 10.1016/j.jpurol.2014.10.009.
|
| [13] |
LISS Z J, OLSEN T M, ROELOF B A, STEINHARDT G F. Duration of urinary leakage after open non-stented dismembered pyeloplasty in pediatric patients[J]. J Pediatr Urol, 2013, 9: 613-616. DOI:10.1016/j.jpurol.2012.06.002 |
| [14] |
BILEN C Y, BAYAZIT Y, GÜDELOĞLU A, ABAT D, INCI K, DORAN S. Laparoscopic pyeloplasty in adults:stented versus stentless[J]. J Endourol, 2011, 25: 645-650. DOI:10.1089/end.2010.0401 |
| [15] |
LIN H, XU M, JIANG D, XU G, FANG X, HE L, et al. Latrogenic fibroepithelial polyps in children with hydronephrosis[J]. Urology, 2017, 104: 172-174. DOI:10.1016/j.urology.2017.02.007 |
| [16] |
MOSCARDI P R, BARBOSA J A, ANDRADE H S, MELLO M F, CEZARINO B N, OLIVEIRA L M, et al. Reoperative laparoscopic ureteropelvic junction obstruction repair in children:safety and efficacy of the technique[J]. J Urol, 2017, 197: 798-804. DOI:10.1016/j.juro.2016.10.062 |
| [17] |
NISHI M, TSUCHIDA M, IKEDA M, MATSUDA D, IWAMURA M. Laparoscopic pyeloplasty for secondary ureteropelvic junction obstruction:long-term results[J]. Int J Urol, 2015, 22: 368-371. DOI:10.1111/iju.12686 |
| [18] |
DAVIS T D, BURNS A S, CORBETT S T, PETERS C A. Reoperative robotic pyeloplasty in children[J/OL]. J Pediatr Urol, 2016, 12: 394.e1-394.e7. doi: 10.1016/j.jpurol.2016.04.045.
|
| [19] |
任吉忠, 徐丹枫, 姚亚成, 刘玉杉, 高轶, 阴雷, 等. 输尿管狭窄疑难病例的输尿管肾镜硬镜下处理技巧[J]. 第二军医大学学报, 2007, 28: 871-874. REN J Z, XU D F, YAO Y C, LIU Y S, GAO Y, YIN L, et al. Management skills of intractable ureterostenosis under ureteroscope[J]. Acad J Sec Mil Med Univ, 2007, 28: 871-874. DOI:10.3321/j.issn:0258-879x.2007.08.014 |
| [20] |
ELMUSSAREH M, TRAXER O, SOMANI B K, BIYANI C S. Laser endopyelotomy in the management of pelviureteric junction obstruction in adults:a systematic review of the literature[J]. Urology, 2017, 107: 11-22. DOI:10.1016/j.urology.2017.04.018 |
 2020, Vol. 41
2020, Vol. 41


