2. 上海海事大学信息工程学院计算机科学系, 上海 201306
2. Department of Computer Science, Institute of Information Engineering, Shanghai Maritime University, Shanghai 201306, China
随着超声分辨率的提高及相关新技术的发展,超声检查在骨骼肌肉系统疾病中的应用越来越多,其因高分辨率、实时动态、经济便捷等优势成为临床超声实践中的研究热点[1]。外伤、体育运动、体力劳动等均可导致不同类型、不同程度的肌肉损伤,10~12 MHz的高频率探头可明确肌肉损伤的细微结构和血流改变,提供更多疾病信息,对筛查肌肉损伤具有重要价值[2-3]。
我们前期通过离体动物实验已证实肌肉损伤的超声图像一致性判读会受到不同检查者的主观影响,且已证实超声图像纹理分析技术在猪横纹肌损伤模型的纹理识别中具备定量诊断能力[4]。借鉴计算机辅助超声图像定量分析技术提取基于人肌肉损伤后肌纹理结构的定量参数,可望为肌肉损伤的定量诊断提供一种有价值的评价方法[5-6]。本研究拟从人上臂肌肉急性挫伤后的高频二维超声图像入手,利用纹理特征分解技术提取其表征纹理分布的均匀性、方向性、周期性等纹理数学几何特征,探讨所选取的肌肉高频超声二维图像纹理特征能否提高对临床肌肉挫伤的定量诊断价值。
1 对象和方法 1.1 研究对象入选对象为2018年1月至2018年12月在海军军医大学(第二军医大学)长征医院超声科进行健康体检的10名男性健康志愿者和同期临床诊断为上臂肌肉单纯急性挫伤的10例男性患者。10名男性健康志愿者年龄为(32.7±4.3)岁,BMI为(23.3±0.5)kg/m2,均无上臂创伤及其他先天性、代谢性肌肉疾病史。10例男性上臂肌肉单纯急性挫伤患者(外伤史短于3 d,排除肌肉断裂、撕裂等严重情况)年龄为(31.2±3.8)岁,BMI为(22.5±0.7)kg/m2。所有受检者均为右利手。两组年龄、BMI等基线资料差异均无统计学意义(P均 > 0.05),具有可比性。所有研究对象均经过医院伦理委员会专家论证,均签署知情同意书。
1.2 超声仪器及检查方法采用高频彩色多普勒超声诊断仪(Philips iU22型,荷兰飞利浦公司)对患者进行肱二头肌肌腹高频超声检查,匹配L12-5型探头(高频探头频率为10~12 MHz)。上臂肌肉急性挫伤患者均采取仰卧位,保持患肢水平置于身体侧方,此时上臂肌肉处于放松的舒张状态,对受损肌肉进行连续多切面动态扫查,采集受损肌肉沿肌束走行的最大纵切面高频超声二维图像。整个扫查过程以探头垂直贴于肌肉表面,保持适度接触但不施压,放置角度无倾斜。调节机器系统参数为灰阶增益值70 dB,压缩55%,时间增益0补偿,聚焦深约1.0~2.5 cm,热指数0.1,机械指数0.6。健康志愿者检查体位和方法与上臂肌肉急性挫伤患者相同。
1.3 图像处理与定量分析(1)上臂肌肉急性挫伤患者:于脱机状态下采用Matlab 7.0图像处理软件(美国MathWorks公司)选取感兴趣区(region of interest,ROI)。选取同一图像上的同深度、同大小、同形状的肌纹理正常ROI(ROI1)和肌纹理疑似损伤ROI(ROI2),每个ROI重复取样60像素×60像素3次,共计30个取样,提取纹理灰度值的平均值(Mean)、灰度值的标准差(standard deviation,SDev)、纹理基元数量的密致性(number of blobs,NOB)、纹理基元形状的不规则度(irregularity,IRGL)、纹理基元的平均大小(size of blobs,SOB)、纹理分布的均匀性(homogeneity of distribution,HOD)、纹理分布的方向性(directionality of distribution,DOD)和纹理分布的周期性(periodicity of distribution,POD)8个纹理特征参数[5],用超声回波强度界面多级分解法自动计算任意ROI2相对于任意ROI1之间8个纹理特征的相似度差值(ΔROI2-1)。(2)健康志愿者:选择与患者挫伤肌肉同部位的正常肌肉进行扫查,采集该处肌肉最大纵切面高频超声二维图像,采用Matlab 7.0软件选取每名健康志愿者同深度、同大小、同形状的肌纹理清晰的正常ROI(ROI1),每个ROI重复取样60像素×60像素3次,共计30个取样,用超声回波强度界面多级分解法自动计算任意两个ROI1之间上述8个纹理特征的相似度差值(ΔROI1-1)。
1.4 统计学处理应用SPSS 17.0软件进行统计学分析。各组ROI区提取的纹理参量的相似度差值以x±s表示,采用独立样本t检验进行比较。检验水准(α)为0.05。
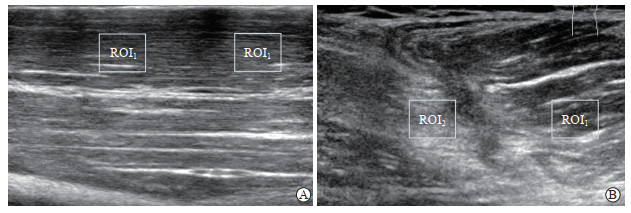
2 结果 2.1 高频超声表现健康志愿者上肢肌肉高频超声表现一致,肌纤维束呈中等回声,连续性好,层次分明,肌纤维束和高回声肌内膜/肌束膜构成的特定网络样纹理结构清晰(图 1A)。上肢肌肉急性挫伤患者在就诊当天其肌肉高频超声表现不同,肌肉局部损伤区ROI2内肌纤维回声较周边肌纹理正常区ROI1回声变化显著,回声强度增高,连续性中断,肌纹理网络样结构模糊(图 1B)。
|
图 1 健康志愿者和急性上臂肌肉挫伤患者上臂肌肉高频超声二维图像 Fig 1 Two-dimensional high-frequency ultrasonograms of upper limb muscles of healthy volunteers and patients with acute upper limb muscle contusion A: Two-dimensional high-frequency ultrasonogram of normal upper limb muscles of healthy volunteers showed clear muscle texture and homogeneous echo texture (ROI1 represents normal region); B: Two-dimensional high-frequency ultrasonograms of the injured region of acute upper limb muscle contusion patients showed discontinuous layers of local muscle fiber structure, fuzzy texture, increased echo level and non-uniformity (ROI2 represents contusion region, and ROI1 represents normal region) |
2.2 超声纹理特征的定量分析
计算机自动检测出10例急性上臂肌肉急性挫伤患者肌纹理疑似损伤ROI和肌纹理正常ROI之间8个纹理特征的相似度差值(ΔROI2-1)和10名健康志愿者任意两个ROI之间8个纹理特征的相似度差值(ΔROI1-1)。统计学分析发现,急性上臂肌肉挫伤患者疑似损伤ROI和肌纹理正常ROI之间5个纹理特征(IRGL、DOD、POD、Mean和SDev)的相似度差值(ΔROI2-1)与健康志愿者上臂同部位正常肌肉该5个纹理特征相似度差值(ΔROI1-1)差异均有统计学意义(P均 < 0.01)。见表 1。
|
|
表 1 健康志愿者和急性上臂肌肉挫伤患者上臂肌肉8个纹理特征相似度差值比较 Tab 1 Comparison of similarity difference values of eight texture features between healthy volunteers and patients with acute upper limb muscle contusion |
3 讨论 3.1 肌肉高频超声检查的优势
无创性、多模式的高频超声成像在肌肉损伤影像诊断中具有组织分辨率高、实时便携、检查效率高、能够节约检查成本等优势,现已被作为临床诊断肌肉损伤、疼痛及功能障碍的首选检查手段[7-9]。正常上臂肌肉属于横纹肌,在横切面上,肌肉内的深筋膜所形成的高回声网络连续,但筋膜回声呈断续的短线或斑点状高回声,可显示肌群之间的分界;而肌肉低回声与筋膜高回声所形成的独特肌肉超声纹理,则在沿肌束长轴的纵切面上具有更清晰的特有纹理表现[10]。
肌肉受到不同损伤类型和不同程度的损伤后,在超声图像上表现为肌纹理发生相应改变,结构模糊不清等[11]。席占国等[12]研究表明高频超声较MRI更能清晰地显示受损肌肉的形态走行及内部纹理模糊等改变,其对肌肉断裂的诊断结果与MRI检查结果相一致。本研究发现,正常上臂肌肉纹理表现为低回声的肌束与强回声的肌束膜相间的线状或轻度网络样排列,而急性上臂肌肉挫伤局部损伤区内肌纤维回声较周边肌纹理正常区回声强度增高,连续性中断,肌纹理网络样结构模糊,其高频超声图像特征与正常肌组织显著不同。
3.2 计算机辅助肌肉超声图像纹理分析的应用价值我们前期研究通过离体动物模型发现,不同技术等级的超声科医师均能够独立判断肌肉受到不同物理和化学因素损伤后的超声图像改变,然而定性描述易受检查医师主观经验的影响,导致诊断差异[4]。长期从事肌肉超声诊断的超声科医师虽然操作手法熟练,能够对典型超声图像特征如损伤区肌肉的边界、形态、回声强度、回声均匀性和肌理清晰度等得出较一致的诊断结论,但这种人工肉眼判图模式高度依赖操作者的技术水平,若仅依靠主观语言描述其图像特点或人工测量受损肌肉的厚度,难以准确、客观地全面反映肌肉纤维形态结构的超声图像纹理,可能导致不同超声科医师对同一张图像或同一位超声科医师在不同条件下读图时因各自操作习惯和视觉敏锐度的差异造成不同诊断结果。
目前,计算机辅助医学图像处理已被广泛应用于各学科的基础或临床分析。肌肉损伤因病因、病情不同可导致肌肉超声图像上显示特定的纹理变化,需要采取一种自动化、智能化的定量识别方法丰富超声诊断体系[13]。纹理分析是超声组织定征的重要手段,近年来有学者曾应用ImageJ(v.148)软件提取并比较肌萎缩性侧索硬化患者和健康对照超声图像上四肢肌群灰度共生矩阵参数的差异,发现该参数与肌肉的回波强度和厚度等指标均有望成为肌肉超声定量诊断中新的结构参数,最佳AUC可达90%以上[14]。另有学者通过提取股四头肌超声图像纹理参数平均值、偏度、峰度、反差分矩、熵和角度二次矩定量评估老化肌肉的形态改变[15]。笔者在前期离体模型、动物实验中已证实不同理化因素可导致超声图像上横纹肌纹理发生特征性改变[10, 16],这种图像改变可进一步借助可视化、敏锐度高的计算机视觉予以智能识别并进行统计学分析。本研究采用的超声回波强度界面多级分解法是笔者基于对超声图像灰度和空间尺度进行结构化分解的多尺度斑块特征(multiscale blob feature,MBF)而构建的纹理分析法,其在联合大规模纹理集上的正确分类率高达90%以上,显著高于同期其他分析法[17]。
本研究借鉴离体动物研究和动物实验的成功经验,针对人急性上臂肌肉挫伤出现的纹理消失和回声增强区进行了纹理特征参量的提取和定量分析,将定量指标与定性描述有机结合,尝试为临床提供全面的肌肉损伤超声影像信息[18]。由于肌肉组织本身具有各向异性,其超声图像表现与年龄、性别、生理状态等密切相关,故本研究在选择研究对象时,严格控制基本资料具有可比性。本研究结果表明,青年男性急性上臂肌肉挫伤患者肌肉局部损伤区内肌纤维回声与周边肌纹理正常区之间5个纹理特征(IRGL、DOD、POD、Mean和SDev)的相似度差值与健康青年男性志愿者上臂同部位正常肌肉纹理特征相似度差值差异有统计学意义(P均 < 0.01)。由于纹理分析多注重生物组织本身的声学参数、结构参数与组织状态间的相关关系,在肌肉高频超声图像上使用高斯核函数[19]多次从分辨率尺度和灰度级维度逐级进行滤波分解纹理图像[20],提取分解后的不同灰度级强度值的二值图像阵列,统计描述测得肌肉ROI内肌纤维基元规则度、周期性、方向性、平均超声回声强度值、回声强度差异性等纹理特征,可以作为区别正常区和挫伤区肌肉组织状态和性质的数学几何参量,具有定量诊断评估价值。
3.3 临床应用超声纹理分析方法定量评估肌肉急性挫伤的局限性及改进方向本研究基于超声图像回波强度界面多级分解法的基本思路,对急性上臂肌肉挫伤的肌肉纹理进行计算机定量检测分析和探讨,证实该纹理分析方法具有一定的应用价值,可以提取基于肌肉肌纹理结构的定量参数,有望成为对肌肉病损诊断与疗效评估的定量诊断评价方法。
然而,人体骨骼肌形态结构特征受很多因素影响。本研究作为计算机辅助肌肉纹理定量分析临床应用的初步尝试,仅选择了青年男性作为研究对象。此外,若单独分析每例患者的损伤区纹理变化绝对值,难以确保采图取样平面的一致性而造成统计结果的偏差。为了保持每例患者同一图片上提取纹理分析的可比性,本研究采取了纹理特征相似度相对差值作为统计量,更新Matlab软件的相关算法,提取同一超声图片上显示的任意纹理模糊区域和周边正常区域的纹理特征相似度差值(ΔROI2-1),与健康志愿者同部位上臂肌肉超声图片上任意两个正常区域的纹理特征相似度差值(ΔROI1-1)进行对比分析,避免了采图取样时因患者病情不同、超声图片不同、超声仪器参数设置不同而造成的差别。
下一步研究中,可纳入肥胖、年龄等其他影响因素进行更深入的对比分析,并对临床多种不同病损类型的肌肉纹理特征参量进行探讨,尤其是在如何把握各类肌肉病损类型中各个纹理参量所占的权重、如何确定适合所有类型病损中肌肉纹理的共同量化参数和相应的病理生理机制等方面,仍需要长期大样本量的深入学习和进一步阐明。
| [1] |
孙宏, 梁晓宁, 曹文, 卢瑞刚, 郭瑞君.肌肉骨骼超声应用进展[J/CD].中华医学超声杂志(电子版), 2015, 12: 21-24. http://www.cnki.com.cn/Article/CJFDTotal-ZHCD201501006.htm
|
| [2] |
高邓琴, 卢漫, 王硕华, 肖敏, 戴潇禹. 高频超声诊断肌肉损伤68例分析[J]. 实用医院临床杂志, 2014, 11: 148-150. |
| [3] |
WOODHOUSE J B, MCNALLY E G. Ultrasound of skeletal muscle injury:an update[J]. Semin Ultrasound CT MR, 2011, 32: 91-100. DOI:10.1053/j.sult.2010.12.002 |
| [4] |
赵佳琦, 章建全, 盛建国, 赵璐璐, 潘倩.不同技术级别超声医师对离体猪横纹肌理化损伤模型超声定性诊断的局限性分析[J/CD].中华医学超声杂志(电子版), 2014, 11: 763-769. http://www.cnki.com.cn/Article/CJFDTotal-ZHCD201409016.htm
|
| [5] |
ZHAO J, ZHANG J, XU Q, SHENG J, DIAO Z, LIU S. Quantitative evaluation of striated muscle injury by multiscale blob features method[J]. J Med Ultrason (2001), 2016, 43: 337-345. DOI:10.1007/s10396-016-0708-y |
| [6] |
DARBY J, HODSON-TOLE E F, COSTEN N, LORAM I D. Automated regional analysis of B-mode ultrasound images of skeletal muscle movement[J]. J Appl Physiol (1985), 2012, 112: 313-327. DOI:10.1152/japplphysiol.00701.2011 |
| [7] |
张栋.青少年颈痛患者颈后伸肌的肌骨超声表现特点及其相关性研究[D].北京: 北京中医药大学, 2016. http://cdmd.cnki.com.cn/Article/CDMD-10026-1016069019.htm
|
| [8] |
刘元石.非特异性下腰痛结筋病灶点经筋分布规律及超声下病变特点的研究[D].北京: 中国中医科学院, 2013. http://cdmd.cnki.com.cn/Article/CDMD-84502-1013311024.htm
|
| [9] |
刘华. 高频超声诊断肌肉损伤的临床应用价值分析[J]. 当代医学, 2016, 22: 44-45. |
| [10] |
赵佳琦, 章建全, 徐琪, 陈雁秋, 盛建国, 卢峰, 等.超声图像纹理分析技术对离体猪横纹肌理化损伤模型的定量研究[J/CD].中华医学超声杂志(电子版), 2013, 10: 674-680. http://www.cnki.com.cn/Article/CJFDTotal-ZHCD201308018.htm
|
| [11] |
周翔, 张青萍, 乐桂蓉. 肌肉高频超声成像及其纹理分析[J]. 中国超声医学杂志, 2001, 17: 70-72. |
| [12] |
席占国, 乔亚亚, 沈素红. 超声诊断肌肉损伤的临床价值[J]. 医药前沿, 2014(18): 206-207. |
| [13] |
PILLEN S, VAN KEIMPEMA M, NIEVELSTEIN R A, VERRIPS A, VAN KRUIJSBERGEN-RAIJMANN W, ZWARTS M J. Skeletal muscle ultrasonography:visual versus quantitative evaluation[J]. Ultrasound Med Biol, 2006, 32: 1315-1321. DOI:10.1016/j.ultrasmedbio.2006.05.028 |
| [14] |
MARTÍNEZ-PAYÁ J J, RÍOS-DÍAZ J, DEL BAÑO-ALEDO M E, TEMBL-FERRAIRÓ J I, VAZQUEZ-COSTA J F, MEDINA-MIRAPEIX F. Quantitative muscle ultrasonography using textural analysis in amyotrophic lateral sclerosis[J]. Ultrason Imaging, 2017, 39: 357-368. DOI:10.1177/0161734617711370 |
| [15] |
WATANABE T, MURAKAMI H, FUKUOKA D, TERABAYASHI N, SHIN S, YABUMOTO T, et al. Quantitative sonographic assessment of the quadriceps femoris muscle in healthy Japanese adults[J]. J Ultrasound Med, 2017, 36: 1383-1395. DOI:10.7863/ultra.16.07054 |
| [16] |
赵佳琦, 章建全, 赵璐璐, 宋家琳, 潘倩, 盛建国, 等.不同消融功率致兔骨骼肌急性微波热损伤修复的超声影像演变特征[J/CD].中华医学超声杂志(电子版), 2016, 13: 780-789. http://www.cnki.com.cn/Article/CJFDTotal-ZHCD201610016.htm
|
| [17] |
XU Q, WU H S, CHEN Y Q. Statistical multiscale blob features for classifying and retrieving image texture from large-scale databases[J/OL]. J Electron Imag, 2010, 19: 043006. doi: 10.1117/1.3491420.
|
| [18] |
MOLINARI F, CARESIO C, ACHARYA U R, MOOKIAH M R, MINETTO M A. Advances in quantitative muscle ultrasonography using texture analysis of ultrasound images[J]. Ultrasound Med Biol, 2015, 41: 2520-2532. DOI:10.1016/j.ultrasmedbio.2015.04.021 |
| [19] |
JAIN A K, FARROKHNIA F. Unsupervised texture segmentation using Gabor filters[J]. Pattern Recognition, 1991, 24: 1167-1186. DOI:10.1016/0031-3203(91)90143-S |
| [20] |
DELIBASIS K, UNDRILL P E, CAMERON G G. Designing texture filters with genetic algorithms:an application to medical images[J]. Signal Processing, 1997, 57: 19-33. DOI:10.1016/S0165-1684(96)00183-1 |
 2020, Vol. 41
2020, Vol. 41


