2. 南华大学附属第一医院肝胆外科, 衡阳 421001;
3. 暨南大学医学部生理学教研室, 广州 510632;
4. 海军军医大学(第二军医大学)东方肝胆外科医院麻醉科, 上海 200438
2. Department of Hepatobiliary Surgery, The First Affiliated Hospital of University of South China, Hengyang 421001, Hunan, China;
3. Department of Physiology, Faculty of Medical Science, Jinan University, Guangzhou 510632, Guangdong, China;
4. Department of Anesthesiology, Eastern Hepatobiliary Surgery Hospital, Naval Medical University(Second Military Medical University), Shanghai 200438, China
肝动脉-门静脉瘘(hepatic arterioportal fistula,HAPF)是指在先天性或后天性瘘因素作用下,肝动脉和门静脉2个系统的血流通过瘘口相互交通,其主要临床表现为门脉高压症[1]。创伤性和医源性有创检查导致的HAPF多为个案报告或散发病例报告[2-5],鲜有对HAPF进行系统分析的文献报道。本研究通过高分辨率计算机断层扫描(computed tomography,CT)及血管三维重建技术对1例HAPF患者进行诊断,以清晰展现瘘口情况并分析HAPF发病原因。此外,本研究通过PubMed和中国知网(CNKI)进行关键词检索,收集并回顾性分析1970-2017年创伤性或医源性HAPF病例资料并总结其临床表现。
1 资料和方法 1.1 病例资料患者女,29岁,因“中上腹疼痛3 d,腹泻20 d”于2017年3月14日入住海军军医大学(第二军医大学)东方肝胆外科医院。患者1999年7月14日因车祸致肝右叶挫裂伤,于外院急诊行“肝破裂修补术”,术中未输血,术后恢复良好。2012年8月29日剖宫产顺利诞下一男婴,否认肝炎病史及药物服用史。患者20 d前无明显诱因出现腹泻,6~8次/d,大便成形,无里急后重,无稀水样及洗肉样便,无血便及黑便;3 d前中上腹持续性隐痛明显,疼痛未向他处放射,腹泻后腹痛缓解不明显,无畏寒、发热,无恶心、呕吐,无反酸、嗳气等。入院体格检查:贫血貌,精神较差,巩膜无黄染;心肺未见异常;全腹膨隆,腹壁浅静脉明显,以脐为中心向四周伸展,中上腹压痛,无反跳痛,肝肋下未及,脾肋下4 cm,移动性浊音阳性、有液波震颤、可闻及右上腹收缩期血管杂音,未向他处传导。入院后行CT平扫+增强检查示:肝右前叶见片状高密度影,门静脉明显扩张,肝内胆管扩张,肝脏及腹腔内见积液,增强后动脉期门静脉早显,腹腔干增粗;多平面重建可见肠系膜上静脉充盈缺损,系膜静脉血管显示不清,空肠及结肠壁明显水肿、增厚,脾脏体积明显增大,未见明显异常密度影。胆囊体积明显增大,囊内未见明显异常密度影。肠系膜根部纠集。影像学诊断:肝脏破裂术后改变,HAPF,门静脉高压、脾大、腹腔积液,空肠及结肠壁水肿、增厚,肠系膜上静脉血栓形成(图 1)。胃镜检查示重度食管胃底静脉曲张。进一步行血管三维成像检查示:肠系膜上静脉充盈缺损,肝右前叶见片状高密度影,门静脉明显扩张,可见门静脉与肝动脉异常沟通,腹腔干增粗。肠系膜上动脉起源及走行正常,管腔未见明显狭窄。诊断同前。
|
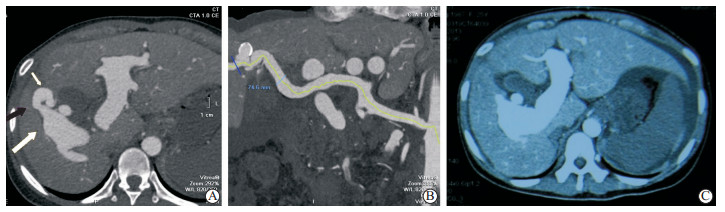
图 1 计算机断层扫描检查结果 A:肝动脉-门静脉瘘及瘘口所在位置(黑色箭头示瘘口所在位置, 白色箭头示增宽的肝动脉与门静脉); B:肝动脉在肝内完整走行; C:计算机断层扫描增强检查动脉期示门脉系统提前显影 |
1.2 献检索
以中文关键词“肝动脉-门静脉瘘”“肝动脉-静脉瘘”“创伤性”“医源性”和英文关键词“hepatic arterioportal fistula”“hepatic arteriovenous fistula”“traumatic”“iatrogenic”在CNKI及PubMed数据库系统检索1970—2017年的相关数据,筛选诊断为创伤性或医源性HAPF、肝动脉-肝静脉瘘的病例并对其临床表现、诊断、治疗情况进行分析。纳入标准:(1)临床和影像学明确诊断为肝动脉-门静脉瘘、肝动脉-肝静脉瘘;(2)有明确肝脏外伤史或肝脏穿刺史;(3)病例资料完整。排除由肝脏原发性或继发性恶性肿瘤引起的HAPF、肝动脉-肝静脉瘘。
2 结果 2.1 患者治疗结果与预后根据患者临床表现、既往病史及各项辅助检查结果,该患者入院诊断为HAPF、门静脉高压症(失代偿期)、肠系膜上静脉血栓形成、肝脏破裂修补术后。患者临床表现、血液学检查结果及治疗情况见表 1。
|
|
表 1 本例患者临床表现、各项辅助检查结果及治疗情况 |
2.2 文献分析
筛选文献55篇,加上本研究报道病例,共73例创伤性及医源性HAPF患者纳入分析,男34例、女37例、2例性别不详,年龄范围为17个月至77岁,瘘口的产生至出现典型临床症状的时间范围为1 h至50年。73例HAPF患者中9例无明显临床表现,余64例患者中较常见临床表现为腹痛(34例,53.13%)、上消化道出血(29例,45.31%)、腹腔积液(28例,43.75%)、腹部血管杂音(21例,32.81%)、脾脏肿大(11例,17.19%)、腹泻(8例,12.50%),而急性肝功能衰竭(5例,7.81%)、急性肾功能衰竭(5例,7.81%)、腹部震颤(4例,6.25%)、肝脏肿大(3例,4.69%)、心力衰竭(2例,3.12%)、下消化道出血(2例,3.12%)是HAPF较少见的临床表现。
在病因方面,73例HAPF患者中34例患者(46.58%)因肝脏闭合性或开放性创伤导致;39例(53.42%)患者为医源性损伤因素导致,其中25例(34.24%)接受单纯肝脏穿刺活组织检查,6例(8.22%)在肝移植术前、术后接受肝脏穿刺活组织检查,4例(5.48%)接受肝脏部分切除手术,3例(4.11%)在肝移植术后接受经皮肝胆管造影,1例(1.37%)在肝脏穿刺活组织检查术后接受同期放射、化学治疗。
在诊断方面,血管造影检查明确诊断HAPF患者58例,腹部超声检查明确诊断9例,上腹部CT增强检查明确诊断2例,腹部超声联合血管造影检查明确诊断2例,CT增强联合血管造影检查明确诊断1例(本研究报道病例),1例患者文献中未说明诊断方法。
在治疗方面,50例HAPF患者仅接受肝脏血管介入栓塞术,12例仅接受包含瘘口在内的肝脏部分切除术,1例接受肝移植术,2例接受肝移植联合肝脏血管介入栓塞术,2例接受肝移植联合肝脏部分切除术。以上67例患者行手术治疗后,HAPF症状完全缓解达到治愈。2例患者未接受任何有创治疗,仅动态监测瘘口大小,最终因瘘口无继续扩大(1例)及瘘口自行封闭(1例)而自愈。包括本研究报道病例在内4例患者因放弃治疗最终死亡。
3 讨论 3.1 创伤及医源性操作对Glisson系统解剖结构的影响Kayser等[4]研究认为,只要经由肝脏的有创介入性治疗都可能导致HAPF,只是绝大部分患者并不会表现出相应的临床症状。由于Glisson系统中肝动脉与门静脉特殊的解剖关系,手术中用缝合针将Glisson鞘内肝动脉及门静脉分支刺破,或缝合线捆扎肝动脉及门静脉分支都可造成HAPF[5-6]。此外,肝动脉损伤后破口与血肿相通,动脉血持续喷入血肿腔内则形成肝动脉假性动脉瘤,局部出血、感染及胆汁溶解血凝块则被认为导致血管壁坏死,直接或间接参与了HAPF的发生过程[7]。通过文献复习发现,创伤性或医源性HAPF易发生于:(1)肝脏创伤后修补时仅进行肝脏表面伤口的修补缝合,对深部血管损伤无明确探查或无牢固缝扎,未清除深部坏死组织;(2)手术操作时细针(缝合针或穿刺针)直接扎破肝动脉,或缝合线捆扎肝动脉及门静脉分支,但未发现及处理;(3)肝移植或肝硬化等常因病情需要行肝脏活组织检查的患者,随着穿刺次数的增多,因操作误伤肝动脉的风险也相应增加。
3.2 HAPF的病理生理学改变HAPF的病理生理学改变相当复杂,但“分流效应”有助于理解其对门静脉、肝动脉及体循环的影响:(1)随着血液在HAPF瘘口中心区域处高速反流而不断冲击,导致瘘口逐渐扩大,大的瘘口可引发连续血管收缩期杂音及腹部震颤。当高压血流从肝动脉通过瘘口进入到低压的门静脉时,压力差会使后者出现“动脉化”现象,而当门静脉压力上升到一定程度时则会出现门静脉高压表现,从而导致门静脉系统的毛细血管床滤过压升高而形成腹腔积液,严重者可能会出现胃底静脉曲张和破裂从而引起上消化道出血。(2)HAPF患者门静脉压力的增高是肝血流增加所致,这与通常见到的肝性门静脉高压存在一定差异。因此,在没有其他肝脏疾病的情况下,患者肝功能基本正常。(3)HAPF对患者心血管系统的损害较小。重新出现的毛细血管床和肝血窦能够对体内的回心血量及血流阻力增加起到一定的缓冲作用,但是依然会有少数患者会因回心血量增加使其右心输出量增多,从而导致肺动脉压增高发生右心衰竭。(4)因患者体内肝动脉血流阻力降低使其血流量增加,腹腔血流重新进行分布,肠系膜血供减少,此时会出现“动脉窃血”现象而使患者出现小肠疼痛感,这种疼痛是因缺血所致,经解痉、引流腹腔积液等处理后多无明显缓解。(5)肝动脉-门静脉直接交通可使部分动脉血未流经灌注组织的毛细血管而直接流入门静脉,造成无灌注组织缺血坏死,甚至发生急性肝功能衰竭。(6)由于门静脉高压,交感神经张力增高和肾血流量减少时肾血管强力收缩使肾皮质的血流明显减少,导致肾小球滤过率降低,而肾髓质血流相对增多,使髓襻浓缩和重吸收增加,患者可表现出少尿或无尿及水、钠潴留等急性肾功能衰竭症状。
3.3 HAPF的诊断创伤性及医源性HAPF在临床上十分少见,其临床表现与其他肝脏疾病相似。本研究通过对国内外文献进行分析、对比和总结发现,即使是创伤性或医源性HAPF诊断明确的患者,在就诊之初其自身亦多伴有肝血管瘤、肝炎病毒感染、肝硬化等肝脏或其他脏器疾病,因此,在初次作出诊断时往往需要仔细斟酌。我们认为从以下几方面考虑有助于提高HAPF的初次确诊率:(1)患者如出现不明原因的腹痛、肝脾肿大、腹腔积液、上消化道出血等门静脉高压表现时,应详细询问既往病史,如有外伤史、腹部手术史或有创检查史,应警惕创伤性及医源性HAPF的可能;(2)体格检查时应注意腹部听诊和触诊,有无腹部震颤和连续收缩期血管杂音;(3)HAPF的确诊有赖于完善的影像学检查。
血管造影对于诊断血管疾病如HAPF具有重要价值,其基本表现为:(1)静脉显影相对较其他显影技术早;(2)能显示出“窃血现象”;(3)能清晰显示侧支血管。因此血管造影不仅是国际公认的诊断HAPF“金标准”,还能够明确瘘口数目、部位甚至瘘口周围血管的病变程度,从而进行介入手术以达到封堵瘘口、根治HAPF的目的。
本例患者确诊HAPF依赖上腹部CT平扫+增强+血管三维重建,清晰显示了瘘口所在位置及周围血管情况。结合患者的临床表现、既往病史、体格检查及各项辅助检查结果综合分析后考虑:此瘘口是19年前行肝脏修补术所在位置,可能是修补术中手术针刺破肝动脉、门静脉或缝合线将二者缝扎所致。在CT图像中,HAPF的特征主要是“门静脉提前显影”,具体表现在:(1)患者的门静脉与肝动脉在动脉期可同时显影;而在静脉期,门静脉主干的显影密度大于肠系膜上静脉和脾静脉,甚至接近主动脉的密度。(2)因为患者的动脉血代偿性增加,当造影剂从高压进入到低压时会造成肝实质区域型强化现象,导致动脉期短暂的、周边的、楔形的肝实质强化,并且边界平直,而门静脉期肝脏密度正常或接近正常。
血管三维重建安全性高,通过重建得到的二维和三维血管图像能够从多角度、多方向进行观察和测量,还有助于了解周围组织和血管的解剖关系,耗费的时间较短,能够满足在多期显示动脉血管成像和静脉血管成像的需求。
3.4 HAPF的治疗介入手术因具有创伤小、风险低、能够重复进行栓塞及治疗费用低等优点,应作为治疗HAPF的首选。当栓塞失败或多次栓塞治疗导致患者有出血现象且病情未见明显好转时,可考虑肝动脉结扎、半肝切除及肝移植术等外科手术方法[8]。
| [1] |
EASTRIDGE B J, MINEI J P. Intrahepatic arterioportal fistula after hepatic gunshot wound:a case report and review of the literature[J]. J Trauma, 1997, 43: 523-526. DOI:10.1097/00005373-199709000-00024 |
| [2] |
孙磊, 施海彬, 刘圣, 杨正强, 周春高, 冯耀良, 等. 肝细胞癌肝动脉门静脉分流形成的相关因素分析[J]. 介入放射学杂志, 2012, 21: 206-210. DOI:10.3969/j.issn.1008-794X.2012.03.008 |
| [3] |
王宁宁, 孙明军. 肝动脉门静脉瘘致消化道大出血一例诊治体会[J]. 临床内科杂志, 2016, 33: 524-525. DOI:10.3969/j.issn.1001-9057.2016.08.006 |
| [4] |
KAYSER S, MARINCEK B, SCHLUMPF R, FRIED M, WIRTH H P. Rapidly progressive portal hypertension 23 years after post-traumatic arterioportal fistula of the liver[J]. Am J Gastroenterol, 1996, 91: 1442-1446. |
| [5] |
刘东阳, 唐缨. 肝移植术后肝穿刺活检引起肝动脉-门静脉瘘超声表现1例[J]. 中国临床医学影像杂志, 2015, 26: 301-302. |
| [6] |
VAN HAEFTEN F F, BRÖKER F H. Post-traumatic intrahepatic arteriovenous fistula[J]. Injury, 1984, 15: 311-315. DOI:10.1016/0020-1383(84)90053-6 |
| [7] |
ZIRONI G, PISCAGLIA F, GAIANI S, MASI L, BOLONDI L. Intrahepatic artery pseudoaneurysm:a possible complication of blind thoracentesis[J]. J Clin Ultrasound, 1999, 27: 151-155. DOI:10.1002/(SICI)1097-0096(199903/04)27:3<151::AID-JCU9>3.0.CO;2-Q |
| [8] |
魏波, 李肖, 唐承薇. 动脉门静脉瘘在门静脉高压中的作用及诊治[J]. 中华消化杂志, 2011, 31: 500-502. DOI:10.3760/cma.j.issn.0254-1432.2011.07.019 |
 2019, Vol. 40
2019, Vol. 40


