右心室流出道重建术(或右心室-肺动脉管道连接术)已成为最常用的先天性心脏病外科术式,同种或异种、带瓣或不带瓣、心包或人造织物补片等材料都在右心室流出道重建术中得到了广泛应用。牛颈静脉管道由于天然具有静脉瓣,可有效减轻术后右心功能受损,且易商品化,被认为是较理想的右心室流出道重建材料[1],其在欧美国家已被大量使用,中远期临床效果满意[2-5]。本研究回顾性通过分析2013年5月至2016年7月我院心血管外科应用国产牛颈静脉带瓣管道和自体心包管道重建右心室流出道的18例复杂先天性心脏病患者的临床资料,比较两种外管道材料重建右心室流出道的中期疗效。
1 资料和方法 1.1 病例资料回顾性分析2013年5月至2016年7月在我院心血管外科接受外管道右心室流出道重建术的先天性心脏病患者的病例资料,根据手术所用重建材料将患者分为牛颈静脉管道组和自体心包管道组。牛颈静脉带瓣管道由中南大学湘雅二院吴忠仕团队研制,采用光氧化反应去细胞处理,具有生物相容性良好、无细胞毒性、钙化程度低等优点[6]。术前所有患者及家属均详细了解牛颈静脉带瓣管道的相关信息,并签署知情同意书。本研究通过我院伦理委员会审批[伦审(2012)第011号]。
1.2 手术方法患者全身麻醉,取胸骨正中开胸,去除胸腺组织。自体心包管道组充分游离双侧纵隔胸膜以最大限度留取心包(两侧距膈神经1~2 cm,上至主动脉返折,下至膈肌水平),心包离体后用0.6%戊二醛溶液固定15 min,然后用生理盐水反复冲洗5次,缝制成自体心包管道备用。牛颈静脉管道组从保存液中取出牛颈静脉管道,翻转内膜面,观察静脉瓣有无破损,然后用生理盐水反复冲洗5次备用。常规建立体外循环,体外循环采用中低温(28~32 ℃),心肌保护液采用组氨酸-色氨酸-酮戊二酸盐液(histidine-tryptophane-ketoglutarate solution,HTK液)从主动脉根部灌注。术中矫治心内合并畸形后,取牛颈静脉带瓣管道或缝制的自体心包管道并裁剪至合适长度,以5-0或6-0无损伤Prolene缝线连续缝合连接右心室-肺动脉。外管道口径的选择参考患者体表面积相对应的正常右心室流出道大小[7]。
1.3 观察指标术后对比两组的体外循环时间、主动脉阻闭时间、停机后右心室流出道跨瓣压差、右心室压/桡动脉压比值、术后机械通气时间、重症监护病房(intensive care unit,ICU)时间、输血量、住院总费用、围手术期死亡及并发症。随访采用电话、门诊复诊等方式,应用心脏超声及心脏计算机断层扫描血管成像(computed tomography angiography,CTA)评估右心室流出道跨瓣压差、肺动脉瓣反流情况。观察术后随访期间不良事件的发生情况,包括死亡、感染性心内膜炎、吻合口重度狭窄[跨瓣压差>50 mmHg,1 mmHg=0.133 kPa]、管道瘤样扩张、再手术、重度肺动脉瓣反流。
1.4 统计学处理采用SPSS 20.0软件进行统计学分析。计数资料以例数表示,组间比较采用四格表χ2检验或Fisher确切概率法。呈正态分布的计量资料以x±s表示,组间比较采用独立样本t检验。检验水准(α)为0.05。
2 结果 2.1 一般资料接受外管道右心室流出道重建术的先天性心脏病患者18例,男11例、女7例,年龄为2~16(5.22±4.12)岁,其中肺动脉闭锁合并室间隔缺损7例、右心室双出口合并肺动脉瓣狭窄4例、永存动脉干3例、永存动脉干合并右肺动脉缺如1例、矫正型大动脉转位合并肺动脉瓣狭窄1例、完全大动脉转位合并肺动脉瓣狭窄2例。术中采用完整国产牛颈静脉带瓣管道重建右心室流出道11例(牛颈静脉管道组),采用自体心包管道重建右心室流出道7例(自体心包管道组)。两组患者性别构成比、年龄、体质量、血氧饱和度、McGoon比值、左心室舒张末期容积指数、术前诊断差异均无统计学意义(P均>0.05),见表 1。
|
|
表 1 两组先天性心脏病患者基线资料的比较 Tab 1 Comparison of baseline characteristics of congenital heart disease patients beween two groups |
2.2 围手术期情况
两组患者均顺利完成手术。牛颈静脉管道组无围手术期死亡病例;自体心包管道组围手术期死亡2例,死因分别为术后肺动脉高压危象(1例)和低心排出量综合征(1例)。由表 2可见,牛颈静脉管道组右心室压/桡动脉压比值、术后机械通气时间、ICU时间均小于自体心包管道组,差异均有统计学意义(P均<0.05);两组患者体外循环时间、主动脉阻闭时间、停机后右心室流出道跨瓣压差、输血量及住院总费用差异均无统计学意义(P均>0.05)。
|
|
表 2 两组先天性心脏病患者围手术期资料的比较 Tab 2 Comparison of perioperative characteristics of congenital heart disease patients beween two groups |
2.3 中期随访疗效
术后16例患者完成随访,其中牛颈静脉管道组11例、自体心包管道组5例;随访时间为4~56个月,平均(31.03±12.41)个月。两组随访期间均无死亡病例;牛颈静脉管道组无再次手术病例,自体心包管道组1例因严重右心功能不全于术后2年行机械瓣膜带瓣管道植入术。
两组术后随访资料见表 3。分析术后管道梗阻情况,牛颈静脉管道组患者出院前(围手术期)超声测量右心室流出道跨瓣压差为(20.45±6.70)mmHg,术后最后一次随访时超声测量右心室流出道跨瓣压差为(22.91±7.31)mmHg,两者差异无统计学意义(P>0.05)。自体心包管道组患者出院前(围手术期)超声测量右心室流出道跨瓣压差为(16.14±4.02)mmHg,术后最后一次随访时超声测量右心室流出道跨瓣压差为(29.20±18.09)mmHg,两者差异有统计学意义(P<0.05)。
|
|
表 3 两组先天性心脏病患者术后随访资料的比较 Tab 3 Comparison of follow-up characteristics of congenital heart disease patients between two groups |
术后最后一次随访时超声测量肺动脉瓣反流程度,牛颈静脉管道组轻度反流8例、中度反流3例,自体心包管道组轻度反流1例、中度反流2例、重度反流2例,两组间差异有统计学意义(P<0.05)。
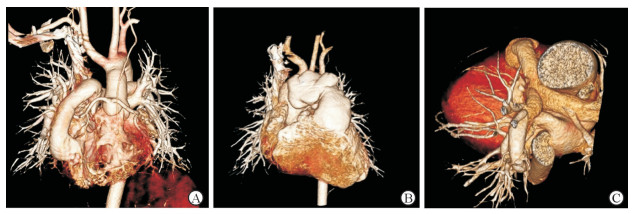
2.4 不良事件发生情况术后随访时超声检查显示,牛颈静脉管道组管道内瓣叶组织均有不同程度增厚,但未见钙化,瓣叶活动良好,均无血栓形成及感染性心内膜炎发生;自体心包管道组管道内瓣叶均无未见钙化,亦均无血栓形成及感染性心内膜炎发生。见表 3,术后随访时心脏CTA检查发现,牛颈静脉管道组有1例患者管道中段出现瘤样扩张、1例近端吻合口出现瘤样扩张,自体心包管道组管道均未见瘤样扩张(图 1),两组差异无统计学意义(P>0.05)。
|
图 1 术后随访时心脏计算机断层扫描血管成像检查结果 Fig 1 Postoperation cardiac computed tomography angiography results during follow-up A: Normal bovine jugular vein conduit valvular after operation; B: Postoperative follow-up revealed that the middle segment of the bovine jugular vein conduit had tuberculous dilatation; C: Normal autologous pericardium conduit after operation |
3 讨论
大部分发绀型先天性心脏病需要重建一个右心室流出道,重建方法有跨瓣环补片及应用外管道连接右心室-肺动脉。应用单纯跨瓣环补片的患者术后常出现严重的右房室瓣反流及右心室功能不全,这是由于术后肺动脉瓣反流导致右心室容量负荷增加,右心功能受损,增加患者死亡率[8]。应用功能完整的肺动脉瓣可有效减轻这一血流动力学损害。同种主动脉或肺动脉带瓣管道最早应用于临床,曾被认为是重建右心室流出道的金标准,但由于伦理学问题导致来源不足、缺少适合小儿的口径等原因,在我国应用不多。应用带单瓣的心包补片[9]或膨体聚四氟乙烯外科软组织补片(expended polytetrafluoroethylene,ePTFE)[10]重建肺动脉瓣,方法简单,取材方便,围手术期效果良好,但瓣膜持久性差,早期衰败率高,相比外管道其应用范围局限。自体心包管道具有制作简单、适于吻合、通畅率高等优点,相较于心包补片应用范围更广,有报道认为在姑息性右心室流出道重建术中自体心包管道的疗效优于Gore-Tex人工血管及牛颈静脉管道[11],但由于缺少瓣膜,自体心包管道术后并发严重肺动脉瓣反流的问题始终难以避免。本研究中,自体心包管道组中期随访显示5例肺动脉瓣反流患者中有2例存在重度反流。近期ePTFE带瓣管道也被应用于临床,中期随访显示肺动脉瓣仅有微量至轻度反流,右心室流出道跨瓣压差为(22.4±15.1)mmHg[12],但ePTFE带瓣管道制作工艺复杂、价格昂贵,远期效果也有待进一步评估。
牛颈静脉材质柔软,天然带有静脉瓣,在低压条件下具有良好的抗反流性能,且具有采集容易、制备工艺简单、口径范围大、易于吻合等优点,被认为是较理想的右心室流出道重建材料[1]。美国Medtronic公司研发的ContegraTM管道是最早上市的商业化牛颈静脉带瓣管道,已经在欧美国家大规模使用,中远期临床效果满意。Christenson等[2]对比了120例应用同种带瓣管道患者与54例应用ContegraTM管道患者的中远期疗效,2年免于再手术率分别为93.3%和98.9%,9年免于再手术率分别为63.0%和89.0%,说明牛颈静脉管道在远期疗效上明显优于同种带瓣管道。应用ContegraTM管道鲜有围手术期死亡情况,个别死亡病例死亡原因也非管道相关,但应用ContegraTM管道术后可能出现感染性心内膜炎、吻合口狭窄及管道瘤样扩张等不良事件。Beckerman等[3]报道了228例患者应用ContegraTM管道的不良事件发生情况,在平均6年的随访中,25%的管道发生感染性心内膜炎,最常见的致病菌为草绿色链球菌(13.25%);ContegraTM管道10年免于感染性心内膜炎发生率为77%,与同种带瓣管道相比其感染性心内膜炎发生率更高(P<0.01)。Meyns等[4]报道了应用ContegraTM管道的58例患者的中期疗效,其中2例死于术后感染性心内膜炎,术后2年远端吻合口重度狭窄(跨瓣压差>50 mmHg)比例高达50%,低龄和小管道尺寸被认为是导致术后重度狭窄的危险因素;另外还有12%的病例出现管道扩张情况,病理检查显示狭窄及扩张的管道远端吻合口水平均存在过度增生的新生内膜组织,具体机制尚不明确。因此作者建议对新生儿及婴儿患者不常规使用牛颈静脉管道。Rastan等[5]对应用ContegraTM管道的78例患者的中期随访发现,再手术的危险因素有年龄<1岁、管道口径为12 mm、右心室压力高和永存动脉干。作者认为牛颈静脉管道应用于1岁以上患者的再手术率较低,不推荐<1岁的婴儿使用。
国内阜外医院胡盛寿等[13]应用自行研制的牛颈静脉管道对14例患者重建右心室流出道,早期疗效满意。北京佰仁公司研发的肺动脉带瓣管道(牛颈静脉)于2017年上市,具体疗效有待临床验证。本研究采用的牛颈静脉管道由中南大学湘雅二院吴忠仕团队研制,采用光氧化反应去细胞处理,更接近自然生物材料且不会明显增加原生物材料的硬度,具有良好的生物相容性,而且由于不经过戊二醛固定处理,无细胞毒性,钙化反应也明显降低[6]。本研究分析了18例2~16岁患者应用外管道重建右心室流出道的疗效,结果发现牛颈静脉管道组围手术期及中期随访均未出现死亡病例,患者中期随访发生肺动脉瓣反流和管道梗阻的风险与自体心包管道组相比更低;随访过程中牛颈静脉管道组右心室流出道跨瓣压差没有明显增加,管道或瓣膜未见钙化,显示了优良的性能。但随访中我们也发现2例患者牛颈静脉管道出现瘤样扩张情况,1例位于管道中段、1例位于近端吻合口。虽然管道扩张未引发严重肺动脉瓣反流,患者无明显症状,暂时无需再次手术干预,但必须密切随访观察。这一发现也提示本研究采用的牛颈静脉管道制备工艺还须进一步改进。
综上所述,本研究发现国产牛颈静脉带瓣管道适用于各类复杂先天性心脏畸形患者右心室流出道重建手术,围手术期安全性好,中期随访显示牛颈静脉管道抗反流性能良好,无严重梗阻、钙化及感染性心内膜炎发生,明显优于自体心包管道。但部分国产牛颈静脉带瓣管道术后中期有瘤样扩张发生,有待进一步改进工艺。本研究为单中心回顾性研究,研究中不可避免地存在一些偏倚,加上入选的患者数量较少,可能会对研究结果产生一定影响。今后还需要开展多中心随机对照试验,通过长期随访进一步评价国产牛颈静脉带瓣管道的效果。
| [1] |
CORNO A F, HURNI M, GRIFFIN H, JEANRENAUD X, VON SEGESSER L K. Glutaraldehyde-fixed bovine jugular vein as a substitute for the pulmonary valve in the Ross operation[J]. J Thorac Cardiovasc Surg, 2001, 122: 493-494. DOI:10.1067/mtc.2001.114780 |
| [2] |
CHRISTENSON J T, SIERRA J, COLINA MANZANO N E, JOLOU J, BEGHETTI M, KALANGOS A. Homografts and xenografts for right ventricular outflow tract reconstruction:long-term results[J]. Ann Thorac Surg, 2010, 90: 1287-1293. DOI:10.1016/j.athoracsur.2010.06.078 |
| [3] |
BECKERMAN Z, DE LEÓN L E, ZEA-VERA R, MERY C M, FRASER C D Jr. High incidence of late infective endocarditis in bovine jugular vein valved conduits[J/OL]. J Thorac Cardiovasc Surg, 2018, 156: 728-734.e2. doi: 10.1016/j.jtcvs.2018.03.156.
|
| [4] |
MEYNS B, VAN GARSSE L, BOSHOFF D, EYSKENS B, MERTENS L, GEWILLIG M, et al. The Contegra conduit in the right ventricular outflow tract induces supravalvular stenosis[J]. J Thorac Cardiovasc Surg, 2004, 128: 834-840. DOI:10.1016/j.jtcvs.2004.08.015 |
| [5] |
RASTAN A J, WALTHER T, DAEHNERT I, HAMBSCH J, MOHR F W, JANOUSEK J, et al. Bovine jugular vein conduit for right ventricular outflow tract reconstruction:evaluation of risk factors for mid-term outcome[J]. Ann Thorac Surg, 2006, 82: 1308-1315. DOI:10.1016/j.athoracsur.2006.04.071 |
| [6] |
LÜ W D, ZHANG M, WU Z S, HU T H, XU Z J, LIU W, et al. The performance of photooxidatively crosslinked acellular bovine jugular vein conduits in the reconstruction of connections between pulmonary arteries and right ventricles[J]. Biomaterials, 2010, 31: 2934-2943. DOI:10.1016/j.biomaterials.2009.12.046 |
| [7] |
JONSSON H, IVERT T, JONASSON R, HOLMGREN A, BJÖRK V O. Work capacity and central hemodynamics thirteen to twenty-six years after repair of tetralogy of Fallot[J]. J Thorac Cardiovasc Surg, 1995, 110: 416-426. DOI:10.1016/S0022-5223(95)70238-5 |
| [8] |
STEPHENS E H, TINGO J, NAJJAR M, YILMAZ B, LEVASSEUR S, DAYTON J D, et al. Cardiac function after tetralogy of Fallot/complete atrioventricular canal repair[J]. World J Pediatr Congenit Heart Surg, 2017, 8: 189-195. DOI:10.1177/2150135116682719 |
| [9] |
林曦, 张卫达, 王晓武, 马涛, 袁彬彬, 梅鲁刚. 带单瓣自体心包补片在右室流出道重建术中的临床研究[J]. 华南国防医学杂志, 2011, 25: 116-118. |
| [10] |
YAMAGISHI M, KUROSAWA H, NOMURA K, KITAMURA N. Fan-shaped expanded polytetrafluoroethylene valve in the pulmonary position[J]. J Cardiovasc Surg (Torino), 2002, 43: 779-786. |
| [11] |
李坤, 李守军, 公兵, 杨克明. 姑息性右心室-肺动脉连接术中管道材料及型号的选择与应用[J]. 中国胸心血管外科临床杂志, 2013, 20: 632-636. DOI:10.7507/1007-4848.20130201 |
| [12] |
OOTAKI Y, WELCH A S, WALSH M J, QUARTERMAIN M D, WILLIAMS D A, UNGERLEIDER R M. Medium-term outcomes after implantation of expanded polytetrafluoroethylene valved conduit[J]. Ann Thorac Surg, 2018, 105: 843-850. DOI:10.1016/j.athoracsur.2017.07.013 |
| [13] |
胡盛寿, 李守军, 宋云虎, 宋学营, 张浩, 王欣, 等. 国产牛颈静脉带瓣管道重建右室流出道临床应用[J]. 中华胸心血管外科杂志, 2005, 21: 328-330. DOI:10.3760/cma.j.issn.1001-4497.2005.06.003 |
 2019, Vol. 40
2019, Vol. 40


