2. 海军军医大学(第二军医大学)长海医院皮肤科, 上海 200433
2. Department of Dermatology, Changhai Hospital, Naval Medical University(Second Military Medical University), Shanghai 200433, China
家族性良性慢性天疱疮又称Hailey-Hailey病(Hailey-Hailey disease,HHD),是一种少见的常染色体显性遗传性皮肤病[1]。HHD典型的临床表现为颈部、腋下、腹股沟、外阴等皮肤皱褶部位反复出现红斑、水疱、糜烂,自觉瘙痒;通常于青春期后发病,临床上常误诊为湿疹或股癣,但其组织病理具有特征性,表现为表皮内棘层松解,呈倒塌砖墙样外观[2]。目前研究表明Hailey-Hailey病是由一种编码细胞钙泵的ATP2C1基因突变所致[3-4]。ATP2C1基因包含27个外显子,HHD的突变位点主要位于外显子12、13、21、23、24和25[5-6]。本研究通过Sanger直接测序法对HHD一家系成员进行了ATP2C1基因检测并予以分析,发现患者第21号外显子的第472位核苷酸由G变为A,导致错义突变,经检索文献,未见有关该突变的报道,现将本研究结果报告如下。
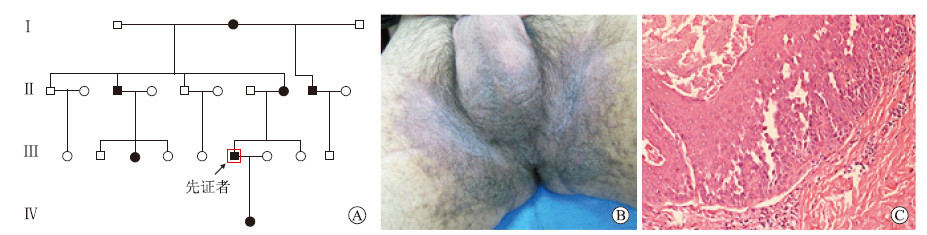
1 资料和方法 1.1 临床资料收集HHD家系成员的一般资料进行临床调查。共调查了该家系4代共23人,其中HDD患者7例,男3例、女4例,25~33岁发病,家系谱见图 1A。先证者,男,32岁,双侧腹股沟和腋下红斑、糜烂反复发作7年,皮损夏天加重、冬天趋于缓解。专科体格检查:双侧腋下散在多个暗褐色斑疹,无水泡、糜烂、渗出,双侧腹股沟、阴囊、肛周有弥漫性暗褐色斑片,苔藓化明显,边界不清,表面粗糙,呈增殖性损害,无红斑、水泡及糜烂(图 1B)。皮损组织病理检查提示:基底层上裂隙和“绒毛”形成,可见许多棘刺松解细胞,呈倒塌砖墙样外观(图 1C)。根据患者的临床表现及组织病理特征确诊为HHD。
|
图 1 HHD家系图谱及先证者相关图片 A: HHD家系图谱; B:先证者临床表现(腹股沟有弥漫性暗褐色斑片, 呈增殖性损害); C:先证者皮损组织H-E染色结果(基底层上裂隙和“绒毛”形成, 可见许多棘刺松解细胞, 呈倒塌样砖墙样外观). HHD:家族性良性慢性天疱疮. Original magnification: ×200 (C) |
1.2 外周血DNA的提取
该家系共7例患者,其中1例患者已去世,另2例患者不愿接受我们的检查,最终本研究收集了4例患者的外周血。患者及家属签署知情同意书后,抽取家系中这4例患者外周血5 mL,经2% EDTA抗凝,用试剂盒(美国Promega公司)提取基因组DNA,同样抽取家系中3例健康者和100例无亲缘关系的正常人进行对照,以排除基因的多态性。
1.3 引物设计在线(http://asia.ensemb1.org)检索ATP2C1基因mRNA序列,经序列对比得到ATP2C1基因的全基因组序列,应用Primer 5.0软件设计ATP2C1基因的27对引物,其中用于扩增的21号外显子的引物序列为:上游引物5'-TTC TGG CTT CTG CAG TCA TCA-3',下游引物5'-AAG CAA CTG TAA CGA ATA G-3'。所有引物均由生工生物工程(上海)股份有限公司合成。
1.4 PCR扩增PCR反应体系共25 μL:上下游引物(0.4 mmol/L)各1 μL,模板DNA 1 μL,Taq酶1.25 U,dNTP(0.4 mmol/L)0.5 μL、MgCl2(2.0 mmol/L)1.5 μL,其余用ddH2O补足至25 μL。在9700型PCR扩增仪(美国Applied Biosystems公司)上进行PCR扩增,反应条件:94 ℃ 5 min;94 ℃ 45 s,55~60 ℃ 50 s,72 ℃ 50 s,共35个循环;72 ℃ 8 min。PCR扩增产物经1%琼脂糖凝胶电泳检测,使用PCR产物纯化试剂盒[生工生物工程(上海)股份有限公司]纯化,将纯化产物送生工生物工程(上海)股份有限公司进行测序,确定突变位点。
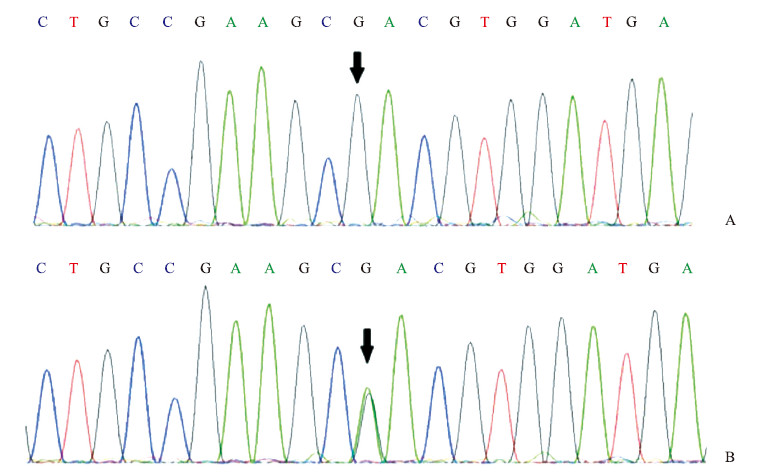
2 结果基因测序结果(图 2)显示,HHD家系4例患者ATP2C1基因的第21号外显子的第472位核苷酸由G变为A,该突变导致原先158位的天冬氨酸变为天冬酰胺(p.Asp158Asn)的错义突变,其编码的蛋白质发生结构和功能丧失。该家系中3例健康者和100例无亲缘关系的正常人均未发现此突变。结果证明此突变是该HHD家系的致病突变而非单核苷酸多态性。
|
图 2 HHD家系ATP2C1基因测序结果(箭头所示:c.472G>A) A:正常对照; B: HHD患者. HHD:家族性良性慢性天疱疮 |
3 讨论
HHD是一种少见的常染色体显性遗传性皮肤病,本研究报道的该HHD家系中4代共23人,其中HDD患者7例,在25~33岁发病,男女皆有发病,符合常染色体显性遗传模式,且从家系图谱上我们发现该家系存在同母异父的现象,先证者的外婆为患者,有过2次婚姻,且两边家庭成员均有发病。
本研究对该HHD家系进行基因检测分析,发现了ATP2C1基因一个新的突变位点,即第21号外显子第472位核苷酸由G变为A,该突变导致原先158位的天冬氨酸变为天冬酰胺(p.Asp158Asn)的错义突变。Hu等[3]研究发现,第21号外显子编码的氨基酸参与Mn2+的结合,对维持蛋白质的结构和功能起重要作用,该基因突变导致编码蛋白质的结构和功能丧失,从而出现相应的临床表现。本研究该家系中3例健康者和100例无亲缘关系的正常人均未发现此突变。
2000年Hu等[3]和Sudbrak等[4]分别通过家系连锁分析与定位克隆技术找到HHD的致病基因为ATP2C1基因。ATP2C1基因定位于人染色体3q21-q22,包含27个外显子[5]。ATP2C1基因编码的蛋白质是一种存在于高尔基体的新型钙泵ATP酶,又称为人类分泌途径Ca2+/Mn2+-ATP酶(hSPCA1),hSPCA1功能障碍导致表皮颗粒层中Ca2+浓度降低,从而影响桥粒的完整性和Ca2+敏感受体激活,而Ca2+敏感受体在触发细胞与细胞间黏附、颗粒层细胞分化与Ca2+的重新分布中发挥重要作用[7]。Behne等[8]研究发现HHD患者表皮游离Ca2+浓度与正常皮肤相比减少,而Ca2+浓度对维持桥粒结构的完整性起重要作用,这也解释了HHD患者发生棘层松解的原因。
目前研究确定至少有177个突变位点散布于ATP2C1基因中,其突变类型分别为:51个(28.8%)错义突变,44个(24.9%)小缺失突变,36个(20.3%)剪接突变,25个(14.1%)无义突变,12个(6.8%)重复突变,4个(2.3%)复杂重排,3个(1.7%)大片段缺失,2个(1.1%)插入缺失突变[6]。62.1%(110/177)的突变属于点突变;37.3%(66/177)的ATP2C1突变位点主要位于外显子12、13、21、23、24和25,其中第12号和23号外显子编码的氨基酸对Ca2+结合发挥至关重要的作用,第13号外显子编码的氨基酸参与磷酸化,第21号外显子编码的氨基酸参与Mn2+的结合[6],Matsuda等[9]推测,若这些区域发生突变将会对SPCA1的功能产生严重影响。在本研究报道的这个家系中,我们通过基因检测发现ATP2C1基因突变位点位于第21号外显子,导致原先158位天冬氨酸变为天冬酰胺(p.Asp158Asn)的错义突变,推测该基因突变可能导致编码的蛋白质发生结构和功能丧失,从而影响Mn2+的结合,这可能是该家系发病的主要原因。
目前,已报道的中国人HHD患者ATP2C1基因突变有29种,其中错义突变5种、剪切位点突变7种、无义突变8种、移码突变7种、其他方式2种[10-11]。突变位点分布于整个ATP2C1基因,没有突变热点区,大部分突变均导致提前终止密码子。朱亚刚等[10]研究发现,基因突变的类型与临床表现并无明确的关系,即使相同的突变也会导致不同的临床表现,认为机械摩擦、高温等环境因素也会影响患者的临床表现。
综上所述,本研究基因检测结果显示,ATP2C1基因的第21号外显子的第472位核苷酸由G变为A,导致原先158位天冬氨酸变为天冬酰胺(p.Asp158Asn)的错义突变,这可能是该HHD家系发病的主要原因,为该家系成员进行产前诊断及遗传咨询奠定了基础。
志谢 感谢海军军医大学(第二军医大学)长海医院皮肤科陈琢医师、胡蕴琦医师在样本采集及病史采集中提供的帮助。
| [1] |
ROSENTHAL L H. Familial benign chronic pemphigus (Hailey)[J]. Arch Derm Syphilol, 1948, 57(3 Pt 2): 433. |
| [2] |
赵辨. 中国临床皮肤病学[M]. 4版. 南京: 江苏科学技术出版社, 2010: 1470-1472.
|
| [3] |
HU Z, BONIFAS J M, BEECH J, BENCH G, SHIGIHARA T, OGAWA H, et al. Mutations in ATP2C1, encoding a calcium pump, cause Hailey-Hailey disease[J]. Nat Genet, 2000, 24: 61-65. DOI:10.1038/71701 |
| [4] |
SUDBR AK R, BROW N J, DOBSON-STONE C, CARTER S, RAMSER J, WHITE J, et al. Hailey-Hailey disease is caused by mutations in ATP2C1 encoding a novel Ca2+ pump[J]. Hum Mol Genet, 2000, 9: 1131-1140. DOI:10.1093/hmg/9.7.1131 |
| [5] |
TON V K, MANDAL D, VAHADJI C, RAO R. Functional expression in yeast of the human secretory pathway Ca2+, Mn2+-ATPase defective in Hailey-Hailey disease[J]. J Biol Chem, 2002, 277: 6422-6427. DOI:10.1074/jbc.M110612200 |
| [6] |
NELLEN R G, STEIJLEN P M, VAN STEENSEL M A, VREEBURG M, European Professional Contributors, FRANK J, et al. Mendelian disorders of cornification caused by defects in intracellularcalcium pumps:mutation update and database for variants in ATP2A2 and ATP2C1 associated with Darier disease and HaileyHailey disease[J]. Hum Mutat, 2017, 38: 343-356. DOI:10.1002/humu.2017.38.issue-4 |
| [7] |
BRINI M, CARAFOLI E. Calcium pumps in health and disease[J]. Physiol Rev, 2009, 89: 1341-1378. DOI:10.1152/physrev.00032.2008 |
| [8] |
BEHNE M J, TU C L, ARONCHIK I, EPSTEIN E, BENCH G, BIKLE D D, et al. Human keratinocyte ATP2C1 localizes to the Golgi and controls Golgi Ca2+ stores[J]. J Invest Dermatol, 2003, 121: 688-694. DOI:10.1046/j.1523-1747.2003.12528.x |
| [9] |
MATSUDA M, HAMADA T, NUMATA S, TEYE K, OKAZAWA H, IMAFUKU S, et al. Mutation-dependent effects on mRNA and protein expressions in cultured keratinocytes of Hailey-Hailey disease[J]. Exp Dermatol, 2014, 23: 514-516. DOI:10.1111/exd.2014.23.issue-7 |
| [10] |
朱亚刚, 张学军, 杨森. 家族性慢性良性良性慢性天疱疮2家系的基因突变分析[J]. 中国皮肤性病学杂志, 2012, 26: 189-191. |
| [11] |
ZHANG F, YAN X, JIANG D, TIAN H, WANG C, YU L. Eight novel mutations of ATP2C1 identified in 17 Chinese families with Hailey-Hailey disease[J]. Dermatology, 2007, 215: 277-283. DOI:10.1159/000107620 |
 2019, Vol. 40
2019, Vol. 40


