2. 海军军医大学(第二军医大学)长海医院影像医学科, 上海 200433
2. Department of Radiology, Changhai Hospital, Naval Medical University (Second Military Medical University), Shanghai 200433, China
患者女,73岁,因“突发意识不清、四肢抽搐3 d”于2019年1月8日由我院胃肠外科转入脑血管病中心治疗。患者于2018年12月29日行胃贲门占位切除术,术后恢复可。2019年1月5日15:10拔除右侧颈静脉导管后约1 min突发意识不清,四肢抽搐,牙关紧闭,双眼上翻,小便失禁,无呼吸、心跳停止,测收缩压为160~180 mmHg(1 mmHg=0.133 kPa),舒张压为90~100 mmHg,心率波动在100~140 / min,诊断为“癫持续状态”,给予保持呼吸道通畅,地西泮10 mg静推止惊,丙戊酸钠缓慢静滴,10 min后停止抽搐,但意识仍不清,偶有阵发性左侧肢体抽动。16:12急查头颅计算机断层扫描(computed tomography,CT)示左侧额叶皮质下、双侧海绵窦区气栓(图 1),考虑脑空气栓塞(cerebral air embolism,CAE),给予持续高流量面罩吸氧(6~8 L / min),氯吡格雷抗血小板聚集,次日12:00左右意识逐渐恢复正常,能和家属简单交流,但言语欠流利,四肢无力,右侧显著;查头颅磁共振成像,T2加权和弥散加权成像均显示双侧大脑半球皮质弥漫性高信号(图 2)。转入脑血管病中心后体格检查示:体温36.8 ℃,脉搏72 / min,呼吸17 / min,血压103 / 76 mmHg,意识清楚,部分性运动性失语,双侧瞳孔等大等圆,瞳孔对光反射灵敏,双侧额纹对称,右侧鼻唇沟浅,右上肢肌力0级,右下肢肌力Ⅲ级,左侧肢体肌力Ⅳ级,双侧巴宾斯基征(+)。查血尿大便常规、血糖、血生物化学、心肌酶、B型脑钠肽、血脂均未见明显异常;经胸超声、双下肢静脉超声检查均未见明显异常。转入脑血管病中心后第3天患者出现气急、气喘,急查血气分析示氧饱和度93.4%、氧分压61.8 mmHg、二氧化碳分压30.40 mmHg,凝血功能示D-二聚体12.87 μg / mL、纤维蛋白降解产物67.00 μg / mL,胸部CT检查示左下肺少量胸腔积液、双下肺膨胀不全,肺动脉计算机断层扫描血管成像(computed tomography angiography,CTA)检查示双侧肺动脉主干及其分支动脉多发栓塞(图 3),诊断为肺栓塞。给予丙戊酸钠+左乙拉西坦抗癫,以及先后低分子肝素钠、华法林抗凝等对症支持治疗。转入脑血管病中心10 d后气急、气喘消失,但肢体无力未见明显好转,复查血气分析示氧饱和度97.8%、氧分压90.6 mmHg、二氧化碳分压32.1 mmHg,凝血功能示D-二聚体3.67 μg / mL、纤维蛋白降解产物17.60 μg / mL、国际标准化比值1.86,头颅CT检查示左侧额叶梗死灶(图 4),并于2019年1月22日出院。出院后3个月随访言语正常,左侧肢体肌力Ⅴ级,右侧肢体肌力Ⅴ-级,生活基本自理,经颅多普勒超声发泡试验未探及栓子信号,复查肺动脉CTA提示双侧肺动脉通畅。
|
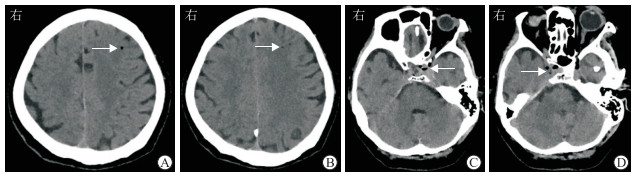
图 1 2019年1月5日头颅计算机断层扫描检查结果 A, B:左侧额叶皮质下气栓(箭头所示); C, D:双侧海绵窦区气栓(箭头所示) |

|
图 2 2019年1月6日头颅磁共振T2加权(A)、弥散加权(B)成像示双侧大脑半球皮质弥漫性高信号 |
|
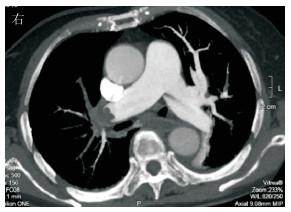
图 3 2019年1月11日肺动脉计算机断层扫描血管成像示双侧肺动脉主干及其分支动脉多发栓塞 |

|
图 4 2019年1月18日复查头颅计算机断层扫描示左侧额叶梗死灶 |
2 讨论
CAE是一种罕见但具有潜在致命风险的急症,与医源性操作有关[1-4],死亡率可达25%[5]。文献报道CAE主要由各种手术或有创操作引起,以中心静脉导管插入或拔除时多见[1-2, 6-7]。如果大气压超过静脉压,空气可通过导管拔除后遗留的通道进入静脉系统,尤其在坐位时容易发生。本例患者于颈静脉导管拔除后即刻发生癫持续状态,考虑CAE的发生与导管移除密切相关。
目前认为引起CAE的机制主要有两方面:(1)气栓量超出肺过滤能力或存在心、肺内右向左分流(如卵圆孔未闭和肺动静脉畸形),这种机制也称为反常性空气栓塞;(2)气栓直接逆行至脑静脉系统。根据受累血管不同,可分为脑动脉空气栓塞和脑静脉空气栓塞,后者比前者少见,也常被忽视,两者可通过头颅计算机断层扫描诊断、区分。海绵窦区是逆行性脑静脉空气栓塞易受累的区域[6, 8]。本例患者气栓集中于双侧海绵窦区,认为由颈静脉逆行所致。关于脑动脉空气栓塞,根据Jeon和Kang[9]研究结果,认为气泡表面张力与直径成反比,较小气泡更能抵抗破裂,大脑前动脉与大脑中动脉供血交界区的动脉血流速度最慢、压力梯度最低,气泡最易在额叶皮质区直径为30~60 μm的小动脉内滞留。因此,额叶皮质区往往是脑动脉空气栓塞最易累及的部位。本例患者气栓部位、缺血范围与之符合。需要进一步说明的是,本例患者经颅多普勒超声发泡试验、经胸超声检查均未见存在右-左分流的直接证据,但双侧肺动脉主干栓塞间接反映了进入静脉系统内空气负荷量极大,因此推测气栓量超出肺过滤能力,通过肺毛细血管床扩散至动脉的可能性较大。
CAE的病理生理学机制尚未明确,尤其是脑静脉空气栓塞更是知之甚少。目前认为脑动脉空气栓塞可引起2种病理生理学变化[4, 10]:(1)动脉阻塞导致脑组织缺血;(2)气泡本身对血管的炎症反应。动物模型研究显示,血管内气泡使白细胞活化并引起可导致血脑屏障破坏的炎症反应,从而导致脑水肿及继发性缺血[10]。弥散加权成像显示病灶呈弱高信号,可能是这种炎症变化的间接反映。而有学者提出脑静脉空气栓塞的病理生理机制可能是气泡逆行至脑实质,诱导中性粒细胞活化并促进淤滞,从而导致静脉性梗死[11]。
CAE的治疗主要包括特伦德伦堡体位和高压氧。多数学者建议将患者置于特伦德伦堡体位,以促进气泡返回中心静脉循环,但对反常性空气栓塞可能无效。高压氧是唯一被证明对静脉和动脉空气栓塞均有效的治疗方法[12]。高压氧能够压缩气泡体积,并保持血液中的高氧含量,以优化缺血组织的氧合,从而降低颅内压,降低脑血管通透性,减轻脑水肿和白细胞黏附至内皮细胞。CAE患者的预后取决于气栓量、空气积累速率和受累部位。本例患者以癫持续状态起病,因病情重未予高压氧治疗,但给予高流量吸氧、抗癫治疗,因兼顾肺栓塞,给予抗凝治疗,获得了良好的临床结局。
| [1] |
LAI D, JOVIN T G, JADHAV A P. Cortical vein air emboli with gyriform infarcts[J]. JAMA Neurol, 2013, 70: 939-940. DOI:10.1001/jamaneurol.2013.1949 |
| [2] |
BARTOLINI L, BURGER K. Pearls & Oy-sters: cerebral venous air embolism after central catheter removal: too much air can kill[J/OL]. Neurology, 2015, 84: e94-e96. doi: 10.1212/WNL.0000000000001414.
|
| [3] |
MIRTCHEV D, MEHTA T, DANIEL A, FINSTEIN T, MCCULLOUGH L. Pearls & Oy-sters:enhancing vigilance for detection of cerebral air embolism:from syncope to death[J]. Neurology, 2018, 91: 717-720. DOI:10.1212/WNL.0000000000006324 |
| [4] |
CHAMORRO C, ROMERA M A, PARDO C. Gas embolism[J]. N Engl J Med, 2000, 342: 2001. |
| [5] |
HECKMANN J G, LANG C J, KINDLER K, HUK W, ERBGUTH F J, NEUNDÖRFER B. Neurologic manifestations of cerebral air embolism as a complication of central venous catheterization[J]. Crit Care Med, 2000, 28: 1621-1625. DOI:10.1097/00003246-200005000-00061 |
| [6] |
CHENG C K, CHANG T Y, LIU C H, CHANG C H, HUANG K L, CHIN S C, et al. Presence of gyriform air predicts unfavorable outcome in venous catheter-related cerebral air embolism[J]. J Stroke Cerebrovasc Dis, 2015, 24: 2189-2195. DOI:10.1016/j.jstrokecerebrovasdis.2015.04.028 |
| [7] |
宗酉明, 郁慧杰, 王海波. 中心静脉导管拔管后致脑空气栓塞一例[J]. 中华医学杂志, 2014, 94: 880. DOI:10.3760/cma.j.issn.0376-2491.2014.11.023 |
| [8] |
VAN IERSSEL S, SPECENIER P, BAAR I, DE BELDER F, JORENS P G, VERMORKEN J B. Acute hemiplegia caused by a retrograde cerebral venous air embolism after central venous catheter removal:an illustrative case[J]. Acta Clin Belg, 2010, 65: 51-53. DOI:10.1179/acb.2010.009 |
| [9] |
JEON S B, KANG D W. Cerebral air emboli on T2-weighted gradient-echo magnetic resonance imaging[J]. J Neurol Neurosurg Psychiatry, 2007, 78: 871. DOI:10.1136/jnnp.2006.102954 |
| [10] |
VAN HULST R A, KLEIN J, LACHMANN B. Gas embolism:pathophysiology and treatment[J]. Clin Physiol Funct Imaging, 2003, 23: 237-246. DOI:10.1046/j.1475-097X.2003.00505.x |
| [11] |
SCHLIMP C J, BOTHMA P A, BRODBECK A E. Cerebral venous air embolism: what is it and do we know how to deal with it properly?[J/OL]. JAMA Neurol, 2014, 71: 243. doi: 10.1001/jamaneurol.2013.5414.
|
| [12] |
BLANC P, BOUSSUGES A, HENRIETTE K, SAINTY J M, DELEFLIE M. Iatrogenic cerebral air embolism:importance of an early hyperbaric oxygenation[J]. Intensive Care Med, 2002, 28: 559-563. DOI:10.1007/s00134-002-1255-0 |
 2019, Vol. 40
2019, Vol. 40


