2. 海军军医大学(第二军医大学)长海医院介入诊疗科, 上海 200433
2. Department of Interventional Radiology, Changhai Hospital, Naval Medical University (Second Military Medical University), Shanghai 200433, China
胰腺实性假乳头状瘤(solid pseudopapillary tumor of pancreas,SPTP)为罕见胰腺肿瘤性病变,占所有胰腺肿瘤的1%以下[1]。1959年Frantz [2]首次将其描述为胰腺乳头状囊性肿瘤。1996年,世界卫生组织将其统一命名为胰腺实性假乳头状肿瘤[3],并描述SPTP为低级别的恶性肿瘤,主要患病人群为年轻女性[4-7]。SPTP常发生出血、囊变。以往发表了许多关于SPTP的报道,但其发生、发展过程尚不清楚。本研究通过总结SPTP的影像学表现探究其生长特点。
1 资料和方法 1.1 临床资料回顾性分析2012年5月至2018年11月于我院行手术切除且术后病理证实为SPTP的患者的病例资料。排除标准:手术、病理资料不完整者。本研究通过海军军医大学(第二军医大学)长海医院生物医学研究伦理委员会审批。
1.2 计算机断层扫描(computed tomography,CT)平扫加增强检查采用德国西门子公司64层螺旋CT扫描仪进行CT检查,管电压为120 kV,管电流为432 mA,螺距为1.8,层厚5.0 mm,层间距0.5 mm,重建图像层厚为1.5 mm。造影剂采用碘海醇(碘浓度300 mg/mL)80 ~ 90 mL,注射速率为3 ~ 4 mL/s,分别于注射造影剂后20 ~ 25 s、60 ~ 70 s、110 ~ 130 s行动脉期、门静脉期和延迟期扫描。
1.3 磁共振成像(magnetic resonance imaging,MRI)平扫加增强检查采用美国GE Healthcare公司Signa HDxt 3.0T MR仪完成MRI检查。常规自旋回波序列T1加权成像(T1-weighted imaging,T1WI)、抑脂T2加权成像(T2-weighted imaging,T2WI):层厚为3 mm,层间距为1 mm,视野为375 mm×300 mm。动态增强扫描采用梯度回波(gradient echo,GRE)容积内插体部检查(volume interpolated body examination,VIBE)序列:重复时间(repetition time,TR)为3.97 ms,回波时间(echo time,TE)为1.26 ms,矩阵为208×164,视野为375 mm×296 mm;造影剂为钆喷酸葡胺,剂量为0.1 mmol/kg,注射速率为3.0 mL/s,分别于注射造影剂后25 ~ 28 s、45 ~ 50 s、65 ~ 80 s行动脉期、门静脉期和延迟期扫描。
1.4 图像分析由2位影像医学科医师共同分析图像,意见不同时讨论后达成一致。CT、MRI主要观察指标包括肿瘤部位(胰腺头部、体部、尾部)、形状(圆形、类圆形、分叶状)、最大径、质地(实性、囊实性、囊性)、出血、钙化、强化方式等。肿瘤实性成分>90%定认为实性肿瘤,囊性成分>90%为囊性肿瘤。
1.5 分层分析依据文献[8],按患者性别、年龄、肿瘤最大径、肿瘤部位不同,对男性和女性、>40岁和≤ 40岁、肿瘤最大径>3 cm和≤ 3 cm及肿瘤位于胰头、胰体、胰尾的患者资料进行分层分析。
1.6 统计学处理应用SPSS 20.0软件进行数据处理和统计学分析。计量资料以x±s表示,2组间比较采用独立样本t检验;计数资料采用例数和百分数表示,组间比较采用χ2检验。检验水准(α)为0.05。
2 结果 2.1 患者基本特征共纳入103例SPTP患者104枚病灶的病例资料,发病年龄为12 ~ 65岁,平均发病年龄为(34.6±12.2)岁;总体最大径为10.1 ~ 139.9 mm,平均为(46.8±30.4)mm。其中男25例(24.3%),女78例(75.7%),男性患者的平均发病年龄为(40.4±11.3)岁,女性患者为(32.9±12.0)岁,差异有统计学意义(t = 2.951,P = 0.004);男性患者的肿瘤平均最大径为(36.8±25.3)mm,女性患者为(50.0±31.2)mm,差异有统计学意义(t = - 2.012,P = 0.046)。
2.2 肿瘤病灶特征肿瘤发生于胰头及钩突者36例,胰体21例,胰尾47例,其中1例患者胰头、胰尾各有1枚病灶(图 1)。肿瘤为圆形、椭圆形92枚,分叶状12枚。有假包膜75枚,无假包膜29枚,其中1枚假包膜破裂(图 2),其最大径为79.7 mm。有假包膜肿瘤的平均最大径为(56.7±30.1)mm。实性肿瘤60枚,囊实性36枚,囊性8枚。实性肿瘤平均最大径为(29.3±14.5)mm,囊实性肿瘤平均最大径为(71.9±31.9)mm,囊性肿瘤平均最大径为(65.6±21.9)mm。瘤内伴出血43枚,无出血61枚。瘤内不同程度钙化31枚,其中5枚为内部点状、结节状、不规则钙化,26枚为壁或分隔的点状、弧形或蛋壳样钙化;无钙化73枚。动态增强特征均表现为实性部分渐进性强化,但其增强达峰时间不同:69例患者行CT增强检查(31例门静脉期达峰,38例延迟期达峰),59例患者行MRI增强检查(14例门静脉期达峰,45例延迟期达峰);其中25例患者既行CT增强检查又行MRI增强检查,7例2种检查的增强达峰时间不一致(5例CT门静脉期达峰,MRI延迟期达峰;2例CT延迟期达峰,MRI门静脉期达峰)。主胰管扩张8例。左侧肾上腺受累2例。
|
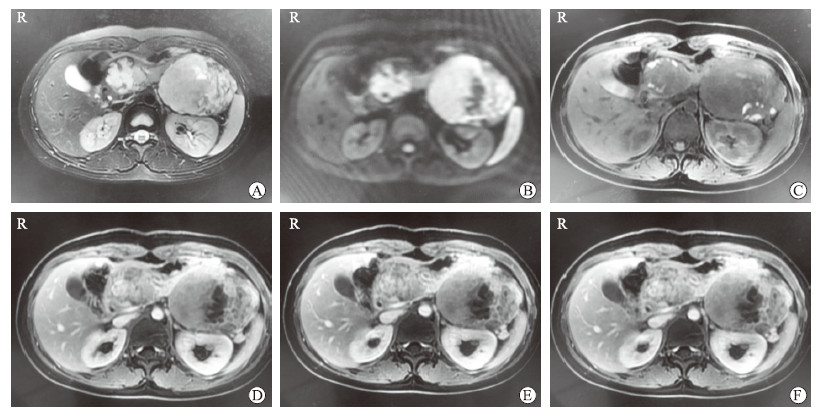
图 1 1例胰头、胰尾各1枚病灶SPTP患者的磁共振成像检查结果 Fig 1 Magnetic resonance imaging of a SPTP patient with 1 lesion in the head and 1 lesion in the tail of pancreas Female, 20 years old, upper abdominal pain for more than 1 month. One tumor was found in the head of pancreas and one in the tail of pancreas. The maximum diameter of the tumor in the head of pancreas was 44.6 mm, and that in the tail of pancreas was 84.8 mm. A: T2-weighted imaging; B: Diffusion-weighted imaging; C: T1-weighted imaging plain scan; D: T1-weighted imaging arterial phase; E: T1-weighted imaging portal vein phase; F: T1-weighted imaging delayed phase. SPTP: Solid pseudopapillary tumor of pancreas; R: Right |
|
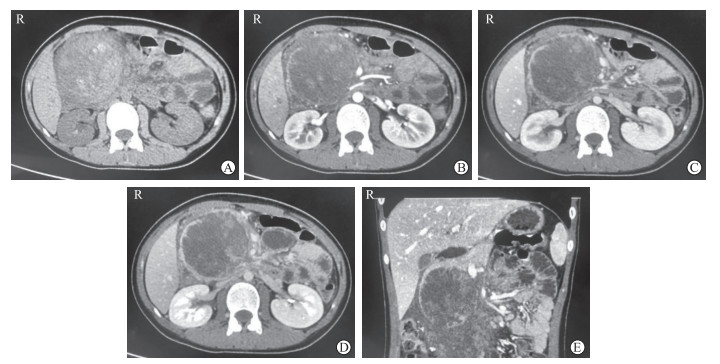
图 2 1例肿瘤假包膜破裂SPTP患者的计算机断层扫描检查结果 Fig 2 Computed tomography findings of a SPTP patient with ruptured pseudocapsule Female, 14 years old, abdominal discomfort for 2 months. The maximum diameter of the tumor was 79.7 mm and the pseudocapsule was ruptured. A: Axial position of plain scan; B: Axial position of arterial phase; C: Axial position of portal vein phase; D: Axial position of delayed phase; E: Coronary position of portal vein. SPTP: Solid pseudopapillary tumor of pancreas; R: Right |
2.3 分层分析结果
见表 1,女性SPTP患者肿瘤更容易出现假包膜、囊性退变及瘤内出血,与男性患者相比差异均有统计学意义(χ2 = 6.620、12.386、4.083,P均<0.05);男女SPTP患者的肿瘤部位、肿瘤最大径、肿瘤形状及瘤内钙化情况差异均无统计学意义(P均>0.05)。
|
|
表 1 SPTP患者104枚病灶的影像学特征分层分析结果 Tab 1 Stratified analysis results of image characteristics of 104 lesions in SPTP patients |
见表 1,年龄≤ 40岁SPTP患者更容易出现肿瘤囊性退变及瘤内出血,与年龄>40岁患者相比差异均有统计学意义(χ2 = 12.872、14.956,P均<0.01);在肿瘤部位、肿瘤最大径、肿瘤形状、是否有假包膜及瘤内钙化方面,年龄>40岁和≤ 40岁SPTP患者之间差异均无统计学意义(P均>0.05)。
见表 1,最大径>3 cm和≤ 3 cm的SPTP在肿瘤部位及是否有假包膜、囊性退变、瘤内钙化方面差异均有统计学意义(χ2 = 15.860、33.339、28.557、9.306,P均<0.01);最大径>3 cm的肿瘤主要分布在胰尾(33例,51.6%),其次为胰头(26例,40.6%),更容易形成假包膜及发生囊性退变、瘤内钙化;而最大径≤ 3 cm的肿瘤比较均匀地分布在胰头、胰体、胰尾,较少出现假包膜、囊性退变及瘤内钙化。在肿瘤形状、是否有瘤内出血方面,肿瘤最大径>3 cm和≤ 3 cm的SPTP之间差异均无统计学意义(P均>0.05)。肿瘤由实性向囊实性转变的最大径临界值为44.05 mm。
见表 1,在假包膜形成和囊性退变方面,胰腺不同位置的SPTP患者之间差异均有统计学意义(χ2 = 12.884、11.884,P = 0.002、0.003),其中胰尾肿瘤更容易形成假包膜及发生囊性退变,其次为胰头肿瘤;在肿瘤形状、是否有瘤内出血及钙化方面,不同部位的肿瘤之间差异均无统计学意义(P均>0.05)。
3 讨论既往报道中,SPTP好发年龄为20 ~ 39岁,男性占8.3% ~ 13.5% [9]。本研究中,SPTP的平均发病年龄为(34.6±12.2)岁,与既往报道相仿。其中24.3%(25/103)为男性,高于之前的报道,可能与随着健康体检普及与诊断水平的提高病灶检出率提高有关。男性患者的平均发病年龄[(40.4±11.3)岁]高于女性患者[(32.9±12.0)岁],而女性患者肿瘤平均最大径[(50.0±31.2)mm]大于男性患者[(36.8±25.3)mm],均与既往报道[10-11]相符。这些结果表明,SPTP患者中女性的发病年龄较男性更早并且女性肿瘤较男性大,有文献报道这是由于在发育过程中原始胰腺细胞靠近卵巢脊所致[12]。本研究中SPTP好发部位为胰尾,与既往文献报道[5]相仿。
本研究性别分层分析结果显示,女性患者肿瘤更容易出现假包膜、囊性退变及瘤内出血。有学者认为假包膜是肿瘤生长较大时压迫周围正常胰腺实质或肿瘤周围反应性纤维增生形成[13]。本组患者的基本特征显示,女性肿瘤最大径平均值较男性大,因此女性患者肿瘤更容易出现假包膜。有文献报道,SPTP是由囊性区域和实性区域及介于其中的假乳头状结构组成,假乳头即退变的肿瘤细胞、因黏附力下降而脱落的细胞及囊腔共同形成的组织结构,由肿瘤细胞围绕纤维血管分布构成,位于实性成分向囊性成分过渡区域。这些假乳头状结构呈网状,构成血窦[14],因而假乳头退化容易出血,出血吸收后则发生囊变。女性患者肿瘤内更容易发生囊性退变及出血,考虑与肿瘤较大有关。本研究肿瘤最大径分层分析结果也显示,最大径>3 cm的肿瘤更容易形成假包膜及发生囊性退变和瘤内钙化,与最大径≤ 3 cm的肿瘤相比差异均有统计学意义,这也进一步证明肿瘤较大更容易形成假包膜,肿瘤内更易发生囊性退变。另外,本研究1枚肿瘤包膜破裂,其最大径为79.7 mm,大于有假包膜肿瘤的平均最大径[(56.7±30.1)mm],推测肿瘤增大有假包膜破裂的风险。
本研究年龄分层分析结果显示,≤ 40岁的SPTP患者更容易出现肿瘤囊性退变及瘤内出血,结合患者基本特征分析结果,女性患者平均发病年龄低于男性患者,推测较年轻患者的肿瘤易发生囊性退变和瘤内出血的可能原因是女性患者较男性患者发病时间早、病程更长所致。但目前尚无大宗数据支持,有待进一步进行临床观察。
本研究肿瘤部位分层分析结果显示,胰尾肿瘤更容易形成假包膜及发生囊性退变,其次为胰头肿瘤,差异均有统计学意义(P均<0.01),结合肿瘤最大径分层分析结果,最大径>3 cm的肿瘤主要分布在胰尾,进一步证明了较大肿瘤更容易形成假包膜、发生囊性退变,因此胰尾肿瘤容易形成假包膜及发生囊性退变。
肿瘤由实性向囊实性转变的最大径临界值为44.05 mm,也就是说最大径<44.05 mm的肿瘤多表现为实性肿块,当肿瘤最大径>44.05 mm时肿瘤内部开始出血、囊变,钙化考虑为出血吸收后钙盐沉积所致。实性肿瘤平均最大径为(29.3±14.5)mm,囊实性肿瘤平均最大径为(71.9±31.9)mm,囊性肿瘤平均最大径为(65.6±21.9)mm。究其原因,可能为肿瘤由实性演变成囊实性时由于内部出血导致体积明显增大,而由囊实性演变成囊性时由于内部出血吸收、钙盐沉积使肿瘤体积有所减小。基于以上分析结果,推测SPTP初始主要是质地均匀的实性结构,后来随着肿瘤逐渐生长发生囊性退变、肿瘤出血,导致内部实性成分逐渐减少,囊性成分逐渐增多,故表现为实性、囊实性和囊性3种类型,3种类型逐步发生是一个动态过程。这可能也是大肿瘤更容易发生出血、囊性退变及钙化的原因。
SPTP需与以下肿瘤鉴别诊断:(1)胰腺导管腺癌,为乏血供肿块,内部出血、钙化少见,上游主胰管明显扩张,嗜血管、嗜神经生长。(2)胰腺神经内分泌肿瘤,小肿瘤强化均匀,大肿瘤内部出血囊变、坏死、钙化,特征性强化类型是动脉期强化明显。文献报道41.5%的胰腺神经内分泌肿瘤可能无明显强化[15]。乏血供的神经内分泌肿瘤因其增强后各期强化程度均低于正常胰腺实质,与SPTP很难鉴别,有待后期大样本研究进一步探索。(3)胰腺囊腺瘤,包括浆液性囊腺瘤及黏液性囊腺瘤。浆液性囊腺瘤多为多囊性肿瘤,中心为钙化结节或纤维瘢痕,内见多发分隔。黏液性囊腺瘤多数为寡囊性肿瘤,壁厚薄不均,内部成分黏稠。增强后囊腺瘤的囊性成分无强化,囊壁及分隔明显强化,不同于SPTP的渐进性强化。
综上所述,SPTP的生长过程可能是起初为完全实性肿瘤,随着肿瘤生长内部发生出血实性成分逐渐减少、囊性成分逐渐增多,整个过程中伴出血、囊性退变及钙化。在SPTP生长过程的不同阶段,影像学表现随着肿瘤内部成分的不同而发生改变。女性患者、≤ 40岁患者、胰尾、最大径>3 cm的肿瘤更容易形成假包膜及发生囊性退变、瘤内出血和钙化。
| [1] |
KLIMSTRA D S, WENIG B M, HEFFESS C S. Solid-pseudopapillary tumor of the pancreas:a typically cystic carcinoma of low malignant potential[J]. Semin Diagn Pathol, 2000, 17: 66-80. |
| [2] |
FRANTZ V K. Tumors of the pancreas[M]//ROSAI J, SORBIN L. Atlas of tumor pathology. Washington, DC: Armed Forces Institute of Panthology, 1959: 32-33.
|
| [3] |
KLÖPPEL G, SOLCIA E, SOBIN L H, LONGNECKER D S, CAPELLA C. Histological typing of tumours of the exocrine pancreas[M]//World Health Organization. Histological typing of tumours of the exocrine pancreas. Berlin: Springer, 1996: 1.
|
| [4] |
LAW J K, AHMED A, SINGH V K, AKSHINTALA V S, OLSON M T, RAMAN S P, et al. A systematic review of solid-pseudopapillary neoplasms:are these rare lesions?[J]. Pancreas, 2014, 43: 331-337. DOI:10.1097/MPA.0000000000000061 |
| [5] |
PATIL T B, SHRIKHANDE S V, KANHERE H A, SAOJI R R, RAMADWAR M R, SHUKLA P J. Solid pseudopapillary neoplasm of the pancreas:a single institution experience of 14 cases[J]. HPB (Oxford), 2006, 8: 148-150. DOI:10.1080/13651820510035721 |
| [6] |
JAGANNATH P, BHANSALI M S, MURTHY S K, MOHANDAS K M, SWAROOP V S, DESOUZA L J. Solid and cystic papillary neoplasm of pancreas-a report of seven cases[J]. Indian J Gastroenterol, 1994, 13: 112-114. |
| [7] |
BHUTANI N, KAJAL P, SINGLA S, SANGWAN V. Solid pseudopapillary tumor of the pancreas:experience at a tertiary care centre of Northern India[J]. Int J Surg Case Rep, 2017, 39: 225-230. DOI:10.1016/j.ijscr.2017.07.064 |
| [8] |
陈文芳, 顾君英. 胰腺实性-假乳头状瘤的非典型影像学表现[J]. 中国临床医学, 2017, 24: 433-438. |
| [9] |
PAPAVRAMIDIS T, PAPAVRAMIDIS S. Solid pseudopapillary tumors of the pancreas:review of 718 patients reported in English literature[J]. J Am Coll Surg, 2005, 200: 965-972. DOI:10.1016/j.jamcollsurg.2005.02.011 |
| [10] |
MACHADO M C, MACHADO M A, BACCHELLA T, JUKEMURA J, ALMEIDA J L, CUNHA J E. Solid pseudopapillary neoplasm of the pancreas:distinct patterns of onset, diagnosis, and prognosis for male versus female patients[J]. Surgery, 2008, 143: 29-34. DOI:10.1016/j.surg.2007.07.030 |
| [11] |
GUERRACHE Y, SOYER P, DOHAN A, FARAOUN S A, LAURENT V, TASU J P, et al. Solid-pseudopapillary tumor of the pancreas:MR imaging findings in 21 patients[J]. Clin Imaging, 2014, 38: 475-482. DOI:10.1016/j.clinimag.2014.01.015 |
| [12] |
KOSMAHL M, SEADA LS, JÄNIG U, HARMS D, KLÖPPEL G. Solid-pseudopapillary tumor of the pancreas:its origin revisited[J]. Virchows Arch, 2000, 436: 473-480. DOI:10.1007/s004280050475 |
| [13] |
吴珂, 许伟, 谭向龙, 张兴华, 李颖. 胰腺实性假乳头状瘤MRI表现和外科治疗[J]. 中国医学影像学杂志, 2018, 26: 418-421. DOI:10.3969/j.issn.1005-5185.2018.06.005 |
| [14] |
马小龙, 汪建华, 蒋慧, 陆建平, 刘崎. 胰腺实性-假乳头状瘤的不同类型影像学表现与病理对照分析[J]. 中华医学杂志, 2012, 92: 170-174. DOI:10.3760/cma.j.issn.0376-2491.2012.03.007 |
| [15] |
HUMPHREY P E, ALESSANDRINO F, BELLIZZI A M, MORTELE K J. Non-hyperfunctioning pancreatic endocrine tumors:multimodality imaging features with histopathological correlation[J]. Abdom Imaging, 2015, 40: 2398-2410. DOI:10.1007/s00261-015-0458-0 |
 2019, Vol. 40
2019, Vol. 40


