2. 海军军医大学(第二军医大学)长征医院普外三科, 上海 200003
2. Department of General Surgery(Ⅲ), Changzheng Hospital, Naval Medical University(Second Military Medical University), Shanghai 200003, China
随着医学影像检查手段的丰富和更新,甲状腺结节的检出率呈增高趋势,甲状腺癌的发病率亦随之递增,然而有报道认为甲状腺癌的过度诊断比例高达77%[1],常导致过度治疗,造成不必要的手术和不可逆的损伤[2]。因此,对甲状腺结节良恶性质的判断尤为重要。超声检查是诊断甲状腺结节的有效影像学检查手段[3],但超声影像高度依赖机器操控,具有实时动态的特点,其产生的数据庞大复杂,人工分析时工作量巨大且准确性易受人为主观因素影响[4]。近年来,国内自主研发出针对甲状腺结节的人工智能(artificial intelligence,AI)自动检测系统AI-SONICTM Thyroid,其可快速、精准、客观地在短短几秒内锁定病灶,进行自动分析、自动生成诊断报告,为超声医师甲状腺结节良恶性的判读提供了高准确度、高效率的决策支持[5]。
本研究通过回顾性分析98例手术患者共137个甲状腺结节的超声影像资料,以术后病理结果为金标准,比较常规超声检查、AI自动检测系统检测两种方法术前评估甲状腺结节良恶性的诊断效能,探讨AI自动检测系统在甲状腺结节术前超声诊断中的应用价值。
1 资料和方法 1.1 研究对象选取2019年4月至2019年7月于我院普通外科接受手术治疗的甲状腺结节患者。所有患者术前均接受常规超声检查和AI自动检测系统检测。排除标准:曾诊断为偏良性结节仅进行超声随访者;超声诊断为偏恶性结节未进行手术者;诊断为偏恶性结节,进行细胞学穿刺,而未实施手术者。共98例患者137个结节纳入分析,其中男23例、女75例,年龄为26~71(48.1±10.2)岁。术后病理确诊恶性结节96个,平均最大径为(11.20±6.31)mm,其中77个为乳头状癌、4个为滤泡上皮性肿瘤、1个为髓样癌、10个为不典型增生、4个为其他恶性肿瘤;良性结节41个,平均最大径为(20.65±7.83)mm,其中14个为腺瘤、14个为结节性甲状腺肿、9个为桥本甲状腺炎相关性结节、2个为滤泡结节增生、1个为胶质潴留、1个为术后胶质凝集。
1.2 仪器与方法 1.2.1 常规超声检查采用Hitachi Preirus超声诊断仪(日本日立公司)进行甲状腺常规超声检查,探头型号L74M,频率5~13 MHz。系统参数恒定:增益30 dB,时间增益补偿为中间位(零补偿),图像聚焦区深度2.0~3.75 cm,组织热指数<0.4,机械指数1.2。
由2名从事甲状腺超声诊断工作10年以上的超声医师按照上海市超声质量控制要求和《超声医学》第6版[6]甲状腺超声操作要点及诊断标准,对术前患者的甲状腺组织(两侧叶、峡部)进行全面细致检查。检查中若发现结节,则需反复重点扫查,并将检查到的甲状腺结节声学特征按照美国放射学会(American College of Radiology,ACR)甲状腺影像报告和数据系统(Thyroid Imaging Reporting and Data System,TI-RADS)分类标准[7-8]进行评估,以实性、低回声或极低回声、边界不规则或边缘小分叶、纵横比>1、微钙化这5项特征作为判断偏恶性的条件,确立TI-RADS 3类(无恶性超声表现)、4a类(1个恶性超声表现)、4b类(2个恶性超声表现)、4c类(3个或4个恶性超声表现)和5类(5个恶性超声表现)。将TI-RADS 4~5类归为偏恶性,TI-RADS 3类归为偏良性[9-10],如2名医师共同判读甲状腺结节TI-RADS分类在4a及以上,则评判为偏恶性可能。
1.2.2 AI自动检测系统检测采用AI-SONICTM Thyroid甲状腺结节人工智能辅助诊断系统(DEMETICS®超声诊断机器人,浙江德尚韵兴医疗科技有限公司),该系统经过6万余例甲状腺结节穿刺及病理结果对照的深度学习。所有参与研究的对象均经过我院伦理委员会专家论证,受检者检查前均签署了知情同意书。检查步骤同常规超声检查,由2名从事甲状腺超声诊断工作10年以上的超声医师进行操作,并由AI自动检测系统公司专业技术人员对超声操作医师进行系统的AI诊断流程培训,以便于获取标准化的超声切面图像。检查时重点观察结节的大小、边界、形态、内部回声、有无钙化等超声影像特征,将扫查结节的纵、横最大切面多角度、多幅显示的JPEG格式静态图以DICOM格式实时传输存储到AI-SONICTM Thyroid自动检测系统,进行自动标记、处理、分析,通过AI算法自动量化识别甲状腺结节的大小、边界、形态、内部回声、钙化灶5类特征,每个结节分别经过4次纵、横切面显示,实时冻结存储传输至自动判读系统,直至TI-RADS分类及良恶性概率值趋于稳定时,记录系统自动判读结节的最高一次TI-RADS分类及良恶性概率值(概率值范围为0~1,其中0~0.5为偏良性,0.6~1为偏恶性)。
1.3 统计学处理应用SPSS 21.0软件进行统计学分析,数据均以个数和百分数表示,并以术后病理结果为金标准,采用基于Kappa 系数的一致性检验[11]分别评估常规超声检查、AI自动检测系统检测与术后病理结果的一致性,计算Kappa 系数、灵敏度、特异度、准确度。Kappa 系数越大说明两种检测结果一致性越高,Kappa≥0.75说明结果一致性好,0.4≤Kappa<0.75说明结果一致性一般,Kappa<0.4说明缺乏一致性。检验水准(α)为0.05。
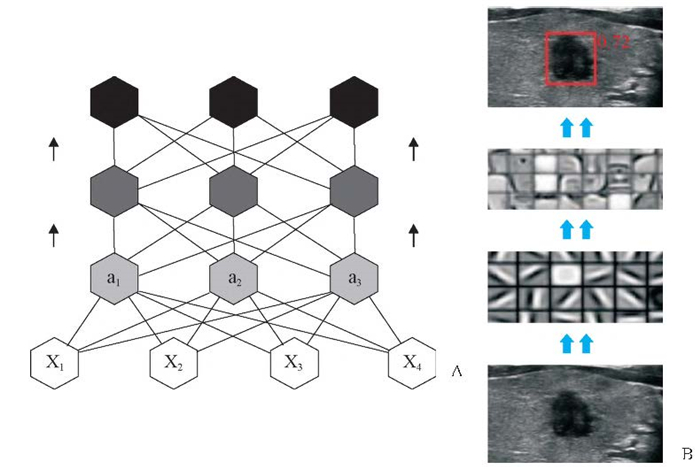
2 结果 2.1 两种检查方法的术前超声诊断结果AI自动检测系统通过卷积神经网络针对甲状腺结节超声图像特征进行大数据分析(图 1),较常规超声检查更精细、更直观(图 2、3)。137个结节中,常规超声检查提示39个偏良性、98个偏恶性;AI自动检测系统提示36个偏良性、97个偏恶性,漏诊4个。
|
图 1 AI自动检测系统通过卷积神经网络提取甲状腺病灶超声图像特征示意图 Fig 1 Ultrasonic image feature extraction of thyroid lesions by AI automatic detection system A: A neural network has thousands of features that are simultaneously adjusted in the direction of increasing classification ability, that is, changes into true common features. As sample size increases, the characteristics of true commonality will remain, and the features that occur by chance will tend to be randomly distributed in positive and negative samples (X1-X4: Respective structural features of different types of thyroid nodules; a1-a3: Common features after classification of different types of thyroid nodules; Black arrows represent different characteristics toward directional adjustment of classification ability). B: From bottom to top, AI automatic detection system recognizes thyroid nodules→precise segmentation→pixel-by-pixel quantitative analysis of structural features→AI automatic detection system gives benign and malignant probability of thyroid nodules. AI: Artificial intelligence |
|
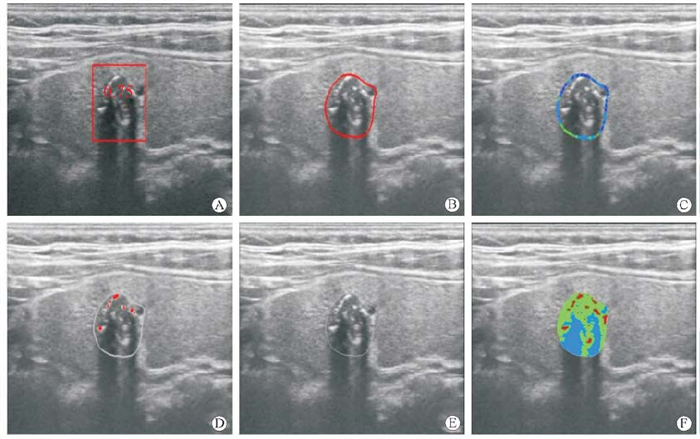
图 2 AI-SONICTM Thyroid系统自动识别标记并量化甲状腺结节特征(TI-RADS 4c类,病理结果证实甲状腺乳头状癌) Fig 2 AI-SONICTM Thyroid System automatically recognizes markers and quantifies thyroid nodule characteristics (TI-RADS 4c, papillary thyroid carcinoma confirmed by pathological findings) A: On the longitudinal section of the right thyroid nodule, the benign and malignant probability of this lesion was 0.75 detected by AI; B: Automatic analysis of red boundary line suggested puncture; C: Edge feature analysis, the color changed from blue, green, yellow and red in turn to clear to blur; D: Dotted red represented a strong echo; E: AI automatic detection showed that the components of the lesion were mainly solid ingredient; F: The internal echogenic color of the lesion changed from homogenous to heterogeneous from blue, green, yellow and red. AI: Artificial intelligence; TI-RADS: Thyroid Imaging Reporting and Data System |

|
图 3 AI-SONICTM Thyroid系统自动识别标记并量化甲状腺结节特征(TI-RADS 3类,病理结果证实甲状腺腺瘤囊性变) Fig 3 AI-SONICTM Thyroid System automatically recognizes markers and quantifies thyroid nodule characteristics (TI-RADS 3, cystic degeneration of thyroid adenoma confirmed by pathological findings) A: On the longitudinal section of the right thyroid nodule, the benign and malignant probability of this lesion was 0.08 detected by AI; B: Automatic analysis of red boundary line suggested follow-up observation; C: Edge feature analysis, the color changed from blue, green, yellow and red in turn to clear to blur; D: Dotted red represented a strong echo; E: AI automatic detection showed that the purple area was the cystic component of the lesion; F: The internal solid ingredient echogenic color of the lesion changed from homogenous to heterogeneous from blue, green and red. AI: Artificial intelligence; TI-RADS: Thyroid Imaging Reporting and Data System |
2.2 两种检查方法诊断结果与术后病理结果的一致性
137个结节中,常规超声检查发现137个,其中123个结节与术后病理结果一致,14个结节与术后病理结果不一致。
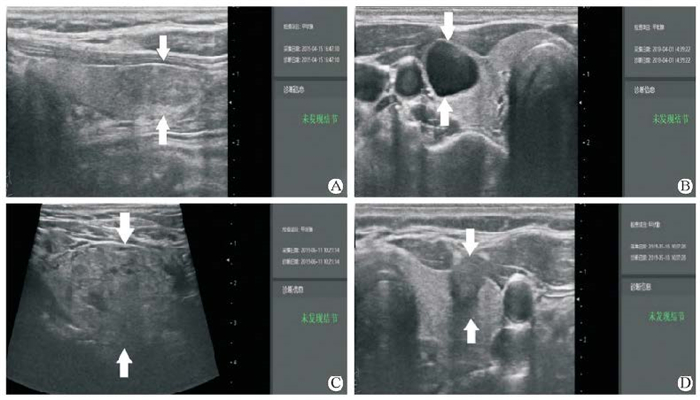
123个与术后病理结果一致的结节中,33例常规超声诊断偏良性,90例常规超声诊断偏恶性;14个与术后病理结果不一致的结节中,8个良性结节常规超声诊断偏恶性,6个恶性结节常规超声诊断偏良性。AI自动检测系统发现结节133个、漏诊(AI自动检测系统报告均提示未发现结节)4个,其中114个结节与术后病理结果一致,23个结节与术后病理结果不一致。114个与术后病理结果一致的结节中,28例AI自动检测系统诊断偏良性,86例AI自动检测系统诊断偏恶性;23个与术后病理结果不一致的结节中,11个良性结节AI自动检测系统诊断偏恶性,8个恶性结节AI自动检测系统诊断偏良性,漏诊的4个结节术后病理诊断2个为良性结节、2个为恶性结节(图 4)。
|
图 4 AI-SONICTM Thyroid系统未识别的4例甲状腺结节病例 Fig 4 Four unidentified cases of thyroid nodules by AI-SONICTM Thyroid System A: A 33-year-old woman with right thyroid papillary carcinoma (arrows), and nodule was not found by AI on longitudinal section; B: A 42-year-old woman with cystic changes in the right thyroid adenoma (arrows), and nodules were not found by AI on transverse section; C: A 39-year-old woman with a right nodular goiter penetrating the sternum (arrows), and nodule was not found by AI on longitudinal section; D: A 49-year-old woman with left papillary carcinoma of the thyroid (arrows), and nodule was not found by AI on transverse section. AI: Artificial intelligence |
常规超声诊断甲状腺结节良恶性的灵敏度为93.75%(90/96),特异度为80.49%(33/41),准确度为89.78%(123/137),与病理诊断结果一致性较高(Kappa=0.75,P<0.001);AI自动检测系统甲状腺结节良恶性的灵敏度为89.58%(86/96),特异度为68.29%(28/41),准确度为83.21%(114/137),与病理诊断结果一致性一般(Kappa=0.59,P<0.001)。
3 讨论随着人们生活方式的改变,超声检查已成为筛查甲状腺结节的主要方式。超声检查具有无创、便捷、费用低、可重复等优点,可显示甲状腺结节的个数、提示结节的物理性质,为甲状腺结节的临床治疗策略的制定提供参考依据[12]。本研究纳入我院术前行甲状腺超声检查的98例患者共计137个结节为研究对象,证实超声检查可较好地显示结节的位置、大小、边缘、形态、回声、钙化等特征,并可有倾向地提示结节的物理性质;以术后病理结果为金标准,常规超声检查的灵敏度(93.75%,90/96)和准确度(89.78%,123/137)较高,与病理结果的诊断一致性较高(Kappa=0.75,P<0.001)。
有经验的超声医师可以熟练进行甲状腺超声检查并做出较为准确的ACR TI-RADS分类,但是不同技术级别的医师诊断操作时难免存在主观差异。如能基于甲状腺病变的超声特征,采用计算机技术对结节内部囊实成分、回声强度、边界清晰度、形态规则度、钙化程度、形状、纹理异质度等进行智能化恶性风险判读并计算,得到可靠的量化超声特征参数,则有助于甲状腺疾病的辅助诊断。目前已上市的甲状腺超声图像分析系统AmCAD-UT® Detection利用计算机视觉技术量化分析甲状腺结节的超声特征,即时生成数字化超声报告,预测甲状腺结节良恶性风险值[13]。已有研究表明,AI通过深度学习和有效训练可快速自动识别甲状腺结节并绘制结节边界框,对异常区域进行自动分割、量化分析,对检测出的结节进行良恶性风险数值评估,快速生成精准的超声诊断结果,降低人为因素导致的医疗错误[14-15]。本研究表明,AI自动检测系统在甲状腺结节良恶性诊断中的灵敏度、准确度分别为89.58%(86/96)、83.21%(114/137),与病理诊断结果的一致性一般(Kappa=0.59,P<0.001),稍逊于有10年以上工作经验的超声医师使用常规超声检查诊断甲状腺结节良恶性的灵敏度(93.75%)和准确度(89.78%),但已较为接近。
入选研究的137个甲状腺结节中,AI自动检测系统漏诊2个良性结节、2个恶性结节。其中1个甲状腺恶性结节边界清晰、内部回声为等回声,与正常甲状腺本底回声较相近,故AI不易识别出甲状腺结节的存在;且相比于纵切面,在横切面扫查时AI可参考的腺体实质图像范围变小,识别度大大减低。1个甲状腺囊性结节紧靠腺体边缘,易误判为包膜外血管横断面结构,导致该结节无法被识别显示。1个结节性甲状腺肿因结节位置较深,体积较大,并向胸骨后延伸,占据整个纵切面,AI将切面显示的结节整体识别成正常甲状腺实质,缺少正常甲状腺实质回声作为参照,导致该结节无法被识别。1个甲状腺恶性结节横切面显示结节突破前包膜,并与周边毗邻组织相粘连,干扰AI对结节轮廓的自动识别,导致该结节无法被AI识别。
临床上对于超声诊断偏良性的甲状腺结节患者大多采取定期随访的处理方案,较少进行手术切除加病理诊断,因此AI对于良性结节可搜集获取学习的数据较少,缺乏深度学习训练的机会,导致其对甲状腺良性结节识别的准确度降低。本研究结果显示AI诊断甲状腺结节的特异度仅为68.29%(28/41),推测原因如下:(1)超声扫查存储图像过程中结节边缘会因冻结非标准切面等原因显示欠清晰;(2)腺体内部血管横切面被AI错误识别成甲状腺结节;(3)因病灶边缘与邻近的气管、大血管、脂肪结缔组织、颈前肌等结构分界不清,从而可能导致误判。不同于计算机断层扫描、磁共振成像等静态影像,超声检查是实时、动态、可重复的影像检查技术,在图像传输过程中任何一帧画面的丢失,都可能造成信息的漏诊或误诊。目前AI软件仍缺少动态视频、彩色多普勒图像及弹性图像的多模态诊断信息。在今后AI自动检测系统中如能补充对甲状腺结节位置的准确描述、彩色多普勒血流显像以及弹性超声评估等数据,并能实时、动态多切面显示病灶所在具体位置(如上极、下极、中部、包膜下及结节周边毗邻的空间组织结构等),给予同步精准的定位信息,则有利于提高AI对甲状腺结节的自动准确识别。
基于本次研究结果,AI自动检测系统诊断甲状腺结节良恶性的灵敏度、准确度稍逊于常规超声检查,但已较为相近,可作为术前评估甲状腺结节良恶性的有效补充。目前利用AI自动检测系统可以辅助完成甲状腺结节术前超声诊断,针对结节良恶性质的风险进行概率值预测,这虽然不能显著提高具有丰富工作经验的超声医师的诊断准确率,但有望缩短年轻超声医师和基层超声医师的培养周期,减少不同超声医师之间的诊断差异,提高工作效率[16-17]。
目前AI辅助甲状腺结节超声诊断尚处于初级阶段,我院自2019年4月1日起在国内率先开展AI自动检测系统辅助临床术前超声诊断甲状腺结节工作,但应用时间尚短,后续可增大样本量,细化结节分类及研究入选标准,进一步提高AI自动检测系统诊断甲状腺结节的准确度。本次研究是AI在医院临床使用中的先行探索,实验设计中为了确保AI感兴趣区人工操作的稳定性,我们慎重选用2名从事甲状腺超声诊断工作10年以上的超声医师进行操作,并由AI自动检测系统公司专业技术人员对超声操作医师进行系统的AI诊断流程培训,掌握标准化操作规范,以获取统一标准化切面的超声图像,便于AI进行自动识别勾画感兴趣区,确保对甲状腺结节识别和判断的较高准确度。今后我们会进一步优化人工智能分析算法,对目标区域进行降噪、增强、细化图像特征等预处理,提升AI诊断的稳定性。目前使用的AI分析软件仅基于灰阶图像,研发有效分析动态视频、彩色多普勒图像及弹性图像的多模态诊断结果将为临床医师提供更全面的信息,提高诊断准确性。
| [1] |
VACCARELLA S, FRANCESCHI S, BRAY F, WILD C P, PLUMMER M, DAL MASO L. Worldwide thyroid-cancer epidemic? The increasing impact of overdiagnosis[J]. N Engl J Med, 2016, 375: 614-617. DOI:10.1056/NEJMp1604412 |
| [2] |
LA VECCHIA C, MALVEZZI M, BOSETTI C, GARAVELLO W, BERTUCCIO P, LEVI F, et al. Thyroid cancer mortality and incidence:a global overview[J]. Int J Cancer, 2015, 136: 2187-2195. DOI:10.1002/ijc.29251 |
| [3] |
中华人民共和国国家卫生健康委员会.甲状腺癌诊疗规范(2018年版)[J/CD].中华普通外科学文献(电子版), 2019, 13:1-15. http://www.cnki.com.cn/Article/CJFDTotal-ZHPD201901002.htm
|
| [4] |
章晶, 徐辉雄, 张一峰, 徐军妹, 刘畅, 郭乐杭, 等.甲状腺影像报告和数据系统在甲状腺结节分类中的前瞻性验证[J/CD].中华医学超声杂志(电子版), 2014, 11:167-171. http://www.cnki.com.cn/Article/CJFDTotal-ZHCD201402015.htm
|
| [5] |
刘隆忠, 李擎, 龙杏章, 刘颖, 云苗, 李安华.基于计算机辅助诊断技术的超声图像处理软件对甲状腺结节诊断效能的初步研究[J/CD].中华医学超声杂志(电子版), 2018, 15:942-947. http://www.cnki.com.cn/Article/CJFDTotal-ZHCD201812011.htm
|
| [6] |
郭万学, 燕山, 杨浣宜, 伍于添, 王志刚.超声医学[M]. 6版.北京: 人民军医出版社, 2011: 263-278.
|
| [7] |
于立超, 吴长君. 结合甲状腺影像报告及数据系统的甲状腺超声CAD的研究进展[J]. 临床与病理杂志, 2018, 38: 628-633. DOI:10.3978/j.issn.2095-6959.2018.03.028 |
| [8] |
TESSLER F N, MIDDLETON W D, GRANT E G, HOANG J K, BERLAND L L, TEEFEY S A, et al. ACR thyroid imaging, reporting and data system (TI-RADS):white paper of the ACR TI-RADS Committee[J]. J Am Coll Radiol, 2017, 14: 587-595. DOI:10.1016/j.jacr.2017.01.046 |
| [9] |
宋琳琳, 周贵明, 朱莉, 孟召伟, 仇晓菲, 陈冬玥.甲状腺影像报告和数据系统联合甲状腺细胞病理学Bethesda报告系统对甲状腺结节的应用价值[J/CD].中华医学超声杂志(电子版), 2018, 15: 713-718. http://www.cnki.com.cn/Article/CJFDTotal-ZHCD201809013.htm
|
| [10] |
候雪琴, 范雪, 杨凌菲, 董建, 宋涛. 甲状腺影像报告和数据系统分类诊断甲状腺结节良恶性的准确性[J]. 中国影像医学杂志, 2015, 23: 489-493. |
| [11] |
郭轶斌, 郭威, 秦宇辰, 何倩, 张新佶, 吴骋. 基于Kappa系数的一致性检验及其软件实现[J]. 中国卫生统计, 2016, 33: 169-174. |
| [12] |
刘如玉, 姜玉新, 杨筱, 王莹, 高璐滢, 刘佳, 等.甲状腺结节的影像报告与数据系统分级与2015年美国甲状腺学会推荐超声恶性风险分层的比较研究[J/CD].中华医学超声杂志(电子版), 2017, 14: 263-268. http://www.cnki.com.cn/Article/CJFDTotal-ZHCD201704008.htm
|
| [13] |
MA J, WU F, ZHU J, XU D, KONG D. A pre-trained convolutional neural network based method for thyroid nodule diagnosis[J]. Ultrasonics, 2017, 73: 221-230. DOI:10.1016/j.ultras.2016.09.011 |
| [14] |
PARK C S, KIM S H, JUNG S L, KANG B J, KIM J Y, CHOI J J, et al. Observer variability in the sonographic evaluation of thyroid nodules[J]. J Clin Ultrasound, 2010, 38: 287-293. |
| [15] |
CHOI S H, KIM E K, KWAK J Y, KIM M J, SON E J. Interobserver and intraobserver variations in ultrasound assessment of thyroid nodules[J]. Thyroid, 2010, 20: 167-172. DOI:10.1089/thy.2008.0354 |
| [16] |
NARAYAN N S, MARZILIANO P, KANAGALINGAM J, HOBBS C G. Speckle patch similarity for echogenicity-based multiorgan segmentation in ultrasound images of the thyroid gland[J]. IEEE J Biomed Health Inform, 2017, 21: 172-183. DOI:10.1109/JBHI.2015.2492476 |
| [17] |
EL-HASSOUN O, MARUSCAKOVA L, VALASKOVA Z, BUCOVA M, POLAK S, HULIN I. Artificial intelligence in service of medicine[J]. Bratisl Lek Listy, 2019, 120: 218-222. |
 2019, Vol. 40
2019, Vol. 40


