甲状腺相关眼病(thyroid associated ophthalmopathy,TAO)是一种复杂的自身免疫性疾病,以眶周结缔组织水肿和炎症为主要特征[1-3],其发病率居成人眼眶病发病率的首位[4]。甲状腺相关视神经病变(dysthyroid optic neuropathy,DON)是TAO中最严重的类型,约占TAO的5%~7%,一旦发生则严重影响患者的视功能,表现为视力下降、视野缺损、色觉减退、视盘水肿等[5-7]。其发病机制可能是眼眶内增殖的成纤维细胞和脂肪组织分泌过多的糖胺聚糖导致眶周组织水肿、眶尖拥挤,从而抑制轴浆回流或诱导视神经缺血[8]。但目前尚无统一标准明确诊断DON。DON的危险因素包括年龄、性别、吸烟史、甲状腺功能状态等,且这些危险因素也可以加速DON的发展[9-10]。本研究回顾性分析在我院就诊的98例DON患者的临床资料,旨在探寻DON最具诊断意义的临床特征,并且对这些DON患者的人口资料信息进行统计分析,筛选出DON的高危因素,以期在临床工作中能够对高危TAO患者开展灵敏度较高的检查,达到早期诊断DON的目的。
1 资料和方法 1.1 研究对象回顾2015年1月至2017年12月在我院住院治疗的98例DON患者的病例资料。TAO诊断标准[11]:(1)上睑退缩,且满足甲状腺功能异常、眼球突出>21 mm、眼外肌受累或视功能障碍中的任一条件; (2)无上睑退缩,但甲状腺功能异常,且合并眼球突出>21 mm、眼外肌受累或视功能障碍中的任一条件。TAO视神经受累的判断标准[11]:(1)视力下降;(2)色觉异常;(3)相对性瞳孔传入阻滞(relative afferent papillary defect,RAPD)阳性;(4)视野改变;(5)眼底改变,如视盘水肿、视盘苍白;(6)CT或MRI检查发现眶尖拥挤征象。纳入标准:(1)年龄>18岁;(2)至少有一只眼可疑或确诊为DON;(3)具有眼眶水平位+冠状位CT扫描或MRI检查图像;(4)调查前未接受治疗或已接受过部分治疗的患者。排除标准:(1)其他可引起视功能障碍的疾病,如严重的白内障、屈光不正、青光眼、翼状胬肉及角膜病变等;(2)有眼外伤史。本研究通过我院医学伦理委员会审批。
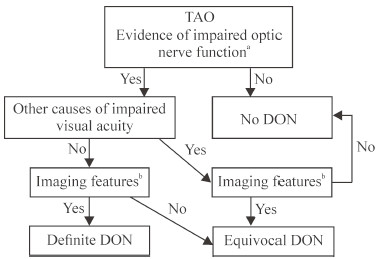
1.2 患者分级结合Wakelkamp等[12]和McKeag等[13]研究使用方法对所有眼进行诊断,分为确诊(诊断明确)、可疑(诊断不明确但可疑)、排除(没有证据支持诊断),详见图 1。
|
图 1 DON诊断分级流程图 Fig 1 Diagnostic hierarchical flow chart of DON a: Any of the evidences of vision loss, reduced colour vision, visual field defects, optic disc swelling or pallor, relative afferent papillary defect or abnormal visual evoked potential latency amplitude; b: Either of the imaging features of apical crowding or optic nerve stretch. TAO: Thyroid associated ophthalmopathy; DON: Dysthyroid optic neuropathy |
1.3 观察项目
记录98例DON患者(196只眼)的年龄、性别、病程、吸烟史、甲状腺功能状态以及眼部临床表现和影像学检查结果等资料。观察患者最佳矫正视力(best corrected visual acuity,BCVA)、色觉、眼压、眼球突出度、眼底光学相干断层扫描、眼底照相、视野、眼眶CT(水平位+冠状位)、眼球运动等眼科检查结果。根据临床活动度评分(clinical activity score,CAS)进行评分。CAS评分标准如下:(1)自发性眼球后疼痛;(2)眼球转动时诱发疼痛;(3)眼睑充血;(4)结膜充血;(5)泪阜或皱襞肿胀;(6)眼睑肿胀;(7)结膜水肿。每项得1分,共7分;7项中出现3项及以上为活动期,否则为非活动期。
1.4 统计学处理采用SPSS 17.0软件对数据进行统计学分析。呈正态分布的计量资料以x±s表示,组间比较采用两独立样本比较的t检验;计数资料以例数和百分数表示。检验水准(α)为0.05。
2 结果 2.1 患者基本情况98例DON患者中男性59例、女性39例,男女比例为1.51:1;年龄为34~74岁,平均(52.51±10.25)岁。男性平均年龄为(54.10±11.27)岁、女性(50.10±8.03)岁,男女年龄比较差异有统计学意义(t =2.050,P=0.043)。98例患者病程平均为(27.08±39.60)个月,均有吸烟或接触二手烟史。96例DON患者在诊断为TAO时或之前有甲状腺功能亢进病史,2例有甲状腺功能减退病史,均服用抗甲状腺药物或甲状腺素片,其中10例行放射性碘治疗、5例行甲状腺切除术治疗。
2.2 DON患者诊断情况对98例患者196只眼分别进行评估,确诊122只眼、可疑56只眼、排除18只眼。纳入确诊和可疑DON眼共178只,其中右眼87只、左眼91只。18例单眼DON患者中6例为可疑,80例双眼DON患者中12例为可疑。98例患者中有1例黄斑裂孔,1例曾患视网膜分支静脉阻塞,10例轻度白内障,2例视网膜玻璃膜疣,2例老年性黄斑变性。
2.3 眼部检查结果178只确诊和可疑DON眼中130只(73.03%)色觉减退。其中确诊DON的122只眼中101只(82.79%)色觉减退;可疑DON的56只眼中29只(51.79%)色觉减退;非DON的18只眼中17只(94.44%)色觉正常,仅1只眼色觉减退,该眼既往曾患视网膜分支静脉阻塞。196只眼的眼部检查结果见表 1。
|
|
表 1 98例DON患者眼部检查结果 Tab 1 Eye examination results of 98 patients with DON |
2.3.1 BCVA
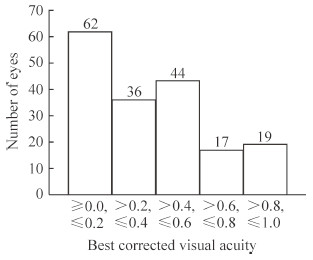
178只确诊和可疑DON眼中BCVA≤0.6有142只(79.78%),其中确诊DON的122只眼中有99只(81.15%),可疑DON的56只眼中有43只(76.79%);非DON的18只眼中有3只(16.67%),这3只眼既往分别患有视网膜分支静脉阻塞、青光眼、黄斑裂孔。BCVA为1.0的DON患者有8例,其中3只眼确诊DON,5只为可疑DON。详见图 2。
|
图 2 178只确诊和可疑DON眼最佳矫正视力 Fig 2 Best corrected visual acuity of 178 DON eyes DON: Dysthyroid optic neuropathy |
2.3.2 RAPD
122只确诊DON眼中50只(40.98%)RAPD阳性,56只可疑DON眼中22只(39.28%)RAPD阳性,非DON眼均无RAPD阳性。
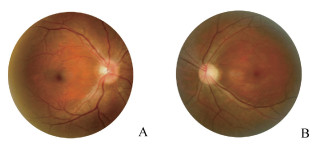
2.3.3 眼底检查结果178只确诊和可疑DON眼中38只(21.35%)眼视盘水肿,56只(31.46%)眼视盘苍白,84只(47.19%)眼视盘正常;18只非DON眼中17只(94.44%)视盘正常。典型DON患者眼底照相见图 3。
|
图 3 双侧DON患者眼底照相 Fig 3 Fundus photography of bilateral DON patients Female, 46 years old, after left orbital decompression. Vod was 0.4 and Vos was 0.3. Exophthalmos of right eye was 22 mm, exophthalmos of left eye was 16 mm, and interorbital distance was 103 mm. A: Right eye with the boundary of the optic disc being unclear and edema; B: Left eye with a pale optic disc. DON: Dysthyroid optic neuropathy; Vod: Visual acuity of oculus dexter; Vos: Visual acuity of oculus sinister |
2.3.4 眼球突出度检查结果
98例DON患者右眼球突出度平均为(20.61±3.39)mm,左眼球突出度平均为(20.71±3.42)mm。眼球突出度≤21 mm的确诊DON眼有38只(31.15%),可疑DON眼有16只(28.57%),非DON眼有9只(50.00%)。
2.3.5 非接触眼压检查结果178只确诊和可疑DON眼的平均眼压为(19.11±4.95)mmHg(1 mmHg=0.133 kPa),非DON眼的平均眼压为(18.89±4.65)mmHg,两者差异无统计学意义(t =-0.183,P=0.855)。
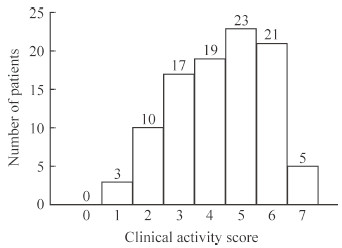
2.3.6 CAS结果98例DON患者的CAS平均为4.44±1.53,CAS≤3的患者有30例(30.61%)。男性患者的CAS平均为4.41±1.65,女性平均为4.49±1.35,男女患者的差异无统计学意义(t =-0.253,P=0.801)。DON患者CAS分布见图 4。
|
图 4 98例DON患者临床活动度评分 Fig 4 Clinical activity scores of 98 patients with DON DON: Dysthyroid optic neuropathy |
2.3.7 影像学检查结果
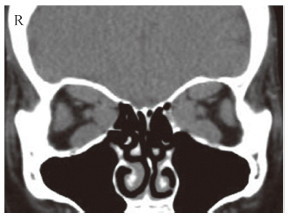
98例患者中96例有肌肉增粗。确诊的80例DON患者中78例双侧肌肉增粗,2例为单眼DON且患眼肌肉增粗。可疑DON患者中18例双侧肌肉增粗。非DON眼无肌肉增粗。80例确诊DON的患者均有眶尖拥挤综合征,其中双侧67例(83.75%)、单侧13例(16.25%)。18例可疑DON患者中16例(88.89%)有眶尖拥挤综合征,其中双侧11例(61.11%)、单侧5例(27.78%),2例(11.11%)无眶尖拥挤综合征者均为女性。眶尖拥挤综合征典型病例CT检查结果见图 5。
|
图 5 冠状位CT检查示眶尖拥挤综合征 Fig 5 Coronal CT showing crowded orbital apex syndrome Female, 55 years old, DON patient. Vod was 0.6 and Vos was 0.01. The bilateral conjunctivae had hyperemia edema and protruded to the palpebral fissure. The upper and lower eyelid receded. Exophthalmos of right and left eyes was both 24 mm, and interorbital distance was 100 mm. Orbital coronal CT showed that the bilateral extraocular muscles were thickened and the orbit was crowded, which caused compression of optic nerve. CT: Computed tomography; DON: Dysthyroid optic neuropathy; Vod: Visual acuity of oculus dexter; Vos: Visual acuity of oculus sinister |
2.3.8 视野检查结果
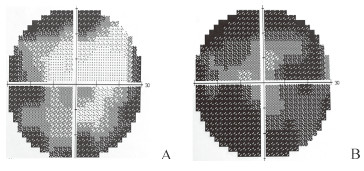
122只确诊DON眼中85只(69.67%)视野缺损;56只可疑DON眼中39只(69.64%)视野缺损;18只非DON眼中仅1只(5.56%)视野缺损,该患者既往发生视网膜分支静脉阻塞。典型DON患者30°静态视野检查图见图 6。
|
图 6 DON患者30°静态视野图 Fig 6 The 30°static visual field of DON patients A: The left eye view of a male DON patient aged 46 years old. Vod was 0.8 and Vos was 0.3. The 30°static visual field showed that varying of absolute dark space was observed in left eye; B: The right eye view of a female DON patient aged 65 years old. Vod was 0.05 and Vos was 0.1. The 30°static visual field showed absolute dark area in the right eye, more serious than that showed in the Fig 6A. DON: Dysthyroid optic neuropathy; Vod: Visual acuity of oculus dexter; Vos: Visual acuity of oculus sinister |
3 讨论
DON是TAO最严重的并发症类型之一。TAO常见于40~60岁女性[14-15],本研究男女比例为1.51:1,男性多于女性,可推测虽然女性好发TAO,但并发DON的患者以男性居多,可见男性TAO患者更容易发生视功能障碍。本研究中男性DON患者的发病年龄高于女性且差异有统计学意义。此外纳入DON患者均有吸烟或接触二手烟史,可以认为除了主动吸烟,被动接触二手烟也可使病情恶化、加重,最终损伤视功能发展为DON。此外,本研究所有患者中既往有甲状腺功能亢进病史的患者占比很大,甲状腺功能减退者仅有2例。因此可以认为中老年、男性、主动吸烟和被动接触以及甲状腺功能亢进均可能是DON的危险因素。
在临床工作中,DON患者常因视力下降就诊,病情可以发展迅速,也可缓慢进展,甚至起病隐匿,眼部表现各异。本研究中142只(79.78%)DON眼的BCVA≤0.6,提示DON患者可出现严重的视力下降。但是在DON患者中仍有8例BCVA为1.0,因此在临床工作中对视力正常的TAO患者仍应仔细鉴别是否合并DON。如果这部分视力正常患者的既往视力可达1.5或1.2,检查时发现BCVA为1.0也意味着视力在原有基础上下降,也是临床诊断的有效评估指标。
本研究98例患者178只DON眼中130只(73.03%)色觉减退,而非DON的18只眼中17只色觉正常,仅1只眼色觉减退,且该眼既往曾患视网膜分支静脉阻塞,提示色觉减退是DON较为显著的临床特征之一。值得注意的是,3例BCVA为1.0的DON患者出现色觉减退,提示色觉减退可能早于视力下降出现。本研究38只(21.35%)眼视盘水肿、56只(31.46%)眼视盘苍白、84只(47.19%)眼视盘正常,在非DON眼中视盘正常的比例很高,提示视盘水肿或苍白为诊断DON的重要依据。可能原因是DON患者的眼外肌增粗,限制了眼球的前移突出,易导致眶尖拥挤、眶压升高,最终使视功能受损。故在DON患者中眼球突出度不能作为单纯的、有效的评判标准。纳入患者中虽然RAPD阳性比例不足一半,但非DON眼均无RAPD阳性,因此对于RAPD阴性的TAO患者不能排除DON,且RAPD阳性者需高度怀疑DON。本研究中CAS≤3的患者约占1/3,提示眼部刺激症状如眼部红肿、胀痛不明显者仍有约30%的可能合并DON,提示CAS亦不是诊断DON明确且具特异性的证据。122只确诊DON眼中85只(69.67%)有视野缺损,而18只非DON眼仅1只眼视野缺损,且该患者既往发表视网膜分支静脉阻塞,DON中视野缺损阳性率高,视野检查可作者其辅助诊断手段之一。
DON患者在影像学上可以分为肌肉增多为主和脂肪增多为主的2个亚型。其中肌肉增多亚型主要表现为眶尖拥挤综合征,脂肪增多亚型主要由于脂肪增多导致眼球高度突出,将视神经拉直造成视神经损伤。大部分视神经病变由眶尖拥挤导致,对于脂肪增多亚型引起的视神经损伤的报道较为少见。本研究80例确诊DON患者中78例有双侧肌肉增粗,2例单侧肌肉增粗,该2例均为单眼即患眼肌肉增粗;18例可疑DON患者均有双侧肌肉增粗;非DON眼均无肌肉增粗。进一步证实肌肉增粗是眶尖拥挤综合征的基础条件。98例DON患者中96例有眶尖拥挤综合征,表明眶尖拥挤综合征可作为DON的特征性指标,也进一步证实眶尖拥挤可能参与了DON发病。
综上,中老年、男性、吸烟或接触二手烟史和甲状腺功能亢进均是DON的危险因素,对于有这些危险因素的TAO患者应加强对视力的监测。视力下降,色觉减退,以及视盘水肿、苍白是DON的特征性临床征象,但对视力暂时无明显变化的患者也应嘱其对色觉进行自我监测,如发现辨色能力减弱、视物发暗等需及时就诊;TAO患者视力下降,即使十分轻微也应及时进行眼底、视野、RAPD及眼眶CT检查,以及时诊治DON。
| [1] | NEIGEL J M, ROOTMAN J, BELKIN R I, NUGENT R A, DRANCE S M, BEATTIE C W, et al. Dysthyroid optic neuropathy. The crowded orbital apex syndrome[J]. Ophthalmology, 1988, 95: 1515–1521. DOI: 10.1016/S0161-6420(88)32978-7 |
| [2] | LAZARUS J H. Epidemiology of Graves' orbitopathy (GO) and relationship with thyroid disease[J]. Best Pract Res Clin Endocrinol Metab, 2012, 26: 273–279. DOI: 10.1016/j.beem.2011.10.005 |
| [3] | STAN M N, BAHN R S. Risk factors for development or deterioration of Graves' ophthalmopathy[J]. Thyroid, 2010, 20: 777–783. DOI: 10.1089/thy.2010.1634 |
| [4] | TROBE J D, GLASER J S, LAFLAMME P. Dysthyroid optic neuropathy. Clinical profile and rationale for management[J]. Arch Ophthalmol, 1978, 96: 1199–1209. DOI: 10.1001/archopht.1978.03910060033007 |
| [5] | BEDEN Ü, KAYA S, YETER V, ERKAN D. Contrast sensitivity of thyroid associated ophthalmopathy patients without obvious optic neuropathy[J/OL]. ScientificWorldJournal, 2013, 2013: 943789. doi: 10.1155/2013/943789. http://cn.bing.com/academic/profile?id=2b5abdfecfeeb911e973ae7b594b9ac0&encoded=0&v=paper_preview&mkt=zh-cn |
| [6] | LIPSKI A, ECKSTEIN A, ESSER J, LOESCH C, MANN K, MOHR C, et al. Course of pattern-reversed visual evoked cortical potentials in 30 eyes after bony orbital decompression in dysthyroid optic neuropathy[J]. Br J Ophthalmol, 2011, 95: 222–226. DOI: 10.1136/bjo.2009.173658 |
| [7] | TSALOUMAS M D, GOOD P A, BURDON M A, MISSON G P. Flash and pattern visual evoked potentials in the diagnosis and monitoring of dysthyroid optic neuropathy[J]. Eye (Lond), 1994, 8(Pt 6): 638–645. |
| [8] | McCANN J D, GOLDBERG R A, ANDERSON R L, BURROUGHS J R, BEN SIMON G J. Medial wall decompression for optic neuropathy but lateral wall decompression with fat removal for non visionthreatening indications[J]. Am J Ophthalmol, 2006, 141: 916–917. DOI: 10.1016/j.ajo.2006.01.066 |
| [9] | DOUGLAS R S, BRIX T H, HWANG C J, HEGEDÜS L, SMITH T J. Divergent frequencies of IGF-I receptorexpressing blood lymphocytes in monozygotic twin pairs discordant for Graves' disease:evidence for a phenotypic signature ascribable to nongenetic factors[J]. J Clin Endocrinol Metab, 2009, 94: 1797–1802. DOI: 10.1210/jc.2008-2810 |
| [10] |
王秋红, 曾程程, 牟旆, 高连娣, 沈亚, 魏锐利. 香烟烟雾提取物及尼古丁诱导甲状腺相关眼病患者眼眶成纤维细胞氧化应激反应并上调NF-κB表达[J]. 第二军医大学学报, 2016, 37: 1239–1244.
WANG Q H, ZENG C C, MOU P, GAO L D, SHEN Y, WEI R L. Cigarette smoke extract and nicotine induce oxidative stress and up-regulate NF-κB expression in orbital fibroblasts of patients with thyroid-associated opthalmopathy[J]. Acad J Sec Mil Med Univ, 2016, 37: 1239–1244. |
| [11] | BARTLEY G B, GORMAN C A. Diagnostic criteria for Graves' ophthalmopathy[J]. Am J Ophthalmol, 1995, 119: 792–795. DOI: 10.1016/S0002-9394(14)72787-4 |
| [12] | WAKELKAMP I M, BALDESCHI L, SAEED P, MOURITS M P, PRUMMEL M F, WIERSINGA W M. Surgical or medical decompression as a first-line treatment of optic neuropathy in Graves' ophthalmopathy? A randomized controlled trial[J]. Clin Endocrinol (Oxf), 2005, 63: 323–328. DOI: 10.1111/cen.2005.63.issue-3 |
| [13] | McKEAG D, LANE C, LAZARUS J H, BALDESCHI L, BOBORIDIS K, DICKINSON A J, et al. Clinical features of dysthyroid optic neuropathy:a European Group on Graves' Orbitopathy (EUGOGO) survey[J]. Br J Ophthalmol, 2007, 91: 455–458. DOI: 10.1136/bjo.2006.094607 |
| [14] | HARRIS M A, REALINI T, HOGG J P, SIVAKCALLCOTT J A. CT dimensions of the lacrimal gland in Graves orbitopathy[J]. Ophthal Plast Reconstr Surg, 2012, 28: 69–72. DOI: 10.1097/IOP.0b013e31823c4a3a |
| [15] | BINGHAM C M, HARRIS M A, REALINI T, NGUYEN J, HOGG J P, SIVAK-CALLCOTT J A. Calculated computed tomography volumes of lacrimal glands and comparison to clinical findings in patients with thyroid eye disease[J]. Ophthal Plast Reconstr Surg, 2014, 30: 116–118. DOI: 10.1097/IOP.0000000000000015 |
 2018, Vol. 39
2018, Vol. 39


