2. 上海中医药大学附属第七人民医院重症医学科, 上海 200137
2. Department of Critical Care Medicine, Seventh People's Hospital of Shanghai University of Traditional Chinese Medicine, Shanghai 200137, China
急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)是一种由严重感染、休克、创伤等多种病因引起的以肺间质和肺毛细血管损伤为主要表现的临床综合征。ARDS患者肺毛细血管内皮和肺泡上皮细胞损伤导致肺间质和肺泡水肿,是以肺容积减少、肺顺应性降低、通气/血流比例严重失调为病理生理特征及以进行性低氧血症、呼吸窘迫为主要临床表现的危重症,其病死率高达40%[1-2]。研究发现,ARDS患者顽固性低氧血症、病死率居高不下的重要原因可能是血管外肺水(extravascular lung water,EVLW)增加和严重通气/血流比例失调[2],因此,降低EVLW、有效减少和防止肺水肿是ARDS治疗的重要方向。
EVLW是指分布于肺血管外的一切液体,由细胞内液、肺泡内液和肺间质液组成,研究表明,EVLW与ARDS的严重程度、患者机械通气时间、ICU时间和病死率密切相关[3-5]。2005年Agricola等[6]分别采用脉波指示剂连续心输出量(pulse indicator continous cadiac output,PiCCO)监测技术和B超评估心脏术后肺水肿的情况,发现超声诊断有良好的敏感度(90%)和特异度(89%)。本研究使用床边肺部超声检查观察ARDS患者的肺通气评分,以了解其与急性生理和慢性健康状况评估Ⅱ(acute physiology and chronic health evaluation Ⅱ,APACHE Ⅱ)评分、EVLW指数(extravascular lung water index,EVLWI)、氧合指数(oxygenation index,PaO2/FiO2)、中心静脉压(central venous pressure,CVP)的相关性。
1 资料和方法 1.1 研究资料回顾性研究2015年6月至2017年2月上海中医药大学附属第七人民医院重症医学科收治的入科7 d内治疗好转的32例ARDS患者的临床资料,所有患者均符合2012年ARDS柏林定义诊断标准[7],入科时和入科7 d后均接受肺部超声检查、PiCCO监测。本研究通过上海中医药大学附属第七人民医院医学伦理委员会审批(批件号2017-IRBQYYS-18)。
1.2 研究方法与观察指标 1.2.1 一般资料收集患者的性别、年龄,入科时和入科7 d后APACHEⅡ评分。
1.2.2 治疗过程中的监测指标留置中心静脉导管监测CVP,留置PiCCO导管监测EVLWI,常规血气分析监测动脉血氧合指数。
1.2.3 肺部超声检查方法与指标超声检查参数:使用迈瑞M7超声仪,探头为凸阵探头,频率为3.5 MHz。由经过统一培训和认证的操作者进行超声检查操作。以患者前正中线、锁骨中线、腋前线、腋后线、肩胛下线、后正中线为体表标志,先将患者单侧划为5个区域,再取每个区域的3等分点(去除肩胛骨遮盖的部分),双侧共计28个点。
肺通气状况的影像学定义和评分标准[8]为(1)正常通气区域(图 1A、1B):出现肺滑动征和A线或孤立的B线(小于3条),标记为N;(2)中度肺组织失气化(图 1C):表现为多条间隔清晰的B线,标记为B1;(3)重度肺组织失气化(图 1D):表现为密集融合的B线,标记为B2;(4)肺实变(图 1E):肺出现类似肝样组织结构和支气管充气征,标记为C;当肺实变合并胸腔积液时(图 1F),标记为C/P。每个区域选择通气最差值。
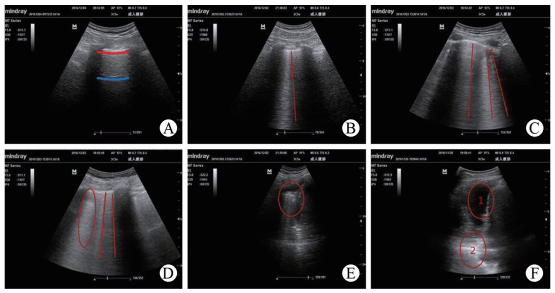
|
图 1 肺通气状况的超声影像 Fig 1 Imaging of pulmonary ventilation A: Normal ventilation area, red line represents the pleura line, and blue line represents the A line; B: Normal ventilation area, red line represents the B line; C: Moderate pulmonary tissue loss of gasification, red line represents the B line; D: Severe pulmonary tissue loss of gasification, red line represents the B line, and red circle represents the fusion B line; E: Pulmonary consolidation, red circle represents pulmonary consolidation; F:"1"represents pleural effusion, and"2"represents pulmonary consolidation |
肺部超声肺通气评分方法:N为0分,B1为1分,B2为2分,C或C/P为3分。将每个部位的评分累积,即为肺部的肺通气总评分。
1.3 统计学处理应用SPSS 19.0软件进行数据处理,由专业人员完成统计学分析。计量资料以x±s表示,采用t检验进行数据比较;Pearson相关分析检验两变量之间的直线相关性。检验水准(α)为0.05。
2 结果 2.1 患者的一般资料共32例ARDS患者纳入本研究,其中肺部感染16例、多发创伤8例、腹腔内感染5例、重症胰腺炎3例。男女比例为17:15,平均年龄为(53.18±13.29)岁,入科时平均APACHEⅡ评分为(18.16±2.76)分。
2.2 患者治疗前后各监测指标的比较经入科后治疗好转的ARDS患者,入科7 d后APACHEⅡ评分、肺通气总评分、EVLWI与入科时比较均下降,氧合指数与入科时比较升高,差异均有统计学意义(P均<0.01);与入科时相比,CVP也有所下降,但两组差异无统计学意义(P>0.05)。见表 1。
|
|
表 1 患者治疗前后观察指标的变化 Tab 1 Changes of indices of ARDS patients before and after treatment |
2.3 相关性分析结果
患者肺通气总评分与APACHE Ⅱ评分、EVLWI、氧合指数、CVP之间相关性分析结果见图 2。肺通气总评分与APACHE Ⅱ评分、EVLWI、CVP均呈正相关(r=0.95、0.95、0.64,P均<0.01),与氧合指数呈负相关(r=-0.94,P<0.01)。
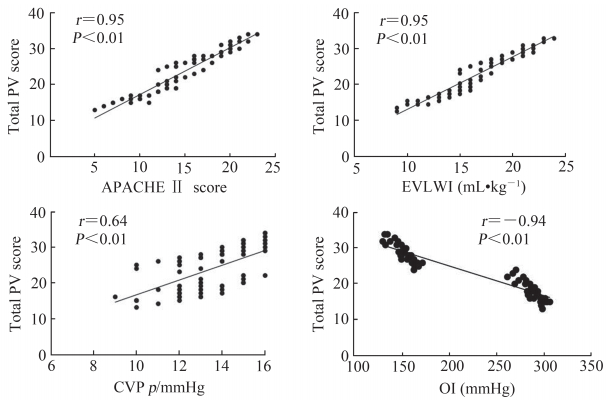
|
图 2 肺通气总评分与APACHE Ⅱ评分、EVLWI、OI、CVP之间相关性分析 Fig 2 Correlations between total PV score and APACHE Ⅱ score, EVLWI, OI and CVP 1 mmHg=0.133 kPa.APACHEⅡ: Acute physiology and chronic health evaluation Ⅱ; PV: Pulmonary ventilation; EVLWI: Extravascular lung water index; CVP: Central venous pressure; OI: Oxygenation index.n=64 |
3 讨论
研究发现,在维持循环稳定的基础上适当限制补充液体是ARDS液体管理的策略;限制性液体复苏策略有助于减少患者接受机械通气治疗的时间,并改善临床预后[9]。ARDS患者的预后与肺水肿的严重程度密切相关,通过对EVLW改变进行动态观察和定量监测可评估肺水肿发生、发展和严重程度[10]。目前监测EVLW的方法包括:(1)无创法,包括单频电阻抗法、双频电阻抗法、生物电阻抗断层成像(electrical impedance tomography,EIT)、正电子发射计算机断层成像(positron emission computed tomography,PET)、心阻抗血流图法(impedance cardiography,ICG);(2)有创法,包括单热指示剂稀释法、温度-染料双试剂稀释法、PiCCO;(3)影像学方法,包括胸部X线片、胸部CT检查、肺部超声。PiCCO技术结合了经肺热稀释法和动脉脉搏轮廓分析2种技术原理,是目前监测EVLW最准确的方法,其计算的肺水指标包括EVLW和肺血管通透性指数(pulmonary vascular permeability index,PVPI)。
2004年,Jambrik等[11]比较了胸部X线片和超声心动图观察B线数目评估EVLW,并得出明显相关性结论。Baldi等[12]于2012年比较B线数目与CT定量法,再次肯定其评估EVLW的实用性。当肺间质和肺泡内液体量增加时,肺组织中气体和水的比例发生明显变化,气液体间的声阻抗差增大,超声在气体和水的界面上即产生强烈的混响,声束在体内来回往返,形成多次反射,表现为肺部超声彗星尾征(ultrasound lung comet,ULC);若一个扫查切面内ULC的数量超过3个,则提示扫查区域存在肺组织水肿,即在肺通气状况超声影响学中表现为B1、B2、C、P。Picano等[13]证实ULC与肺组织内液体含量关系密切,可作为一种简便的检查手段,对患者肺水肿严重程度进行半定量的评价。近年来,还有研究发现,出院前肺水B线的数量与患者再次入院以及不良预后有关,肺部超声作为评估肺水肿的新型无创影像技术,在液体管理中可以起到早期预警和预测临床不良结局的作用[14-15]。
本研究回顾相关数据并经统计学分析得出,在治疗后好转的ARDS患者中,早期APACHEⅡ评分、肺通气总评分和EVLWI处于高水平的状态,氧合指数处于低水平状态,而随着ARDS患者病情好转后,APACHEⅡ评分、肺通气总评分与EVLWI明显好转,而氧合指数明显上升;Pearson相关分析也表明,肺通气总评分与APACHEⅡ评分、EVLWI、氧合指数存在良好的相关性。分析发现,治疗前后患者的CVP差异无统计学意义,提示CVP影响因素较多,EVLW减少只是影响监测CVP的某一部分因素。综上所述,ARDS患者病情危重程度与EVLW的程度呈正相关,通过综合治疗手段,患者病情的好转与EVLW的减少明显相关。目前监测EVLW最准确的手段是PiCCO,但PiCCO需要放置动脉导管和深静脉导管,材料和监护费用高,有引起穿刺并发症以及导管相关血流感染的可能性,加重患者负担。本研究证实,肺部超声通过监测肺通气评分能准确评估EVLW,并且肺部超声具有无创、床旁、即时、低费用的好处,能作为除PiCCO外监测ARDS患者EVLW的有效手段,指导临床治疗,并能实时评估治疗效果,值得推广。
本研究仍存在以下局限性:(1)尽管本研究有2位超声操作者对同一图像进行解读,以减少不同操作者的影响,但仍难以避免对结果的判定产生影响。(2)本研究样本量不大,可能无法准确评价肺通气评分与EVLW及氧合指数的相关性,希望能进一步进行多中心的研究,以期获得更大的样本量,更准确评价肺部超声监测肺通气评分在ARDS患者EVLW评估中的价值。
| [1] | PHUA J, BADIA J R, ADHIKARI N K, FRIEDRICH J O, FOWLER R A, SINGH J M, et al. Has mortality from acute respiratory distress syndrome decreased over time? A systematic review[J]. Am J Respir Crit Care Med, 2009, 179: 220–227. DOI: 10.1164/rccm.200805-722OC |
| [2] | KIM W Y, HONG S B. Sepsis and acute respiratory distress syndrome:recent update[J]. Tuberc Respir Dis (Seoul), 2016, 79: 53–57. DOI: 10.4046/trd.2016.79.2.53 |
| [3] | SAKKA S G, KLEIN M, REINHART K, MEIER-HELLMANN A. Prognostic value of extravascular lung water in critically ill patients[J]. Chest, 2002, 122: 2080–2086. DOI: 10.1378/chest.122.6.2080 |
| [4] | CRAIG T R, DUFFY M J, SHYAMSUNDAR M, McDOWELL C, McLAUGHLIN B, ELBORN J S, et al. Extravascular lung water in dexed to rendicted body weight is a novel predictor of intensive care unit mortality in pataents with acute lung injury[J]. Crit Care Med, 2010, 38: 114–120. DOI: 10.1097/CCM.0b013e3181b43050 |
| [5] | PHILLIPS C R, CHESNUTT M S, SMITH S M. Exteavascular lung water in sepsis-associated acute reapiratory distress syndrome:indexing witu predicted body weight improves correlation with severty of illness and survival[J]. Crit Care Med, 2008, 36: 69–73. DOI: 10.1097/01.CCM.0000295314.01232.BE |
| [6] | AGRICOLA E, BOVE T, OPPIZZI M, MARINO G, ZANGRILLO A, MARGONATO A, et al. "Ultrasound comet-tail images":a marker of pulmonary edema:a comparative study with wedge pressure and extravascular lung water[J]. Chest, 2005, 127: 1690–1695. DOI: 10.1378/chest.127.5.1690 |
| [7] | TheARDS Definition Task Force, RANIERI V M, RUBENFELD G D, THOMPSON B T, FERGUSON N D, CALDWELL E, FAN E, et al. Acute respiratory distress syndrome:the Berlin Definition[J]. JAMA, 2012, 307: 2526–2533. |
| [8] | SOUMMER A, PERBET S, BRISSON H, ARBELOT C, CONSTANTIN JM, LU Q, et al. Ultrasound assessment of lung aeration loss during a successful weaning trial predicts postextubation distress[J]. Crit Care Med, 2012, 40: 2064–2072. DOI: 10.1097/CCM.0b013e31824e68ae |
| [9] | ROCH A, GUERVILLY C, PAPAZIAN L. Fluid management in acute lung injury and ARDS[J/OL]. Ann Intensive Care, 2011, 10: 16. doi: 10.1186/2110-5820-1-16. http://www.academia.edu/14477702/Fluid_Management_in_Acute_Lung_Injury_and_ARDS |
| [10] | MATSUKAWA K, KOBAYASHI T, NAKAMOTO T, MURATA J, KOMINE H, NOSO M. Noninvasive evaluation of cardiac output during postural change and exercise in humans:comparison between the modelflow and pulse dye-densitometry[J]. Jpn J Physiol, 2004, 54: 153–160. DOI: 10.2170/jjphysiol.54.153 |
| [11] | JAMBRIK Z, MONTI S, COPPOLA V, AGRICOLA E, MOTTOLA G, MINIATI M, et al. Usefulness of ultrasound lung comets as a nonradiologic sign of extravascular lung water[J]. Am J Cardiol, 2004, 93: 1265–1270. DOI: 10.1016/j.amjcard.2004.02.012 |
| [12] | BALDI G, GARGANI L, ABRAMO A, D'ERRICO L, CARAMELLA D, PICANO E, et al. Lung water assessment by lung ultrasonography in intensive care:a pilot study[J]. Intensive Care Med, 2013, 39: 74–84. DOI: 10.1007/s00134-012-2694-x |
| [13] | PICANO E, FRASSI F, AGRICOLA E, GLIGOROVA S, GARGANI L, MOTTOLA G. Ultrasound lung comets:a clinically useful sign of extravascular lung water[J]. J Am Soc Echocardiogr, 2006, 19: 356–363. DOI: 10.1016/j.echo.2005.05.019 |
| [14] | ARAS M A, TEERLINK J R. Lung ultrasound:a 'B-line' to the prediction of decompensated heart failure[J]. Eur Heart J, 2016, 37: 1252–1254. DOI: 10.1093/eurheartj/ehw094 |
| [15] | PICANO E, PELLIKKA P A. Ultrasound of extravascular lung water:a new standard for pulmonary congestion[J]. Eur Heart J, 2016, 37: 2097–2104. DOI: 10.1093/eurheartj/ehw164 |
 2018, Vol. 39
2018, Vol. 39


