对于难治性循环衰竭或呼吸衰竭的危重患者,迅速且有效的呼吸循环辅助支持成为首选治疗方法[1]。自1972年Hill等[2]报道采用体外膜肺氧合(extracorporeal membrane oxygenation,ECMO)技术成功抢救1例24岁的呼吸衰竭患者至今,ECMO技术已成功抢救无数危重患者;1980年,美国成立了世界上第1个ECMO中心[3]。作为危重患者的体外生命支持技术之一,ECMO主要用于心脏支持、呼吸支持和心肺复苏(CPR)。根据目前国内外应用现状,大致可分为传统的心脏病开胸术后的心功能替代、非心脏病引起的严重心肺衰竭需呼吸循环支持替代和常规CPR无效的心搏骤停。由于经济条件等限制,我国ECMO起步相对较晚,总体水平仍有待提高,但随着经济的发展和ECMO技术的不断进步,目前也已累计近千例ECMO临床经验。为了总结ECMO救治危重患者的建立时机、建立流程和适应证,分析我院与国际ECMO救治应用的差距,并进一步落实管理团队的建设方案,本研究回顾性分析了我院2014年1月至2016年11月间18例施行ECMO患者的临床资料,现总结如下。
1 资料和方法 1.1 临床资料我院于2014年1月至2016年11月间应用ECMO抢救危重患者18例,男性11例、女性7例,年龄(40.6±10.4)岁。心脏术后低心排血量患者6例,手术包括主动脉根部和主动脉瓣置换术(Bentall手术)+冠状动脉旁路移植术(CABG)1例、A型主动脉夹层行全弓置换术1例、CABG手术1例、感染性心内膜炎行双瓣膜置换术(DVR)1例、巨大左室行主动脉瓣置换术1例、慢性心包炎行心包剥脱术1例;急性重症病毒性心肌炎2例;急性重症肺炎2例;肺泡蛋白沉积症1例;原发性肺动脉高压术后肺高压危象1例;重度烧伤后成人呼吸窘迫综合征(ARDS)3例;外伤后ARDS 1例;肝移植后ARDS 1例;全髋关节置换术后ARDS 1例。其中,ECMO联合应用主动脉球囊反搏(IABP)患者3例,ECMO辅助过程中使用连续性肾脏替代治疗(CRRT)5例。主要因循环衰竭行ECMO辅助8例,因呼吸衰竭辅助10例。依据ECMO主要辅助原因将患者分为循环衰竭组(n=8)和呼吸衰竭组(n=10)。呼吸衰竭患者又根据呼吸衰竭是否由于肺部疾病引起分为肺部原因性ARDS组(n=4)和非肺部原因性ARDS组(n=6)。
1.2 ECMO建立与管理所有患者采用静脉―动脉ECMO(VA-ECMO)模式12例,采用静脉―静脉ECMO(VV-ECMO)模式4例,采用静脉―动脉―动脉ECMO(VAA-ECMO)模式2例。VA-ECMO模式为采用股静脉作为引流管,股动脉或腋动脉作为动脉供血管;VV-ECMO模式为采用股静脉作为引流管,右颈静脉作为供血管;VAA-ECMO模式为采用股静脉作为引流管,股动脉及腋动脉作为供血管。ECMO建立后,常规监测ECMO流量、转速、氧合器血浆渗漏情况,并持续监测患者血流动力学、激活全血凝固时间(activated clotting time of whole blood,ACT)等血气分析结果,以及血常规及凝血常规指标。ECMO流量维持在2~4 L/min,根据病情变化适时调整,吸入氧浓度(fraction of inspiration O2,FiO2)保持在0.6~0.8,根据患者血气结果进行调节,体温维持在36.5~37.0 ℃,肝素使用负荷剂量加术中微量注射泵持续泵注,维持ACT为180~220 s。ECMO的撤离取决于患者心肺功能的恢复情况,撤机前对患者进行全面评估。VV-ECMO逐渐降低气流量和氧浓度,甚至停止供气后患者相关指标无明显变化;VA-ECMO患者仅依靠低剂量正性肌力药物即可维持循环稳定,超声显示心脏收缩、舒张正常,逐渐减低流量至低于500 mL/min,观察30 min,停机拔管,机内液回输。
1.3 统计学处理应用SPSS 24.0软件进行数据处理。符合正态分布的计量资料以x±s表示,不符合正态分布的计量资料以中位数表示;计数资料以率或百分比表示。循环衰竭组、肺部原因性ARDS组与非肺部原因性ARDS组患者ECMO后的存活率采用Mantel-Haenszel检验。检验水准(α)为0.05。
2 结果 2.1 患者一般情况18例患者的ECMO支持时间为5~459 h,中位时间为150 h,成功脱机7例(38.9%,7/18),生存5例(27.8%,5/18)。主要用于循环支持的患者中,心脏手术患者成功脱机3例(50.0%,3/6),生存1例(16.7%,1/6),脱机后死亡原因为感染引起的多脏器功能衰竭;急性重症病毒性心肌炎2例(100%)均存活;ECMO救治循环衰竭患者的脱机率为62.5%(5/8),成功率为37.5%(3/8)。呼吸衰竭组中,急性重症肺炎患者存活1例(50%,1/2)。重度烧伤后、创伤后及手术后ARDS的6例患者无一例成活,死亡原因主要为烧伤后容量维持困难及ECMO辅助期间出血、感染、高血糖等严重并发症;ECMO救治呼吸衰竭患者脱机率和成功率均为20%(2/10)。见表 1。
|
|
表 1 18例危重症患者的ECMO支持效果 |
2.2 存活率分析
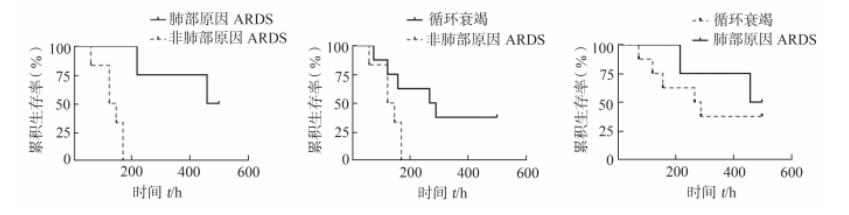
对各组患者的存活率行进一步分析发现,由肺部疾病导致ARDS患者的存活率高于非肺部原因继发的ARDS患者(HR=12.3,95%CI:2.2~69.9;P<0.01),循环衰竭患者的存活率也高于非肺部原因继发的ARDS患者(HR=4.6,95%CI:1.1~19.5;P<0.05),而循环衰竭患者与肺部疾病导致ARDS患者的存活率差异无统计学意义(HR=0.6,95%CI:0.1~2.7;P>0.05)。见图 1。ECMO辅助是重症ARDS整体治疗的一部分,非肺部疾病导致ARDS患者预后差的根源在于原发病及并发症较难治疗。
|
图 1 循环衰竭、肺部原因ARDS与非肺部原因ARDS患者ECMO辅助的存活率比较 ECMO:体外膜肺氧合; ARDS:成人呼吸窘迫综合征 |
3 讨论 3.1 ECMO等体外生命支持(extracorporeal life support,ECLS)的应用现状及适应证
ECLS系统包括ECMO、体外肺支持、体外CO2 排除、体外心肺支持(CPS)等[1, 4]。ECMO的基本原理是将静脉血引流至体外,经过膜式氧合器氧合后,在血泵的驱动下再输回体内,可纠正呼吸衰竭患者的低氧血症,减少肺血流和减轻肺间质水肿,有利于肺功能的恢复;还可减轻循环衰竭患者的心室前负荷,维持良好的动脉压及组织供氧,有利于心脏功能的恢复。因此,ECMO既可用于救治呼吸衰竭,也可救治循环衰竭,或者两者兼有的患者[5]。随着ECMO技术的进步,其应用领域已不仅局限于心脏外科,《2015中国心脏外科和体外循环数据白皮书》报道ECLS的支持例数为5 569例,其中ECMO为974例[4]。ECMO的技术和设备从陌生走向成熟,为患者提供了更多的抢救时间,成功挽救了危重患者的生命[6]。ECMO的适应证随ECMO技术的不断完善而逐渐扩大,包括心脏术后低心排、心肌梗死后心源性休克、心肌炎、心脏移植过渡桥梁等[7-10],各种原因引起的呼吸功能衰竭且呼吸机难以维持的患者[2, 11-13],小儿或新生儿出现ARDS的患儿,其他非心脏手术后出现的心肺功能衰竭患者[14],急性中毒引起肺功能严重损害的患者,以及重要脏器移植时的生命支持如肺移植等[6]。
3.2 ECMO应用时机的选择在我国,ECMO在成人心脏方面的支持效果还没有完全显现出来,主要影响因素包括ECMO的使用时机、原发病的处理是否彻底,以及手术适应证的准确掌握等。本研究的6例心脏术后患者中有3例脱机,但只有1例成功存活,分析失败原因除患者术前病情危重外,ECMO的应用时机延迟等也导致其辅助效果较国际水平有明显的差距。ECMO在救治病毒性心肌炎患者中表现出良好的辅助效果,2例急性重症病毒性心肌炎患者均存活,表明患者一旦确定为急性重症病毒性心肌炎,在各种内科治疗均无法维持生命体征的情况下,应尽早使用ECMO,以提供足够多的时间来处理原发病,纠正心脏功能。烧伤的ECMO治疗在小面积重度烧伤患者中已有成功报道[11]。本院救治的3例烧伤患者在使用ECMO后生命体征得以维持,有1例在心肺复苏3 h后由于使用了ECMO,很快恢复了心跳,证明ECMO能给危重烧伤患者提供有效的呼吸和循环支持。Askegard-Giesmann等[11]报道18岁以下烧伤儿童ECMO救治成功率为53%,但未见成人烧伤后呼吸循环衰竭患者ECMO支持成功的报道。本组3例重度烧伤患者的最长支持时间为168 h,可见对于重度烧伤成人患者ECMO的容量维持是最大的难题,加上烧伤患者的病情复杂,缺乏有效的针对基础疾病的治疗措施,3例患者均未成功,提示对于重度烧伤成人患者需慎重选择ECMO。生存分析结果表明,ECMO用于呼吸支持和循环支持的疗效近似,其对心肺原发疾病导致的呼吸衰竭和循环衰竭的治疗效果优于继发于其他疾病的呼吸衰竭。重症ARDS患者使用ECMO辅助的时间长、费用高及并发症多,应用前需评估肺功能的可逆性,及时选择ECMO的救治时机、完善建立流程、积极治疗原发病、防止相关并发症的发生是ECMO救治成功的关键。
3.3 多学科多部门合作ECMO救治梯队建设ECMO技术是一项复杂、高风险的生命支持技术,运行中需要投入大量的人力、物力,其成功应用代表医院的整体急救水平,建立优秀的ECMO团队是优秀医院迫切而重要的标志之一[15-16]。我国ECMO的低成功率与ECMO救治期间严重并发症的发生及处理不当关系密切,由于我国ECMO设备不配套、相对陈旧,开展初期经受了氧合器渗漏、严重出血、溶血等许多教训,随着ECMO应用数量的增加和管理经验的积累,我国ECMO救治的成功率也在逐步提高[17]。而在ECMO实施过程中需要施行主任负责制,由心外科主任或负责医疗的医院领导兼任主要负责协调全院的医疗资源,充分调动全院的技术力量;由经验丰富的体外循环医师负责设备管理,平时装备责任到个人,随时可以参加抢救;其他人员包括ICU医师、急救科医师、呼吸治疗师以及负责患者基础疾病的专业人员等[16]。本科室在患者的ECMO运行过程中发现,ECMO团队的建立和管理要责任到人,分工明确,设备要始终处于备战状态,ECMO工作团队需常态化,建立应急通道,形成全院的多学科ECMO救治梯队,努力提高危重患者的急救水平。
循环衰竭和肺部疾病引起的ARDS使用ECMO救治预后优于非肺部原因继发的ARDS,因此循环衰竭和肺部疾病引起的ARDS是使用ECMO救治的潜在指征。选择恰当的ECMO救治时机、积极治疗原发病,及防止相关并发症的发生是ECMO救治成功的关键。
| [1] | 刘东, 王盛宇, 孙凌波, 陈雷, 薛金熔, 赵铁夫, 等. ECMO的临床应用[J]. 北京生物医学工程, 2008, 27: 305–308, 327. DOI: 10.3969/j.issn.1002-3208.2008.03.022 |
| [2] | HILL J D, O'BRIEN T G, MURRAY J J, DONTIGNY L, BRAMSON M L, OSBORN J J, et al. Prolonged extracorporeal oxygenation for acute post-traumatic respiratory failure (shock-lung syndrome). Use of the Bramson membrane lung[J]. N Engl J Med, 1972, 12: 629–634. |
| [3] | ZWISCHENBERGER J B, NGUYEN T T, UPP J R Jr, BUSH P E, COX C S Jr, DELOSH T, et al. Complications of neonatal extracorporeal membrane oxygenation. Collective experience from the Extracorporeal Life Support Organization[J]. J Thorac Cardiovasc Surg, 1994, 107: 838–949. |
| [4] | 赵举, 黑飞龙. 2015中国心脏外科和体外循环数据白皮书[J]. 中国体外循环杂志, 2016, 14: 130–132. |
| [5] | MAGOVERN G J Jr, MAGOVERN J A, BENCKART D H, LAZZARA R R, SAKERT T, MAHER T D Jr, et al. Extracorporeal membrane oxygenation:preliminary results in patients with postcardiotomy cardiogenic shock[J]. Ann Thorac Surg, 1994, 57: 1462–1471. DOI: 10.1016/0003-4975(94)90101-5 |
| [6] | DZIERBA A L, ABRAMS D, BRODIE D. Medicating patients during extracorporeal membrane oxygenation:the evidence is building[J]. Crit Care, 2017, 21: 66. DOI: 10.1186/s13054-017-1644-y |
| [7] | FRASER C D Jr, JAQUISS R D, ROSENTHAL D N, HUMPL T, CANTER C E, BLACKSTONE E H, et al. Prospective trial of a pediatric ventricular assist device[J]. N Engl J Med, 2012, 367: 532–541. DOI: 10.1056/NEJMoa1014164 |
| [8] | SCHMIDT M, ZOGHEIB E, ROZE H, REPESSE X, LEBRETON G, LUYT C E, et al. The PRESERVE mortality risk score and analysis of long-term outcomes after extracorporeal membrane oxygenation for severe acute respiratory distress syndrome[J]. Intensive Care Med, 2013, 39: 1704–1713. DOI: 10.1007/s00134-013-3037-2 |
| [9] | CONRAD S A, RYCUS P T. Extracorporeal membrane oxygenation for refractory cardiac arrest[J]. Ann Card Anaesth, 2017, 20(Supplement): S4–S10. |
| [10] | YAM N, McMULLAN D M. Extracorporeal cardio-pulmonary resuscitation[J]. Ann Transl Med, 2017, 5: 72. DOI: 10.21037/atm |
| [11] | ASKEGARD-GIESMANN J R, BESNER G E, FABIA R, CANIANO D A, PRESTON T, KENNEY B D. Extracorporeal membrane oxygenation as a lifesaving modality in the treatment of pediatric patients with burns and respiratory failure[J]. J Pediatr Surg, 2010, 45: 1330–1335. DOI: 10.1016/j.jpedsurg.2010.02.106 |
| [12] | KLUGE S, SENSEN B, BRAUNE S. [Extracorporeal lung support in patients with ARDS][J]. Dtsch Med Wochenschr, 2017, 142: 88–95. DOI: 10.1055/s-0042-105942 |
| [13] | ZHANG Z, GU W J, CHEN K, NI H. Mechanical ventilation during extracorporeal membrane oxygenation in patients with acute severe respiratory failure[J/OL]. Can Respir J, 2017, 2017:1783857. doi:10.1155/2017/1783857. |
| [14] | 黄伟明, 荣健, 朱艳玲, 黄文起. 体外膜肺氧合在心肺辅助循环中的应用[J]. 中国体外循环杂志, 2005, 40: 233–235. DOI: 10.3969/j.issn.1672-1403.2005.04.013 |
| [15] | 黄琳娜, 詹庆元. ECMO治疗成人重症ARDS与传统机械通气的比较及研究新进展[J]. 医学综述, 2015, 21: 1644–1647. DOI: 10.3969/j.issn.1006-2084.2015.09.040 |
| [16] | 李欣, 徐凌峰, 郭震, 王华. 体外膜肺氧合临床应用与团队建设——附17例临床报告[J]. 中国体外循环杂志, 2005, 3: 239–242. DOI: 10.3969/j.issn.1672-1403.2005.04.015 |
| [17] | 何发明, 梁志强, 李晓召, 张巧玲, 曹向波, 朝亮, 等. 心脏外科术后ECMO的应用和管理[J]. 医药论坛杂志, 2016(6): 10–11. |
 2018, Vol. 39
2018, Vol. 39


