炭疽杆菌表面糖抗原(图 1)是炭疽杆菌细胞荚膜的主要成分[1],炭疽杆菌表面糖抗原的人工合成对炭疽疫苗的研发具有重大意义[2]。1-叔丁基二苯基硅烷基-2-叠氮-3-O-(α-四-O-苄基-1-氧代-β-D-吡喃半乳糖基)-4, 6-O-对甲氧基苄基-β-D-吡喃葡萄糖苷(1)是化学合成炭疽杆菌表面糖抗原的重要中间体。同类β-硫苷糖基化得到的1,3位连接的二糖产物为α、β构型混合物,α构型产率基本维持在17%~54%[3-5],由于本研究中单糖受体上的保护基位阻较大,导致路线(图 2)中的二糖化合物(1)的预实验产率仅为21.1%,大大阻碍了后续合成工作的进展。文献报道用硫苷作供体的苷化反应,其立体化学结果受多重因素影响,即温度、溶剂、受体及反离子等的改变都可能会大大改变α与β的构型比[6]。本研究拟采用正交试验设计探寻其最佳反应条件,从而提高产率。

|
图 1 炭疽杆菌表面糖抗原的化学结构式 |
|
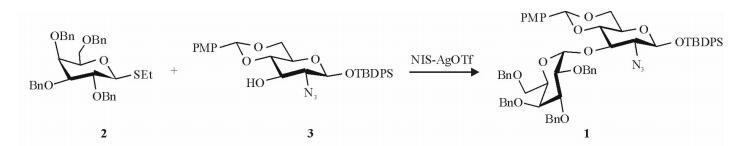
图 2 目标化合物1的合成路线 1: 1-叔丁基二苯基硅烷基-2-叠氮-4, 6-O-对甲氧基苄基-β-D-吡喃葡萄糖苷; 2:四-O-苄基-1-硫代-β-D-吡喃半乳糖乙苷; 3: 1-叔丁基二苯基硅烷基-2-叠氮-3-O-(α-四-O-苄基-1-氧代-β-D-吡喃半乳糖基)-4, 6-O-对甲氧基苄基-β-D-吡喃葡萄糖苷. NIS-AgOTf: N-碘代丁二酰亚胺/三氟甲磺酸银 |
1 材料
四-O-苄基-1-硫代-β-D-吡喃半乳糖乙苷(2) 按文献[7]方法制备。1HNMR (300 MHz,CDCl3)化学位移:7.50~7.24 (m,20H,Ar),4.99~4.56(m,6H),4.51~4.36 (m,3H),3.96 (d,J=2.6 Hz,1H),3.82 (t,J=9.4 Hz,1H),3.63~3.51 (m,4H),2.84~2.62 (m,2H),1.30 (t,J=7.4 Hz,3H,CH3)。1-叔丁基二苯基硅烷基-2-叠氮-4,6-O-对甲氧基苄基-β-D-吡喃葡萄糖苷(3)按文献[8]方法制备。1HNMR(300 MHz,CDCl3)化学位移:7.69 (d,J=7.2 Hz,4H,Ar),7.49~7.29 (m,8H,Ar),6.85 (d,J=8.7 Hz,2H,Ar),5.41 (s,1H),4.50 (d,J=7.5 Hz,1H),3.94 (dd,J=10.5、5.0 Hz,1H),3.77 (s,3H,CH3),3.63~3.37 (m,4H),2.99 (m,1H),2.57 (s,1H),1.11(s,9H,CH3)。其余化学试剂均为市售分析纯或化学纯。
2 方法和结果 2.1 正交试验设计硫苷法糖基化反应通常需要在低温下进行,且常用溶剂为二氯甲烷、四氢呋喃、乙醚等[9-10]。而单糖化合物2、3在二氯甲烷和四氢呋喃中溶解度较好,故溶剂选用二氯甲烷和四氢呋喃。本研究选用了硫苷糖基化反应中最经典的催化剂N-碘代丁二酰亚胺/三氟甲磺酸银(NIS-AgOTf)[11]。根据L9(43)正交表设计实验,以目标化合物的产率为考核指标,重点考察4个主要因素[温度(A),反应时间(B),溶剂(C),单糖供体2和单糖受体3的物质的量投料比(D)],各因素设计3个水平(表 1)。
|
|
表 1 正交试验设计因素水平表 |
2.2 二糖化合物1的制备
在一定温度(A)下,取x mmol单糖供体2、y mmol单糖受体3、分子筛和溶剂(C)置于50 mL茄形瓶中,氮气保护下搅拌30 min后加入催化量的NIS-AgOTf,反应一定时间(B)。反应结束后,加适量三乙胺中和过量的酸(pH约为7),过滤除去分子筛,滤液加入200 mL二氯甲烷后先用饱和硫代硫酸钠溶液萃取,再用饱和碳酸氢钠溶液和饱和氯化钠溶液各萃取2次。除去水层后,使用无水硫酸钠干燥有机层。蒸干有机溶剂,快速硅胶柱层析(洗脱剂石油醚:乙酸乙酯=10:1) 得白色固体产物,真空干燥后称质量,计算产率。每组实验重复3次(表 1)。1HNMR(600 MHz,CDCl3)化学位移:7.81~7.76(m,4H,Ar),7.51~7.27(m,26H,Ar),7.16(d,J=7.1 Hz,2H,Ar),6.90~6.85(m,2H,Ar),5.66(d,J=2.4 Hz,1H,Gal-H-1),5.39(s,1H),5.02~4.93(m,2H),4.83(d,J=11.6 Hz,1H),4.66~4.51(m,6H),4.41(t,J=6.6 Hz,1H),4.13(d,J=9.3 Hz,1H),4.09(s,2H),3.96(dd,J=10.5、5.0 Hz,1H),3.90~3.85(m,1H),3.82(s,3H,CH3),3.71~3.58(m,4H),3.06(m,1H),1.22(s,9H,CH3)。HR-QTOF-MS:C64H69N3O11Si[M+Na]+m/z,理论值1 106.459 4,实测值1 106.462 4。
2.3 正交试验结果按表 2编号所示实验顺序,依次采用相应条件, 每组实验重复3次,以产率的平均值为最终结果。各组的极差分析数据及其计算结果见表 2。由于本实验设计了4个影响因素,使得L9(43)正交表中无空白列作单因素方差分析对照,所以采用重复实验方差分析方法[12]求得各因子列的比值,所得方差分析结果如表 3所示。
|
|
表 2 L9(43)正交实验结果和极差分析 |
|
|
表 3 方差分析结果 |
3 讨论 3.1 目标化合物的构型鉴定
D-吡喃型糖上的苷键为α构型时,C1位质子为竖键,耦合常数为2~4 Hz[13]。化合物1的1HNMR数据显示半乳糖基上C2位氢的化学位移为[5.66 (d, J=2.4 Hz, 1H)],表明所制得的化合物为α构型产物。
3.2 α-二糖中间体1合成条件的优化 3.2.1 反应温度的影响方差分析结果表明,反应温度(A)对产物的产率有显著影响(P<0.01)。极差分析结果(k3>k2>k1)表明,反应温度从0 ℃降到-40 ℃,产率显著提高。因此反应温度为-40 ℃(A3) 为最佳。
3.2.2 反应时间的影响极差和方差分析结果显示,反应时间(B)对产物产率的影响相对较小。从反应过程看,从开始反应到1 h之后薄层层析检测发现物点不再有明显变化,杂点有增多。所以反应时间以1 h (B1) 为宜。
3.2.3 反应溶剂的影响方差分析结果表明,反应溶剂(C)对产率有较大的影响。极差分析结果(k2>k3≈k1)显示,使用二氯甲烷和四氢呋喃的混合液为溶剂时产率显著提高,即C2条件为最佳。
3.2.4 供体与受体物质的量投料比的影响方差分析结果表明,单糖供体2与单糖受体3的物质的量投料比(D)对产物产率的影响非常显著(P<0.01)。极差分析结果(k2>k3>k1)表明,随着硫苷供体浓度的增加,产率先增加后减少,且物质的量投料比为1.5:1时,产率提高达到最大值,即D2条件最佳。
3.2.5 二糖化合物1合成的最优反应条件方差分析结果表明,因素A、B、C、D对实验结果均有显著影响。而极差分析结果进一步显示,因素D对实验结果的影响最大,其次是因素A,最后是因素B。综上分析,制备该二糖化合物1的最佳反应条件为D2A3C2B1。
3.3 二糖化合物1最优合成反应条件的验证以4.38 g (7.5 mmol)单糖供体2和2.80 g (5 mmoL)单糖受体3为起始原料按D2A3C2B1条件重复实验3次,平均产率为83.60%,且产率稳定。
综上,本工艺以正交试验设计对1-叔丁基二苯基硅烷基-2-叠氮-3-O-(α-四-O-苄基-1-氧代-β-D-吡喃半乳糖基)-4, 6-O-对甲氧基苄基-β-D-吡喃葡萄糖苷(1)的合成反应条件进行了优化,获得其最佳反应条件为D2A3C2B1(化合物2和3的投料比为1.5:1,反应温度-40 ℃,二氯甲烷和四氢呋喃的混合液为溶剂,反应时间1 h),显著提高了炭疽杆菌表面糖抗原合成工艺的效率。本研究对硫苷糖基化的构型选择性条件控制的探究为糖基化立体构型的控制研究提供了科学依据。
| [1] | CHOUDHURY B, LEOFF C, SAILE E, WILKINS P, QUINN C P, KANNENBERG E L, et al. The structure of the major cell wall polysaccharide of Bacillus anthracis is species-specific[J]. J Biol Chem, 2006, 281: 27932–27941. DOI: 10.1074/jbc.M605768200 |
| [2] | ROY R. New trends in carbohydrate-based vaccines[J]. Drug Discov Today:Technologies, 2004, 1: 327–336. DOI: 10.1016/j.ddtec.2004.10.005 |
| [3] | GEMMA E, LAHMANN M, OSCARSON S. Synthesis of monodeoxy analogues of the trisaccharide alpha-D-Glcp-(1→3)-alpha-D-Manp-(1→2)-alpha-D-ManpOMe recognised by calreticulin/calnexin[J]. Carbohydr Res, 2006, 341: 1533–1542. DOI: 10.1016/j.carres.2006.03.015 |
| [4] | TATAI J, FVGEDI P. A new, powerful glycosylation method:activation of thioglycosides with dimethyl disulfide-triflic anhydride[J]. Org Lett, 2007, 9: 4647–4650. DOI: 10.1021/ol702139u |
| [5] | SON S, TANO C, FURUKAWA J, FURUIKE T, SAKAIRI N. Stereoselective tris-glycosylation to introduce beta-(1→3)-branches into gentiotetraose for the concise synthesis of phytoalexin-elicitor heptaglucoside[J]. Org Biomol Chem, 2008, 6: 1441–1449. DOI: 10.1039/b800809d |
| [6] | 蔡孟深. 苷键的生成[M]//蔡孟深, 李忠军. 糖化学——基础、反应、合成、分离及结构. 北京: 化学工业出版社, 2006: 112-117. |
| [7] | SEO S, WEI A. Probing osmotic effects on invertase with L-(-)-sucrose[J]. Org Biomol Chem, 2008, 6: 3362–3365. DOI: 10.1039/b810158b |
| [8] | 蔡孟深. 保护基[M]//蔡孟深, 李忠军. 糖化学——基础、反应、合成、分离及结构. 北京: 化学工业出版社, 2006: 34-64. |
| [9] | LIAN G, ZHANG X, YU B. Thioglycosides in carbohydrate research[J]. Carbohyd Res, 2015, 403: 13–22. DOI: 10.1016/j.carres.2014.06.009 |
| [10] | YU S, WANG Q, ZHANG L, WU Q, GUO Z. Synthesis and evaluation of protein conjugates of GM3 derivatives carrying modified sialic acids as highly immunogenic cancer vaccine candidates[J]. Medchemcomm, 2011, 2: 524–530. DOI: 10.1039/c1md00033k |
| [11] | KONRADSSON P, MOOTOO D R, McDEVITT R E, FRASER REID B. Lodonium ion generated in situ from N-iodosuccinimide and trifluoromethanesulfonic acid promotes direct linkage of 'disarmed' pent-4-enyl glycosides[J]. J Chem Soc Chem Commun, 1990: 271. |
| [12] | 王政, 魏莉. 利用SPSS软件实现药学实验中正交设计的方差分析[J]. 数理医药学杂志, 2014, 27: 99–102. |
| [13] | 章由林, 文翰. 糖的结构鉴定[M]//蔡孟深, 李忠军. 糖化学——基础、反应、合成、分离及结构. 北京: 化学工业出版社, 2006: 370-411. |
 2017, Vol. 38
2017, Vol. 38


