老年股骨转子间骨折是骨质疏松性髋部骨折的常见类型,治疗方式包括非手术治疗和手术治疗。非手术治疗包括卧床牵引、支具固定及营养支持等,手术治疗包括髓内固定、髓外固定、外固定支架固定、人工髋关节置换等。老年骨质疏松性骨折患者卧床容易出现深静脉血栓、压疮、肺部感染及泌尿系统感染等严重并发症,而且骨折后易发生畸形愈合或骨折不愈合。在综合考虑患者的手术风险、麻醉风险及评估预后功能的情况下,对可以耐受手术的老年髋部骨折患者尽早完成骨折的复位固定已经取得临床医生的广泛共识[1]。
防旋转股骨近端髓内钉 (proximal femoral nail antirotation,PFNA) 因具有手术切口小、组织损伤小、生物力学稳定、有利于早期负重等优点,是近年来广泛用于治疗股骨转子间骨折的代表性髓内固定系统。骨质疏松症仍然是导致老年性股骨转子间骨折PFNA术后内固定失败、螺旋刀片旋出、再发骨折的重要原因[2],但许多临床医生并不重视骨质疏松症的治疗[3]。目前临床上广泛应用的抗骨质疏松治疗药物包括基础治疗药物 (钙剂及活性维生素D)、抗骨吸收药物 (降钙素、双膦酸盐类、雌激素等) 及促骨形成药物 (甲状旁腺激素等),本研究回顾性分析了应用PFNA联合抗骨质疏松药物治疗老年骨质疏松性股骨转子间骨折围手术期应用的临床疗效,为探讨围手术期及术后抗骨质疏松药物的规范性应用提供依据。
1 资料和方法 1.1 一般资料本研究为回顾性研究,从2012年6月—2014年6月我们收治的病例中选取符合纳入标准和排除标准的病例。纳入标准:(1) 依据《骨质疏松性骨折诊疗指南》[4],经双能X线骨密度仪测量腰椎或髋部骨密度T值≤-2.5个标准差的患者,或由低能量或非暴力性外伤引起且被临床诊断为骨质疏松症的患者;(2) 年龄≥60岁的单侧新鲜闭合性股骨转子间骨折,对侧髋关节无既往骨折或其他特殊情况;(3) 患者及家属知情同意,能耐受麻醉,行PFNA固定术治疗;(4)6个月内均未服用抗骨质疏松药物;(5) 围手术期及术后能遵医嘱进行抗骨质疏松治疗;(6) 有完整随访资料。排除标准:(1) 继发性骨质疏松症;(2) 合并其他进展性疾病 (如恶性肿瘤、精神疾病等);(3) 需要长期使用影响骨代谢的药物,如糖皮质激素、肝素、利尿药物等;(4) 有抗骨质疏松药物使用禁忌证,包括抗骨松药物过敏、实验室检查提示低钙血症、严重肝肾功能不全、本次手术前6个月口腔拔牙病史等。
参照以上标准,选取2012年6月至2014年6月共78例在本治疗组采用PFNA手术治疗且随访资料完整的老年股骨转子间骨折患者纳入本研究。根据患者围手术期及随访期间是否应用抗骨质疏松药物治疗,分为抗骨质疏松药物治疗组和对照组。其中治疗组40例,对照组38例,两组患者年龄、性别、身高、体质量、体质量指数及骨折分型等资料差异均无统计学意义,具有可比性 (表 1)。
|
|
表 1 两组患者的基本资料 |
1.2 治疗方法
患者全麻后,仰卧于骨折牵引床上,患肢外旋并纵向牵引后内旋,使用C形臂X线机透视观察骨折的复位情况。于股骨大转子顶点处作纵向切口并沿股骨长轴向近端延伸约5 cm,逐层切开皮肤及阔筋膜,分离显露大转子顶点,选取顶点内侧为进钉点。用开孔器开孔后,置入导针并透视确认导针位置,用空心钻沿导针方向对股骨近端成形后,沿导针插入PFNA主钉,选取合适大小的主钉型号,透视下调整主钉的深度,在瞄准器的导向下将导针打入股骨颈,透视下观察并调整导针的位置,使导针平行于股骨颈中轴偏后下方。测量螺旋刀片的长度,在股骨外侧皮质开口,打入螺旋刀片。在瞄准器导向下锁定远端螺钉,近端拧入尾帽,用C形臂X线机透视患髋正、侧位,确认PFNA及骨折位置良好后,根据术中情况决定是否放置引流,最后缝合切口。
1.3 术后处理术后24 h,待引流量小于10 mL时拔除引流管;术后应用抗生素预防感染,2周拆线。术后6 h鼓励患者卧床在不负重状态下进行股四头肌等长收缩训练和关节活动;对无禁忌证的患者,联合患肢抬高、使用间歇加压充气装置等措施,术后24 h开始口服利伐沙班10 mg,每日1次,持续10~14 d,预防下肢深静脉血栓形成;2周后根据影像学及患者具体情况开始部分负重锻炼,影像学复查骨折愈合后完全负重。
1.4 围手术期及术后抗骨质疏松药物治疗方案对于入组抗骨质疏松药物治疗组的所有患者,根据入院后相关检查,若无禁忌证即开始口服钙剂 (钙尔奇D)600 mg,维生素D (骨化三醇)0.25 μg,钙片及维生素D每日2次,每次各1片,连续服用至术后12周;然后改为每日1次,每次各1片,至术后1年。除外禁忌证后即予皮下注射鲑鱼降钙素 (北京诺华制药有限公司)50 IU,每日1次,连用3周;术后2周,静脉滴注5 mg唑来膦酸 (北京诺华制药有限公司)。对照组不给予抗骨质疏松药物治疗。
1.5 观察指标及疗效评价术后1、3、6、12个月复查X线片,观察骨折愈合情况。采用美国GE公司生产的双能X线骨密度测量仪,分别于术前以及术后6、12、18个月测量健侧髋部骨密度。
采用Harris评分评价髋关节功能[5]。该评分从疼痛、功能、畸形和关节活动度4个方面进行评价,满分为100分,得分90~100分为优,80~89分为良,70~79分为可,≤69分为差。
记录患者手术相关并发症及其他部位再骨折的情况;观察使用降钙素和唑来膦酸的药物不良反应,如恶心、呕吐、面部潮红、发热、流感症状等。
1.6 统计学处理采用SPSS 19.0软件进行统计学分析。计量资料以x±s表示,两组间差异的比较采用独立样本t检验;计数资料以例数和构成比表示,两组间差异的比较采用χ2检验。检验水准 (α) 为0.05。
2 结果 2.1 围手术期及随访情况所有患者均顺利完成手术,术后2周按时拆线,未发生伤口感染、内固定失败,未观察到骨折术后髋内翻、股骨短缩畸形等并发症。所有患者获得18~24个月随访,经X线片证实均能达到临床骨性愈合,均未出现骨折延迟愈合或不愈合情况,治疗组和对照组骨折愈合时间比较差异无统计学意义 (P > 0.05,表 2)。术后18个月随访时,根据Harris髋关节功能评分,治疗组与对照组髋关节功能差异无统计学意义 (P > 0.05),但治疗组再骨折风险下降 (P < 0.05,表 2)。治疗组共4例新发骨折 (新发椎体骨折3例,桡骨远端骨折1例),而对照组9例发生再发骨折 (新发椎体骨折5例,桡骨远端骨折3例,对侧髋关节骨折1例)。
|
|
表 2 两组患者术后18个月Harris评分、再骨折发生率及影像学骨折愈合时间比较 |
2.2 两组健侧髋关节骨密度的比较
两组术前健侧髋关节骨密度测量值差异无统计学意义 (P > 0.05);术后6、12、18个月随访时,治疗组骨密度测量值高于对照组 (P < 0.05,表 3)。
|
|
表 3 两组患者术前及术后6、12、18个月健侧髋关节骨密度 (T值) 比较 |
2.3 使用骨质疏松药物的不良反应
使用唑来膦酸5 mg静脉滴注后,出现发热6例,流感样症状3例,经对症处理后均恢复正常,未发现其他无法耐受的不良反应。2例患者应用降钙素后出现面部潮红,但未影响继续用药,未出现其他并发症。
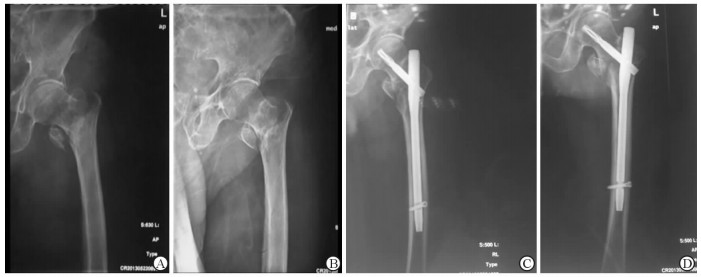
2.4 典型病例89岁男性患者,因“摔伤后左髋关节疼痛伴活动受限6 h”入院,入院后X线片提示Evans Ⅳ型骨折,健侧髋部骨密度 (T值) 为-2.6。血常规、生化结果提示无明显禁忌证,予口服钙剂 (钙尔奇D)600 mg,维生素D (骨化三醇) 0.25 μg,每次各1片,每日2次。同时给予鲑鱼降钙素50 IU皮下注射,每日1次。入院第3天行PFNA固定术,术前、术后X线片见图 1。术后继续予以口服钙剂、维生素D联合降钙素治疗,常规抗感染,口服利伐沙班10 mg每日1次预防深静脉血栓,进行床上主动、被动功能锻炼。术后第14天,静脉滴注5 mg唑来膦酸,输注前后分别静脉予500 mL生理盐水水化,输注前服用塞来昔布200 mg。唑来膦酸使用后继续观察2 d,伤口愈合后拆线出院,出院后继续抗骨质疏松基础治疗 (钙剂联合维生素D)。术后1年复查健侧骨密度 (T值) 为-1.1。
|
图 1 89岁男性Evans Ⅳ型股骨转子间骨折患者PFNA术前、术后X线片 A:术前髋关节正位片;B:术前髋关节侧位片;C:术后2周患侧髋关节正位片;D:术后2周患侧髋关节侧位片. PFNA:防旋转股骨近端髓内钉 |
3 讨论
髋部骨折是最常见、也是危害最大的骨质疏松性骨折。流行病学数据表明,髋部骨折发生后,20%的患者在骨折后第1年死亡,20%的患者失去独立生活的能力,10%~20%的患者需要长期护理[6-9]。尽早恢复髋关节的负重和运动功能、减少骨折并发症、提高患者的生活质量是骨质疏松性髋部骨折的总体治疗目标。围绕这一目标,髋部骨折的预防与治疗一直是学术界关注的焦点。我们主张对能耐受手术的老年股骨转子间骨折患者采用积极手术治疗,以缩短病患卧床时间,积极功能锻炼,减少并发症发生。目前临床上用于股骨转子间骨折的内固定可分为髓内固定与髓外固定系统,前者以PFNA和Gamma钉为代表,后者以股骨近端解剖型锁定钢板 (proximal femur anatomic locking plate, PFALP) 和动力髋螺钉 (dynamic hip screw, DHS) 为代表。对于不稳定型的股骨转子间骨折病例,大部分学者仍推荐使用髓内系统治疗[10-11]。
PFNA是国际AO组织在股骨近端髓内钉 (PFN) 基础上改进而来,它应用单一的螺旋刀片取代2枚螺钉,增加了旋转及成角的稳定性。PFNA螺旋刀片通过挤压松质骨能提供额外的把持力,同时能提供抗旋转的作用,对于骨质疏松性骨折有明显更高的抗切割力及更佳的螺钉把持力。有研究回顾性分析比较DHS、Gamma钉与PFNA治疗老年股骨转子间骨折的疗效,认为PFNA在缩短手术时间、减少术中出血、缩短卧床时间及促进关节功能恢复等方面显著优于前二者,对于治疗老年股骨转子间骨折更具优势[12-13]。本组获得完整随访的78例老年骨质疏松性股骨转子间骨折患者均采用PFNA治疗,所有患者骨折均获得愈合,无骨折延迟愈合或不愈合情况,随访周期中未发现螺钉切出、股骨干骨折等并发症,进一步肯定了PFNA治疗骨质疏松性股骨转子间骨折的手术效果。
老年髋部骨折患者常伴随不同程度的骨质疏松,增加了骨折复位及固定的难度,易导致固定失败、螺钉松动脱出等术后并发症,还容易导致术后再发骨折,因此在重视局部骨折治疗本身的同时,应积极关注治疗系统性骨质疏松症。钙和维生素D一直以来都是治疗骨质疏松的基础用药,2015年《中国骨质疏松性骨折诊疗指南》建议在正常饮食情况下,每日额外补充元素钙500~600 mg,每日补充普通维生素D 800~1 000 IU[14]。骨折早期会出现快速骨丢失,本组在围手术期采用常规剂量加倍的方案,即每次口服钙剂 (钙尔奇D) 600 mg和维生素D (骨化三醇) 0.25 μg、每日2次的方案作为每日基础治疗量,术后3个月改为每日1次[15]。
降钙素能抑制破骨细胞活性,减少破骨细胞数量从而阻止骨量丢失,还可与下丘脑网状结构降钙素受体结合,升高内啡肽,抑制前列腺素分泌的中枢止痛作用,适用于骨质疏松性骨折急性期合并疼痛患者。欧洲人用药品委员会 (CHMP) 调查认为,降钙素鼻喷剂长期治疗骨质疏松症患者获益未显著高于风险,同时也肯定了降钙素注射剂型在预防急性制动引起的急性骨丢失获益大于风险,并将此适应证下降钙素的建议治疗时间设为2周,最长不超过4周[16]。因而,本组病例采用鲑鱼降钙素术后皮下注射3周的治疗方式,获得满意疗效。
唑来膦酸是双膦酸盐类的代表药物,注射类唑来膦酸的特点是起效快、作用强、疗效长、使用方便,每年注射1次即可,能有效保证患者的依从性。HORIZON研究证实,唑来膦酸 (5 mg/年) 治疗3年时患者髋部骨密度、股骨颈骨密度分别增加了6.02%和5.06%,髋部骨折相对风险降低41%[17]。虽然唑来膦酸盐类药物在治疗骨质疏松方面的疗效已经得到广泛认可,但长期应用唑来膦酸盐类导致的非典型性股骨骨折及下颌骨坏死等罕见并发症也得到越来越多的重视[18-19]。关于髋部骨折术后双膦酸盐类的应用时机也得到了来自循证学的证据支持。研究通过纳入2 127例骨质疏松性髋部骨折的患者 (1 065例给予唑来膦酸盐5 mg, 1 062例给予安慰剂),从术后开始每2周为1个时间点分组运用唑来膦酸盐治疗直到术后90 d,通过比较各组患者在骨密度、骨折和病死率方面的差异,证实唑来膦酸盐的最佳应用时间在术后2~12周,最久不应超过术后90 d[20]。本组病例采取的是术后第2周开始应用。
抗骨质疏松药物除本研究中应用的基础治疗药物 (钙剂及活性维生素D3) 及抗骨吸收为主要机制的药物 (双膦酸盐类、降钙素类) 外,目前应用于临床的还有促骨形成类药物 (甲状旁腺类激素、维生素K、锶盐等) 及主要应用于绝经后女性的抗骨吸收类药物 (雌激素类药物及选择性雌激素受体调节剂)。鉴于此,女性骨质疏松患者和男性骨质疏松患者在用药选择上有所不同,前者治疗靶点更为丰富。对于非肿瘤性女性骨质疏松患者,甲状旁腺类激素rhPTH1-34临床效果更确切[21]。当然,骨质疏松症发病的根本原因在于骨吸收与骨形成的失衡。鉴于抑制骨吸收药物治疗的相对局限性,而促骨形成药物开发相对不足,近年来骨硬化素抗体、Wnt通路相关蛋白、促干细胞成骨分化以及干细胞移植等生物手段有望成为抗骨质疏松领域新的突破方向[22]。
综上所述,对于老年骨质疏松性股骨转子间骨折病例,采用PFNA髓内固定符合微创理念,操作简单,稳定性强,能有效降低术后髋内翻、股骨短缩畸形等手术并发症。在治疗局部骨折的同时,针对围手术期骨代谢特点,适当增加钙剂及维生素D等基础治疗量,采用降钙素与唑来膦酸盐的序贯治疗方案,能有效减少骨折急性期骨丢失,增加骨密度,降低再骨折风险,有效避免骨质疏松病情的恶化。
| [1] | BOTTLE A, AYLIN P. Mortality associated with delay in operation after hip fracture:observational study[J]. BMJ, 2006, 332: 947–951. DOI: 10.1136/bmj.38790.468519.55 |
| [2] | LIU J J, SHAN L C, DENG B Y, WANG J G, ZHU W, CAI Z D. Reason and treatment of failure of proximal femoral nail antirotation internal fixation for femoral intertrochanteric fractures of senile patients[J]. Genet Mol Res, 2014, 13: 5949–5956. DOI: 10.4238/2014.August.7.10 |
| [3] | 张立, 粱铂坚, 刘玉槐. 对骨质疏松性骨折不要忽视对骨质疏松症的治疗[J]. 中国骨质疏松杂志, 2011, 17: 457–459. DOI: 10.3969/j.issn.1006-7108.2011.05.020 |
| [4] | 中华医学会骨科学分会骨质疏松学组. 骨质疏松性骨折诊疗指南[J]. 中华骨科杂志, 2017, 37: 1–10. DOI: 10.3760/cma.j.issn.0253-2352.2017.01.001 |
| [5] | HARRIS W H. Traumatic arthritis of the hip after dislocation and acetabular fractures:treatment by mold arthroplasty.An end-result study using a new method of result evaluation[J]. J Bone Joint Surg Am, 1969, 51: 737–755. DOI: 10.2106/00004623-196951040-00012 |
| [6] | COOPER C, COLE Z A, HOLROYD C R, EARL S C, HARVEY N C, DENNISON E M, et al. Secular trends in the incidence of hip and other osteoporotic fractures[J]. Osteoporos Int, 2011, 22: 1277–1288. DOI: 10.1007/s00198-011-1601-6 |
| [7] | XIA W B, HE S L, XU L, LIU A M, JIANG Y, LI M, et al. Rapidly increasing rates of hip fracture in Beijing, China[J]. J Bone Miner Res, 2012, 27: 125–129. DOI: 10.1002/jbmr.519 |
| [8] | JOHNELL O, KANIS J A. An estimate of the worldwide prevalence, mortality and disability associated with hip fracture[J]. Osteoporos Int, 2004, 15: 897–902. DOI: 10.1007/s00198-004-1627-0 |
| [9] | HAENTJENS P, MAGAZINER J, COLÓN-EMERIC C S, VANDERSCHUEREN D, MILISEN K, VELKENIERS B, et al. Meta-analysis:excess mortality after hip fracture among older women and men[J]. Ann Intern Med, 2010, 152: 380–390. DOI: 10.7326/0003-4819-152-6-201003160-00008 |
| [10] | OZKAN K, TÜRKMEN Ï, SAHIN A, YILDIZ Y, ERTURK S, SOYLEMEZ M S. A biomechanical comparison of proximal femoral nails and locking proximal anatomic femoral plates infemoral fracture fixation:a study on synthetic bones[J]. Indian J Orthop, 2015, 49: 347–351. DOI: 10.4103/0019-5413.156220 |
| [11] | TETSWORTH K D, BORSHCH A Y, DLASKA C E, HOHMANN E. Does the relative density of periarticular bone influence the failure pattern of intra-articular fractures?[J]. Injury, 2016, 47: 1770–1776. DOI: 10.1016/j.injury.2016.05.014 |
| [12] |
黄俊, 纪方, 曹磊, 蔡晓斌, 付青格. DHS、Gamma钉和PFNA治疗老年骨质疏松性股骨粗隆间骨折[J]. 第二军医大学学报, 2008, 29: 1261–1264.
HUANG J, JI F, CAO L, CAI X B, FU Q G. DHS, Gamma nail and PFNA in treatment of osteoporotic intertrochanteric fracture in the elderly:a retrospective study[J]. Acad J Sec Mil Med Univ, 2008, 29: 1261–1264. DOI: 10.3321/j.issn:0258-879X.2008.10.030 |
| [13] | 蔡保塔, 徐成毅, 曹军, 胡广州, 杨绍安, 李松建. 三种内固定方式治疗老年股骨转子间骨折的疗效比较[J]. 中华创伤骨科杂志, 2016, 18: 564–568. DOI: 10.3760/cma.j.issn.1671-7600.2016.07.003 |
| [14] | 邱贵兴, 裴福兴, 胡侦明, 唐佩福, 薛庆云, 杨惠林, 等. 中国骨质疏松性骨折诊疗指南 (骨质疏松性骨折诊断及治疗原则)[J]. 中华骨与关节外科杂志, 2015, 8: 371–375. |
| [15] | 中国老年学学会骨质疏松委员会维生素D学组专家委员会, 廖祥鹏, 张增利, 张红红, 朱汉民, 周建烈, 黄琪仁, 等. 维生素D与成年人骨骼健康应用指南 (2014年标准版)[J]. 中国骨质疏松杂志, 2014, 20: 1011–1028. DOI: 10.3969/j.issn.1006-7108.2014.09.002 |
| [16] | European Medicines Agency. Calcitonin[EB/OL].(2012-07-19). http://www.ema.europa.eu/ema/index.jsp?curl=pages/medicines/human/referrals/Calcitonin/human_referral_000319.jsp&mid=WC0b01ac05805c516f. |
| [17] | JACQUES R M, BOONEN S, COSMAN F, REID I R, BAUER D C, BLACK D M, et al. Relationship of changes in total hip bone mineral density to vertebral and nonvertebral fracture risk in women with postmenopausal osteoporosis treated with once-yearly zoledronic acid 5 mg:the HORIZON-Pivotal Fracture Trial (PFT)[J]. J Bone Miner Res, 2012, 27: 1627–1634. DOI: 10.1002/jbmr.1644 |
| [18] | KHAN A A, MORRISON A, HANLEY D A, FELSENBERG D, MCCAULEY L K, O'RYAN F, et al. International Task Force on Osteonecrosis of the Jaw.Diagnosis and management of osteonecrosis of the jaw:a systematic review and international consensus[J]. J Bone Miner Res, 2015, 30: 3–23. DOI: 10.1002/jbmr.2405 |
| [19] | MARX R E, SAWATARI Y, FORTIN M, BROUMAND V. Bisphosphonate-induced exposed bone (osteonecrosis/osteopetrosis) of the jaws:risk factors, recognition, prevention, and treatment[J]. J Oral Maxillofac Surg, 2005, 63: 1567–1575. DOI: 10.1016/j.joms.2005.07.010 |
| [20] | ERIKSEN E F, LYLES K W, COLÓN-EMERIC C S, PIEPER C F, MAGAZINER J S, ADACHI J D, et al. Antifracture efficacy and reduction of mortality in relation to timing of the first dose of zoledronic acid after hip fracture[J]. J Bone Miner Res, 2009, 24: 1308–1313. DOI: 10.1359/jbmr.090209 |
| [21] | NEER R M, ARNAUD C D, ZANCHETTA J R, PRINCE R, GAICH G A, REGINSTER J Y, et al. Effect of parathyroid hormone (1-34) on fractures and bone mineral density in postmenopausal women with osteoporosis[J]. N Engl J Med, 2001, 344: 1434–1441. DOI: 10.1056/NEJM200105103441904 |
| [22] |
陈晓, 苏佳灿. 骨质疏松研究热点:骨髓间充质干细胞分化命运[J]. 第二军医大学学报, 2017, 38: 397–404.
CHEN X, SU J C. New focus on osteoporosis:differentiation fate of bone marrow-derived mesenchymal stem cells[J]. Acad J Sec Mil Med Univ, 2017, 38: 397–404. |
 2016, Vol. 38
2016, Vol. 38


