随着腹腔镜技术的发展,腹腔镜下肾部分切除术(laparoscopic partial nephrectomy,LPN)的开展愈发广泛,T1aN0M0期的肾癌患者治疗首选LPN已成为共识[1-3],而对于T1bN0M0期肾癌患者,根治性肾切除术或肾部分切除术都是可选择的治疗手段[4-6]。LPN入路主要有经腹途径和经后腹腔途径[7-8],经后腹腔途径是国内微创泌尿外科医师最熟悉的一种手术入路,已被广泛采用。在肾部分切除术中,该入路具有独特的优势,可便捷地显露肾脏动脉[9]。然而,大量临床实践证实经后腹腔途径也存在不足,如手术操作空间狭窄、缺乏明确的解剖标志、操作技术要求高、学习曲线长等[5];其中最主要的技术难点是缝合难度较大,尤其是对于上下两极的肿瘤。因此,研究如何充分发挥经后腹腔途径对肾动脉显露的优势,并最大限度降低缝合关闭肾脏的难度具有重要意义。本科室利用相对运动原理摸索并总结了5大技巧:“1动、2加、3推、4拉、5换”,即通过各种方式将需要缝合的创面移动至持针器前,以获得最佳的进针和出针角度。现将5大技巧的初期临床运用情况报道如下。
1 资料和方法 1.1 临床资料回顾性纳入本院2014年1月至2016年5月由同一术者完成LPN的患者共89例。其中2014年1月至2015年2月期间行传统手术的42例患者设为对照组;2015年3月本科室对5大技巧进行了系统总结,并严格运用于后期手术操作,2015年3月至2016年5月期间运用5大技巧进行手术的47例患者设为技巧组。对照组男性20例,女性22例,年龄(56.5±12.9)岁;技巧组男性26例,女性21例,年龄(57.2±11.8)岁。两组患者均为肾单发肿瘤,对照组肿瘤平均最大径(3.2±0.6) cm,技巧组(3.3±0.8) cm。肾癌TNM肿瘤分期为对照组T1a期37例,T1b期5例;技巧组T1a期40例,T1b期7例。对照组单根肾动脉者38例,多根肾动脉者4例;技巧组单根肾动脉者41例,多根肾动脉者6例。对照组R.E.N.A.L.评分(5.5±2.0)分,技巧组(5.6±1.2)分。所有手术均由同一术者施行。
1.2 手术方法患者全麻后,取健侧折刀位,躯体平床缘,妥善固定。采用气囊扩张法建立腹膜后CO2气腹腔,气腹压14 mmHg(1 mmHg=0.133 kPa)。建立3处穿刺套管通道,分别为腋中线髂脊头侧2 cm、患侧肋缘下腋后线、肋缘下腋前线,若肿瘤较大或显露困难,可于腋前线套管针下方建立辅助通道。游离腹膜后脂肪,打开Gerota筋膜,以超声刀解剖出肾动脉,在肾包膜外充分解剖显露肾脏肿瘤,电钩标记肾肿瘤的切缘,阻断肾动脉,记录热缺血开始时间;沿肿瘤边缘0.5 cm处用剪刀将肿瘤完整切除,检查创面,如集合系统破坏则连续缝合关闭集合系统,随后倒刺线及Hem-o-lock夹缝合肾脏髓质,再以大针缝合肾脏皮质。松开肾动脉阻断钳,记录肾脏热缺血时间,仔细检查肾脏缝合处有无出血,确认术野无活动性出血。用取物袋将肿瘤标本取出。放置肾周引流管,关闭各穿刺点,术毕。
技巧组在缝合过程中严格运用“1动、2加、3推、4拉、5换”5大技巧暴露肿瘤并缝合肾脏创面,而对照组尚未严格执行5大技巧,仅凭术者以往经验缝合关闭肾脏创面。5大技巧具体总结如下。
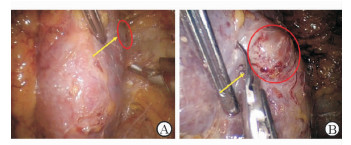
1动:肿瘤位于肾脏中极稍上、略偏背侧是最适合经后腹腔途径入路的病例。但一旦肿瘤位于上下两极或靠近腹侧,若没有做好充分的准备,缝合关闭将十分困难,经常看不到进针点和够不着出针点。因此,无论肿瘤位于何处,阻断前都需要充分游离肾脏,使肿瘤和预计的创面移动到术者“眼前”(图 1)。判断游离是否充分有两个标准:(1)术者能否容易且清楚地看到预计创面边缘,即进针点和出针点;(2)用持针器夹针模拟缝合角度是否合适。
|
图 1 右肾上极游离前(A)、后(B)的肿瘤位置(箭头) Fig 1 Tumor location (arrows) before (A) and after (B) dissection of kidney |
2加:当肾脏被完全游离后,活动度明显增加,这也会加大肿瘤切除和缝合的难度。此时,增加一个5 mm的辅助孔,使用无损伤钳或吸引器固定肾脏将更便于操作。经后腹腔途径空间有限,本研究总结出增加第4套管的最佳且唯一位置是腹侧套管下方5 cm处,与观察孔基本平行,距离髂前上棘边缘至少2指(图 2)。

|
图 2 左侧增加辅助孔的示意图(A)和实景图(B) Fig 2 Schematic diagram (A) and photo (B) of adding auxiliary hole in left abdomen 1: Handle hole, at the anterior axillary line below arcus costarum; 2: Handle hole, at costolumbar point; 3: Handle hole, at 2 cm above iliac crest |
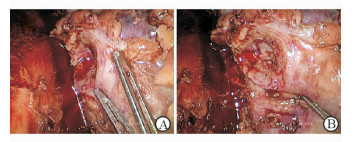
3推:增加辅助孔后,助手根据手术的具体情况利用器械推挡,调整肾脏位置和转向,将肿瘤或创面尽可能放置在主刀面前,以便于操作。一般上极为压,下极为挑,腹侧为推(图 3)。
|
图 3 助手辅助下压前(A)、后(B)的创面位置 Fig 3 Position of surgical wounds before (A) and after (B) pushing by assistant |
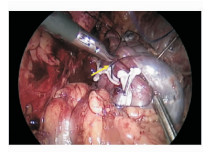
4拉:如果助手经验丰富、操作能力强,对手术理解透彻,主刀可以完全依靠助手调整肾脏位置和角度,来满足缝合要求。当助手不能很好地配合显露时,主刀可用左手借助缝线对肾脏进行牵拉,从而调整其角度和位置,配合右手缝合(图 4)。
|
图 4 主刀左手牵拉缝线,固定肾脏并协助显露(箭头) Fig 4 Operator pulls suture to fixate the kidney and facilite the exposure (arrow) |
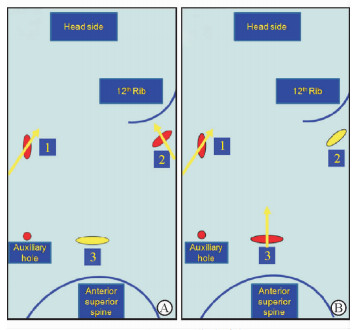
5换:经过以上4个技巧后,通常都能很好地将肾脏创面调整到合适的角度和位置。某些极端情况下,还可通过换手或换套管进行进一步调整。如换成左手拿持针器进行缝合,将观察镜从正中套管换至腋前线或腋后线位置。该方法虽然改变了操作习惯,但可降低缝合难度,仍具有一定的价值,术者平时可有意练习(图 5)。
|
图 5
操作通道的选择
Fig 5
Choosing trocars as operation holes
A: Choosing 1 and 2 trocars; B: Choosing 1 and 3 trocars. 1: Handle hole, at the anterior axillary line below arcus costarum; 2: Handle hole, at costolumbar point; 3: Handle hole, at 2 cm above iliac crest |
1.3 观察指标
记录患者年龄、性别、肿瘤最大径及分期、R.E.N.A.L.评分、肾动脉支数、手术时间、术中热缺血时间、术中输血量、出血量、血管损伤的情况以及有无术后并发症等,比较两组患者相关指标差异。
1.4 统计学处理应用SPSS 16.0软件处理数据。呈正态分布的计量资料以x±s表示,两组间比较采用独立样本t检验。计数资料用百分比表示,两组间比较采用χ2检验。检验水准(α)为0.05。
2 结果89例手术均顺利完成。两组患者的年龄、性别、肿瘤最大径及分期、R.E.N.A.L.评分等差异均无统计学意义(P>0.05),具有可比性。利用5大技巧后技巧组手术时间较对照组缩短(P=0.03),热缺血时间也短于对照组(P=0.04)。两组术中输血、出血量及血管损伤情况差异均无统计学意义。两组术中均无中转开放或切除患肾病例。对照组术后血尿1例,技巧组术后血尿2例,给予对症治疗后均好转;所有患者均无术后漏尿等并发症。见表 1。
|
|
表 1 技巧组与对照组围手术期资料比较 Tab 1 Comparison of peri-operative data between the skill and control groups |
3 讨论
1993年,Winfield等[10]首次报道了LPN。目前LPN已成为T1a期肾肿瘤的首选治疗方案[1, 11],其切缘阴性率和中远期无瘤生存率与开放手术相比差异无统计学意义[12-13]。经后腹腔途径LPN入路可直达肾门,方便分离肾血管,但操作空间狭小,持针角度固定[14],对术者腔内缝合水平要求较高。国内有学者报道经腹和后腹腔联合入路进行手术,整合了经腹途径操作空间大和经后腹腔途径分离肾血管方便的优势,尤其是在遇到有肾动脉出现变异的患者时,其优势明显[15]。研究认为肾脏的热缺血总时间最好控制在20~25 min[16],每减少1 min都对肾功能的恢复十分重要[17]。决定肾脏热缺血时间长短的一个重要因素是肾脏创面的缝合速度,其影响因素很多。首先,受手术方式和手术入路的影响;其次,受肾脏创面的深浅及角度的影响。较深的创面不容易对合,过浅的创面因创面弧度较大不利于缝合,当创面位置和角度不佳时对缝合技术的要求更高。LPN的关键是要提高肾脏创面的缝合技术,尽可能缩短热缺血时间。因而优化肾脏缝合方式,快速、精准、可靠地缝合肾脏创面尤为重要。本研究中技巧组与对照组患者年龄、肿瘤分期和R.E.N.A.L.评分等术前临床资料上差异无统计学意义(P>0.05),故具有可比性,但技巧组较对照组肿瘤最大径略偏大,T1b期患者比例略高。技巧组较对照组手术时间和肾脏热缺血时间均缩短,两组术后并发症无差异(P>0.05),均未发生术后大出血及漏尿等严重并发症,表明5大技巧可最大限度地简化并加快肾脏创面缝合过程,切实缩短肾脏热缺血时间以保护患者肾功能。两组患者术后肾小球滤过率水平短期随访差异无统计学意义,但技巧组术后肾小球滤过率略高于对照组,后期肾功能恢复水平及恢复时间需长期随访进行评估及完善。
本研究尚处于初期阶段,即使选取的病例均为同一术者完成以避免不同学习曲线所造成的统计学偏移,但非随机的分组,对照组或多或少也用到了5大技巧,可能会影响本研究结果。因此,将来更多的经验总结以及大样本的前瞻性随机对照研究有助于对5大技巧进行全面评估和验证,5大技巧也应该在未来的临床实践中不断发展和完善。总之,依据相对运动原理总结的5大技巧化繁为简,实用性强,易于被低年资泌尿外科医师接受和掌握。同时,在手术操作中,5大技巧既相互独立又相辅相成,可灵活组合以应对不同肿瘤情况,其在LPN中的可行性和安全性已在单中心临床实践中得到验证,值得进一步临床应用及推广。
| [1] | HEUER R, GILL I S, GUAZZONI G, KIRKALI Z, MARBERGER M, RICHIE J P, et al. A critical analysis of the actual role of minimally invasive surgery and active surveillance for kidney cancer[J]. Eur Urol, 2010, 57: 223–232. DOI: 10.1016/j.eururo.2009.10.023 |
| [2] | CRÉPEL M, JELDRES C, SUN M, LUGHEZZANI G, ISBARN H, ALASKER A, et al. A population-based comparison of cancer-control rates between radical and partial nephrectomy for T1A renal cell carcinoma[J]. Urology, 2010, 76: 883–888. DOI: 10.1016/j.urology.2009.08.028 |
| [3] | GILL I S, KAVOUSSI L R, LANE B R, BLUTE M L, BABINEAU D, COLOMBO J R, et al. Comparison of 1, 800 laparoscopic and open partial nephrectomies for single renal tumors[J]. J Urol, 2007, 178: 41–46. DOI: 10.1016/j.juro.2007.03.038 |
| [4] | BECKER A, RAVI P, ROGHMANN F, TRINH Q D, TIAN Z, LAROUCHE A, et al. Laparoscopic radical nephrectomy vs laparoscopic or open partial nephrectomy for T1 renal cell carcinoma:comparison of complication rates in elderly patients during the initial phase of adoption[J]. Urology, 2014, 83: 1285–1291. DOI: 10.1016/j.urology.2014.01.050 |
| [5] | DEKLAJ T, LIFSHITZ D A, SHIKANOV S A, KATZ M H, ZORN K C, SHALHAV A L. Laparoscopic radical versus laparoscopic partial nephrectomy for clinical T1bN0M0 renal tumors:comparison of perioperative, pathological, and functional outcomes[J]. J Endourol, 2010, 24: 1603–1607. DOI: 10.1089/end.2009.0312 |
| [6] | TAN H J, NORTON E C, YE Z, HAFEZ K S, GORE J L, MILLER D C. Long-term survival following partial vs radical nephrectomy among older patients with early-stage kidney cancer[J]. JAMA, 2012, 307: 1629–1635. DOI: 10.1001/jama.2012.475 |
| [7] | MARSZALEK M, CHROMECKI T, AL-ALI B M, MEIXL H, MADERSBACHER S, JESCHKE K, et al. Laparoscopic partial nephrectomy:a matched-pair comparison of the transperitoneal versus the retroperitoneal approach[J]. Urology, 2011, 77: 109–113. DOI: 10.1016/j.urology.2010.02.057 |
| [8] | WRIGHT J L, PORTER J R. Laparoscopic partial nephrectomy:comparison of transperitoneal and retroperitoneal approaches[J]. J Urol, 2005, 174: 841–845. DOI: 10.1097/01.ju.0000169423.94253.46 |
| [9] | REN T, LIU Y, ZHAO X, NI S, ZHANG C, GUO C, et al. Transperitoneal approach versus retroperitoneal approach:a meta-analysis of laparoscopic partial nephrectomy for renal cell carcinoma[J/OL]. PLoS One, 2014, 9:e91978. doi:10.1371/journal.pone.0091978. |
| [10] | WINFIELD H N, DONOVAN J F, GODET A S, CLAYMAN R V. Laparoscopic partial nephrectomy:initial case report for benign disease[J]. J Endourol, 1993, 7: 521–526. DOI: 10.1089/end.1993.7.521 |
| [11] | CAMPBELL S C, NOVICK A C, BELLDEGRUN A, BLUTE M L, CHOW G K, DERWEESH I H, et al. Guideline for management of the clinical T1 renal mass[J]. J Urol, 2009, 182: 1271–1279. DOI: 10.1016/j.juro.2009.07.004 |
| [12] | LANE B R, CAMPBELL S C, GILL I S. 10-year oncologic outcomes after laparoscopic and open partial nephrectomy[J]. J Urol, 2013, 190: 44–49. DOI: 10.1016/j.juro.2012.12.102 |
| [13] | MARSZALEK M, MEIXL H, POLAJNAR M, RAUCHENWALD M, JESCHKE K, MADERSBACHER S. Laparoscopic and open partial nephrectomy:a matched-pair comparison of 200 patients[J]. Eur Urol, 2009, 55: 1171–1178. DOI: 10.1016/j.eururo.2009.01.042 |
| [14] | MCALLISTER M, BHAYANI S B, ONG A, JAFFE W, MALKOWICZ S B, VANARSDALEN K, et al. Vena caval transection during retroperitoneoscopic nephrectomy:report of the complication and review of the literature[J]. J Urol, 2004, 172: 183–185. DOI: 10.1097/01.ju.0000132143.33340.51 |
| [15] |
杨波, 高小峰, 王辉清, 张超, 李凌, 彭泳涵, 等. 腰腹联合三步法腹腔镜肾部分切除术的初期临床应用体会[J]. 第二军医大学学报, 2016, 37: 83–86.
YANG B, GAO X F, WANG H Q, ZHANG C, LI L, PENG Y H, et al. Laparoscopic partial nephrectomy via combined "trans-retro-peritoneal three-step" approach:an initial experience[J]. Acad J Sec Mil Med Univ, 2016, 37: 83–86. |
| [16] | GODOY G, RAMANATHAN V, KANOFSKY J A, O'MALLEY R L, TAREEN B U, TANEJA S S, et al. Effect of warm ischemia time during laparoscopic partial nephrectomy on early postoperative glomerular filtration rate[J]. J Urol, 2009, 181: 2438–2445. DOI: 10.1016/j.juro.2009.02.026 |
| [17] | THOMPSON R H, LANE B R, LOHSE C M, LEIBOVICH B C, FERGANY A, FRANK I, et al. Every minute counts when the renal hilum is clamped during partial nephrectomy[J]. Eur Urol, 2010, 58: 340–345. DOI: 10.1016/j.eururo.2010.05.047 |
 2017, Vol. 38
2017, Vol. 38


