颅脑战创伤是现代战争中导致舰员伤亡的重要因素。现代战争条件下的海战由于武器和环境的差异,既不同于既往海战,与现代陆战特点也有明显区别[1]。由于国内外均缺乏实战数据,对现代海战下的颅脑战创伤特点和机制等缺乏足够了解,制约了颅脑海战伤的研究进展,颅脑海战伤的分级救治也因此缺乏基本依据。海战有两种基本致伤环境,一是海水及舰艇环境下的武器爆炸毁伤,二是海水因素的影响,这两种因素明显有别于陆战环境;而且在舰船的不同舱室,人员受到的冲击程度有明显差别。本研究通过模拟舰艇多舱室内爆炸试验建立比格犬爆震伤模型,分析其颅脑损伤的伤情特点,为进一步研究人体颅脑爆震伤的致伤机制提供实验和理论依据。
1 材料和方法 1.1 实验动物与分组体质量为9~11 kg的健康比格犬24只,雌雄不限,购于北京玛斯生物技术有限公司,动物生产许可证号:SCXK (京)2016-0001。采用完全随机的方法分成2组,每组12只。定义炸药安放舱为当舱,相邻舱室为邻舱,两组比格犬分别置于当舱和邻舱中接受试验。
1.2 多舱室模型和爆源选择参照海军舰船的相关重点舱室(配电室及计算机室)的材料及结构,建立海军多舱室等比例模型,舱室模型结构长4 m,宽2 m,高2.5 m;舱室采用与船用钢动态力学性能相似且成本相对较低、适用于开展大规模实尺度舱室模型试验的钢材制造而成。通常,实船的主甲板比下层甲板厚,本试验模型的上甲板厚为10 mm,下甲板厚为5 mm,舱壁厚度4 mm。舱室模型共3个(若一侧被破坏太严重无法修复时,另一侧作备用),沿长度方向布置,如图 1A所示。

|
图 1 舱室模型和动物放置实物图及舱室示意图 A:舱室模型;B:动物放置情况;C:舱室示意图. P1、P2:压力传感器放置位置 |
目前西方国家舰艇主炮口径分别为76 mm和127 mm,试验中主炮口径选择我国标配的76 mm口径炮弹的等效裸药,经过测算,76 mm口径炮弹的等效裸药量为0.65 kg TNT[2],因此选择0.65 kg TNT裸药作为实验爆源,在模拟舰船舱室内爆炸。
1.3 动物模型的建立按照40 mg/kg的剂量腹腔内注射戊巴比妥钠,以0.2 mg/kg的剂量肌内注射速眠新,麻醉比格犬。
76 mm口径炮弹能使舱壁产生破口的临界破坏距离约为0.5 m;因此,舱内爆炸时,将等效裸药安放于横舱壁中点处,并距横舱壁0.5 m,距下甲板1.25 m。选取与等效裸药水平距离2 m、等高度的战位在两个舱室内放置实验动物并固定,裸药与动物放置实物图和示意图如图 1B、1C所示。
将压力传感器固定于当舱和邻舱的舱壁用于测定冲击波强度,传感器位置与爆源等高,距离爆源1.28 m,具体布放位置如图 1C中P1、P2处所示。准备完全后充电引爆炸药,爆炸后立即现场记录犬的存活情况,随后将犬取出,对死亡动物进行大体解剖,幸存动物作进一步观察。采用Wavebook516A数据采集系统收集爆炸冲击波物理参数,Origin 7.0软件进行滤波和分析处理。
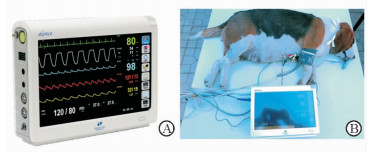
1.4 观察指标 1.4.1 比格犬生命体征使用élance 5型生命体征监护仪记录实验前及爆炸后不同时间点比格犬的基本生命体征,包括肛温、心率、呼吸频率、血压以及血氧饱和度(图 2)。
|
图 2 生命体征监护仪(A)及比格犬生命体征监测(B) |
1.4.2 比格犬伤后功能评分
采用改良Tarlov评分法[3]和大动物神经功能评分法[4],对舱室爆炸后存活的比格犬进行评分,评分的时间点为爆炸后即刻、爆炸后3 h以及爆炸后24 h。
改良Tarlov评分法分为优(5分)、良(4分)、可(2~3分)、差(0~1分)4种状态。评分标准:0分,后肢无活动,不能负重;1分,后肢可见活动,不能负重;2分,后肢活动频繁或有力,不能负重;3分,后肢可支持体重,能走1~2步;4分,可行走,仅有轻度障碍;5分,行走正常。
大动物神经功能评分法分为正常(18~20分)、独立生存(13~17分)、人工饲养生存(8~12分)和濒死(≤7分) 4种状态。评分标准:从意识状态、运动、肌张力、视力、饮食、疼痛反应、排尿和排便8个方面分别计分。意识状态:清醒(3分)、嗜睡(2分)、昏迷(1分)、深昏迷(0分);运动:正常行走(3分)、跛行(轻瘫)(2分)、不能站立(1分)、不动(0分);肌张力:正常(3分)、增高(2分)、减弱(1分)、无张力(0分);视力:正常观看(3分)、有视反应(2分)、有瞳孔反应(1分)、无反应(0分);饮食:自己进食(2分)、仅有进食反应(1分)、无反应(0分);疼痛反应:灵敏(2分)、迟钝(1分)、无反应(0分);排尿:正常(2分)、尿失禁(1分)、尿潴留(0分);排便:正常(2分)、大便失禁(1分)、不能排便(0分)。
所有幸存动物在各评分时间点分别采用两种方法进行评分,两种评分间隔30 min、采用双人双盲独立观察,观察者为熟悉评分标准的非本组实验人员,观察期为5 min,每只动物测3次,取平均值,最后结果为两位观察者的平均记录分数。评价前检查所有动物膀胱是否充盈,避免膀胱充盈而影响活动。
1.4.3 比格犬颅脑标本采集爆炸后即刻死亡的比格犬,立即留取脑组织;爆炸后存活犬观察24 h后,采用戊巴比妥钠40 mg/kg腹腔麻醉,于股动脉放血处死,解剖观察颅脑组织损伤情况,留取脑组织置于10%甲醛溶液中固定,留作后期病理学检查。
1.5 统计学处理采用SPSS 19.0软件进行统计学分析。数据以x±s表示,两组间比较采用两样本均数比较的t检验;多组间比较采用单因素方差分析,进一步两两比较采用SNK-q检验。检验水准(α)为0.05。
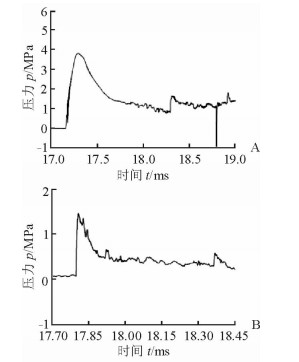
2 结果 2.1 冲击波压力和准静态压力0.65 kg TNT爆炸时,布置在爆炸当舱的舱壁上的压力传感器距离爆点为1.28 m,其冲击波压力曲线如图 3A所示。从图中可以看出该点的第1个反射冲击波压力峰值为3.78 MPa,正压作用约为1.2 ms;第2个反射冲击波压力峰值为1.73 MPa。布置在爆炸邻舱的舱壁上的压力传感器距离爆点为1.28 m,其冲击波压力曲线如图 3B所示。从图中可以看出邻舱测点的第1个反射冲击波压力峰值为1.47 MPa,正压作用约为1.3 ms;第2个反射冲击波压力峰值为0.67 MPa。第2个反射冲击波压力峰值约为第1个反射冲击波压力峰值的46%。与爆炸当舱的冲击波压力相比,邻舱的冲击波压力峰值要小得多,约为爆炸当舱冲击波压力峰值的39%,并且正压作用时间没有明显延长。
|
图 3 0.65 kg TNT爆炸舱室测点的冲击波压力曲线 A:当舱;B:邻舱 |
2.2 动物存活情况
24只比格犬中,爆炸24 h内共死亡11只。爆炸后现场即刻死亡7只,其中当舱爆炸后即刻死亡5只,邻舱爆炸后即刻死亡2只;死因为多种损伤造成的复合伤,主要原因可能是脑组织和肺组织的冲击波伤,以及冲击波造成身体跌落碰撞的机械损伤;7只比格犬均有颅骨骨折,其中2只有明显的颅脑开放伤,脑组织外露、破碎。伤后24 h内死亡4只,其中当舱比格犬中爆炸后1.5 h死亡1只、爆炸后2.5 h死亡1只、爆炸后17 h死亡1只,邻舱比格犬中爆炸后14 h死亡1只;主要死因可能是脑组织和肺组织的冲击波伤,均有脑组织出血、水肿和肺出血等损伤。比格犬死亡率为45.83%(11/24),其中当舱动物死亡率为66.67%(8/12),邻舱动物死亡率为25.0%(3/12)。
2.3 基本生命体征使用élance 5型生命体征监护仪记录爆炸前比格犬的基本生命体征,舱室爆炸后仍存活的比格犬在爆炸后即刻、爆炸后3 h以及爆炸后24 h再次记录其基本生命体征(表 1)。爆炸后即刻存活的比格犬心率、呼吸频率、血压都有增加,血氧饱和度下降(P < 0.05),冲击波对比格犬的急性损伤会在早期显现;经过3 h其心率、呼吸与爆炸后即刻比仍偏高(P < 0.05),血氧饱和度仍偏低;到24 h后比格犬基本生命体征大致恢复至爆炸前水平。
|
|
表 1 舱室爆炸前后比格犬基本生命体征情况 |
根据对基本生命体征的分析,比格犬在爆炸后即刻心率、呼吸频率、血压和血氧饱和度等生命体征变化最为明显,将爆炸后即刻当舱存活的7只和邻舱存活的10只比格犬基本生命体征进行比较(表 2),发现在爆炸后即刻除直肠温度外,其他基本生命体征在当舱和邻舱之间差异有统计学意义(P < 0.05),当舱比格犬的生命体征情况相对要差,其爆震伤后的损伤情况较重。
|
|
表 2 当舱和邻舱爆炸后即刻比格犬基本生命体征情况 |
2.4 比格犬改良Tarlov评分和大动物神经功能评分
爆炸后比格犬改良Tarlov评分和大动物神经功能评分(表 3)显示其运动功能和神经功能都受到明显的影响,冲击波对动物颅脑造成急性损伤,影响其神经功能,但爆炸后24 h动物的运动功能和神经功能基本恢复正常。
|
|
表 3 舱室爆炸后比格犬改良Tarlov评分和大动物神经功能评分 |
2.5 脑组织病理
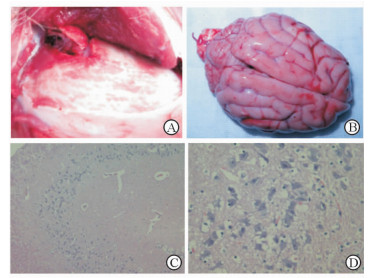
解剖发现爆炸后即刻死亡的比格犬颅骨有粉碎性骨折(图 4A),脑组织有明显的挫裂伤,脑组织表面有少量微小血管破裂出血(图 4B),严重者脑组织破碎,且当舱爆炸后即刻死亡的比格犬颅脑损伤重于邻舱,其中当舱爆炸后即刻死亡的比格犬有2只脑组织外露、缺如;爆炸后24 h内死亡的比格犬脑组织可见脑出血和脑水肿的损伤。
|
图 4 爆炸后比格犬脑组织病理 A:颅骨粉碎性骨折;B:脑组织大体观;C,D:脑组织H-E染色.Original magnification: ×100 (C), ×400 (D) |
爆炸后存活的比格犬脑组织中的海马在光镜下也可见部分形态结构和神经元结构的异常,有少许死亡坏死区,部分神经元出现核固缩深染、核溶解或核仁消失,细胞界限模糊(图 4C、4D)。
3 讨论舰艇部队是海上作战的主力军,因此,舰员冲击安全性的研究是国内外研究的重点。爆炸物在舱室内爆炸后产生的冲击波损伤强度要比自由场大2~9倍,还会形成二次反射冲击波,舰艇的舱室作为一个密闭舱室能明显放大冲击波的损伤效应,加重对生物体的损伤[5]。除了爆炸冲击波直接造成的损伤外,冲击波还对船体造成强烈的振动,形成机械冲击环境。
爆震伤一般按致伤因素分为4级[6]:初级损伤是其特征性的损伤方式,由爆炸产生的冲击波引起,二级、三级、四级分别是由破片、身体跌落碰撞和爆炸产生的高温、火球、有毒气体等引起。本实验中,虽然比格犬是固定于舱室内,但冲击波仍导致部分动物跌落和碰撞,造成了严重的机械损伤。因此,爆炸后现场死亡的比格犬死因多为复合伤,主要为冲击波伤和身体跌落碰撞造成的机械损伤;而爆炸后24 h内死亡的比格犬死因主要为冲击波伤;爆炸后存活的比格犬也主要受到冲击波的损伤。
爆炸瞬时产生的高压冲击波在通过密度不同的界面时会引起压力的突然改变,从而导致物质的变形和损伤。组织间密度差别越大,越容易受到冲击波的损伤,因此颅脑是最易受到损伤的器官之一, 冲击波对脑组织损伤的阈值在所有器官中最低(低于1 MPa)[7]。一般认为冲击波是通过局部作用和全身效应两方面对脑组织产生损伤,局部作用是指冲击波穿过头皮和颅骨等组织,引起脑组织移位变形而产生损伤;全身效应则是指冲击波作用于胸腹部,瞬时挤压该处的大血管,压力经大血管传导入颅并阻碍颅内静脉回流而致伤[8-9]。
脑组织损伤的程度与冲击波的波形、压力峰值和持续时间密切相关[10]。本实验采用与真实舰艇重点舱室相同大小和相似材质的连续舱室作为爆炸环境,以与76 mm口径舰炮炮弹等效的裸药作为爆源,力求最大限度再现实战场景。在舱室爆炸后,由于舱壁和舱室内机柜等物体的反射,会有二次反射冲击波的出现,本实验中测得第2个反射冲击波压力峰值为第1个反射冲击波压力峰值的46%,多次反射冲击波的叠加,会增强对舱室内生物体的损伤。另者,邻舱的冲击波压力峰值比爆炸当舱小得多,约为爆炸当舱冲击波压力峰值的39%,正压作用时间没有明显延长。存活的比格犬其基本生命体征和神经功能评分在爆炸后即刻受到明显的影响,可能与冲击波造成的颅脑急性损伤有关。而且,当舱中比格犬的死亡率要远大于邻舱,且多由冲击波导致的复合伤致死。当舱存活的比格犬其基本生命体征比邻舱要差,说明其颅脑冲击波损伤程度更为严重。
爆炸后存活的比格犬在24 h后基本恢复正常的生命体征和神经功能评分,说明在这种当量下的舱室爆炸造成的多为轻度颅脑损伤。而已有研究认为轻度颅脑爆震伤后在出现病理形态学改变之前,神经元细胞膜的完整性就已经受损[11],冲击波峰值越大,这种损伤越明显。美军对颅脑爆震伤死亡人员尸检发现最典型的病理改变是广泛的神经轴索损伤,这也是目前判断颅脑爆震伤损伤严重程度的一个重要神经病理学指标[12],但是神经轴索损伤并不一定伴有明显的形态学改变,因此单纯以轴索是否肿胀判断损伤程度会明显低估损伤程度[13]。本实验中,比格犬脑组织的大体标本有明显的血管损伤,也有神经元细胞的损伤和异常,说明轻度的颅脑爆震伤会导致脑组织多方面的损伤。
临床上发现颅脑爆震伤伤员出现创伤后应激综合征(PTSD)的概率高于普通脑外伤患者,此类伤员脑组织中的海马和杏仁核部位有损伤表现,可能存在发生PTSD的病理生理基础[14]。存活比格犬的脑组织海马部分在光镜下可见明显的损伤迹象,但本实验并未进行长期的观察研究,对颅脑爆震伤的后续深入研究正在进行,这也是我们下一步实验的方向。
综上所述,在多舱室环境下发生爆炸时,可能由于舱壁的阻挡和反射,当舱冲击波的压力峰值会更高,再叠加上二次反射冲击波,造成的颅脑爆震伤更为严重;邻舱可能由于舱室间壁的部分阻挡作用,其冲击波强度相对要小,但邻舱内生物体也会在冲击波作用下,合并二、三级损伤,造成致命性后果;但造成的颅脑爆震伤的损伤程度相对要低。本实验取得了部分初步结果,对多舱室生物体爆震伤的损伤规律有了新的认识,同时为下一步的救治研究奠定了基础。
| [1] | 胡朝晖, 赵德军, 孙艳新. 现代海战伤特点及早期救治初探[J]. 海军医学杂志, 2012, 33: 380–382. |
| [2] | 田娟, 石全, 王勇. 浅析爆炸振动中冲击波的损伤特性[J]. 装备环境工程, 2008, 5: 70–73. |
| [3] | TARLOV I M, KLINGER H. Spinal cord compression studies. Ⅱ. Time limits for recovery after acute compression in dogs[J]. AMA Arch Neurol Psychiatry, 1954, 71: 271–290. DOI: 10.1001/archneurpsyc.1954.02320390001001 |
| [4] |
张晓鹏, 胡加飞, 蔡如珏, 黄承瑶, 文淑华, 董萍, 等. 一种灵长类动物的中枢神经系统功能评价方法[J]. 第二军医大学学报, 1997, 18: 285–286.
ZHANG X P, HU J F, CAI R J, HUANG C Y, WEN S H, DONG P, et al. An evaluating method of the function of central nervous system in non-human primate[J]. Acad J Sec Mil Med Univ, 1997, 18: 285–286. |
| [5] | LI B, LI Y, XU C, WANG J, CHEN Z, LI G, et al. Blast-induced traumatic brain injury of goats in confined space[J]. Neurol Res, 2014, 36: 974–982. DOI: 10.1179/1743132813Y.0000000314 |
| [6] | PLURAD D S. Blast injury[J]. Mil Med, 2011, 176: 276–282. DOI: 10.7205/MILMED-D-10-00147 |
| [7] | LANCE R M, CAPEHART B, KADRO O, BASS C R. Human injury criteria for underwater blasts[J/OL]. PLoS One, 2015, 10:e0143485. doi:10.1371/journal.pone.0143485. |
| [8] | LING G, BANDAK F, ARMONDA R, GRANT G, ECKLUND J. Explosive blast neurotrauma[J]. J Neurotrauma, 2009, 26: 815–825. DOI: 10.1089/neu.2007.0484 |
| [9] | LONG J B, BENTLEY T L, WESSNER K A, CERONE C, SWEENEY S, BAUMAN R A. Blast overpressure in rats:recreating a battlefield injury in the laboratory[J]. J Neurotrauma, 2009, 26: 827–840. DOI: 10.1089/neu.2008.0748 |
| [10] | ROSENFELD J V, MCFARLANE A C, BRAGGE P, ARMONDA R A, GRIMES J B, LING G S. Blast-related traumatic brain injury[J]. Lancet Neurol, 2013, 12: 882–893. DOI: 10.1016/S1474-4422(13)70161-3 |
| [11] | KOLIATSOS V E, CERNAK I, XU L, SONG Y, SAVONENKO A, CRAIN B J, et al. A mouse model of blast injury to brain:initial pathological, neuropathological, and behavioral characterization[J]. J Neuropathol Exp Neurol, 2011, 70: 399–416. DOI: 10.1097/NEN.0b013e3182189f06 |
| [12] | MCKEE A C, DANESHVAR D H. The neuropathology of traumatic brain injury[J]. Handb Clin Neurol, 2015, 127: 45–66. DOI: 10.1016/B978-0-444-52892-6.00004-0 |
| [13] | MISHRA V, SKOTAK M, SCHUETZ H, HELLER A, HAORAH J, CHANDRA N. Primary blast causes mild, moderate, severe and lethal TBI with increasing blast overpressures:experimental rat injury model[J/OL]. Sci Rep, 2016, 6:26992. doi:10.1038/srep26992. |
| [14] | SULLIVAN E V. War-related PTSD, blast injury, and anosognosia[J]. Neuropsychol Rev, 2012, 22: 1–2. DOI: 10.1007/s11065-012-9188-z |
 2017, Vol. 38
2017, Vol. 38


