2. 中国人民解放军镇江船艇学院门诊部, 镇江 212003;
3. 南京军区福州总医院心内科, 福州 350001
2. Department of Outpatient, Zhenjiang Watercraft College of PLA, Zhenjiang 212003, Jiangsu, China;
3. Department of Cardiology, Fuzhou General Hospital, PLA Nanjing Military Area Command, Fuzhou 350001, Fujian, China
心房纤颤(房颤)是引起脑卒中的主要病因。使用抗凝药物能够使脑卒中风险降低大约60%~70%,同时出血的风险大大增加,特别是老年人[1]。口服抗凝药物华法林能够有效降低脑梗死的发生率,但华法林也有许多缺陷,比如出血并发症高、与其他药物合用相互作用、反复抽血复查国际标准化比值(international normalized ratio,INR)使患者依从性下降等[2],导致目前华法林的普及率并不高。新型抗凝药(达比加群酯等)不需要反复化验,但价格昂贵且出血风险仍然存在。目前数据显示,对于CHA2DS2-VASc评分≥2分的房颤患者,环肺静脉隔离术(pulmonary vein isolation,PVI)并不能完全摒弃抗凝药物或其他脑卒中预防方式的使用[3]。
房颤引起脑卒中主要是因为房颤导致左心房血栓形成,而90%以上的非瓣膜性房颤患者能在左心耳(left atrial appendage,LAA)检测到血栓[4]。因此,左心耳封堵术可有效减少房颤患者脑梗死的发生率。与长期口服抗凝药相比,左心耳封堵器能够有效避免出血风险。
国外的左心耳封堵器如WATCHMAN已获得了很好的临床效果[5],但目前尚无国产左心耳封堵器用于临床。第二军医大学长海医院心血管内科与上海普实医疗器械公司合作,自主研制了一种双盘状左心耳封堵器。本研究通过动物实验,评价该新型左心耳封堵器应用的可行性和有效性,为下一步临床研究提供实验依据。
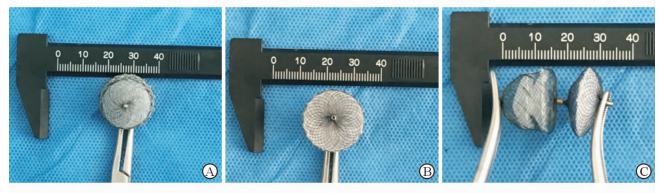
1 材料和方法 1.1 实验动物与材料健康杂种犬12只,体质量12~20 kg,雌雄不限,由上海甲干生物科技有限公司提供[许可证号:SCXK(沪)2010-0028]。房间隔穿刺鞘(Swartz鞘)、0.032英寸(1英寸=2.54 cm)“J”型导引钢丝购自美国St.Jude医疗器械公司,Brockenbrough房间隔穿刺针购自美国美敦力公司,0.032英寸左心房钢丝购自日本TORAY公司,6F猪尾巴造影导管购自美国强生公司。左心耳封堵器输送系统(采用与房间隔封堵器输送系统相类似的输送系统,但头端较Swartz鞘角度大约130°)由上海普实医疗器械公司研制生产。DSA投影成像系统购自乐普(北京)医疗器械股份有限公司,经食管心脏超声诊断仪及探头IE33 S7-2购自荷兰飞利浦公司。自制新型镍钛合金左心耳封堵器(图 1)由第二军医大学长海医院心血管内科与上海普实医疗器械公司研制生产。
|
图 1 封堵器正面观(A,B)和侧面观(C) Fig 1 The front (A,B) and lateral (C) view of occluder |
1.2 麻醉、心电监护及术前准备
实验犬术前先后以硫酸阿托品注射液0.03 mg/kg、盐酸赛拉嗪注射液1.5 mg/kg臀部肌内注射进行麻醉,待麻醉起效后将实验犬固定于“V”字型手术台上,剃净双侧腹股沟及四肢部分体毛,四肢贴电极片接心电监护。术中以1%丙泊酚注射液3~5 mL静推维持麻醉效果。
1.3 穿刺股静脉常规消毒双侧腹股沟皮肤,铺无菌中单,Seldinger穿刺法行股静脉穿刺后置入6 F动脉防漏鞘管。
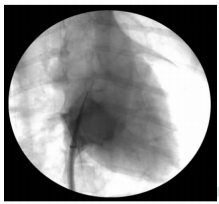
1.4 房间隔穿刺经右侧股静脉鞘置入0.032英寸“J”型导丝,在透视下送至右房,固定导丝并退出股静脉鞘管;将穿刺点充分扩皮后,沿导丝送入Swartz鞘,直至鞘管头端距导丝约5 cm。在透视下旋转穿刺鞘管,直至鞘管长轴显影充分伸展,回撤导丝重新出鞘管头端,此时可将导丝顺利送入上腔静脉。术者右手固定导丝,左手推送鞘管至上腔静脉,直至距导丝头端4~5 cm,撤出导丝,回抽内鞘充分排气后以稀释肝素水冲洗Swartz鞘。将Brockenbrough房间隔穿刺针头端加大弯曲塑形后沿Swartz鞘送入,直至穿刺针头端距鞘管头端约1~2 cm。在后前位透视下将穿刺针尾端指向12点方向,缓慢回撤Swartz鞘及穿刺针,同时注意观察鞘管随心脏跳动情况;第一次出现跳动表明Swartz鞘已靠近主动脉根部附近,继续缓慢回撤鞘管,当再一次出现跳动时,鞘管头端已在卵圆窝附近(大致相当于心影的中下1/3交界处),此时取右前斜30°透视,可观察到鞘管头端近乎成一直线。术者适当前送Swartz鞘管使其轻抵房间隔,左手固定鞘管,右手旋转穿刺针指向3点钟方向出针,使针尾完全抵住Swartz鞘尾端,此时可感觉到穿过房间隔的突破感。用5 mL一次性注射器抽取造影剂后轻轻回抽可见血液回流,透视下推注造影剂少许,可见造影剂迅速在左房弥散,提示穿刺成功(图 2)。
|
图 2 房间隔穿刺成功后可见造影剂迅速在左房弥散 Fig 2 Contrast agent quickly dispersed in the left atrium after successful puncture |
1.5 左心耳造影及测量
穿刺成功后固定穿刺针尾端,推送Swartz鞘管直至鞘管头端超出穿刺针头端约2 mm,固定Swartz鞘管,缓慢退出穿刺针。经鞘管送入0.032英寸左房钢丝至左房内,确认钢丝在左房内盘曲2~3圈,此时术者右手同时固定左房钢丝及扩张鞘,左手推送外鞘至左房内中央。撤出扩张鞘及左房钢丝,经外鞘造影确认其在左房内且再次确认无心包积液。
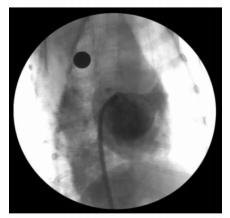
将左房钢丝经房间隔外鞘送入左房内,确保左房钢丝盘曲2~3圈,继续前送房间隔外鞘至接近左心耳开口处。撤出左房钢丝,以钢球(直径14 mm)作为测量对照,分别于左前斜30°、右前斜30°+头、足10°~20°行左心房造影,以能使左心耳颈部清晰显示体位为准。测量左心耳颈部直径(D1),取钢球直径为D2,按公式计算左心耳颈部实际直径(D):D=14×D1/D2(图 3)。再次沿房间隔穿刺外鞘送入左房钢丝,保留左房钢丝,撤出外鞘,沿左房钢丝送入左心耳封堵器输送鞘管。当内鞘穿过房间隔后,同时固定左房钢丝及扩张鞘,推送输送外鞘至左心房内中部,此时保留左房钢丝撤出扩张鞘,沿左房钢丝送入6F猪尾巴导管至左房内,调整猪尾巴导管使其头端进入左心耳内,固定猪尾巴导管,推送房间隔穿刺外鞘至左心耳内并通过造影确认无误。
|
图 3 选取左心耳颈部显影清晰体位测量 Fig 3 Selecting clearly developed position of left atrial appendage neck to measure |
1.6 左心耳封堵器的选取及植入
在左心耳颈部实测值的基础上,选取直径大2 mm的封堵器,将封堵器连接推送杆回收入负载鞘,浓肝素水内反复冲洗负载鞘内封堵器。将负载鞘接输送鞘管,沿输送鞘管推送封堵器至接近输送鞘管头端时,牵拉推送杆回撤封堵器少许观察封堵器与推送杆连接是否确实,继续前送推送杆将封堵器左心耳内盘片释放。
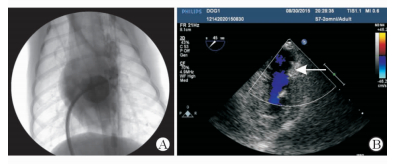
左心耳内盘片释放较理想后,固定推送杆,回撤输送鞘管,使封堵器左房盘片释放,此时轻轻前送推送杆,使封堵器更好地适应左心耳形态。稍稍用力推拉推送杆,封堵器形态无明显改变后,左心房造影确认无明显残余分流后,逆时针旋转推送杆释放封堵器,封堵器释放后即刻造影及经食管超声提示封堵器位置良好(图 4A、4B)。如造影后封堵器形态不理想或残余分流过多,可考虑回撤推送杆将封堵器回收入输送鞘内,然后按照前述过程重新选取位置释放封堵器。手术完毕,将股静脉穿刺点“8”字缝合后覆盖无菌纱布,压迫穿刺点15~20 min,确认局部无血肿后予绷带缠绕包扎。
|
图 4 封堵器释放后即刻造影(A)及经食管超声检查(B)结果 Fig 4 The immediate angiographical (A) and transesophageal echocardiography examination (B) results after the occluder releasing |
1.7 术后处理
实验犬术后3 d内皮下注射依诺肝素20 mg抗凝,1次/12 h;给予注射用青霉素钠针80万IU抗感染,2次/d,肌内注射3~5 d。此后口服拜阿司匹林50 mg、1次/d,氯吡格雷普通片25 mg、1次/d;3个月后继续单用拜阿司匹林50 mg、1次/d至实验结束。
1.8 术后随访观察围手术期实验犬情况,术后1、3、6个月时分别处死实验犬,常规行肢体导联心电图检查并将术前及术后心电图对比。处死实验犬前行常规房间隔穿刺造影,观察术前、术后封堵器有无明显移位及残余分流。实验犬于术后6个月行经食管超声心动图(transesophageal echocardiog-raphy, TEE)检查观察封堵器有无移位及残余分流情况。处死后实验犬常规行大体标本解剖并取封堵器左房盘片上内皮行病理学检查。
2 结 果 2.1 实验犬围手术期随访情况术中即刻12只实验犬中有11例成功植入封堵器,1例术后封堵器脱落手术失败。11例中2例因术中封堵器大小不合适,回收后更换合适封堵器成功植入。详见表 1。
|
|
表 1 实验犬围手术期随访情况 Tab 1 Perioperative follow-up of experimental dogs |
2.2 心电图监测结果
9只存活实验犬按实验节点处死时常规行肢体导联心电图检查,结果与术前心电图相比无明显改变,无心律失常及ST-T改变缺血表现。
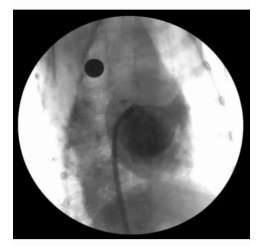
2.3 造影随访术后1、3、6个月时实验犬房间隔穿刺造影结果均显示封堵器无移位,无残余分流,且对冠脉血流无影响(图 5)。
|
图 5 封堵术后6个月时实验犬房间隔穿刺造影图 Fig 5 Atrial septal puncture angiography of experimental canines 6 months after transcatheter closure operation |
2.4 经食管超声心动图
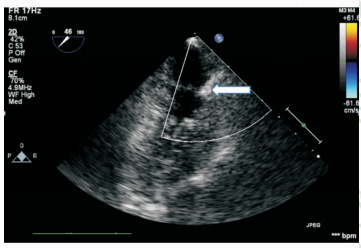
实验犬术后6个月TEE检查示封堵器位置良好,无明显残余分流(图 6)。
|
图 6 封堵术后6个月实验犬经食管超声心动图 Fig 6 Result of transesophageal echocardiography examination for experimental canine 6 months after transcatheter closure operation |
2.5 标本解剖、病理学检查
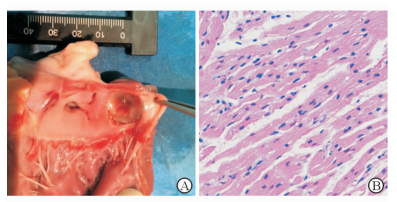
大体观察结果发现肉眼可见封堵器位置良好,表面已完全内皮化,封堵器不影响毗邻的左房室瓣及左上肺静脉(图 7A)。封堵器表面无明显血栓形成,肝、肾、脾大体观察无明显栓塞及梗死灶。病理检查结果可见封堵器表面内皮细胞紧密排列(图 7B)。
|
图 7 封堵术后6个月实验犬心脏大体标本(A)和封堵器左房盘片上内皮组织病理检查(B) Fig 7 Gross specimen of experimental canine heart (A) and the pathologic examination of endothelial tissue on the left atrial disc of the occluder(B) at 6 months after transcatheter closure operation |
3 讨 论
经导管左心耳封堵术适用于抗凝治疗有禁忌、接受了抗凝治疗仍发生栓塞事件或不能耐受抗凝治疗的患者[6]。左心耳封堵术已经被2012欧洲心脏病学会(ESC)和2014美国心脏协会/美国心脏病学会/美国心律学会(ACC/AHA/HRS)列为伴有高危脑卒中且长期口服抗凝治疗有禁忌的房颤患者的Ⅱb类推荐治疗手段[7-8]。
第二军医大学长海医院心血管内科与上海普实医疗器械公司合作,自主研制了新型镍钛合金双盘状左心耳封堵器。该封堵器有以下特点:(1)两个盘片,可以有效减少残余分流的发生率;(2)封堵器外周表面设有两排倒刺,倒刺长度为1~2 mm,可有效预防封堵器脱落;(3)释放后位置不佳可回收。该封堵器为镍钛合金材料,大小不合适时可回收更换,上面的倒刺较软,不会影响封堵器的回收。
目前临床上使用最广泛的Watchman封堵器术后45 d时残余分流率为40.9%,12个月时为32.1%,以少量或微量分流为主[9]。本研究中使用的国产新型镍钛合金双盘状左心耳封堵器于术后6个月TEE检查基本无残余分流,可能与本封堵器采用双盘片设计有一定关系。
房间隔穿刺过程中如发现心肌染色,提示穿刺针误入心肌,此时应回撤穿刺针至鞘管内,调整穿刺高度,稍稍顺时针或逆时针旋转穿刺针后再次出针,如仍不成功,则需重复上述穿刺过程;如发现造影剂误入心包,则需暂停手术,观察15~20 min内心包积液有无增多,如增多需终止实验,在透视下行心包穿刺抽出心包积液。
本实验一般选择比左心耳颈部直径大2 mm的封堵器,这样既能保证封堵器在左心耳腔内不会脱落,亦不会因过度压迫而影响左心耳周围组织结构。封堵器过大可能会压迫左心耳下方的冠状动脉回旋支导致急性心肌梗死发生,同时如果心房内盘片突出可能会影响左上肺静脉及左房室瓣环。封堵器释放后需观察盘片位置和形状,盘片应稍微有压缩改变,理想形态是心耳内盘片稍压缩,左房盘片腰部稍向内凹陷,并要防止植入过深或过浅;释放后同时观察有无心包积液、心律失常及心肌缺血改变,以排除左心耳穿孔及回旋支受压等并发症。本研究中1例出现封堵器脱落,术后解剖证实所选封堵器过小。本实验术后6个月时实验犬解剖病理及电镜检查显示封堵器表面已基本内皮化、无血栓及赘生物,肝、肾、脾亦未见栓塞及梗死灶,证实了封堵器的生物相容性好。
本研究使用国产新型镍钛合金左心耳封堵器完成了经导管左心耳封堵动物实验研究,实验结果提示该封堵器封堵犬左心耳简便易行、封堵效果确切、并发症较少,封堵器左房内盘面内皮化良好,无炎性细胞浸润,提示该封堵器生物相容性良好。本研究的不足之处在于术后随访时间较短,其长期有效性还需要进一步观察。
| [1] | HYLEK E M, EVANS-MOLINA C, SHEA C, HENAULT L E, REGAN S. Major hemorrhage and tolerability of warfarin in the first year of therapy among elderly patients with atrial fibrillation[J]. Circulation , 2007, 115 :2689–2696. DOI:10.1161/CIRCULATIONAHA.106.653048 |
| [2] | GLADER E L, SJÖLANDER M, ERIKSSON M, LUNDBERG M. Persistent use of secondary preventive drugs declines rapidly during the first 2 years after stroke[J]. Stroke , 2010, 41 :397–401. DOI:10.1161/STROKEAHA.109.566950 |
| [3] | OUYANG F, TILZ R, CHUN J, SCHMIDT B, WISSNER E, ZERM T, et al. Long-term results of catheter ablation in paroxysmal atrial fibrillation: lessons from a 5-year follow-up[J]. Circulation , 2010, 122 :2368–2377. DOI:10.1161/CIRCULATIONAHA.110.946806 |
| [4] | BLACKSHEAR J L, ODELL J A. Appendage obliteration to reduce stroke in cardiac surgical patients with atrial fibrillation[J]. Ann Thorac Surg , 1996, 61 :755–759. DOI:10.1016/0003-4975(95)00887-X |
| [5] | HOLMES D R, REDDY V Y, TURI Z G, DOSHI S K, SIEVERT H, BUCHBINDER M, et al. Percutaneous closure of the left atrial appendage versus warfarin therapy for prevention of stroke in patients with atrial fibrillation: a randomised non-inferiority trial[J]. Lancet , 2009, 374 :534–542. DOI:10.1016/S0140-6736(09)61343-X |
| [6] | PROIETTI R, JOZA J, ARENSI A, LEVI M, RUSSO V, TZIKAS A, et al. Novel nonpharmacologic approaches for stroke prevention in atrial fibrillation: results from clinical trials[J]. Med Devices (Auckl) , 2015, 8 :103–114. |
| [7] | JANUARY C T, WANN L S, ALPERT J S, CALKINS H, CIGARROA J E, CLEVELAND J C, et al. 2014 AHA/ACC/HRS guideline for the management of patients with atrial fibrillation: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines and the Heart Rhythm Society[J]. J Am Coll Cardiol , 2014, 64 :e1–e76. DOI:10.1016/j.jacc.2014.03.022 |
| [8] | CAMM A J, LIP G Y, DE CATERINA R, SAVELIEVA I, ATAR D, HOHNLOSER S H, et al. 2012 focused update of the ESC Guidelines for the management of atrial fibrillation: an update of the 2010 ESC Guidelines for the management of atrial fibrillation. Developed with the special contribution of the European Heart Rhythm Association[J]. Eur Heart J , 2012, 33 :2719–2747. DOI:10.1093/eurheartj/ehs253 |
| [9] | VILES-GONZALEZ J F, KAR S, DODUGLAS P, DUKKIUKKIPATI S, FELDMAN T, HORTON R, et al. The clinical impact of incomplete left atrial appendage closure with theWatchman Device in patients with atrial fibrillation: a PROTECT AF(Percutaneous Closure of the Left Atrial Appendage Versus Warfarin Therapyfor Prevention of Stroke in Patients With Atrial Fibrillation) substudy[J]. J Am Coll Cardiol , 2012, 59 :923–929. DOI:10.1016/j.jacc.2011.11.028 |
 2016, Vol. 37
2016, Vol. 37


