2. 第三军医大学附属新桥医院泌尿外科重点实验室, 重庆 400038;
3. 重庆市中山医院ICU, 重庆 400052
2. Key Laboratory of Urology, Xinqiao Hospital, Third Military Medical University, Chongqing 400038, China;
3. Department of ICU, Chongqing Zhongshan Hospital, Chongqing 400052, China
据国际糖尿病联盟资料显示,2014年全球18岁以上成年人中有9%罹患糖尿病,其中高达80%以上在包括我国在内的发展中国家[1]。研究发现,除了持续高浓度的血糖及部分胰岛素抵抗外,糖尿病患者还伴有不同程度血管病变[2]。游离脂肪酸(包括软脂酸和油酸)是脂代谢中最活跃的部分,2型糖尿病患者游离脂肪酸的水平呈现增高[3]。然而,脂肪酸诱发胰岛微血管病变的具体机制目前仍不清楚,如何有效干预糖尿病患者血管病变更是罕见报道。研究发现,胰岛微血管内皮细胞功能的损害是触发2型糖尿病患者血管病变发生的关键病理过程,靶向调节该环节具有遏制血管病变的作用[4]。据此,本研究以小鼠胰岛微血管内皮MS-1细胞为研究对象,探讨茶多酚对脂肪酸诱导的胰岛微血管内皮功能损伤的保护效应及关键信号通路Sonic Hedgehog (Shh)-多聚ADP核糖聚合酶1 [poly (ADP-ribose)polymerase 1, PARP-1]的作用,为防治2型糖尿病血管病变提供实验依据。
1 材料和方法 1.1 材料和试剂小鼠胰岛微血管内皮MS-1细胞,由美国国立细胞库(American Type Culture Collection, ATCC)提供,编号:CRL-2279TM;四甲基偶氮唑盐[3-(4, 5-dimethyl-2-thiazolyl)-2, 5-diphenyl-2-H-tetrazolium bromide, MTT]、软脂酸(palmitate, PA)、油酸(oleate, OA)均购于美国Sigma公司;茶多酚,纯度≥98.0%,购自北京索莱宝科技有限公司,溶解于二甲基亚砜(dimethyl sulphoxide, DMSO);Dulbecco改良Eagle培养基(Dulbecco modified Eagle medium, DMEM)、胰蛋白酶、胎牛血清均由美国Gibco公司生产;AnnexinⅤ FITC/PI细胞凋亡检测试剂盒、总RNA提取试剂盒购自南京凯基生物科技有限公司;一氧化氮(nitric oxide, NO)、总一氧化氮合酶(total nitric oxide synthase, tNOS)、结构型一氧化氮合酶(cNOS)、诱导型一氧化氮合酶(iNOS)、超氧化物歧化酶(superoxide dismutase, SOD)、丙二醛(malondialdehyde, MDA)和还原型谷胱甘肽(glutathione, GSH)检测试剂盒均由南京建成生物工程研究所提供;活性氧(reactive oxygen species, ROS)探针购自北京索莱宝科技有限公司;TaKaRa反转录和荧光定量PCR扩增试剂盒均购于宝生物工程(大连)有限公司;Shh抑制剂环巴胺、PARP-1抑制剂BYK204165、PARP-1抗体、Shh抗体和Shh磷酸化抗体均购自美国Santa Cruz公司;β-actin抗体和辣根过氧化物酶标记二抗均购自北京中杉金桥生物有限公司;其他试剂均为国产分析纯。
1.2 实验分组和处理用含体积分数为10%胎牛血清、100 U/mL青霉素和100 μg/mL链霉素的DMEM培养基,于37℃、5.0% CO2、适当湿度条件下培养,待细胞生长至85%~90%融合时用于实验。实验分组如下:(1)正常对照组和溶剂对照组:DMEM培养液和DMSO处理;(2)脂肪酸组:0.25 mmol/L PA+0.5 mmol/L OA处理;(3)茶多酚组:25 μmol/L茶多酚处理;(4)脂肪酸+茶多酚组:25 μmol/L茶多酚+0.25 mmol/L PA+0.5 mmol/L OA处理;(5)PARP-1抑制剂+脂肪酸组:8 μmol/L BYK204165预处理1 h+0.25 mmol/L PA+0.5 mmol/L OA处理;(6)PARP-1抑制剂+脂肪酸+茶多酚组:8 μmol/L BYK204165预处理1 h+0.25 mmol/L PA+0.5 mmol/L OA+25 μmol/L茶多酚处理;(7)Shh抑制剂+脂肪酸组:2.5 μmol/L环巴胺预处理1 h+0.25 mmol/L PA+0.5 mmol/L OA处理;(8)Shh抑制剂+脂肪酸+茶多酚组:2.5 μmol/L环巴胺预处理1 h+0.25 mmol/L PA+0.5 mmol/L OA+25 μmol/L茶多酚处理;(9)Shh-PARP-1抑制剂+脂肪酸+茶多酚组:8 μmol/L BYK204165、2.5 μmol/L环巴胺预处理1 h+ 0.25 mmol/L PA+0.5 mmol/L OA+25 μmol/L茶多酚处理。
1.3 细胞活力和凋亡水平的测定 1.3.1 MTT比色法检测细胞活力将MS-1细胞以1×104/孔的密度接种于96孔板,37℃、5.0%CO2培养至细胞贴壁,处理结束之后,加入新鲜配制的0.5 mg/L MTT溶液100 μL,37℃避光孵育4 h,吸尽液体,每孔加入100 mol/L DMSO,室温振荡至紫色甲瓒结晶溶解后,应用Model 580型酶标仪(美国Bio-Rad公司)在570 nm波长处测定光密度(D)值,并计算细胞存活率。
1.3.2 流式细胞术检测细胞凋亡将细胞以1×105/孔的密度接种于6孔板,待细胞贴壁后,予以相应的处理;采用Annexin Ⅴ FITC/PI细胞凋亡检测试剂盒于流式细胞仪(美国Beckman公司,型号FC500)上测定细胞的凋亡水平,操作步骤严格依据说明书执行,每个样品检测20 000个细胞,应用WinMID 2.8软件分析并计算各个处理组细胞凋亡率。
1.4 荧光定量PCR法测定PARP-1、Shh基因水平 1.4.1 引物设计与合成PCR引物的合成均由上海Invitrogen公司完成,引物序列参考文献[5-6]。PARP-1上游引物:5′-ATG CTA CCA CGC ACA AC-3′,下游引物5′-CCA ATC GGG TCT CCC T-3′;Shh上游引物5′-AAA GCT GAC CCC TTT AGC CTA-3′,下游引物5′-TTC GCG AGT TTC TTG TGA TCT TCC-3′;GAPDH上游引物5′-GCG ATA CTC ACT CTT CTA CTT TCG A-3′,下游引物5′-TCG TAC CAG GAA ATG AGC TTG AC-3′。
1.4.2 总RNA提取采用TRIzol法提取总RNA,NanoDrop 2000c分光光度计(美国Thermo Fisher公司)测定RNA浓度,取1 μg RNA反转录为cDNA,稀释后置于-80℃冰箱贮存。
1.4.3 实时荧光定量PCR以25 μL体系模板量于TL988型荧光定量PCR仪(美国BioRad公司)行实时荧光定量PCR,反应参数条件:95℃预变性5 min,1个循环;95℃变性10 s、退火(PARP-1 58℃、Shh 60℃)30 s,72℃延伸45 s,持续35个循环;选择SYBR Green Ⅰ/HRM Dye通道,读取Ct值;每个样本每种目的基因设置3个复孔,分别计算各样本各个基因的Ct值,以2-ΔΔCt方法进行定量分析,以GAPDH的Ct值进行校正。
1.5 蛋白质印迹法测定PARP-1、Shh蛋白含量处理结束后,收集细胞、裂解、提取蛋白,每个样本各取50 μg蛋白行SDS-PAGE、转膜、室温封闭2 h,再分别孵育PARP-1一抗(1∶500)、Shh一抗(1∶500)和β-actin(1∶400),4℃孵育过夜,辣根过氧化物酶标记的二抗(1∶6 000)孵育1 h,ECL化学发光后于凝胶成像系统显像,采用Image J软件进行蛋白定量分析,并用β-actin予以校正。
1.6 NO含量及tNOS、iNOS和cNOS活性检测处理结束后收集细胞,冰上裂解,离心取上清液,分别采用NO含量检测试剂盒及tNOS、iNOS和cNOS活性检测试剂盒测定每组细胞样本中上述各项指标的水平,并利用BCA法测定的蛋白浓度予以校正。检测过程均按照说明书要求严格执行,于上海尤尼柯仪器有限公司7200型可见光分光光度计上读取D值。
1.7 ROS、GSH、MDA和SOD水平检测将细胞以1 ×105/孔的密度接种于6孔板中事先放置的盖玻片(24 mm × 24 mm)上,处理结束后,加入终浓度为1.5 μmol/L的DCFH-DA探针,避光37℃孵育1 h,取出载玻片,置于荧光显微镜488~525 nm波长下观察各组处理细胞的绿色荧光强度,采用Image Pro-Plus软件分析和计算平均光密度(average optical density, AOD)。同时,收集同期处理的细胞,充分裂解后取上清,利用GSH、MDA和SOD检测试剂盒分别予以测定,操作过程严格依据说明书要求,D值采用7200型可见光分光光度计读取。
1.8 统计学处理所有实验均独立重复3次,每种处理设置3个以上平行孔。采用SPSS 18.0软件对数据进行整理和分析,符合正态分布且方差齐的资料多组间的比较运用单因素方差分析,组间两两比较利用LSD-t检验;不符合正态性或方差不齐的数据多组间比较利用秩和检验。检验水准(α)为0.05。
2 结果 2.1 茶多酚对脂肪酸诱导的MS-1细胞活力和凋亡的影响及Shh-PARP-1信号通路的调控作用如表 1所示,脂肪酸处理后MS-1的细胞存活率下降至(40.98±3.87)%,低于正常对照组的100%(P < 0.05);但茶多酚+脂肪酸组的存活率则可达(68.28±4.29)%,高于脂肪酸组(P < 0.05);脂肪酸诱导MS-1凋亡水平升高[(13.16±2.19)%],而茶多酚干预则可降低脂肪酸诱发的细胞凋亡水平[(7.02±1.11)%]。采用PARP-1抑制剂BYK204165和Shh抑制剂环巴胺予以预处理,结果发现,BYK204165和环巴胺均可以增强茶多酚的保护作用,2种抑制剂共处理时细胞存活率上升至(96.99±3.72)%,凋亡率下降至(2.19±0.48)%,与对照组比较差异无统计学意义(P>0.05)。
|
|
表 1 茶多酚对脂肪酸诱导的MS-1细胞活力和凋亡的影响及Shh-PARP-1信号通路的调控作用 Tab 1 Effect of tea polyphenols on fatty acid-induced MS-1 cell viability and apoptosis and the regulating role of Shh-PARP-1 pathway |
2.2 茶多酚对脂肪酸诱导的NO含量、NOS活性的影响及Shh-PARP-1信号通路的调控作用
如表 2所示,脂肪酸处理增加了细胞内NO的含量,并增高了tNOS、iNOS和cNOS的活性(P < 0.05);而茶多酚干预则可改善上述指标的变化(P < 0.05);研究结果还显示,PARP-1抑制剂BYK204165和Shh抑制剂环巴胺均可降低各组的NO含量和3种NOS的活性(P < 0.05);而且,Shh-PARP-1信号通路均抑制的情况下,茶多酚对脂肪酸的拮抗效应更为明显,各项指标与对照组比较差异均无统计学意义(P>0.05)。
|
|
表 2 茶多酚对脂肪酸诱导的NO及NOS酶活性增加的影响及Shh-PARP-1信号通路的调控作用 Tab 2 Effect of tea polyphenols on fatty acid-induced NO content and NOS activity and the regulating role of Shh-PARP-1 pathway |
2.3 茶多酚对脂肪酸诱导的氧化应激损伤的影响及Shh-PARP-1信号通路的调控作用
如表 3所示,脂肪酸处理后MS-1细胞的ROS水平急剧升高,脂质过氧化产物MDA含量增加,酶性抗氧化物质SOD的活性和非酶性抗氧化物质GSH的含量均降低(P < 0.05);茶多酚干预处理后,ROS和MDA的水平下降,SOD和GSH改善(P < 0.05);而且,PARP-1抑制剂和Shh抑制剂均可增强茶多酚对脂肪酸诱导的氧化应激的拮抗效应(P < 0.05),两者共同处理条件下该保护作用更为明显,与对照组比较差异无统计学意义(P>0.05)。
|
|
表 3 茶多酚对脂肪酸诱导的氧化应激损伤的影响及Shh-PARP-1信号通路的调控作用 Tab 3 Effect of tea polyphenols on fatty acid-induced oxidative stress and the regulating role of Shh-PARP-1 pathway |
2.4 茶多酚对脂肪酸诱导的PARP-1、Shh和pShh异常表达的影响
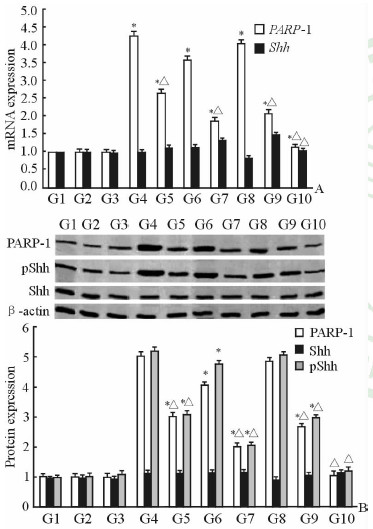
如图 1所示,脂肪酸处理可增加PARP-1的mRNA和蛋白表达量(P < 0.05),且增加pShh的蛋白表达(P < 0.05),但是对Shh mRNA和蛋白的表达无显著影响;茶多酚干预后,PARP-1的mRNA和蛋白表达降低,pShh的蛋白表达降低(P < 0.05);而且在PARP-1和Shh同时抑制条件下,茶多酚的保护效应更为明显。
|
图 1 茶多酚对脂肪酸诱导的PARP-1、Shh和pShh异常表达的影响 Fig 1 Effect of tea polyphenols on fatty acid-induced deregulation of PARP-1, Shh and pShh |
3 讨论
茶多酚是茶叶中多酚类物质的总称,属于儿茶素类化合物,具有抗氧化、抗辐射、抗肿瘤、抗血栓等生物学作用[7]。动物实验发现,适量茶多酚摄入可调控血压和血脂水平,降低动脉粥样硬化等心血管疾病的发生率[8]。体外研究表明,茶多酚具有强效的抗氧化能力,可以抑制胆固醇的氧化,减少脂质过氧化产物在血管壁上的沉积,并能够提高细胞能量和脂肪代谢的能力[9]。茶多酚还能控制糖尿病动物的血糖水平、仿胰岛素、刺激肌糖原合成、降低糖尿病并发症的发病风险[10]。然而,茶多酚是否具有拮抗糖尿病患者血管病变的效应及其具体的作用机制目前仍未见报道。众所周知,血液中游离脂肪酸的含量持续升高可导致肝脏、骨骼肌或脂肪组织等无法再将其氧化生成三酰甘油,造成脂肪酸大量堆积,对正常组织或细胞的生理功能和代谢过程产生损害,产生所谓的“脂毒性”[11]。胰岛微血管内皮细胞主要附于胰岛的微血管内壁,不仅可以向胰岛细胞输送代谢所需的氧或营养物质,还能促进胰岛β细胞的增殖和分泌功能[12]。
本研究结果显示,脂肪酸直接处理MS-1细胞可促使细胞产生大量的ROS,抑制SOD、GSH等抗氧化物质的含量,导致脂质过氧化产物MDA水平急剧升高,进而导致细胞发生凋亡,出现活力水平的降低;同时脂肪酸处理还能直接诱导细胞生成NO,刺激tNOS、iNOS和cNOS等酶的活性及表达水平的上升,继而诱发血管内皮功能的紊乱。茶多酚处理可减轻脂肪酸诱导的血管内皮功能紊乱,减轻氧化应激和凋亡水平,遏制NO的大量生成。这些结果充分表明:(1)脂肪酸是诱发胰岛微血管内皮细胞功能损伤的重要因素;(2)氧化应激和NO生成是导致胰岛微血管内皮功能紊乱的潜在机制;(3)茶多酚对脂肪酸引发的胰岛微血管内皮功能损伤具有保护效应,也表明其拮抗效应的机制可能与氧化应激、NO合成失调和细胞凋亡等紧密相关。
Shh信号通路是Hedgehog(Hh)信号通路中的一种,该通路的活化是通过Shh配体与细胞膜上跨膜受体Patched结合,从而活化Gli转录因子,发挥调控下游靶基因的作用。越来越多的研究显示,Shh信号通路的异常调控与糖尿病并发症(如神经、血管病变等)的发生密切相关[13]。本研究结果也发现,脂肪酸处理后,尽管Shh的mRNA和蛋白表达水平均未发生明显变化,但是pShh的蛋白表达增加,表明Shh信号通路被脂肪酸激活,而且利用环巴胺抑制Shh信号通路还可减轻脂肪酸诱导的胰岛微血管内皮功能的损伤,表明该信号通路在调控胰岛微血管内皮功能中发挥重要作用。PARP-1是一类存在于真核细胞中催化聚ADP核糖化的核酶,过度的PARP-1活化可导致细胞能量耗竭而发生凋亡,而且PARP-1介导的氧化应激反应也是诱发细胞死亡的主要因素之一[5]。有研究发现,Shh-PARP-1存在潜在的交互作用,提示这一信号轴可能共同参与调控糖尿病所致的血管病变[14-15]。本研究采用强效PARP-1抑制剂BYK204165预处理1 h,结果发现:(1)单独PARP-1抑制剂+脂肪酸即可在一定程度上抑制脂肪酸的微血管内皮损伤作用,表明PARP-1可能介导了脂肪酸诱导的微血管氧化应激和凋亡过程,并参与了NO的合成;(2)PARP-1抑制增强了茶多酚的保护效应,一方面提示茶多酚的拮抗机制可能经由PARP-1介导;另一方面说明,两者协同应用可取得更好的保护作用。本研究还发现,Shh-PARP-1同时抑制的条件下,茶多酚的保护效应极大地增大,表明Shh-PARP-1可以共同发挥调控茶多酚拮抗脂毒性的作用,并在该过程中发挥重要的作用。
综上所述,本研究结果显示脂肪酸可直接引起胰岛微血管内皮功能损伤,茶多酚具有拮抗脂肪酸毒性的作用,且抑制Shh-PARP-1信号通路能增强茶多酚的保护效应。该结果表明,应用Shh-PARP-1抑制剂和(或)茶多酚均能够起到拮抗脂毒性的作用,三者联合使用的保护效果更佳。由于本研究纳入的研究对象为体外培养的细胞,此结论是否能够进一步应用于动物和人体仍有待后续实验加以验证。
| [1] | LIU L, LOU Q, GUO X, YUAN L, SHEN L, SUN Z, et al. Management status and its predictive factors in patients with type 2 diabetes in China: a nationwide multicenter study[J]. Diabetes Metab Res Rev , 2015, 31 :811–816. DOI:10.1002/dmrr.2757 |
| [2] | MORGANTINI C, MERIWETHER D, BALDI S, VENTURI E, PINNOLA S, WAGNER A C, et al. HDL lipid composition is profoundly altered in patients with type 2 diabetes and atherosclerotic vascular disease[J]. Nutr Metab Cardiovasc Dis , 2014, 24 :594–599. DOI:10.1016/j.numecd.2013.12.011 |
| [3] | DAIELE G, ELDOR R, MEROVCI A, CLARKE G D, XIONG J, TRIPATHY D, et al. Chronic reduction of plasma free fatty acid improves mitochondrial function and whole-body insulin sensitivity in obese and type 2 diabetic individuals[J]. Diabetes , 2014, 63 :2812–2820. DOI:10.2337/db13-1130 |
| [4] | Look AHEAD Research Group, WING R R, BOLIN P, BRANCATI F L, BRAY G A, CLARK J M, CODAY M, et al. Cardiovascular effects of intensive lifestyle intervention in type 2 diabetes[J]. New Engl J Med , 2013, 369 :145–154. DOI:10.1056/NEJMoa1212914 |
| [5] | SOSNA J, VOIGT S, MATHIEU S, LANGE A, THON L, DAVARNIA P, et al. TNF-induced necroptosis and PARP-1-mediated necrosis represent distinct routes to programmed necrotic cell death[J]. Cell Mol Life Sci , 2014, 71 :331–348. DOI:10.1007/s00018-013-1381-6 |
| [6] | 李韵秋, 匡志鹏, 吴继宁, 孔娜, 杨帆. Hedgehog信号通路分子Shh、Ptch和Smo在化学诱导小鼠肝癌模型过程中的动态表达[J]. 医学研究杂志 , 2014, 43 :65–69. |
| [7] | SENANAYAKE S P J N. Green tea extract: chemistry, antioxidant properties and food applications: a review[J]. J Funct Foods , 2013, 5 :1529–1541. DOI:10.1016/j.jff.2013.08.011 |
| [8] | QUIÑONES M, MIGUEL M, ALEIXANDRE A. Beneficial effects of polyphenols on cardiovascular disease[J]. Pharmacol Res , 2013, 68 :125–131. DOI:10.1016/j.phrs.2012.10.018 |
| [9] | YAMAGATA K, TAGAMI M, YAMORI Y. Dietary polyphenols regulate endothelial function and prevent cardiovascular disease[J]. Nutrition , 2015, 31 :28–37. DOI:10.1016/j.nut.2014.04.011 |
| [10] | BAHADORAN Z, MIRMIRAN P, AZIZI F. Dietary polyphenols as potential nutraceuticals in management of diabetes: a review[J]. J Diabetes Metab Disord , 2013, 12 :143. |
| [11] | LEGRAND-POELS S, ESSER N, L'HOMME L, SCHEEN A, PAQUOT N, PIETTE J. Free fatty acids as modulators of the NLRP3 inflammasome in obesity/type 2 diabetes[J]. Biochem Pharmacol , 2014, 92 :131–141. DOI:10.1016/j.bcp.2014.08.013 |
| [12] | LU C L, WANG Y, YUAN L, LI Y, LI X Y. The angiotensin-converting enzyme 2/angiotensin (1-7)/Mas axis protects the function of pancreatic β cells by improving the function of islet microvascular endothelial cells[J]. Int J Mol Med , 2014, 34 :1293–1300. |
| [13] | PETROVA E, RIOS-ESTEVES J, OUERFELLI O, GLICKMAN J F, RESH M D. Inhibitors of Hedgehog acyltransferase block Sonic Hedgehog signaling[J]. Nat Chem Biol , 2013, 9 :247–249. DOI:10.1038/nchembio.1184 |
| [14] |
刘金苹, 翟乃亮, 刘伟丽, 张璐萍, 丁华. 丹参素对STAT1、PPARγ和HGF在糖尿病小鼠肝脏中表达的影响[J]. 第二军医大学学报 , 2012, 33 :544–548.
LIU J P, ZHAI N L, LIU W L, ZHANG L P, DING H, et al. Effect of Danshensu on expression of STAT1, PPARγ and hepatocyte growth factor in the liver of mice with streptozotocin-induced diabetes[J]. Acad J Sec Mil Med Univ , 2012, 33 :544–548. |
| [15] | LIAN N, JIANG Y, ZHANG F, JIN H, LU C, WU X, et al. Curcumin regulates cell fate and metabolism by inhibiting hedgehog signaling in hepatic stellate cells[J]. Lab Invest , 2015, 95 :790–803. DOI:10.1038/labinvest.2015.59 |
 2016, Vol. 37
2016, Vol. 37


