缺血性脑卒中是导致我国患者残疾和死亡的主要原因之一。脑卒中后的病理生理十分复杂,阐明其病理生理机制、寻找有效治疗药物一直是神经科学研究者努力的方向。Hedgehog(HH)信号参与调控胚胎及出生后大脑的发育[1]。Sonic hedgehog(Shh)是HH信号通路配体之一,近年研究表明Shh信号参与调控卒中后神经功能恢复[2-7],我们的前期研究也表明Shh信号能参与调控体外氧糖剥夺再复氧损伤后神经干细胞的增殖[8-9]。环王巴明(cyclopamine,Cyc)是一种提取自百合类植物的甾类生物碱,为Shh信号通路的特异性抑制剂[7, 10-11],其对脑卒中的影响尚不甚清楚。本研究拟采用大鼠大脑中动脉柱塞再灌注(middle cerebral artery occlusion/reperfusion,MCAO/R)模型,探讨Cyc对大鼠脑缺血再灌注损伤的影响。
1 材料和方法 1.1 实验动物SPF级SD雄性健康成年大鼠,体质量220~250 g,由重庆医科大学实验动物中心提供,动物合格证号:SCXK(渝)2012-0001。
1.2 主要试剂Cyc(纯度≥98%,批号:c4116)和2,3,5-氯化三苯基四氮唑(TTC)购自Sigma公司,TUNEL试剂盒购自Roche公司,免疫组化试剂盒PV-9001、DAB试剂盒购自北京中杉金桥生物有限公司,兔抗caspase-3多克隆抗体购自Bioworld公司,兔抗胶质纤维酸性蛋白(GFAP)多克隆抗体购自Abcam公司,小鼠抗NeuN多克隆抗体购自Millipore公司。其他试剂均为国产分析纯。
1.3 大鼠大脑MCAO/R模型建立及神经功能缺损评分采用Longa改良线栓法[12]建立MCAO/R模型。选用市售进口鱼线,直径0.23~0.26 mm,长4 cm,头端去棱角使其光滑,在距头端2 cm处用黑色记号笔标记,乙醇消毒后备用。大鼠术前禁食12 h,自由饮水,用10%水合氯醛(0.3 mL/100 g)经腹腔注射麻醉后,仰卧位固定,颈部备皮,消毒后,作正中切口,分离并暴露右侧颈总动脉、颈内外动脉,结扎颈总动脉近心端及颈外动脉远心端,在颈内动脉近端备线,远端放置动脉夹,颈总动脉分叉膨大处切口,松开动脉夹,向颈内动脉插入鱼线18~20 mm(视体质量而定),结扎颈总动脉并固定鱼线,外留10 mm线头,缝合皮肤。缺血90 min后,将线栓拉出至结扎端使血流再灌。术后用白炽灯加热维持大鼠体温,待大鼠苏醒后放回鼠笼,自由饮食。按照Longa评分标准评价神经功能缺损:0分为正常,无神经学征象;1分为动物不能完全伸展左前肢;2分为动物左侧肢体瘫痪,行走时向左侧转圈,出现追尾现象;3分为动物行走向左侧跌倒,或动物不能站立或动物打滚;4分为无自发活动,有意识障碍。神经功能缺损评分在1~3分者为模型成功,0分和4分者均剔除。后续实验中予以补充,保证每组大鼠数量不变。
1.4 实验分组及给药将60只大鼠随机分为假手术组(Sham组)、脑缺血/再灌注对照组(Con组)和脑缺血/再灌注Cyc干预组(Cyc组),每组20只。Cyc组于MCAO/R后3 h腹腔注射Cyc(10 mg/kg,溶于1.5 mL无水乙醇),每天1次,连用7 d。Sham组手术分离右侧颈总、颈内外动脉,但不插入线栓。Sham组和Con组于相同时间点给予1.5 mL无水乙醇,每天1次,连用7 d。
1.5 干湿质量法测脑水肿含量各组随机取4只大鼠在术后24 h麻醉后断头取脑,将缺血侧脑组织用滤纸吸去脑表面的水分,称取湿质量,然后置于100℃烤箱内烘至恒质量,称取干质量。脑含水量(%)=(湿质量-干质量)/湿质量×100%。
1.6 TTC法测脑梗死体积各组随机取4只大鼠,术后24 h断头取鲜脑,用锡箔纸包裹置-20℃冰箱速冻30 min,做2 mm厚冠状切片,6片,置于2% TTC染液中,放置于37℃烤箱孵育30 min,期间可翻转组织以便更好着色。白色区域为梗死灶,红色区域为正常组织,数码相机拍照,分离白色和红色区域分别称质量。脑梗死体积(%)=苍白区质量/(苍白区质量+非苍白区质量)×100%[13]。
1.7 H-E染色法观察脑组织病理各组随机取4只大鼠,在术后24 h经10%水合氯醛麻醉后,用4%多聚甲醛灌流取脑。脑组织用4%多聚甲醛固定24 h,冠状切取大脑视交叉部位组织,常规石蜡包埋,制成5 μm厚切片,H-E染色,中性树胶封片,光镜下观察脑组织病理形态学改变。
1.8 TUNEL检测细胞凋亡各组随机取4只大鼠,在术后24 h取脑,冰冻切片。将切片用4%多聚甲醛常温固定20 min,PBS漂洗30 min,细胞通透液0.1% Triton X-100 4℃通透2 min,PBS漂洗2次,每次5 min;加TUNEL反应液(TdT+荧光素标记的dUTP),37℃湿盒中避光孵育60 min,PBS洗3次,每次5 min;加DAPI(1∶400)染核5 min,PBS漂洗3次,每次5 min;加防荧光淬灭封片剂封片。激光共聚焦下观察拍照,所有切片随机选取5个视野(每只大鼠选2张)。
1.9 免疫化学法检测NeuN、caspase-3和GFAP蛋白表达各组随机取4只大鼠,在术后24 h或14 d(caspase-3及NeuN于术后24 h,GFAP于术后14 d)行10%水合氯醛麻醉、4%多聚甲醛灌注取脑。脑组织用4%多聚甲醛固定后行石蜡包埋或冰冻切片。
石蜡切片采用微波修复抗原免疫组化PV二步法染色。于60℃烤箱烤片30 min;二甲苯Ⅰ、Ⅱ各10 min、梯度乙醇脱水各5 min;之后浸入0.01 mol/L枸橼酸盐缓冲液中行微波热修复15 min,PBS洗涤3次,3% H2O2去离子水孵育10 min;PBS洗涤,滴加一抗caspase-3(1∶100)和GFAP(1∶100),置于湿盒中4℃冰箱过夜;PBS洗涤2 min×3次;滴加试剂1(聚合物辅助剂),37℃孵育20 min,PBS洗涤2 min×3次;滴加试剂2(辣根酶标记抗兔IgG聚合物),37℃孵育20 min,PBS洗涤2 min×3次;应用DAB显色;自来水冲洗,复染,脱水,透明,封片。所有切片随机选取5个视野(每只大鼠选2张),在显微镜下观察阳性细胞表达并计数。
冰冻切片行0.4% Triton破膜,冰冻修复液修复30 min,10%山羊血清封闭2 h,滴加一抗NeuN(1∶100)4℃过夜,复温1 h,滴加二抗TRITC(1∶100)孵育90 min,滴加二抗后需注意避光,用DAPI(1∶400)染核5 min,50%甘油封片,激光共聚焦观察拍照,所有切片随机选取5个视野(每只大鼠选2张)计数。
1.10 统计学处理采用SPSS 18.0软件对实验数据进行统计学分析。数据以x±s表示,多组间的比较采用单因素方差分析,检验水准(α)为0.05。
2 结 果 2.1 MCAO/R模型成功情况在60只实验大鼠中,Con组和Cyc组各有3只大鼠神经功能评分为4,被剔除。Con组和Cyc组共有9只在MCAO/R 24 h时死亡,解剖可见颅底大量血凝块,考虑血管破裂导致蛛网膜下隙出血。实验模型成功率90%(54/60),死亡率16.67%(9/54)。后续实验中随机补充,保证每组动物数不变。
2.2 Cyc对MCAO/R损伤后大鼠神经功能的影响Longa评分显示,Sham组大鼠由于没有插入线栓,未出现神经功能缺损症状。术后1 d,Con组和Cyc组大鼠均出现明显的神经功能缺损,Longa评分分别为2.10±0.31和2.85±0.37,其中Cyc组较Con组更为严重(P<0.05);术后14 d,Con组和Cyc组大鼠神经功能缺损有所恢复,但Cyc组(Longa评分为2.50±0.51)仍较Con组(Longa评分为1.25±0.44)严重(P<0.05)。
2.3 Cyc对MCAO/R损伤后大鼠脑梗死体积的影响TTC染色结果(图 1)显示,Sham组无脑梗死;Con组和Cyc组缺血侧出现明显脑梗死,梗死体积分别为(36.41±0.64)%和(44.01±0.53)%,其中Cyc组梗死体积较Con组大(P<0.05)。

|
图 1 Cyc对大鼠大脑中动脉缺血再灌注(MCAO/R)后脑梗死体积的影响 Fig 1 Effect of Cyc on infarct volume after MCAO/R in rats |
2.4 Cyc对MCAO/R损伤后大鼠脑含水量的影响
结果显示,Con组和Cyc组脑含水量分别为(79.48±2.01)%和(87.01±1.44)%,均较Sham组[(74.32±1.15 )%]增加(P<0.05),其中Cyc组较Con组增加更显著(P<0.05)。
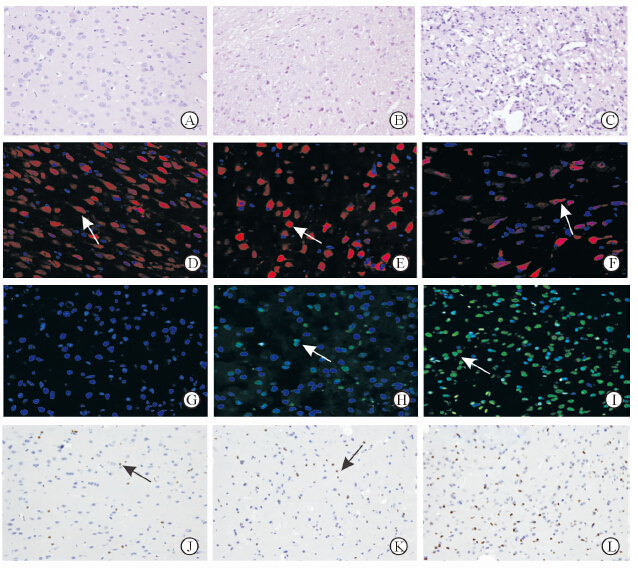
2.5 Cyc对MCAO/R后大鼠脑组织病理改变及NeuN、TUNEL、caspase-3的影响H-E染色结果(图 2A~2C)显示,Sham组大鼠细胞形态、结构正常,间质无水肿;而Con组和Cyc组细胞结构疏松紊乱,可见明显细胞和间质水肿,不同程度的细胞变形、核固缩、细胞坏死等,且Cyc组较Con组损伤更严重。
|
图 2 Cyc对大鼠大脑中动脉缺血再灌注(MCAO/R)后组织病理改变及NeuN、TUNEL、caspase-3的影响 Fig 2 Effects of Cyc on pathology,expressions of NeuN,TUNEL and caspase-3 after MCAO/R in rats |
免疫荧光结果(图 2D~2F)显示,Con组和Cyc组缺血侧缺血半暗带NeuN阳性(红色)细胞数分别为(50.85±3.53)/0.24 mm2和(26.55±2.76)/0.24 mm2,均明显低于Sham组[(95.55±4.25)/0.24 mm2,P<0.05],且Cyc组较Con组更低(P<0.05)。
TUNEL染色结果(图 2G~2I)显示,Sham组偶见TUNEL阳性细胞,阳性细胞数为(2.15±0.86)/0.24 mm2;而缺血24 h时Con组和Cyc组缺血侧缺血半暗带TUNEL阳性细胞增多,分别为(69.85±2.50)/0.24 mm2和(109.68±2.51)/0.24 mm2(P<0.05),且Cyc组较Con组更多(P<0.05)。
Caspase-3免疫组化染色结果(图 2J~2L)显示,Sham组有少量caspase-3阳性细胞,细胞数为(11.13±10.29)/0.24 mm2;而缺血24 h时Con组和Cyc组缺血侧缺血半暗带caspase-3阳性细胞数分别为(77.83±1.62)/0.24 mm2和(103.90±2.37)/0.24 mm2,明显多于Sham组(P<0.05),且Cyc组较Con组更多(P<0.05)。
2.6 Cyc对MCAO/R损伤后大鼠GFAP表达的影响免疫组化结果(图 3)显示,脑缺血后14 d,Con组和Cyc组缺血侧缺血半暗带GFAP阳性细胞数明显多于Sham组(P<0.05),细胞体积更大,突起更长、更粗,GFAP阳性强度更强,且Cyc组表现较Con组更明显(P<0.05)。

|
图 3 Cyc对大鼠大脑中动脉缺血再灌注(MCAO/R)后GFAP表达的影响 Fig 3 Effects of Cyc on expression of GFAP after MCAO/R injury in rats |
3 讨 论
Cyc是一种提取自百合类植物的甾类生物碱,主要通过改变Shh信号通路成分Smo受体蛋白的空间结构而抑制Smo活性,从而抑制Shh信号通路[7]。Shh信号通路与神经系统发育密切相关,激活Shh信号通路能通过抗氧化、抗凋亡、促血管增生等途径减轻脑缺血性损伤,改善神经功能[5-6, 10-11];抑制Shh信号通路能通过加剧氧化途径加重脑缺血性损伤,抑制神经功能的恢复[7, 14-17]。在本研究中,大鼠脑缺血后3 h给予Shh信号通路成分Smo受体特异性抑制剂Cyc干预,能增加脑梗死体积、加重脑水肿、阻碍神经功能恢复,再次证明抑制Shh信号通路能加剧脑缺血性损伤。
脑缺血后,炎症、兴奋毒性、氧化应激等导致神经元的脱失、凋亡。凋亡是脑缺血半暗带细胞死亡的模式之一,为可逆性损伤。脑缺血半暗带凋亡细胞的多少决定脑梗死体积的大小[17-18]。TUNEL法是最常用的检测凋亡的方法,caspase-3是凋亡的另一敏感指标[19]。本研究检测TUNEL阳性细胞和caspase-3蛋白的表达,结果显示脑缺血24 h时,对照组TUNEL阳性细胞和caspase-3蛋白的表达明显增加,同时H-E染色见大量细胞脱失、坏死,免疫荧光也证实大量NeuN阳性细胞脱失,这表明脑缺血导致了神经细胞的脱失和凋亡。在脑缺血后3 h给予Cyc干预,缺血24 h时,TUNEL阳性细胞数、caspase-3蛋白的表达显著高于对照组,H-E染色见细胞脱失、坏死更显著,免疫荧光见NeuN阳性细胞数明显低于对照组。这表明Cyc可加剧缺血性脑损伤后细胞的凋亡、脱失。
脑缺血后神经功能的恢复不仅依赖于神经元脱失、凋亡的程度,也依赖于胶质细胞的变化。近年神经科学研究者逐渐关注到星形胶质细胞的作用不再局限于脑保护及营养支持,其对神经功能的恢复也有重要影响。在脑缺血早期,星形胶质细胞能释放一氧化氮、促进谷氨酸和S-100β释放、上调血管内皮生长因子和基质金属蛋白酶的表达、激活水通道蛋白4,从而加剧神经元的损害,抑制损伤后恢复;在脑缺血晚期,其可异常活化、形成胶质瘢痕、释放炎症因子、抑制轴突再生等,从而阻碍神经功能恢复[20]。因此,寻找有效的药物或其他方法干预星形胶质细胞过度活化及胶质瘢痕形成,有利于神经功能的改善。
GFAP是星形胶质细胞的特异性标志蛋白,广泛用于研究和鉴别星形胶质细胞。据报道在全脑缺血第7天,海马CA1区GFAP阳性细胞数增多,细胞形态增大肿胀,突起增多增粗[21]。本实验在大鼠MCAO/R后14 d也观察到Con组缺血半暗带皮质区GFAP阳性细胞数增加,且细胞体积增大,突起增多增粗,表明脑缺血导致了星形胶质细胞的异常活化和增殖。在MCAO/R后3 h给予Cyc处理,14 d时缺血半暗带皮质区GFAP阳性细胞数高于对照组,且细胞体积较对照组大,突起较对照组多而粗。这表明Cyc增强了星形胶质细胞的异常活化。
综上所述,Cyc可能通过加剧细胞的凋亡、脱失和增强星形胶质细胞的异常活化,从而阻碍神经功能的恢复。我们的前期研究显示Cyc能抑制体外氧糖剥夺后神经干细胞的增殖[8],而Cyc是Shh信号通路成分Smo受体特异性抑制剂,这些从反面证实Shh信号通路在缺血性脑损害后神经功能的恢复中起重要作用。Shh信号通路对缺血性脑损害后神经功能恢复的详细机制有待进一步阐明。
| [1] | HUANG J G, XU L, SHEN C B, LIU S, YANG Q, et al. Effect of primary cilia-mediated Shh signaling on neuronal-like cell differentiation of rat bone marrow stromal cells. Acad J Sec Mil Med Univ[J]. 2013, 34 :934–939 . 黄家贵, 徐兰, 沈长波, 刘舒, 杨琴. 初级纤毛介导的Shh信号对大鼠骨髓基质细胞神经元样细胞分化的影响. 第二军医大学学报[J]. 2013,34 :934–939. |
| [2] | ZHANG L, CHOPP M, MEIER D H, WINTER S, WANG L, SZALAD A, et al. Sonic hedgehog signaling pathway mediates cerebrolysin-improved neurological function after stroke. Stroke[J]. 2013, 44 :1965–1972 . |
| [3] | DING X, LI Y, LIU Z, ZHANG J, CUI Y, CHEN X, et al. The sonic hedgehog pathway mediates brain plasticity and subsequent functional recovery after bone marrow stromal cell treatment of stroke in mice. J Cereb Blood Flow Metab[J]. 2013, 33 :1015–1024 . |
| [4] | JIN Y, RAVIV N, BARNETT A, BAMBAKIDIS N C, FILICHIA E, LUO Y. The shh signaling pathway is upregulated in multiple cell types in cortical ischemia and influences the outcome of stroke in an animal model. PLoS One[J]. 2015, 10 :e0124657. |
| [5] | CHECHNEVA O V, MAYRHOFER F, DAUGHERTY D J, KRISHNAMURTY R G, BANNERMAN P, PLEASURE D E, et al. A smoothened receptor agonist is neuroprotective and promotes regeneration after ischemic brain injury. Cell Death Dis[J]. 2014, 5 :e1481. |
| [6] | HUANG S S, CHENG H, TANG C M, NIEN M W, HUANG Y S, LEE I H, et al. Anti-oxidative, anti-apoptotic, and pro-angiogenic effects mediate functional improvement by sonic hedgehog against focal cerebral ischemia in rats. Exp Neurol[J]. 2013, 247 :680–688 . |
| [7] | JI H, MIAO J, ZHANG X, DU Y, LIU H, LI S, et al. Inhibition of sonic hedgehog signaling aggravates brain damage associated with the down-regulation of Gli1, Ptch1 and SOD1 expression in acute ischemic stroke. Neurosci Lett[J]. 2012, 506 :1–6 . |
| [8] | CHENG W, YU P, WANG L, SHEN C, SONG X, CHEN J, et al. Sonic hedgehog signaling mediates resveratrol to increase proliferation of neural stem cells after oxygen-glucose deprivation/reoxygenation injury in vitro. Cell Physiol Biochem[J]. 2015, 35 :2019–2032 . |
| [9] | 成薇, 沈长波, 王莉, 余萍萍, 杨琴. 白藜芦醇预处理对氧糖剥夺/再复氧损伤大鼠皮质神经干细胞增殖的影响. 中国药理学通报[J]. 2015,31 :113–118. |
| [10] | 牛广义, 白宏英, 曾志磊, 陈苗苗, 刘花艳. 特异激活SHH信号通路对急性脑缺血大鼠NGF、BDNF表达的影响. 中风与神经疾病杂志[J]. 2013,30 :895–897. |
| [11] | 朱美霖, 白宏英, 曾志磊, 张沛琳. 特异性激活SHH 通路对急性脑缺血大鼠血管再生影响. 中风与神经疾病杂志[J]. 2012,29 :1098–1101. |
| [12] | LONGA E Z, Weinstein P R, Carlson S, Cummins R. Reversible middle cerebral artery occlusion without craniectomy in rats. Stroke[J]. 1989, 20 :84–91 . |
| [13] | 任俊伟, 杨琴, 陈娜, 范层层. 白藜芦醇对脑缺血后再灌注后细胞凋亡及Caspase-3表达的影响. 中成药[J]. 2011,33 :570–573. |
| [14] | 张沛琳, 娄季宇, 范波胜, 白宏英, 曾志磊, 朱美霖. 环杷明对急性脑梗死大鼠血管再生的影响. 西安交通大学学报(医学版)[J]. 2013,34 :357–360. |
| [15] | 周逢海, 孙全武, 王养民, 迟强, 赵志强. 环王巴明诱导DU415细胞凋亡的机制研究. 现代肿瘤医学[J]. 2010,18 :1267–1270. |
| [16] | 李锦成, 薛万里, 朱德淼, 陶维. 环王巴明对人乳腺癌细胞系MCF-7的作用. 中国现代医学杂志[J]. 2011,21 :2596–2599. |
| [17] | Mattson M P, Duan W, Pedersen W A, Culmsee C. Neurodegenerative disorders and ischemic brain diseases. Apoptosis[J]. 2001, 6 :69–81 . |
| [18] | BROUGHTON B R, REUTENS D C, SOBEY C G. Apoptotic mechanisms after cerebral ischemia. Stroke[J]. 2009, 40 :e331–e339 . |
| [19] | WANG Y H, SHAO F Y, XIA C L, SUN M M. Changes of caspase-3 activities in rat hippocampal neurons during hypoxia/reoxygenation. Acad J Sec Mil Med Univ[J]. 2002, 23 :1214–1217 . 王宇卉, 邵福源, 夏春林, 孙茂民. 大鼠海马神经元缺氧/复氧后caspase-3活性的变化. 第二军医大学学报[J]. 2002,23 :1214–1217. |
| [20] | ZHAO Y, REMPE D A. Targeting astrocytes for stroke therapy. Neurotherapeutics[J]. 2010, 7 :439–451 . |
| [21] | GIRBOVAN C, PLAMONDON H. Resveratrol downregulates type-1 glutamate transporter expression and microglia activation in the hippocampus following cerebral ischemia reperfusion in rats. Brain Res[J]. 2015, 1608 :203–214 . |
 2016, Vol. 37
2016, Vol. 37


