2. 解放军73071部队, 徐州 221400;
3. 上海体育学院运动科学学院, 上海 200438
2. No. 73071 Troop of PLA, Xuzhou 221400, Jiangsu, China;
3. School of Kinesiology, Shanghai University of Sports, Shanghai 200438, China
晕船是一种常见的航海疾病。研究表明,在恶劣海况条件下,晕船的发生率可达90%[1, 2]。合理使用抗晕药物是防治晕船的重要手段,我们的前期研究证实,组胺H1受体拮抗剂桂利嗪(脑益嗪)与外周多巴胺D2受体拮抗剂多潘立酮联合应用后,受试者Coriolis加速度耐力显著高于抗胆碱药物盐酸苯环壬脂,而与异丙嗪和麻黄素联合用药的效果相当,且不良反应更小[3];但是抗晕药物(东莨菪碱和桂利嗪)与多潘立酮联合应用是否具有实际的抗晕船效果并不明确。抗晕药物的效果与药物代谢速率、用药时机密切相关,且受实际海况等级、航渡时间及个体易感性等的影响。选择药效维持时间长的药物,同时把握对症治疗用药时机,是加强联合用药效果的重要措施。药代动力学研究结果显示,口服东莨菪碱片剂的药效维持时间多为6 h,而东莨菪碱透皮剂则可明显延长作用时间[4]。本研究观察了预防性给予东莨菪碱口服片剂与透皮剂结合多潘立酮的综合应用在不同海况及航程条件下的抗晕效果。
1 材料和方法 1.1 研究对象健康受试者236名,均为男性;年龄17~35岁,平均(21.3±2.8)岁,近期未服用任何抗晕药物和消化系统药物。研究对象本着自愿原则签署知情同意书(志愿者协议书)。本研究获得第二军医大学伦理委员会批准。
1.2 试验条件每批试验受试者均乘坐100 t登陆艇(士兵舱),航速为12节。受试者随机分为3批开展海上航渡试验。试验1:海况1~2级连续海上航渡80海里(n=93);试验2:海况3~4级连续海上航渡80海里(n=73);试验3:海况3~4级连续海上航渡200海里(n=70)。
1.3 试验分组各批受试者均于出海前填写晕动症易感性问卷(motion sickness susceptibly questionnaires,MSSQ)[5],通过计算获得个体晕动症易感指数,随后将每批受试者按晕船敏感性进行匹配分组。综合用药组于航渡前60 min给予0.3 mg东莨菪碱片口服及1.5 mg东莨菪碱透皮剂,航渡过程中首次出现胃部不适感则立即给予5 mg多潘立酮片口服;预防用药组于航渡前60 min给予0.3 mg东莨菪碱片口服及1.5 mg东莨菪碱透皮剂,航渡过程中首次出现胃部不适感则给予100 mg维生素C片口服;安慰剂对照组于航渡前60 min给予100 mg维生素C片口服,航渡过程中首次出现胃部不适感再给予100 mg维生素C片口服。
1.4 晕船严重程度分级受试者于航渡结束前30 min填写Wiker晕船症状量表[6],以7分法对晕船症状进行评分,按严重度将晕船分为3级:轻度晕船(≤2分),中度晕船(3~5分),重度晕船(≥6分)。
1.5 统计学处理采用SPSS 13.0软件进行统计分析,每批试验受试者各组间年龄、身高、体质量及晕动症易感指数采用方差分析进行比较,各组Wiker晕船评分采用单向有序计数资料的非参数检验进行分析,每批各组间轻度、中度及重度晕船发生率采用χ2检验进行比较。检验水准(α)为0.05。
2 结果 2.1 基本情况由表 1可见,在不同航海条件下试航的3批受试者间既往晕动症易感指数差异无统计学意义(P>0.05)。每批受试者各组间年龄、身高、体质量及晕动症易感指数差异均无统计学意义(P>0.05)。
|
|
表 1 不同试验条件下的3批受试者分组后基本情况 |
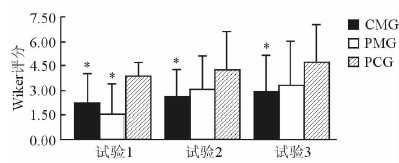
在试验1条件下,综合用药组及预防用药组受试者Wiker评分均低于安慰剂对照组(P < 0.05);而在试验2及试验3条件下,仅综合用药组Wiker评分低于安慰剂对照组(P < 0.05),而预防用药组与安慰剂对照组相比差异无统计学意义(P>0.05),见图 1。
|
图 1 不同试验条件下各组间Wiker评分的比较 试验1: 海况1~2级连续海上航渡80海里; 试验2: 海况3~4级连续海上航渡80海里; 试验3: 海况3~4级连续海上航渡200海里. CMG: 综合用药组; PMG: 预防用药组; PCG: 安慰剂对照组. * P < 0.05与安慰剂对照组比较 |
在试验1条件下,预防用药组轻度晕船发生率高于安慰剂对照组(P < 0.05),综合用药组和预防用药组的中度晕船发生率均低于安慰剂组(P < 0.05);3组重度晕船发生率差异无统计学意义(P>0.05)。在试验2条件下,综合用药组及预防用药组轻度晕船发生率均高于安慰剂对照组(P < 0.05),3组中度晕船发生率差异无统计学意义(P>0.05),综合用药组及预防用药组重度晕船发生率均低于安慰剂对照组(P < 0.05)。在试验3条件下,综合用药组及预防用药组轻度晕船发生率均高于安慰剂对照组(P < 0.01,P < 0.05),3组中度晕船发生率差异无统计学意义(P>0.05),综合用药组重度晕船发生率低于预防用药组及安慰剂对照组(P < 0.05)。详见表 2。
|
|
表 2 不同试验条件下各组轻度、中度和重度晕船发生率 |
本研究发现,在1~2级海况80海里航渡条件下,综合用药组(小剂量东莨菪碱片口服加透皮剂与口服多潘立酮联合应用)和预防用药组(仅给予小剂量东莨菪碱片口服加透皮剂)均可明显缓解晕船反应,并使中度晕船发生率降低;在3~4级海况80海里航渡条件下,仅综合用药组在整体上能有效缓解晕船反应,但综合用药组与预防用药组均可减少重度晕船的发生;在3~4级海况200海里航渡条件下,由于航渡时间超过20 h,仅综合用药组具有抗晕船作用,并减少重度晕船的发生,而预防用药组总体上无明显防治效果。
研究表明,不同类型或剂型的抗晕药物联合使用,可弥补单药或单一剂型的不足和缺陷。乳突区敷贴东莨菪碱透皮剂可延长药物的有效作用时间,且不出现精神及运动障碍[7];但是透皮剂起效较慢,需提前6 h使用,若将透皮剂与小剂量东莨菪碱口服片剂联合使用,既可快速起效,又可使晕船预防效应显著延长,且无明显不良反应[8]。然而,本研究发现,在3~4级海况条件下,预防用药组在联合应用东莨菪碱口服片剂与透皮剂后,仅于80海里航渡条件下(航行时间6 h)具有显著的抗晕效果,却无法有效减少200海里航渡过程中(航行时间20 h)晕船的发生。药代动力学研究发现,东莨菪碱透皮剂的有效血药浓度最长可维持72 h[9];但0.3 mg东莨菪碱口服片剂与1.5 mg贴皮剂联合应用,其有效血药浓度仅能维持22 h,且此时仅有约50%的受试者达到有效浓度,而在用药6 h后则有约90%的受试者达到此浓度[8]。可见,东莨菪碱口服片剂与透皮剂联合使用虽然可减少口服剂量,但无法保证高海况条件下长时间航行(超过20 h)的防晕效果。
多潘立酮可通过阻断外周胃肠道多巴胺受体,加强胃肠蠕动、促进胃排空,从而具有减轻晕船引起的胃不适和抗呕吐作用[10, 11]。本研究结果显示,综合用药组在3~4级海况80海里的航行试验中,重度晕船发生率由安慰剂对照组的33.3%下降至4.0%,与预防给药组(8.3%)相比差异无统计学意义;然而在同等海况条件下连续200海里的航行试验中,综合用药组航渡过程中重度晕船发生率由安慰剂对照组的40.9%下降至4.0%,与预防给药组(21.7%)相比也下降,且多数晕船者(60.0%)仅表现出轻度晕船症状。由于各组重度晕船患者均出现了呕吐,因此,上述结果提示东莨菪碱预防性用药合并多潘立酮联合用药(首次出现轻度胃部不适时使用)可有效抑制呕吐发生;如果仅采用预防给药而忽略对症治疗,则在长期航行过程中,无法在预防药物效能降低时有效控制呕吐等重度晕船症状的出现。曾有文献报道,在晕车后15 min内立刻给予甲氧氯普胺静脉注射,可有效控制呕吐的发生[12];而提前口服止吐药物昂丹司琼,无法有效控制晕船后呕吐的发生[13]。本研究结果提示,在出现晕船症状后立即给予口服多潘立酮可达静脉给药的止吐效果。然而,也有文献报道,口服多潘立酮不能有效抑制航天晕动症引起的空间定向障碍、胃电节律紊乱和晕动症症状[14]。因此,针对不同的晕动症类型,止吐药物使用的效果亦不相同,必须根据临床试验结果合理选用。
本研究结果表明,东莨菪碱透皮剂与小剂量口服制剂联合应用可在一定时间内(6 h)有效预防晕船的发生;而预防药物失效后,如出现胃部不适等轻度晕船症状时,应口服止吐药物多潘立酮,可在较长时间内(20 h)维持抗晕止吐效果,减轻晕船严重程度。但其确切有效作用时间尚需进一步研究。
| [1] | 龚锦涵.航海医学[M].北京:人民军医出版社, 1996:459-505. |
| [2] | Zhang L L, Wang J Q, Qi R R, Pan L L, Li M, Cai Y L. Motion sickness: current knowledge and recent advance[J]. CNS Neurosci Ther, 2016, 22: 15-24. |
| [3] | 王海明, 曹祚焕, 张 麟, 肖建平, 包德海, 郑乐颖, 等.四种抗运动病药物的比较研究[J].第二军医大学学报, 2000, 21:745-748. WANG H M, CAO Z H, ZHANG L, XIAO J P, BAO D H, ZHENG L Y, et al. Comparative study on four anti-motion sickness drugs[J]. Acad J Sec Mil Med Univ, 2000, 21: 745-748. |
| [4] | Spinks A, Wasiak J. Scopolamine (hyoscine) for preventing and treating motion sickness[J]. Cochrane Database Syst Rev, 2011(6): CD002851. |
| [5] | Golding J F. Motion sickness susceptibility questionnaire revised and its relationship to other forms of sickness[J]. Brain Res Bull, 1998, 47: 507-516. |
| [6] | Wiker S F, Kennedy R S, McCauley M E, Pepper R L. Susceptibility to seasickness: influence of hull design and steaming direction[J]. Aviat Space Environ Med, 1979, 50: 1046-1051. |
| [7] | Gleiter C H, Antonin K H, Bieck P R. Transdermally applied scopolamine does not impair psychomotor performance[J]. Psychopharmacology(Berl), 1984, 83: 397-398. |
| [8] | Nachum Z, Shahal B, Shupak A, Spitzer O, Gonen A, Beiran I, et al. Scopolamine bioavailability in combined oral and transdermal delivery[J]. J Pharmacol Exp Ther, 2001, 296: 121-123. |
| [9] | Noy S, Shapira S, Zilbiger A, Ribak J. Transdermal therapeutic system scopolamine (TTSS), dimenhydrinate, and placebo-a comparative study at sea[J]. Aviat Space Environ Med, 1984, 55: 1051-1054. |
| [10] | 翟瑞灵, 李冬梅, 丁学开.多潘立酮治疗晕动病[J].中国新药与临床杂志, 1998, 17:376. |
| [11] | 于桂荣, 包卫芹.吗丁琳治疗晕动病35例报告[J].山东医药, 2002, 42:2. |
| [12] | Rubio S, Weichenthal L, Andrews J. Motion sickness: comparison of metoclopramide and diphenhydramine to placebo[J]. Prehosp Disaster Med, 2011, 26: 305-309. |
| [13] | Carlisle J B, Stevenson C A. Drugs for preventing postoperative nausea and vomiting[J]. Cochrane Database Syst Rev, 2006(3): CD004125. |
| [14] | Kono T, Tokumaru O, Mizumoto C, Tatsuno J, Chen J D. Impaired gastric slow waves induced by spatial disorientation and effect of domperidone[J]. Am J Gastroenterol, 1999, 94: 1224-1229. |
 2016, Vol. 37
2016, Vol. 37


