2. 上海医药工业研究院分析测试中心, 上海 200437;
3. 国家中药制药工程技术研究中心, 上海 201203
2. Instrumental Analysis & Research Center, Shanghai Institute of Pharmaceutical Industry, Shanghai 200437, China;
3. National Engineering Research Center for Traditional Chinese Medicine, Shanghai 201203, China
高乌甲素是从毛茛科植物高乌头(Aconitum sinomontanum Nakai)根中提取的一种二萜类生物碱,常用其氢溴酸盐。高乌甲素作为高乌头镇痛的有效成分,是我国首创的非成瘾性镇痛药。由于其无成瘾性和较强的镇痛效果,国家卫生和计划生育委员会、国际癌痛研究会认定为能够治疗癌症患者中等以上的疼痛,在临床上具有非常良好的应用前景[1, 2, 3]。但高乌甲素给药剂量过大时,容易引起心律失常、心脏中毒、胃肠道刺激、循环系统损害等不良反应[3, 4, 5, 6],且安全范围很窄。临床上应用的各种氢溴酸高乌甲素制剂由于其溶解度低、体内半衰期短,需要长时间频繁给药才能达到止痛效果,患者的顺应性很差。只有维持药物在体内有效的血药浓度,才能提高药物镇痛效果,进而提高患者生活质量,因而开发氢溴酸高乌甲素缓控释片具有重大意义。高源等[7]对氢溴酸高乌甲素亲水性骨架片进行了研究,但骨架缓释片中药物释放易受胃肠道环境的影响,个体差异大。
渗透泵给药系统具有零级释药特征且释药不受胃肠道各种因素的影响,体内外相关性良好,是迄今为止口服控释制剂中最为理想的一种。双层渗透泵控释片,又称推挽式渗透泵片,由含药层、助推层和半透膜组成。在水相中外界水分经过半透膜进入助推层和含药层后,含药层水化形成含药混悬液;而助推层中高分子吸水膨胀,从而推动含药混悬液经释药小孔释放出来。双层渗透泵控释片是难溶性药物实现恒速、长效较为理想的一种新剂型。采用包合技术、固体分散体技术等将难溶性药物制备成单层渗透泵片,虽制备工艺相对简单,易于实现工业化生产,但药物累积释放度不高[8, 9],且在释药过程中很难控制恒速释药。而采用双层渗透泵控释片给药系统借其助推动层的作用,能更好地控制难溶性药物释放,使其更接近恒速并完全释放[10]。由于高乌甲素在胃及各肠段均有吸收,适合制备成缓释制剂[11]。本研究以难溶性药物氢溴酸高乌甲素为模型药,通过优化实验处方制备成零级速率释药特征的氢溴酸高乌甲素双层渗透泵控释片,以期为临床提供更有效的氢溴酸高乌甲素新剂型。
1 仪器和试药 1.1 仪器UV-2401 PC型紫外分光光度仪(日本岛津);TDP型单冲压片机(上海第一制药机械厂);BY300A型小型包衣锅(上海黄海药检仪器厂);ZRS-8型智能溶出试验仪(天津大学无线电厂);BDY-100B型恒温摇床(上海百典仪器有限公司);BP 210D型电子天平(赛多利斯科学仪器有限公司);HWS-12型智能水浴锅(上海一恒科技有限公司);DZF型真空干燥箱(北京中科环试仪器有限公司)。
1.2 试药氢溴酸高乌甲素原料(陕西大河药业有限责任公司,批号:20080201,纯度96.83%);氢溴酸高乌甲素标准品(中国食品药品检定研究院,批号:100289-200902);氯化钠(NaCl,分析纯,天津博迪化工有限公司);PEG 4000(国药集团化学试剂有限公司);聚氧乙烯(PEO,上海卡乐康包衣技术有限公司);硬脂酸镁(辽宁奥达制药有限公司);醋酸纤维素(CA,国药集团化学试剂有限公司);氧化铁红(Fe2O3,上海药用氧化铁颜料厂);十二烷基硫酸钠(SDS,国药集团化学试剂有限公司);氢溴酸高乌甲素片(批号:20120102,规格:5 mg,广西梧州神农药业有限公司);乙腈、甲醇为色谱纯;其余试剂均为分析纯。
2 方法和结果 2.1 含量测定及其方法学研究精密称取氢溴酸高乌甲素9.91 mg,置于100 mL量瓶中,加入0.5%SDS溶解、定容。精密量取0.1、0.5、1.0、2.0、5.0、10.0 mL上述溶液于10 mL量瓶中,并用0.5% SDS溶液稀释、定容至刻度。分别在251 nm波长处测定光密度(D),用氢溴酸高乌甲素浓度(C)与D进行线性回归,得标准曲线方程D=0.012 1C+0.004 27(r=0.999 8),浓度范围0.991~99.1 μg/mL。高、中、低质量浓度的平均方法回收率分别为99.92%、100.17%、100.74%。RSD分别为0.79%、0.82%、0.85%;日内精密度RSD为1.07%、0.84%、1.33%;日间精密度RSD为1.76%、1.69%、1.75%。分别在溶液放置0、2、4、8、12、24 h后测定其D值,RSD分别为0.97%、0.83%、2.04 %,表明样品在24 h内稳定。
2.2 氢溴酸高乌甲素双层渗透泵控释片的制备 2.2.1 片芯的制备含药层:将原辅料分别过80目筛,分别称取处方量的原料药氢溴酸高乌甲素(每片含药20 mg)、PEO N750、30 mg NaCl(过180 μm筛)和0.8%硬脂酸镁等,采用等量递加法混匀。
助推层:将辅料分别过80目筛,分别称取处方量的PEO WSR303、Fe2O3、20 mg NaCl(过180 μm筛)和0.8%硬脂酸镁,采用等量递加法混合均匀。压制片芯时,先将含药层进行预压,再加入助推层压制成双层渗透泵片芯。
2.2.2 包衣称取处方量的CA和PEG 4000,在搅拌条件下加入到包衣溶剂(丙酮∶水=90∶10)中,搅拌12 h,即得包衣液。其中,CA的质量浓度为4%(W/V)。包衣锅转速为45 r/min,包衣温度50℃,包衣液流速为8 mL/min。在40℃下干燥24 h后,于片的含药层(白色) 表面中心位置打0.6 mm的释药孔。
2.3 释放度测定方法取双层渗透泵控释片,以250 mL 0.5%SDS溶液为溶出介质,转速100 r/min,温度(37.0±0.5)℃,分别于1、2、4、6、8、10、12 h后取5 mL,并同时补同温度、同体积的溶出介质。样品经0.45 μm微孔滤膜过滤,取续滤液,在251 nm波长处测定光密度(D)值并计算渗透泵控释片在不同时间的累积释放量。
2.4 氢溴酸高乌甲素双层渗透泵单因素考察在预实验的基础上,最终采用PEO N750作为含药层的助悬剂;PEO WSR303作为助推层的助推剂;PEG 4000作为包衣层的增塑剂,并分别考察不同用量对释药行为的影响。而含药层及助推层中NaCl用量、释药孔孔径等对释药行为影响很小。
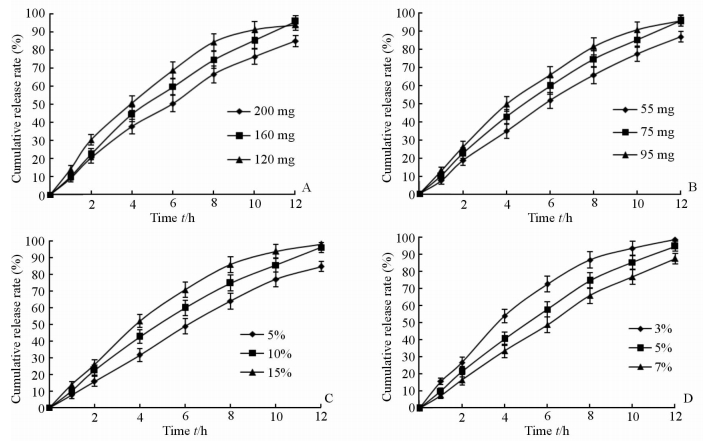
2.4.1 含药层助悬剂用量对释药行为的影响PEO N750不仅助悬效果适中,其遇水后黏度也适中,因此本研究以PEO N750作为含药层的助悬剂。分别考察含药层中PEO N750用量分别为120、160和200 mg时对释药行为的影响,结果见图 1A。助悬剂PEO N750的用量对释药行为有较大影响,当用量较少时(120 mg)释药速率相对较快;而当用量相对较大时(200 mg)释药速率下降;当助悬剂用量为160 mg时释药行为相对理想。
|
图 1 PEO N750用量(A)、PEO WSR303用量(B)、PEG 4000用量(C)和包衣增重(D)对药物释放的影响 Fig 1 Influence of PEO N750 (A), PEO WSR303 (B), and PEG 4000 amounts (C) and coating weight gain (D) on drug release n=3, x±s |
选用PEO WSR303作为助推层的助推剂,并考察其用量为55、75和95 mg时对释药行为的影响,结果见图 1B。随着助推层中助推剂PEO WSR 303用量的增加,释药速率也相应增加;当其用量为75 mg时释药行为相对理想。
2.4.3 包衣液中增塑剂用量对释药行为的影响固定片芯处方不变,分别加入相当于CA质量的5%、10%和15%的PEG 4000,考察不同PEG 4000用量对氢溴酸高乌甲素体外释药行为的影响,结果见图 1C。随着增塑剂用量的增加,释药速率加快,而当PEG 4000用量为10%时释药行为较为理想。
2.4.4 包衣增重对释药行为的影响以包衣增重为指标来衡量包衣膜的厚度。分别考察包衣增加质量为片芯质量的3%、5%、7%时对释药行为的影响,结果见图 1D,随着包衣增重的增加药物释放减慢。
2.5 正交试验优化处方在单因素考察的基础上,选定双层渗透泵控释片含药层中助悬剂PEO N750用量(A)、助推层 PEO WSR303用量(B)、致孔剂PEG 4000用量(C)和包衣增重(D)为影响药物体外释药的主要影响因素,根据以上4个因素,选择3水平进行试验,按L9(34)正交表进行处方优化,见表 1。采用加权评分法评价试验结果[8],渗透泵控释片在2 h 累积释放度以20%为标准,考察有无时滞现象,计算公式为|L1-20%|;6 h的累积释放度以60%为标准,计算公式为|L2-60%|;12 h累积释放度以95%为标准,考察是否释放完全,计算公式为|L3-95%|;以上3个指标权重系数均为1。以相关系数r考察药物是否以零级释放,计算公式为|L4-1|,指标权重系数为3。按下式计算综合得分L,L=|L1-20%|×100×1+|L2-60%|×100×1+|L3-95%|×100×1+|L4-1|×100×3,L越小表示释药效果越理想,结果见表 2、3。
|
|
表 1 正交试验设计 Tab 1 Orthogonal design |
|
|
表 2 正交试验结果 Tab 2 The results of orthogonal test |
|
|
表 3 方差分析结果 Tab 3 Results of variance analysis |
由极差Rj可知,各因素对药物释放影响主次顺序为D>C>A>B,其中,包衣增重差异有统计学意义(P<0.05),各因素的最佳水平组合为A2B2C2D2。因此,氢溴酸高乌甲素双层渗透泵控释片优化后的具体处方为:氢溴酸高乌甲素20 mg、 含药层PEO N750用量为160 mg、助推层PEO WSR303用量为75 mg、增塑剂 PEG 4000用量为10%、包衣增重5%。
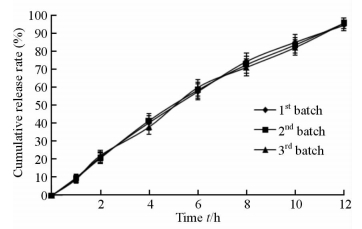
2.6 制备工艺验证按照优化后的处方,制备3批氢溴酸高乌甲素双层渗透泵控释片,测定体外累积释放度,结果见图 2。所制备的双层渗透泵控释片具有良好的零级释放特征,且批间重现性较好。零级释药模型拟合结果为Y=8.087 3t+4.615 9 (r=0.992 1)。
|
图 2 按优化处方制备的氢溴酸高乌甲素双层渗透泵控释片的释放曲线 Fig 2 Drug release profiles of lappaconite hydrobromide push-pull osmotic pump controlled release tablets prepared by the optimized formula n=6, x±s |
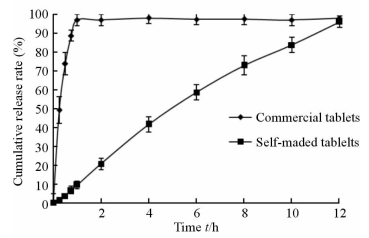
分别取氢溴酸高乌甲素双层渗透泵控释片与上市片,在相同条件下测定两者体外释药曲线,结果见图 3。由于上市片前期释药较快,为了更好地比较自制片与上市片体外释药情况,对2.3项下的取样时间进行了调整,调整为0、0.25、0.5、0.75、1、2、4、6、8、10、12 h,其他条件不变。结果表明,上市片在1 h内释放基本完全,而自制的氢溴酸高乌甲素双层渗透泵控释片呈现缓释特征,12 h累积释放度达到95.02%。
|
图 3 自制氢溴酸高乌甲素双层渗透泵控释片与上市片体外释放曲线 Fig 3 Release profiles of the prepared lappaconite hydrobromide push-pull osmotic pump controlled release tablets and commercial tablets n=6, x±s |
氢溴酸高乌甲素在水中溶解度极差,其氢溴酸盐也是微溶。因此,不能像初级渗透泵那样仅靠渗透压实现零级释放。双层渗透泵控释片由含药层、助推层、半透膜和释药孔组成。本研究制备的双层渗透泵控释片中含药层和助推层均含PEO,但PEO的型号及作用均不同。含药层中的PEO N750(Mr=3×105)起助悬作用,增加药物的混悬效果,使药物在片芯环境中形成均一的溶液或混悬液,以防止难溶性药物沉降析晶,有利于药物释放完全。但相对分子质量或者用量过大时可能会导致包衣膜内压力过高,导致包衣膜的破裂或变形。而助推层中PEO WSR303(Mr=7×106)是系统释药的源动力,当被水化后体积逐渐膨胀,从而推动含药层中药物从释药孔持续释放。
前期研究氢溴酸高乌甲素双层渗透泵控释片时发现,药物释放存在时滞现象,易影响药物药理作用的发挥。为了解决这个问题尝试了很多方法,最终发现在含药层加入水溶性辅料时效果较好。可能是水溶性辅料的加入使含药层水化速率加快,含药层水化形成的混悬液经释药孔释药的时间缩短;另一方面,含药层水化速率的加快也使混悬液浓度降低,减小了释药阻力,最终解决了时滞问题。而助推层中NaCl的主要作用是形成渗透压,随着水相进入助推层,渗透泵内外的渗透压变大,从而增加了水相进入渗透泵片的速率,因而使释药速率增加[10]。
半透膜是双层渗透泵控释片的控释膜,对控制释药速率起非常重要的作用[10, 11, 12, 13, 14]。其中,包衣材料、致孔剂种类及用量、增塑剂种类及包衣增重等是PPOP控释膜设计的重要因素。本研究在以CA作为包衣材料,质量体积分数为4%(W/V)的前提下,主要考察了致孔剂PEG 4000用量和包衣增重。由于PEG 4000是水溶性的,随着用量的增加其在半透膜上形成的孔道越多,使释药速率加快;另一方面也起到保证半透膜完整性的作用。包衣增重用来表示包衣膜厚度,一定的包衣膜厚度可以防止膨胀材料将包衣膜胀破,但厚度过大时会导致释药速率的下降。本实验发现(结果未列出)包衣增重5%以下时包衣膜容易变形甚至破裂,而包衣增重5%时不仅保证包衣膜的完整性,释药速率也相对理想。
本实验经过对含药层中PEO N750用量、助推层中PEO WSR303用量、致孔剂PEG 4000用量以及包衣增重进行单因素考察,再进行正交优化设计使处方控制更加精确。经验证所得优化处方零级释放特征显著,批间重现性良好,初步达到了氢溴酸高乌甲素双层渗透泵控释片的设计要求,该处方是否合理还需结合体内的释药行为来最终确定。
| [1] | Ou S, Zhao Y D, Xiao Z, Wen H Z, Cui J A, Ruan H Z. Effect of lappaconitine on neuropathic pain mediated by P2X3 receptor in rat dorsal root ganglion[J]. Neurochem Int, 2011, 58: 564-573. |
| [2] | 张嘉宝. 高乌甲素抗痛觉过敏机制研究及羟考酮伍用高乌甲素药效学研究初探[D].北京: 北京中医药大学, 2013. |
| [3] | 刘新国, 李居怡, 王 雄, 吴金虎.高乌甲素贴剂的体外释放度与经皮渗透研究[J].中成药, 2012, 34: 1692-1695. |
| [4] | 周远鹏, 刘文化, 曾贵云, 陈迪华, 李慧颖, 宋维良.乌头碱及其类似物的毒性和对心脏收缩功能的影响[J].药学学报, 1984, 19:641-646. |
| [5] | 魏华波, 范艾玲, 秦争平.注射用氢溴酸高乌甲素致耳毒性不良反应2例[J].中国医院药学杂志, 2012, 32:1413-1414. |
| [6] | 姜秀良, 李爱芝, 马宏仲, 梁立升, 于建宏, 王 郜, 等.高乌甲素的腰麻作用和对神经系统毒性的研究[J].临床麻醉学杂志, 2006, 22:367-368. |
| [7] | 高 源, 李凤英, 刘 玲, 李蔚雯, 何 京, 钟海军.氢溴酸高乌甲素亲水凝胶骨架片的制备及体外释放[J].中国现代应用药学, 2013, 30:740-744. |
| [8] | 邓向涛, 郝海军, 韩 茹, 贾幼智.黄芩素包合物单层渗透泵片制备工艺研究[J].第二军医大学学报, 2015, 36:513-517. DENG X T, HAO H J, HAN R, JIA Y Z. Preparation technique of monolithic osmotic pump tablet containing inclusion complex of baicalein[J]. Acad J Sec Mil Med Univ, 2015, 36: 513-517. |
| [9] | 郝海军, 贾幼智, 韩 茹, 张红芹, 王雪萍, 费 浩.坎地沙坦酯固体分散体单层渗透泵片的制备[J].中国新药杂志, 2015, 24:570-575. |
| [10] | Liu X H, Wang S, Chai L Q, Zhang D, Sun Y H, Xu L, et al. A two-step strategy to design high bioavailable controlled-release nimodipine tablets: the push-pull osmotic pump in combination with the micronization/solid dispersion techniques[J]. Int J Pharm, 2014, 461: 529-539. |
| [11] | 许 颖, 倪京满, 马子娇, 王兴刚, 史彦斌, 李 倩.氢溴酸高乌甲素大鼠在体胃肠的吸收动力学研究[J].中国新药杂志, 2010, 19:1995-2000. |
| [12] | 刘玉强, 陈大为, 才 谦.红花黄素磷脂复合物渗透泵胶囊的制备[J].中成药, 2009, 31:57-59. |
| [13] | 吴先闯, 郝海军, 宋晓勇, 张永州, 刘瑜新, 张红芹.槲皮素包合物微孔渗透泵片制备工艺[J].中成药, 2015, 37:1205-1209. |
| [14] | Hao H J, Jia Y Z, Zhang H Q, Han R, Wang X P, Han L M, et al. Preparation of monolithic osmotic tablet of quercetin loaded by solid dispersion[J]. J Chin Pharm Sci, 2015, 24: 383-392. |
 2016, Vol. 37
2016, Vol. 37


