2. 上海医药集团股份有限公司中央研究院, 上海 200123;
3. 第二军医大学药学院药物分析学教研室, 上海 200433
2. Central Research Institute, Shanghai Pharmaceutical (Group) Co., Ltd., Shanghai 200123, China;
3. Department of Pharmaceutical Analysis, School of Pharmacy, Second Military Medical University, Shanghai 200433, China
八宝丹方剂包含牛黄、蛇胆、羚羊角、珍珠、三七、麝香和其他两种尚未明确组分,按照国家保密的制备工艺提取精制而成,具有清热利湿、活血解毒、去黄止痛等功效[1]。方剂中牛黄有化痰开窍、清热解毒之功效,在治疗热病神昏、惊厥抽搐等方面有突出的疗效[2];蛇胆有清热解毒、祛风祛湿的功效,对急性风湿性关节炎、肺热咳嗽等患者的疗效显著[3];羚羊角对高烧惊痢、子痫抽搐等疾病有较好的疗效[4];珍珠主治惊悸失眠、惊风癫瘸[5];三七多作为散瘀止血和消肿定痛的“血分药”[6];麝香是我国的四大名贵药材之一,具有醒脑回苏、活血止痛等作用,临床上主要用于治疗中风偏瘫、神志昏迷等[7]。
八宝丹为国家保密方,其中两味组分未公布,各种化学成分之间的相互作用以及其在人体内的作用机制尚不清楚。文献调研发现,有关八宝丹化学物质的基础研究多侧重于单一组分,未进行化学成分的全面分析,难以体现中药的多成分多靶点特点。超高效液相色谱-电喷雾串联四级杆飞行时间质谱(ultra-high performance liquid chromatography coupled with quadrupole time-of-flight tandem mass spectrometry,UHPLC-Q-TOF/MS)可承受更高的柱压和柱温,分离速率更快、柱效更高,同样条件下UHPLC能分离出的色谱峰多出HPLC的一倍还多[8];Q-TOF/MS既具有飞行时间质谱高分辨的特点,又可以利用四级杆部分提取目标离子进行二级质谱分析[9~10],因而在中药复方复杂体系化合物的快速鉴定中广泛应用。本研究采用UHPLC-Q-TOF/MS技术,首先利用一级质谱给出的精确相对分子质量确定化合物的分子式,再利用二级质谱碎片对鉴别化合物进行二次确认,这为八宝丹药效物质基础的阐明和质量标准的制定提供了依据,同时也为八宝丹的药理机制研究提供参考。
1 仪器和试药 1.1 仪器Agilent 1290 Infinity高效液相色谱系统电喷雾离子源(安捷伦,Palo Alto,CA,USA)串联安捷伦6538四级杆-高分辨飞行时间质谱(UHPLC-Q-TOF/MS),配有MassHunter Acquisition数据采集和MassHunter Qualitative数据分析工作站;METYLER AE240型电子天平(瑞士梅特勒-托利多公司);超纯水净化仪(力康,中国香港);SB3200-T型超声波清洗器(上海科导超声仪器有限公司,50 kHz,120 W)。
1.2 药品与试剂八宝丹(厦门中药厂有限公司生产,上海医药集团股份有限公司中央研究院提供,0.3 g/粒,批号:20150301);缬氨酸,去氧胆酸,鹅去氧胆酸,熊去氧胆酸,石胆酸,牛黄熊去氧胆酸,20(R)-人参皂苷-Rh2,20(R)-人参皂苷-Rg3,20(S)-人参皂苷-Rg3,人参皂苷CK、Re、Rg1,三七皂苷R1,槲皮素14种标准品均购自上海诗丹德生物技术有限公司,纯度>98%。水为超纯水(实验室自制);HPLC级乙腈、HPLC级甲酸 (德国Merck公司);甲醇(色谱纯,德国Merck公司);其他试剂均为分析纯。
2 方法和结果 2.1 色谱条件采用Waters XBridge BEH C18 (2.1 mm ×100 mm,2.5 μm)液相色谱柱,柱温25℃,流速0.8 mL/min,柱后分流比为2∶1;进样量5 μL;流动相为乙腈(A)和0.5%甲酸水(B)。梯度洗脱,0~5 min,5% A;5~25 min,5%~95% A;25~30 min,95% A。
2.2 质谱条件采用电喷雾离子源(ESI)正、负离子模式分析鉴别,雾化气为高纯氮气。具体质谱参数:正离子模式下毛细管电压3 500 V,雾化器压力0.276 MPa,干燥器温度350℃,干燥气流速10 L/min,碎片电压120 eV,参比离子m/z 121.050 873和922.009 798;离子扫描范围m/z 100~1 500;负离子模式下毛细管电压4 000 V,其他参数同正离子模式,参比离子m/z 112.985 587和1 033.988 109。测定样品之前,使用调谐液校准质量轴,以保证质量精度误差小于5×10-6。二级质谱碰撞能量:10~40 eV。
2.3 供试品溶液的制备精密称取八宝丹样品300 mg,置具塞锥形瓶中,加入混合溶剂(甲醇∶二氯甲烷∶水=4∶2∶0.5,V/V)10 mL溶解,密塞,超声提取30 min后,放冷离心,并用0.45 μm微孔滤膜过滤,取续滤液作为供试品溶液,4℃冰箱保存,备用。
2.4 对照品溶液的制备精密称定对照品10 mg,分别置于10 mL量瓶中,加甲醇溶解并定容至刻度,摇匀,即得1 mg/mL的各对照品储备液。分别取各对照品储备液适量,依次稀释、混合后进样分析。
2.5 八宝丹化学成分数据库的构建通过查阅文献并搜索国内外专业数据库,包括中国科学院化学专业数据库、PubMed、ChemSpider,收集了八宝丹中547个化学成分。采用安捷伦“Formula-Database Generator”软件(含各元素精确质量数)分析,根据各成分含碳、氢、氧等的个数计算精确相对分子质量,建立包括化合物名称、分子式、相对分子质量、[M+H]+、[M+Na]+、[M-H]-、[M+HCOO]-、准分子离子峰相对分子质量相应的化学成分数据库。
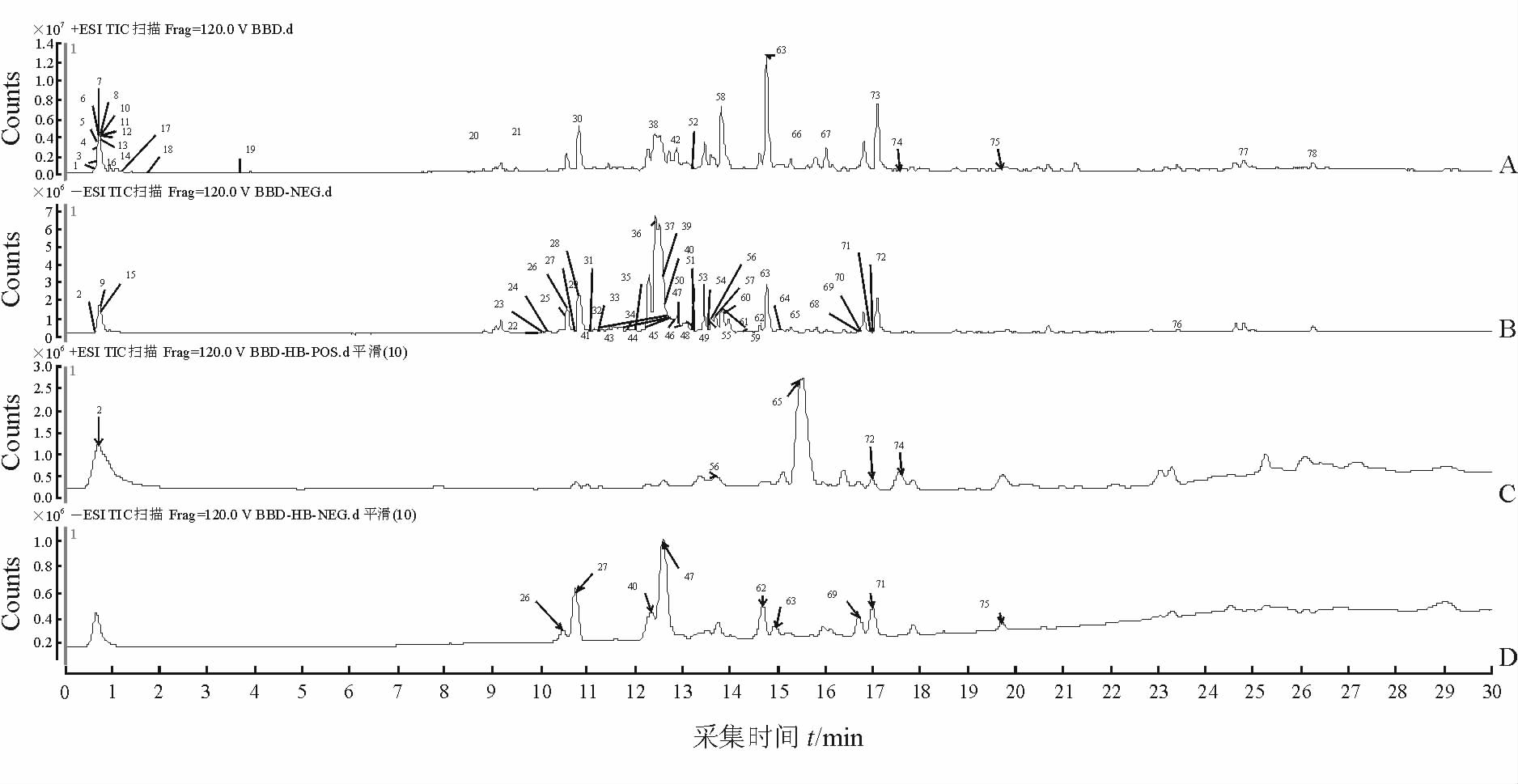
2.6 采用UHPLC-Q-TOF/MS技术对八宝丹中的化学成分进行分析鉴别精密吸取八宝丹样品溶液,按照2.1和2.2项下条件进样分析,得到八宝丹样品溶液的UHPLC-Q-TOF/MS总离子流图(图 1)。
|
图 1 八宝丹样品溶液和混标的正负总离子流图 A: 正离子模式下的样品溶液; B: 负离子模式下的样品溶液; C: 正离子模式下的混标溶液; D: 负离子模式下的混标溶液. 1,2,6~13,51: 珍珠; 3,19~28,30~34,36,38~40,42~50,53,54,58,60,62,63,69,70,72,74,76: 三七; 4,14,41,57,73,77: 麝香; 15~18,29: 羚羊角、珍珠; 35,52,55,59: 牛黄、蛇胆; 61,64,65,68,71,75: 牛黄 |
根据前期预实验结果,得到八宝丹混合对照品共14种,根据14个化合物的精确质荷比及保留时间,对混合对照品溶液总离子流图中的色谱峰进行定性分析。通过调节Q-TOF/MS的二级碎片电压可得各化合物的二级裂解碎片离子,根据各化合物的精确质荷比、保留时间、二级裂解特征性碎片离子对八宝丹中的化学成分进一步确证,结果如表 1所示。从八宝丹样品溶液总离子流图中提取出78个色谱峰的相对分子质量与已知化合物的数据相符,利用TOF/MS准分子离子峰的精确质荷比与数据库中已知化合物进行对比分析,再利用MassHunter Qualitative数据分析软件的计算工具(calculator)对所鉴别化合物进行再验证。得到一个色谱峰的精确相对分子质量数后,计算出该质荷比所代表化合物的可能元素组成,然后将此分子式的理论同位素分布与实验值进行比对来验证推导结果。结合已有文献报道进行交叉验证,同时采用已获得的标准品进行最终确定,共鉴别出八宝丹中72种主要成分,误差值小于5×10-6,另有6个未知化合物。
|
|
表 1 八宝丹提取物中各化学成分的鉴别分析 |
3 讨 论 3.1 色谱质谱条件优化
本实验采用ACQUITY UPLC HSS T3(2.1 mm×100 mm,1.8 μm)和Waters XBridge BEH C18(2.1 mm×100 mm,2.5 μm)色谱柱对八宝丹药材中化合物成分进行分析,发现分离效果最好,尤其是对氨基酸类成分。八宝丹中多种化合物的响应模式不同,经实验发现正离子模式适用于检测杂原子化合物,负离子模式更适用于含多羟基、羧基的化合物,如三七皂苷类、胆酸类。因此采用正、负离子模式进行测定。
3.2 成分鉴别被鉴定出的化合物主要包括皂苷、氨基酸、胆酸及其他类型化合物,其出峰时间主要集中在0~1 min和10~18 min 2个时间段。由于氨基酸类成分极性较强,色谱柱上tR较短,基本在0~2 min以内出峰。其他成分的保留时间较适宜。这几类成分的二级碎片具有特征性规律,其中皂苷类化合物以脱糖基和其他小分子的方式进行裂解,氨基酸类化合物主要裂解氨基侧链和羧基侧链,而胆汁酸类成分一般为脱水分子、烃基侧链或脱羧基的形式。在正离子模式下,色谱峰7的一级质谱给出的离子的分子离子峰实验值为m/z156.076 2,可以推测出该化合物的理论相对分子质量为155,其二级质谱给出的碎片为139.050 2[M+H-NH3]+和93.044 7[M+H-NH3-H2CO2]+,其裂解途径和标准品缬氨酸的裂解途径相同,推测其为氨基酸类化合物;而在负离子模式下,色谱峰28在m/z 99.483 2处形成分子离子峰,在二级质谱中碎片离子m/z 637.428 0、475.378 9在不同能量下出现,很明显为丢失糖苷后形成,其裂解规律符合三萜皂苷的裂解规律,所以推测其为皂苷类成分,特征性的碎片离子m/z 475.378 9提示该化合物属于原人参三醇类的皂苷[11~13],通过与数据库和标准品比对,鉴定为人参皂苷Rf;在负离子模式下,样品溶液中分子离子峰的理论相对分子质量为391.285 4的峰有4个,通过与标准品比对,峰61被鉴定为熊去氧胆酸,峰65被鉴定为去氧胆酸,峰68为猪去氧胆酸,峰71为鹅去氧胆酸[14~15]。
由于UHPLC-Q-TOF/MS无法对同分异构体进行区分,在有对照品的情况下,可以根据对照品的保留时间确定化合物的出峰顺序,如去氧胆酸、熊去氧胆酸、鹅去氧胆酸的鉴别。在没有对照品的情况下,结合ESI/MS(2)技术在碰撞池中对待定的离子进行裂解碰撞,并可进行多级裂解,从而获得丰富的碎片离子信息,同时结合文献对化合物进行解析,从而区分部分同分异构体[16~17],如人参皂苷F2和人参皂苷Rg2。尽管如此,我们仍不能区别全部具有相同分子式的化合物,在接下来的实验中需要进一步的解析和验证。
验证出来的化合物中,三七皂苷类成分可活血祛瘀、通脉活络[18];胆酸类成分可促消化、利胆[19];氨基酸类成分能合成机体内第一营养要素的蛋白质,已鉴别出的缬氨酸、蛋氨酸、苏氨酸等为人体必需氨基酸,能被人体直接利用。精氨酸为人体内半必需氨基酸,现代药理活性表明其能够治疗梗阻性黄疸等疾病[20];组氨酸能够治疗心脏病、贫血、风湿性关节炎等;而麝香中提取物具有β-肾上腺素能增强的性质[21],上述成分确证了八宝丹具有清热利湿、活血解毒、去黄止痛药理活性的物质基础。
本研究采用UHPLC-Q-TOF/MS分析技术对中药复方制剂八宝丹中的化学成分进行快速分析鉴别,共鉴定出72个化学成分,包括34个皂苷类成分、10个胆汁酸类、15个氨基酸和2个大分子环酮类成分,其余包括黄酮和甾醇类等成分。其中皂苷类成分主要来自三七,胆汁酸类主要来自牛黄和蛇胆,氨基酸主要来源于灵芝和羚羊角,大分子环酮类主要来自麝香。所鉴别出的化合物能够很好地表征八宝丹的特征化学物质基础和药理活性基础,证明该制剂组方的合理性和制备工艺的科学性,为进一步的体内深入研究奠定了基础。
| [1] | 陈晓琳. 八宝丹胶囊稳定性研究[J]. 中草药, 2001, 32: 222–223. |
| [2] | 闫焕, 赵文静, 常惟智. 牛黄的药理作用及临床应用研究进展[J]. 中医药信息, 2013, 30: 114–116. |
| [3] | 曾惠芳, 石书江, 陈志维, 武文, 陈剑平, 卢小凤, 等. 蛇胆的本草考证与品质研究[J]. 中医药信息, 2010, 27: 129–132. |
| [4] | 姜清华, 翟延君, 刘艳杰, 张剑. 名贵中药羚羊角研究进展概述[J]. 辽宁中医学院学报, 2005, 7: 29–30. |
| [5] | 莫明月, 林江, 韦明婵. 珍珠粉解毒生肌作用与临床应用研究进展[J]. 广西中医药大学学报, 2015, 18: 77–79. |
| [6] | 占颖, 刘春生, 刘洋洋, 范冰舵, 徐暾海, 刘铜华. 人参和三七活性成分与药理作用对比研究进展[J]. 中国中医药科技, 2014, 21: 711–712. |
| [7] | 尹士敏, 王士贤. 麝香的药理作用及临床研究近况[J]. 天津药学, 2002, 14: 42–44. |
| [8] | 周燕妮, 赵亮, 郑磊, 吕磊. HPLC-TOF-MS对中药石见穿化学成分的快速鉴别[J]. 中国中药杂志, 2013, 38: 4109–4112. |
| [9] | 杨雅欣, 廖尚高, 王正, 李勇军, 梁妍, 郝小燕, 等. 血人参水溶性化学成分的UHPLC-DAD-Q-TOF-MS/MS分析[J]. 中国实验方剂学杂志, 2014, 20: 63–67. |
| [10] | 杨林军, 谢彦云, 李志锋, 李伟, 何明珍, 吴蓓, 等. UPLC/Q-TOF-MS/MS分析中华常春藤中的化学成分[J]. 中草药, 2016, 47: 566–572. |
| [11] | 孙靖辉, 吴巍, 郭迎迎, 秦秋杰, 刘淑莹. 利用ESI-Q-TOF-MS/MS区分人参皂苷Rh2和CK[J]. 质谱学报, 2014, 35: 158–162. |
| [12] | YOSHIKAWA M, MORIKAWA T, KASHIMA Y, NINOMIYA K, MATSUDA H. Structures of new dammarane-type triterpene saponins from the flower buds of Panax notoginseng and hepatoprotective effects of principal ginseng saponins[J]. J Nat Prod, 2003, 66: 922–927. DOI: 10.1021/np030015l |
| [13] | 周思思, 马增春, 梁乾德, 汤响林, 王宇光, 谭洪玲, 等. 基于UPLC-TOF-MS分析人参麦冬配伍后皂苷类成分的变化[J]. 质谱学报, 2013, 34: 88–95. |
| [14] | 刘国文, 刘密新, 吴筑平, 杨成对, 罗国安. 中药复方"清开灵"注射液中胆酸类物质的液相色谱/质谱/质谱分析[J]. 分析化学, 2001, 29: 621–624. |
| [15] | 简龙海, 胡春, 于泓, 王柯, 季申. LC-Q-TOF-MS结合PCC氧化反应快速鉴别熊胆粉中的2个新同分异构体[J]. 中国中药杂志, 2013, 38: 2338–2342. |
| [16] | XIE G, PLUMB R, SU M, XU Z, ZHAO A, QIU M, et al. Ultra-performance LC/TOF MS analysis of medicinal Panax herbs for metabolomic research[J]. J Sep Sci, 2008, 31: 1015–1026. DOI: 10.1002/jssc.v31:6/7 |
| [17] | PATEL P N, KALARIYA P D, SWAMY C V, GANANADHAMU S, SRINIVAS R. Quantitation of acotiamide in rat plasma by UHPLC-Q-TOF-MS: method development, validation and application to pharmacokinetics[J]. Biomed Chromatogr, 2016, 30: 363–368. DOI: 10.1002/bmc.v30.3 |
| [18] | 蔡燕玲, 黎罕文, 杨晓明. 三七的药理研究进展[J]. 陕西中医学院学报, 2001, 24: 57–58. |
| [19] | 邹秦文, 石岩, 魏锋, 林瑞超, 马双成. 牛黄系列药材化学成分比较及其药理作用研究概况[J]. 中国药事, 2014, 28: 646–650. |
| [20] | 宫路路, 林瑞新, 文海荣, 房学东. 精氨酸对恶性梗阻性黄疸患者肿瘤坏死因子-α和可溶性白细胞介素2受体的影响[J]. 肝胆外科杂志, 2007, 15: 297–299. |
| [21] | 胡秉龙, 杨玉珍, 胡素勤, 朱丽. 麝香研究新进展[J]. 中医药信息, 1997, 14: 11–12. |
 2016, Vol. 37
2016, Vol. 37


