随着影像学技术的进步,早期肾癌的检出率日益提高,腹腔镜肾部分切除术也被各类指南推荐为小肾癌的标准手术方式[1]。该手术有两种入路,各有特点:经腰途径具有肿瘤显露快速、动脉分离便捷的优点,但缝合操作空间较小,且缝合角度相对固定,手术难度相对较高;经腹途径具有操作空间大、缝合角度灵活的优势,但需要从静脉后方寻找动脉,费时较长,尤其当动脉存在变异时[2, 3]。我们综合两种入路的优点,创建了腰腹联合三步法腹腔镜肾部分切除术,现将其初步临床应用体会报告如下。
1 资料和方法 1.1 患者资料共32例拟行腹腔镜肾部分切除术的患者进入本研究,包括:2015年9月至11月,接受腰腹联合三步法术式的患者12例(三步法组);2015年7月至9月,接受传统经腹术式患者20例作为对照。入选者需肿瘤最大径线<4 cm,或当肿瘤大于4 cm时,若可行部分切除术,也纳入本研究。所有患者均签署书面知情同意书。记录患者性别、年龄、体质量指数(BMI)、肿瘤直径、动脉分支情况、手术时间、术中出血量等围手术期资料。
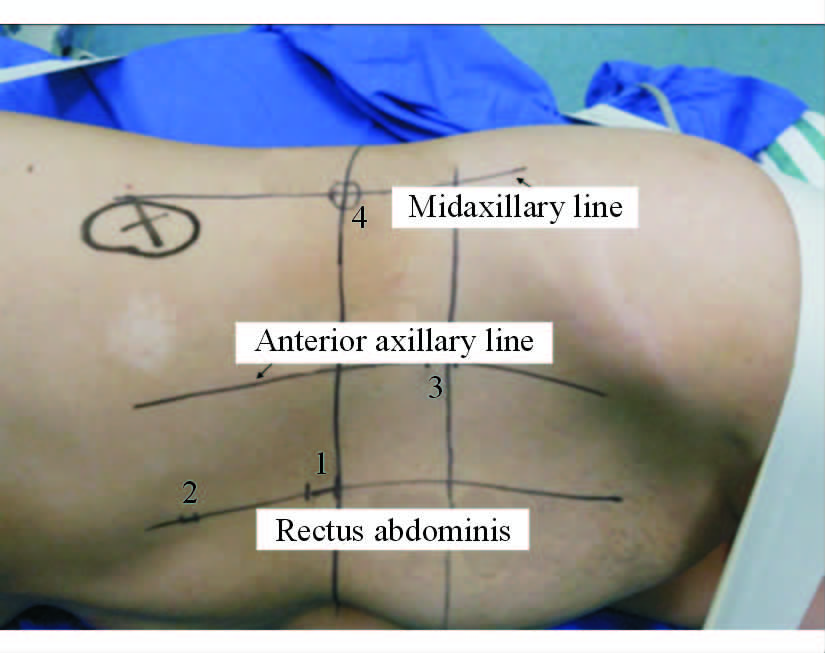
1.2 手术方法 1.2.1 三步法组患者全麻后,取完全侧卧位,躯体平床沿,并固定妥当。采用经腹腔入路,套管三大一小,具体布局见图 1(左侧手术)。右侧手术患者有时需额外在剑突下增加一个5 mm的小套管用来遮挡肝脏。
|
图 1 套管的布局(左侧手术) Fig 1 Trocar placement (left side) Trocar 1 (12 mm): Umbilicus level outside the rectus abdominis; Trocar 2 (5 mm): 6-8 cm on the cephalic side of trocar 1; Trocar 3: Iliac crest on anterior axillary line; Trocar 4: Umbilicus level on the midaxillary line |
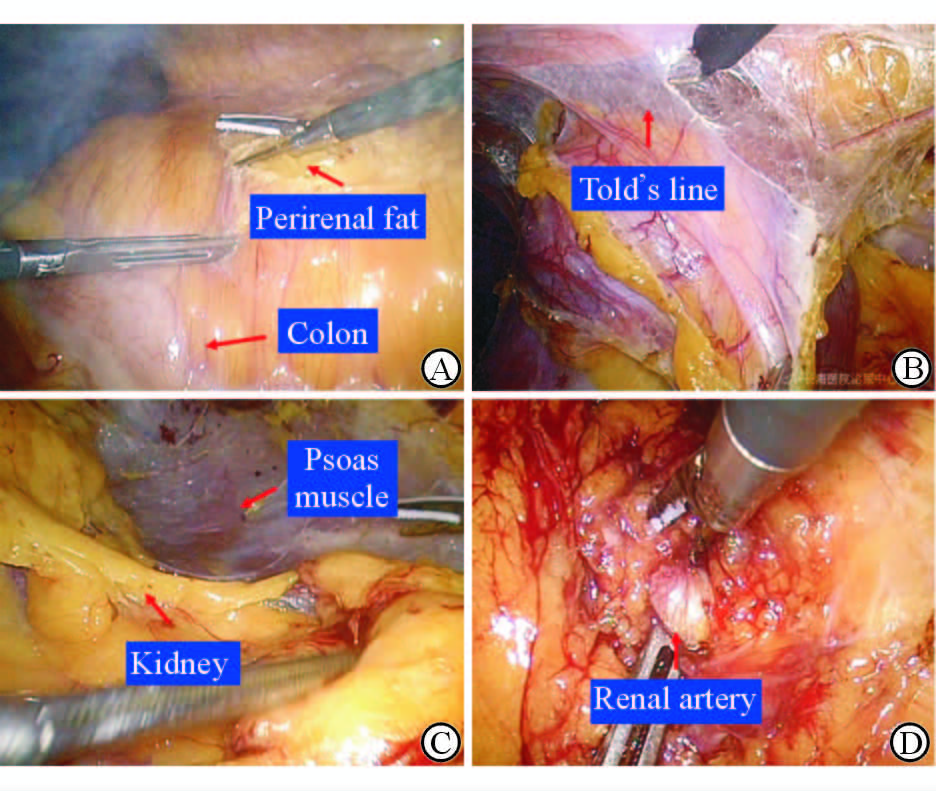
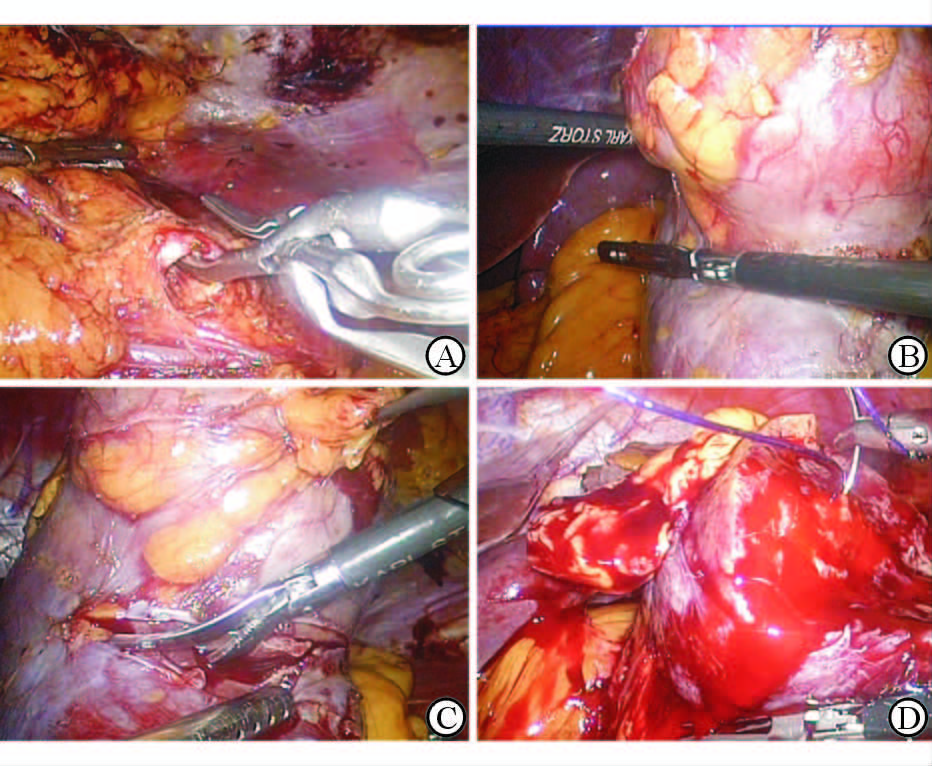
第1步:肾脏的腹侧面分离。建立气腹后,用超声刀沿肾脏中极的腹侧面,直接切开腹膜、肾周筋膜、肾周脂肪,直至肾实质表面,沿肾实质表面游离,充分暴露肿瘤及肿瘤所处的肾脏区域(图 2A)。第2步:肾脏的背侧面分离动脉。电钩沿结肠旁沟Told线切开腹膜至腰大肌,紧贴腰大肌表面将肾脏整体翻向腹侧,直接从背面显露肾动脉(图 2B、2C)。将观察镜移至3号孔,利用1号和4号孔(图 1)分离肾动脉。在肾动脉搏动区,用电钩或超声刀剥开肾动脉鞘,显露肾动脉主干(图 2D)。如存在肾动脉变异,则按CTA图像寻及其余动脉。第3步:完成肾脏肿瘤的切除和重建。用电钩标记肿瘤的切缘。阻断肾动脉后,利用4号孔的辅助器械固定肾脏,并沿标记线剪除肿瘤,用倒刺线双层关闭创面,完成肾部分切除术(图 3)。术毕,固定肾脏于腰大肌表面,并留置负压引流管1根。
|
图 2 显露肿瘤及肾动脉 Fig 2 Exposure of the tumor and renal artery A: Expose the kidney; B: Peritoneum was incised to expose the psoas muscle; C: Identify the renal artery; D: Expose the renal artery |
|
图 3 阻断肾动脉并完成肾部分切除 Fig 3 Clamping renal artery and resecting the tumor A: Clamp of renal artery; B: Tumor was exposed and the edge was marked; C: Resect the tumor alone the mark; D: Reconstruction of the kidney |
患者体位同三步法组,套管三大一小,右侧手术的患者有时需额外在剑突下增加一个5 mm的小套管用来挡肝脏。建立气腹后,打开结肠旁沟Told线、下翻结肠,于髂血管处寻及输尿管,上挑输尿管并游离至腰大肌表面。进一步向头侧游离,直至肾蒂,并于肾静脉后方分离肾动脉。切开肾周筋膜、肾周脂肪,直至肾实质表面,显露肿瘤所在肾脏区域,以电钩标记肿瘤的切缘。阻断肾动脉后,沿标记线剪除肿瘤,用倒刺线双层关闭创面,完成肾部分切除术。
所有手术均由同一术者完成,并记录手术视频,供后续数据统计。
1.3 统计学处理所有数据采用SPSS 16.0软件(SPSS Inc.,美国)进行分析。符合正态分布的数据采用 x± s 表示,组间比较采用独立样本t检验;率的比较采用χ2检验。检验水准(α)为0.05。
2 结果32例手术均顺利完成,无中转开放和术中出血,术后无继发性出血、尿漏等并发症,患者术后卧床(4.0±0.7)d,术后(8.2±0.9)d出院。三步法组和传统组患者围手术期资料详见表 1。两组年龄、性别、BMI、肿瘤直径、动脉数量等指标差异无统计学意义,具有可比性。三步法组手术时间(所有套管安置完毕到肾动脉开放血流,不包含留置引流管和取标本的时间)为(51.8±16.9) min,其中完成第1步的时间为(13.4±5.1)min,完成第2步的时间为(14.2±3.9)min,完成第3步的时间为(24.2±3.3)min,手术时间较传统组缩短(P=0.014)。两组术中出血量差异无统计学意义。
|
|
表 1 三步法组和传统组患者基线资料及围手术期资料比较 Tab 1 Comparison of the baseline data and perioperative data of the 3-step group and traditional group |
保留肾单位手术是治疗T1a期肾肿瘤的金标准[4]。随着微创时代的到来,微创保留肾单位手术(腹腔镜保留肾单位手术和机器人辅助腹腔镜保留肾单位手术)逐渐推广盛行,并逐渐成为治疗T1a期肾肿瘤的首选手术方式,而关于该手术的入路选择,一直存在争议[5]。经腹腔途径的手术入路在国外比较常见,该入路的优势在于操作空间大,解剖标记清晰,尤其适用于达芬奇机器人手术。而国内医生则更多采用经腰的腹膜后入路,其优势在于肾动脉显露便捷,对胃肠的干扰较小[6, 7]。近年来,更是有医生尝试采用经腰入路完成机器人保留肾单位手术,完成了可行性临床验证[8, 9]。
本单位对这两种手术入路都比较熟悉,尤其是大规模开展机器人保留肾单位手术后,更加体会到经腹腔手术途径的优势所在,尤其是对一些位置刁钻的肿瘤,显露尤其满意。但是,从肾脏血管的解剖角度上看,肾动脉绝大多数位于静脉后方,且相对位置变异较大。经腹入路需要从宽大的肾静脉后方寻找隐藏的肾动脉,费时、费力,当静脉分支较多或动脉存在复杂变异时则更为困难,这是经腹入路完成保留肾单位手术的最大弊端。
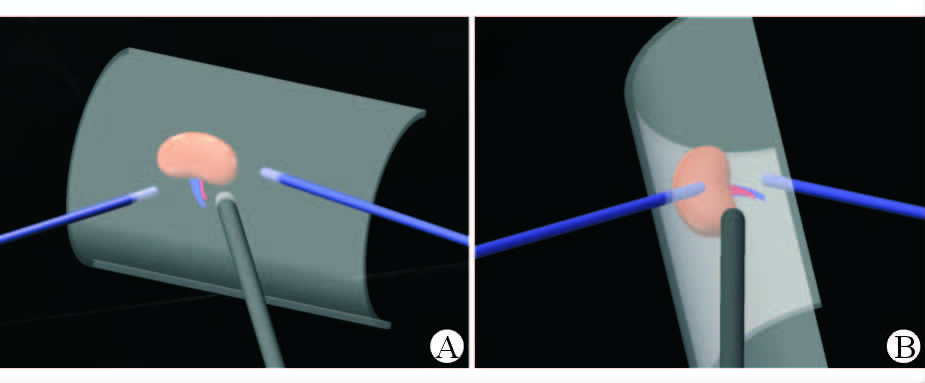
通过这两种手术入路的对比分析,并结合保留肾单位手术的自身特点,我们对经腹腹腔镜肾部分切除术的手术步骤和策略进行重新设计,提出腰腹联合三步法腹腔镜肾部分切除术,将手术视野在经腹和经腰之间灵活切换(图 4),完成初期的临床研究。
|
图 4 手术视野示意图 Fig 4 Demonstration of surgical field A: Transperitoneal field; B: Rretroperitoneal field |
该方法具有以下特点: (1)化繁为简,直奔主题。传统的经腹肾脏手术第1步通常是沿肾周筋膜表面翻开结肠,当寻及肾动脉后,再切开肾周脂肪,游离肾脏并显露肿瘤,该手术步骤是由肾癌根治术演化来。但保留肾单位手术并不要求将肾周脂肪完整切除。因此,我们的第1步则直接从肾实质表面开始,将结肠与肾周脂肪一并翻开,并贴着肾实质,顺势将上下两极分离。这样做的好处是将翻结肠与切开肾周脂肪、游离肾脏、显露肿瘤等多个步骤合为一体,化繁为简,直奔主题,节约时间。而且肾脏的上下两极一旦游离,大大增加了肾脏的活动度,利于后期的创面缝合。 (2)各取所长,合二为一。传统经腹肾脏手术寻找肾动脉的方法通常是在肾下极附近挑起输尿管,贴着腰大肌表面向肾蒂方向游离,最后在肾静脉后方寻找并分离肾动脉。遇到肾动脉位置偏头侧,或多支肾动脉变异时,操作更为复杂,并容易遗漏分支。也有部分医生不分离输尿管,直接在肾静脉后方分离肾动脉,但这样操作虽然节约部分时间,但空间更小,操作难度更大。我们的第2步设计直接从肾脏背侧开始,下翻肾脏,紧贴腰大肌表面分离肾动脉,完全重复经腰途径,动脉显露快,尤其当动脉变异复杂时,优势更为明显。经过我们改良后,可减少分离输尿管的步骤,而且在左侧避开了性腺静脉和腰静脉的严重干扰,操作更为简单、直接。而且,贴腰大肌游离肾动脉,更加靠近肾动脉根部,不容易遗漏分支。最后,分离动脉的过程中,已经将肾脏背侧完全游离,一举两得,减少了后续游离肾脏的工作量。 (3)肾脏游离充分。因为腹腔镜器械无法像手腕一样旋转,持针和缝合的角度都比较固定,所以肾部分切除术中肾脏的游离程度十分重要。我们将肾脏游离的操作步骤融合在肾脏的腹侧显露和肾动脉分离这前两步中,无论腹侧或背侧的肿瘤都能获得良好的显露,再次节约手术时间。通过本研究中三步法组和传统组的比较可以得出,采用腰腹联合三步法行肾部分切除术可有效缩短手术时间(P=0.014)。
此外,我们在术中还发现,当肾脏背侧完全游离后,肾脏随重力下翻,如果要完成腹侧或中线附近的肿瘤切除时,可能需要一助额外用一把器械将肾脏托起并固定。为此,我们后期在游离肾动脉时,不完全离断肾上极与膈肌之间的组织,保证一定的牵连,降低手术难度。
通过初期12例手术的临床研究,我们认为,腰腹联合三步法改良后的腹腔镜肾部分切除术,既保留了经腹途径操作空间大的优点,又结合了经腰途径分离肾动脉便捷的长处,尤其肾动脉出现变异时,优势更加明显,可进行深入的临床对比研究。
| [1] | Ljungberg B, Cowan N C, Hanbury D C, Hora M, Kuczyk M A, Merseburger A S, et al. EAU guidelines on renal cell carcinoma: the 2010 update[J]. Eur Urol,2010,58: 398-406. |
| [2] | Ren T, Liu Y, Zhao X, Ni S, Zhang C, Guo C, et al. Transperitoneal approach versus retroperitoneal approach: a meta-analysis of laparoscopic partial nephrectomy for renal cell carcinoma[J]. PLoS One, 2014, 9:e91978. |
| [3] | Hughes-Hallett A, Patki P, Patel N, Barber N J, Sullivan M, Thilagarajah R. Robot-assisted partial nephrectomy: a comparison of the transperitoneal and retroperitoneal approaches[J]. J Endourol,2013,27: 869-874. |
| [4] | Campbell S C, Novick A C, Belldegrun A, Blute M L, Chow G K, Derweesh I H, et al. Guideline for management of the clinical T1 renal mass[J]. J Urol, 2009, 182:1271-1279. |
| [5] | Fan X, Xu K, Lin T, Liu H, Yin Z, Dong W, et al. Comparison of transperitoneal and retroperitoneal laparoscopic nephrectomy for renal cell carcinoma: a systematic review and meta-analysis[J]. BJU Int, 2013, 111: 611-621. |
| [6] | Harris K T, Ball M W, Gorin M A, Curtiss K M, Pierorazio P M, Allaf M E. Transperitoneal robot-assisted partial nephrectomy: a comparison of posterior and anterior renal masses[J]. J Endourol, 2014, 28: 655-659. |
| [7] | 邵鹏飞,殷长军,孟小鑫,吕 强,李 杰,居小兵,等. 后腹腔镜下肾部分切除术治疗肾肿瘤的疗效评价[J]. 中华泌尿外科杂志,2010,31:658-661. |
| [8] | Hu J C, Treat E, Filson C P, McLaren I, Xiong S, Stepanian S,et al. Technique and outcomes of robot-assisted retroperitoneoscopic partial nephrectomy: a multicenter study[J]. Eur Urol, 2014, 66:542-549. |
| [9] | Kim E H, Larson J A, Potretzke A M, Hulsey N K, Bhayani S B, Figenshau R S. Retroperitoneal robot-assisted partial nephrectomy for posterior renal masses is associated with earlier hospital discharge: a single-institution retrospective comparison[J]. J Endourol, 2015, 29: 1137-1142. |
 2016, Vol. 37
2016, Vol. 37


