环维黄杨星D(cyclovirobuxine D,CB;商品名:黄杨宁)是从中药黄杨中提取的有效单体[1],临床用于治疗气滞血瘀所致的胸痹心痛、脉结代、冠心病、心律失常等[2, 3, 4, 5, 6]。CB对多种心血管疾病具有良好疗效,口服用药安全且长期应用不良反应低,这些为进一步研究和开发CB提供了良好的基础。2010年版《中国药典》中原料及制剂的含量测定分别采用非水滴定法[7]和酸性染料比色法[8],测定的均为总生物碱,专属性差。文献报道的含量测定方法有HPLC-APCI-MS法[9]和LC/MS/MS法[10],以上方法对仪器有不同程度的特殊要求,限制了其应用。本实验建立了采用1-萘基异氰酸酯柱前衍生化HPLC/FLD法测定大鼠血浆中CB含量,取得满意的结果。
CB作为脂溶性生物碱,水溶性差,大大降低了其口服生物利用度。磷脂复合物(phospholipid complex,PC)是药物和磷脂分子通过电荷迁移作用而形成的较为稳定的化合物或络合物。它能够改变药物的溶解性能,增强药物在胃肠道中的吸收,延长药物作用时间,降低药物不良反应,提高药物的生物利用度[11, 12]。并且因其制备简单,成本低廉,近年来在中药PC制剂的研究中取得了较多的成果,被视为传统医药的突破[13, 14]。本课题组将CB制备成PC,研究以CB磷脂复合物(cyclovirobuxine D phospholipid complex,CBPC)为模型药物,口服给药后在大鼠体内的动力学特征,为新药剂型设计提供一定的理论基础和方法。
1 材料 1.1 仪器Agilent 1260高效液相色谱仪,FLD荧光检测器(美国安捷伦科技有限公司);Hypersil ODS色谱柱(大连依利特分析仪器有限公司);TGL-16G高速台式离心机(上海安亭科学仪器厂);分析电子天平(AB204-E,瑞士Mettler Toledo公司);DF-101S集热式恒温加热磁力搅拌器(巩义市予华仪器有限公司);旋涡混合器(QL-901,海门其林贝尔仪器公司);RE-52AA型旋转蒸发仪(上海亚荣生化仪器厂);Milli-Q Biocel A-10超纯水制备系统(美国Millipore公司)。
1.2 药品与试剂CB原料药(纯度>99%,武汉富驰生物科技有限公司);Lipoid S75(PC,德国Lucas Meyer公司);1-萘基异氰酸酯(美国Sigma公司);甲醇(色谱纯,美国天地有限公司);超纯水。
2 方法和结果 2.1 CBPC的制备 2.1.1 溶剂的筛选称取CB与PC比为1∶1,加入等量的不同反应溶剂中,温度50℃水浴中搅拌3 h,分别考察在甲醇、乙醇、丙酮、乙酸乙酯不同溶剂中的澄明状况。结果表明以乙醇做反应溶剂时,溶解药物的效果最好。
2.1.2 反应温度的筛选称取CB与PC比为1∶1,加入适量的乙醇,分别在温度为40℃、50℃、60℃、70℃的水浴中搅拌3 h,考察反应温度对PC复合率的影响。结果表明反应温度为60℃时复合率最高。
2.1.3 CBPC的制备工艺筛选及评价根据预实验结果,选择对CBPC复合率影响显著的2个因素作为考察指标,即PC与CB的投药分子比(molar ratio,X1)、CB的反应浓度(X2,mg·mL-1),每因素设5个水平(X1:0.50、0.87、1.75、2.63、3;X2:1、1.59、3、4.41、5),并以CBPC复合率(Y)为效应进行星点设计-效应面法优化实验,并对实验结果进行拟合(表 1)。复合率的计算公式如下: Y(%)=(M0-M1)/M0 ×100,式中M0为制备CBPC加入的CB的总量,M1为未与磷脂结合的CB的量。
|
|
表 1 CBPC的星点设计实验安排表 Tab 1 Composition of central composite design of CBPC |
使用Design-expert 8.0.6软件,以评价指标(因变量)分别对各因素(自变量)进行多元线性回归和二项式拟合,以相关系数(r)和置信度(P) 评定模型的优度。得多元线性回归方程为:Y=76.878 59+ 6.138 45X1+1.313 04X2(R2=0.708 1,P=0.000 9);二项式方程为:Y=57.334 60+23.828 29X1+5.687 29X2-1.078 00X1X2-4.130 24X12-0.414 63X22(R2=0.981 8,P=0.000 1)。由以上方程可知,二项式拟合相关系数r和P均优于多元线性回归,故选择二项式拟合模型为最佳模型。
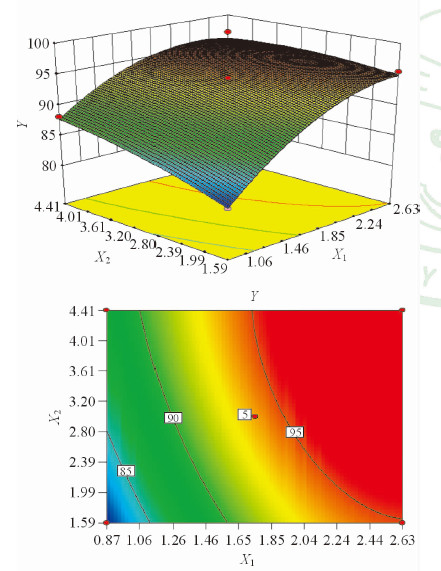
根据上述拟合所得二项式方程,应用Design-expert 8.0.6软件绘制因变量效应指标 Y与2个自变量(X1,X2)的三维效应图和二维等高线图,见图 1。由三维效应图和二维等高线图可知:在一定范围内随着X1的增加,Y先增加后减少;随着X2的增加,Y先增加后减少。由三维效应图和二维等高线图得到CBPC的较优工艺范围是:PC与CB的投药分子比(X1)为0.87~2.63、CB的反应浓度(X2) 为1.59~4.41 mg·mL-1。综合考虑工业可行性及投入产出比,本实验选取的最终优化工艺是PC与CB的投药分子比(X1)为2.40,CB的反应浓度(X2)为3.74 mg·mL-1。
|
图 1 X1、X2与Y的三维效应面图(上)和二维等高线图(下) Fig 1 Predicted 3D response surface graph (upper) and planar contour maps (lower) illustrating the effect of X1, X2 on the concentration of Y |
取CB对照品10 mg,用二氯甲烷溶解后转移至25 mL容量瓶中,定容,得CB储备液,取适量储备液配制成质量浓度为15、30、60、90、150、300、600 ng·mL-1的CB系列对照品溶液,于4 ℃冰箱中保存,备用。
2.2.2 1-萘基异氰酸酯溶液的制备取1-萘基异氰酸酯20 μL置100 mL量瓶中,加二氯甲烷至刻度,摇匀即可(0.2 μL/mL),于4℃冰箱中保存,备用。
2.2.3 血浆样品的处理取血浆150 μL,加入二氯甲烷1 mL,旋涡振荡5 min,2 417 ×g离心10 min,收集下层溶液,加入1-萘基异氰酸酯溶液50 μL,40℃反应60 min,氮气吹干,加150 μL甲醇溶解,9 562 ×g离心10 min,取上清液进样测定。
2.2.4 色谱条件色谱柱:C18柱(250 mm × 4.6 mm,5 μm);流动相:甲醇-水(85∶15,V/V);荧光检查:激发波长231 nm,发射波长385 nm;柱温:25℃;流速:1.0 mL·min-1;进样量:20 μL。
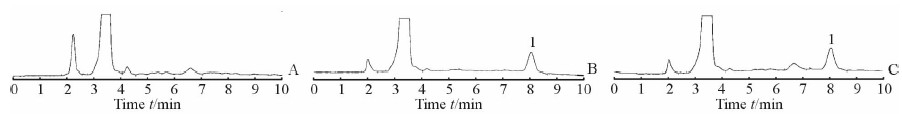
2.3 含量测定方法学考察 2.3.1 专属性空白血浆、空白血浆加对照品的混合物、大鼠灌胃CBPC的血浆样品分别按2.2.3项下方法处理,在2.2.4项色谱条件下进行测定,记录色谱图。结果见图 2,血浆中杂质或内源性物质均不干扰测定,所建立的分析方法专属性强。
|
图 2 血浆样品色谱图 Fig 2 HPLC chromatogram of plasma sample A: Blank rat plasma; B: Mixture of blank rat plasma and standard; C: Plasma sample. 1: Cyclovirobuxine D |
取空白血浆100 μL,加入系列CB对照品溶液50 μL,得到含CB浓度分别为5、10、20、30、50、100、200 ng·mL-1的标准血浆样品。按2.2.3项下方法处理,在2.2.4项色谱条件下测定。以CB峰面积(Y)对浓度(C)进行线性回归,得标准曲线方程为Y=1.326 9C+6.722 9(r2=0.999 4),表明CB血浆质量浓度在5~200 ng/mL范围内具有良好的线性。CB的检测限为1 ng/mL(S/N=3),定量限为5 ng/mL(S/N=10)。
2.3.3 精密度考察取空白血浆100 μL,加入系列CB对照品溶液50 μL,配制成低、中、高3种不同浓度( 5、30、200 ng·mL-1)的标准血浆样品各5份,按2.2.3项下方法处理,在2.2.4项色谱条件下进样分析。连续测定3 d,计算日内、日间精密度。测得低、中、高3种不同浓度的日内精密度RSD分别为6.53%、3.37%、1.54%;日间精密度RSD分别为5.62%、5.60%、1.46%。实验结果表明该法精密度好,符合方法学要求。
2.3.4 提取回收率和方法回收率取空白血浆100 μL,加入CB对照品溶液,分别配制成低、中、高浓度(5、30、200 ng·mL-1)的标准血浆样品各5份,按2.2.3项下方法处理,在2.2.4项色谱条件下进样分析,记录峰面积,计算各浓度的平均峰面积Ar。另以配制相同浓度的对照品溶液直接衍生化后进样,同法操作,计算平均峰面积As。以峰面积之比(Ar/As)计算提取回收率。测得低、中、高3种浓度的标准血浆样品的提取回收率分别为91.77%、95.66%、94.26%。取空白血浆100 μL,加入CB对照品溶液,分别配制成低、中、高浓度(5、30、200 ng·mL-1)的标准血浆样品各5份,按2.2.3项下方法处理,在2.2.4项色谱条件下进样分析,考察相对回收率。测得低、中、高3种浓度的标准血浆样品的回收率分别为97.51%、99.18%、98.67%,以上均符合方法学要求。
2.4 动物给药方案及样品采集雄性SD大鼠[鼠龄:7周,重庆医科大学实验动物中心,动物许可证号:CQLA(渝)2012-1003]体质量200 g左右12只,随机分为2组:第一组口服灌胃给予4 mL的CB(相当于给药量60 mg/kg),第二组口服灌胃给予4 mL的CBPC(相当于给药量60 mg/kg)。给药前禁食12 h,不禁水。在灌胃给药后15 min、30 min、1、2、3、4、5、6、8、12、24、48、72、96、120 h眼底静脉丛取血0.3 mL于肝素浸润过的试管中,604 ×g离心10 min,吸取上层血浆于洁净的EP管中,放入-20℃保存,备用。采用DAS 2.1.1软件对血药浓度-时间数据进行非房室模型拟合,计算各药动学参数。
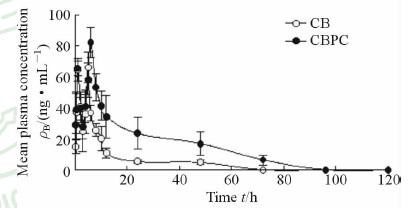
2.5 血药浓度和药动学参数以CB的血药浓度为纵坐标、时间为横坐标作图,得到血药浓度-时间曲线,大鼠灌服CBPC和CB混悬液的平均血药浓度-时间曲线见图 3。药动学数据采用DAS2.1.1软件对所得实验数据进行非房室模型(统计矩)拟合,并用t检验对实验结果进行统计学处理,CBPC和CB主要药动学参数见表 2。由表 2可以看出:(1)将CB制备成CBPC后,其AUC0-t从(619.93±75.67) μg·h·L-1增加到(1 703.81±549.38) μg·h·L-1,提高了2.74倍(P<0.01);最大Cmax从(69.27±8.66) μg·L-1增加到(82.32±9.55) μg·L-1,提高了1.19倍(P<0.01)。表明磷脂起到了表面活性剂对药物在水溶液中的增溶作用,增加了药物的吸收,提高了药物的口服生物利用度;(2)MRT0-t从(13.15±0.88) h增加到(23.80±2.27) h,提高了1.81倍(P<0.01),表明CBPC由于磷脂与脂溶性药物的亲和性延缓了CB从PC向生物膜的扩散,从而在体内表现出了一定的缓释特征。
|
图 3 CBPC和CB的血药浓度-时间曲线 Fig 3 Mean plasma concentration-time profiles of CBPC and CB suspension after oral administration CBPC: Cyclovirobuxine D phospholipid complex; CB: Cyclovirobuxine D. n=5, x±s |
|
|
表 2 SD大鼠口服CBPC和CB混悬液的主要药动学参数 Tab 2 Main pharmacokinetic parameters of SD rats after oral administration of CBPC and CB suspensions |
CB为甾类生物碱,结构中无发色基团和共轭体系,在紫外可见分光200~800 nm范围进行扫描,得到CB在207 nm处有最大吸收峰,但该处末端吸收无法满足体内血药浓度分析的需求。为提高对CB测定的灵敏度,荧光试剂衍生化是一种常用的样品处理方法。本课题组最终采用1-萘基异氰酸酯对CB进行柱前衍生化,并用HPLC/FLD进行含量测定,该方法能够满足CB的体内血药浓度测定要求。
本实验主要考察了将CB制备成CBPC后,经口服灌胃吸收后在SD大鼠体内的药代动力学性质。由药代动力学参数可知,CBPC的AUC0-t、AUC0-∞是CB的2.74倍、2.96倍,生物利用相对于原料药为274.84%,表明CBPC较CB在体内的吸收程度增加,提高了药物的口服生物利用度;同时CBPC的MRT0-t、MRT0-∞、CL分别是CB的1.81倍、2.09倍、0.37倍,说明与CB相比,CBPC在大鼠体内的半衰期延长、体内滞留的时间增加、清除率降低,有利于药物在体内的吸收。
在研究中发现CBPC和CB的体内存在明显双峰现象,分析可能是由于肝肠循环、胃肠道多吸收位点、P-gp在肠道的不均匀分布所造成的。Qu等[15]研究口服鸢尾甘后药-时曲线产生双峰的主要原因是肝肠循环;Schaiquevich等[16]研究了无胆囊大鼠口服雷尼替丁后药-时曲线双峰的原因,可能是由于胃肠道上存在多个吸收位点;有文献报道,由于药物外排转运蛋白P-gp在小肠的表达和分布存在区段性差异,使药物在不同位点的通透性不同,吸收时间和速率不一致,最终导致药-时曲线存在双峰或多峰现象[17]。
| [1] | 梁秉文,邓晨安,王学斌,侯晓清,唐有元,杨渭渔,等.黄杨木碱Ⅰ、Ⅱ、Ⅲ、Ⅳ的分离与结构研究[J].中国药学杂志,1981,16:195-197. |
| [2] | Yu B, Ruan M, Zhou L, Xu L, Fang T. Influence of cyclovirobuxine D on intracellular Ca2+ regulation and the expression of the calcium cycling proteins in rat myocytes[J]. Fitoterapia, 2012, 83:1653-1665. |
| [3] | 陈庆文,单宏丽,孙宏丽,王 赫,杨宝峰.环维黄杨星D对分离大鼠心室肌细胞内Ca2+和L型钙电流的影响[J].药学学报,2004,39:500-503. |
| [4] | 黄丹丹,林 玲,许 立.CB对心衰大鼠心肌损伤及氧化应激的影响[J].中国药业,2014,23:26-27. |
| [5] | 柯仲成,桂双英,虞盛舟,凌 超.黄杨宁的研究进展[J].甘肃中医学院学报,2011,28:71-73. |
| [6] | 黄丹丹,许 立.CB心血管系统药理作用研究进展[J].贵阳中医学院学报,2013,35:241-243. |
| [7] | 国家药典委员会.中国药典[S]. 一部.北京:中国医药科技出版社,2010:382. |
| [8] | 国家药典委员会.中国药典[S]. 一部.北京:中国医药科技出版社,2010:1065. |
| [9] | Ding L, Hu J, Jiang M, Xiong N. Sensitive HPLC-APCI-MS method for the determination of cyclovirobuxine D in human plasma[J]. J Chromatogr B Analyt Technol Biomed Life Sci, 2006, 843:78-83. |
| [10] | Yu P, Zou L, Liu W, Wu C, Sun D, Xu J, et al. High performance liquid chromatography-tandem mass spectrometric determination of cyclovirobuxine D in human plasma[J]. J Pharm Biomed Anal, 2006, 42:488-493. |
| [11] | 李 丽.大豆磷脂及其在药剂中的应用[J].黑龙江医药,2010,23:178-182. |
| [12] | 李 琳,董武军,盛 莉,夏学军,李 燕,刘玉玲.双环醇磷脂复合物制备、复合机制及其对口服吸收的影响[J].药学学报,2014,49:1600-1606. |
| [13] | 丁冬梅,张振海,蒋艳荣,贾晓斌.中药磷脂复合物的研究进展[J].中国中药杂志,2013,38:2046-2050. |
| [14] | 戈延茹,张春燕,吉顺莉.中药活性成分磷脂复合物的研究进展[J].时珍国医国药,2010,21:2107-2109. |
| [15] | Qu J, Gao J, Sun J, Zhang L, Makino T, Yuan D. Pharmacokinetics of conjugated metabolites in rat plasma after oral adminis tration of tectoridin [J]. J Chromatogr B Analyt Technol Biomed Life Sci, 2012, 902:61-69. |
| [16] | Schaiquevich P, Niselman A, Rubio M. Comparison of two compartmental models for describing ranitidine's plasmatic profiles [J]. Pharmacol Res, 2002, 45:399-405. |
| [17] | Wada S, Kano T, Mita S, Idota Y, Morimoto K, Yamashita F, et al. The role of inter-segmental differences in P-glycoprotein expression and activity along the rat small intestine in causing the double-peak phenomenon of substrate plasma concentration [J]. Drug Metab Pharmacokinet, 2013, 28:98-103. |
 2016, Vol. 37
2016, Vol. 37


