2. 江阴市中医院急诊科, 无锡 214400
2. Department of Emergency Medicine, Jiangyin Hospital of Traditional Chinese Medicine, Wuxi 214400, Jiangsu, China
胰十二指肠切除术及远端胰腺切除术是胰腺病变经典的切除方法,但其对机体损伤较大,尤其对胰腺中段良性或低度恶性病变,会导致正常胰腺组织切除过多,对胰腺内、外分泌功能损害较大[1, 2]。为解决此问题,胰腺中段切除术应运而生并逐渐发展完善,成为一种成熟的手术方式应用于胰腺颈、体部良性及低度恶性病变的切除,得到广泛认可[1, 2, 3]。胰腺中段切除术主要适用于胰颈或紧邻胰颈、远端胰腺残端至少保留5 cm、直径<5 cm 的良性或低度恶性肿瘤以及胰腺颈体部外伤,远端胰腺残端的处理是该术式的关键步骤,与患者预后密切相关[4, 5]。
胰腺中段切除术中远端胰腺残端的处理主要涉及消化道的重建,包括胰胃吻合、胰腺空肠吻合两种常见的重建方式,但对两种吻合方式的选择目前仍存有争议[6]。因此,我们对本研究小组的单中心数据进行分析,对比观察胰腺中段切除术中胰胃吻合与胰腺空肠吻合患者各预后指标,评价两者的疗效及安全性,为临床选择提供参考。
1 资料和方法 1.1 一般资料2013年5月至2015年5月本研究小组共施行胰腺中段切除术25例。根据胰腺残端吻合方式不同分成两组:胰胃吻合组(n=14)和胰肠吻合组(n=11)。男性6例,女性19例,平均年龄(44.55±21.30) 岁。
1.2 手术方法分离切断胰颈:于胰腺下缘分离出肠系膜上静脉,胰腺上缘分离出门静脉。电刀切开胰颈后手工缝合关闭或切割闭合器(Endo-GIA stapler)离断并关闭近端胰腺残端[7]。将肿瘤及胰体向前腹壁提起,沿脾静脉小心分离胰腺后方组织,直至肿瘤完全抬起,注意保护脾动静脉,于肿瘤胰尾侧胰体上下缘各做一“8”字缝合后,于肿瘤胰尾侧2 cm离断胰腺,移除标本。暴露远端胰腺残端,游离1.5~2.0 cm,胰腺断端止血,主胰管直径约2~8 mm,开口通畅,置入硅胶引流管1根,待吻合用。
胰胃吻合:在胃后壁与胰腺残端对应位置,电凝切开与胰管直径大小相当的胃壁,使胃黏膜唇状外翻,待吻合用。磁感应线式缝合方法吻合胰管和胃黏膜唇状开口,一般断面轮辐状均匀缝合约6针(图 1)。硅胶引流管置入胃黏膜开口。距离吻合面1圈做浆膜层间断缝合加固,一般均匀缝合,在胰管胃黏膜开口吻合前后分2次,各约4~6针。
|
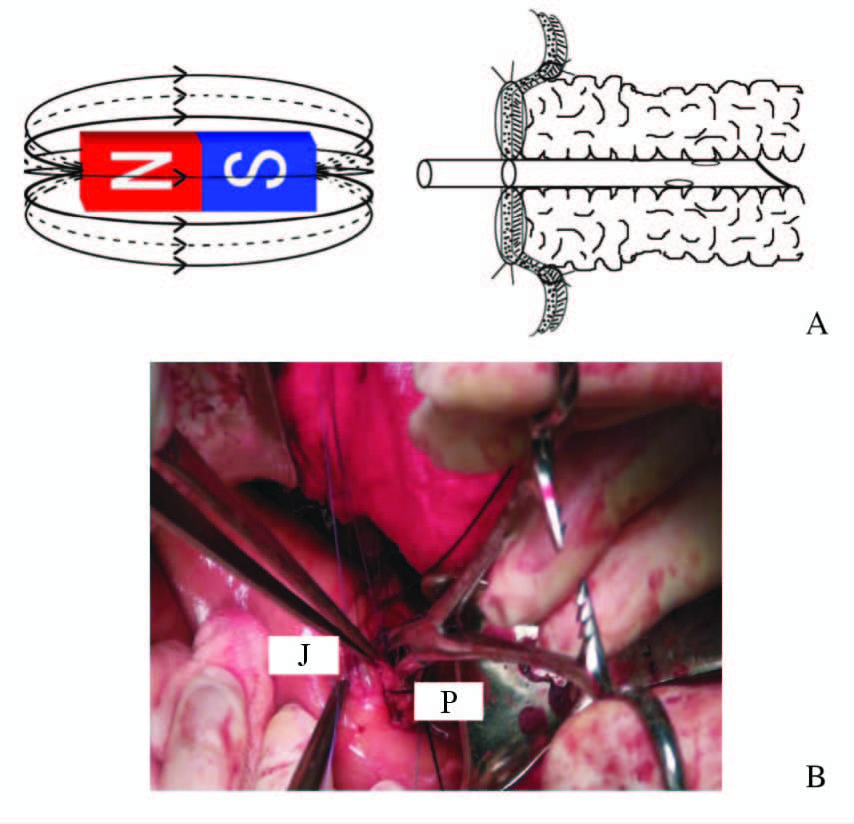
图 1 磁感应线式缝合方法示意图(A)及术中所见(B) Fig 1 Schematic diagram of magnetic induction line suture (A) and operation scene (B) J: Jejunum; P: Pancreas |
胰肠吻合:取无血管区打开横结肠中段系膜,选择距离屈氏韧带15 cm处合适空肠襻,通过横结肠系膜孔上提至胰腺残端附近,对空肠系膜缘电凝切开与胰管直径大小相当的肠壁,制成外翻黏膜瓣,待吻合用。磁感应线式缝合方法吻合胰管和空肠黏膜唇状开口,一般断面轮辐状均匀缝合约6针(图 1)。硅胶引流管置入空肠黏膜开口。间断加固同胰胃吻合。另空肠距离胰肠吻合口约50 cm处行Roux-Y术侧侧吻合。
1.3 术后观察指标术后观察两组患者一般情况及术后胰瘘发生率、住院时间等指标,对比两种吻合方式的疗效及安全性。胰瘘诊断参照胰瘘国际协作组对术后胰瘘的定义[8]:术后3 d以上、腹腔引流液淀粉酶活性大于血清淀粉酶活性正常高限3倍。
1.4 统计学处理采用SPSS 16.0软件,计量资料以
胰胃吻合组:共14例,男2例,女12例,年龄(43.5±17.5)岁,肿瘤直径(2.9±1.6) cm。术后病理:胰腺神经内分泌肿瘤3例,胰腺浆液性囊腺瘤5例,胰腺导管内乳头状黏液性肿瘤3例,胰腺实性假乳头状瘤2例,胰腺潴留性囊肿1例。胰肠吻合组:共11例,男4例,女7例,年龄(46.0±31.0)岁,肿瘤直径(3.1±1.9) cm。术后病理:胰腺实性假乳头状瘤4例,胰腺导管内乳头状黏液性肿瘤3例,胰腺浆液性囊腺瘤1例,慢性胰腺炎1例,胰腺导管腺癌1例,胰腺外伤导致胰管狭窄1例。两组患者年龄、性别构成比差异无统计学意义,具有可比性。
2.2 手术情况及随访结果 2.2.1 两组患者术后住院时间对比胰胃吻合组和胰肠吻合组术后患者住院时间差异无统计学意义[(11.5±3.5) d vs (10.5±5.5) d,P=0.778 3]。
2.2.2 两组患者术后胰瘘发生率对比25例患者术后发生胰瘘2例(8.0%)。 其中胰肠吻合组1例 胰腺导管内乳头状黏液性肿瘤患者于术后第5天发生胰瘘,腹腔引流液淀粉酶1 700 U,给予原位乳胶引流管改双套管冲洗、低负压引流以及奥曲肽等药物治疗,术后第47天痊愈出院。胰胃吻合组1例胰腺导管内乳头状黏液性肿瘤患者于术后第3天发生胰瘘,腹腔引流液淀粉酶3 250 U,第9天腹腔引流液淀粉酶大于12 000 U,术后第12天出现腹腔内出血,经原位乳胶引流管改双套管冲洗、低负压引流以及奥曲肽等药物治疗,同时给予肠外营养、输血支持、腹部出血部位间断压迫13 d控制;术后第30天发生上消化道出血,间断日呕血量50~200 mL不等,胃镜提示引流管刺入胃腔导致胃黏膜出血;适当退出腹腔引流管,经止血、抑酸、加强营养支持等保守治疗8 d后上消化道出血停止,患者术后第49天痊愈出院。 胰胃、胰肠吻合组患者术后胰瘘发生率差异无统计学意义(7.14% vs 9.09%,P=0.858 6)。
2.2.3 其他并发症发生情况25例患者术后切口脂肪液化患者2例(每组各1例),敞开引流,坚持换药,均获得延期愈合。25例患者饮食恢复后未发生术后吻合口出血、腹腔脓肿、明显胃排空障碍等并发症。
3 讨 论 3.1 胰腺中段切除手术吻合方法的选择本研究两组比较因样本量小未能体现并发症明显差异,但我们分析胰腺中段切除后行胰胃吻合,胃液酸性不易激活胰酶,同时胃管可以为胰腺残端有效减压,胰胃吻合在预防胰瘘和术后并发症方面有优势。胰腺中段切除术后采用远端胰腺残端与胃吻合,使手术范围局限在横结肠系膜上,保留了原消化道的连续性。此手术方法保护了胰头部结构,留存胰腺多,胰腺外分泌功能受影响小,患者消化功能恢复快。我们推荐胰腺质地较软、胰管直径正常的病例实施胰胃吻合术。Goudard等[9]通过研究评价单手术中心12年治疗经验,胰腺中段切除胰胃吻合术运用于良性或低度恶性胰腺病变患者,可以保护胰腺功能及获得良好的长期治疗效果。目前,腹腔镜微创行胰腺中段切除术国外也有推荐[10]。在两种吻合方法运用于十二指肠切除术方面,Menahem 等[11]选择符合纳入标准的7个前瞻性随机对照试验共1 121例患者进行meta分析。结果显示,与胰肠吻合组相比,胰胃吻合组能显著降低胰十二指肠切除术后胰瘘发生率。我们手术组认为,吻合方法的比较必须建立在娴熟、可靠的手术技巧上,纯粹依靠吻合方法来避免胰瘘及并发症是不可取的。按照术者习惯及熟练方式吻合,同时不断提高和完善吻合的质量即为最佳。
3.2 胰胃(肠)吻合的技巧和近端胰腺残端的处理胰胃(肠)吻合要点:(1)胰腺残端适当游离,目的在于可抬起和胃后壁或空肠无张力吻合,但要避免游离过长,因可能导致游离段胰腺缺血坏死。(2)利用胃(肠)浆膜层覆盖胰腺断面,有效阻挡胰腺渗血及胰液腐蚀周围组织。(3)单股缝线间断缝合,选择表面光滑、摩擦力小、可减少吻合部位感染的可吸收的缝线(Vicryl Plus、抗菌薇乔),运针抽线顺畅同时可以抵抗胰液腐蚀。在近端胰腺残端的处理上,Endo-GIA处理胰腺残端在胰体尾切除术中的应用效果相当于手工缝合法,Endo-GIA应用于胰体尾切除术安全可靠,疗效明确[7]。该术式在保证安全的同时有效节省手术时间,避免手术并发症。
3.3 磁感应线式缝合方法吻合优点磁铁等同于胰管胃(肠)黏膜开口对合处,磁感应线即为缝合线,此法吻合带入较多胰腺及胃(肠)组织,较单纯胰管胃(肠)黏膜缝合可避免组织坏死、线圈脱落;虽此法缝合穿透胰腺组织,本研究的25例均未发生吻合口出血。术者认为针线技巧重要,缝合必须流畅到位,反针缝合熟练运用,避免在胰腺组织中来回反复针尖穿刺;打结松紧合适,切忌太紧造成缝线切割胰腺。可靠的吻合能直接减少患者术后并发症,有利于缩短住院时间,让患者尽早恢复正常生活。
综上所述,胰腺中段切除术能较好地保持胰腺功能,且胰胃与胰肠吻合术均安全、有效,但相关结论仍有待更大样本验证。
| [1] | Xiang G M, Tan C L, Zhang H, Ran X, Mai G, Liu X B. Central pancreatectomy for benign or borderline lesions of the pancreatic neck: a single centre experience and literature review[J].Hepatogastroenterology,2012,59:1286-1289. |
| [2] | Iacono C, Verlato G, Ruzzenente A, Campagnaro T, Bacchelli C, Valdegamberi A, et al. Systematic review of central pancreatectomy and meta-analysis of central versus distal pancreatectomy[J].Br J Surg,2013,100:873-885. |
| [3] | Senthilnathan P, Gul S I, Gurumurthy S S, Palanivelu P R, Parthasarathi R, Palanisamy N V, et al. Laparoscopic central pancreatectomy: our technique and long-term results in 14 patients[J].J Minim Access Surg, 2015,11:167-171. |
| [4] | 廖 泉,赵玉沛.胰腺节段切除手术技巧及并发症预防和处理[J].中国实用外科杂志,2009,29:186-188. |
| [5] | 覃 虹,董 明,田利国.保留器官功能胰腺手术方式研究进展[J].中国实用外科杂志, 2011, 31:975-978,980. |
| [6] | Liu F B, Chen J M, Geng W, Xie S X, Zhao Y J, Yu L Q, et al. Pancreaticogastrostomy is associated with significantly less pancreatic fistula than pancreaticojejunostomy reconstruction after pancreaticoduodenectomy: a meta-analysis of seven randomized controlled trials[J].HPB (Oxford),2015,17:123-130. |
| [7] | 陈金水,胡先贵,金 钢,邵成浩,蔡晓棠.切割闭合器在胰体尾切除术中的应用[J].肝胆胰外科杂志,2013,25:13-19. |
| [8] | Bassi C, Dervenis C, Butturini G, Fingerhut A, Yeo C, Izbicki J, et al. Postoperative pancreatic fistula: an international study group (ISGPF) definition[J].Surgery,2005,138:8-13. |
| [9] | Goudard Y, Gaujoux S, Dokmak S, Cros J, Couvelard A, Palazzo M, et al. Reappraisal of central pancreatectomy a 12-year single-center experience[J].JAMA Surg,2014,149:356-363. |
| [10] | Song K B, Kim S C, Park K M, Hwang D W, Lee J H, Lee D J, et al. Laparoscopic central pancreatectomy for benign or low-grade malignant lesions in the pancreatic neck and proximal body[J].Surg Endosc,2015,29:937-946. |
| [11] | Menahem B, Guittet L, Mulliri A, Alves A, Lubrano J. Pancreaticogastrostomy is superior to pancreaticojejunostomy for prevention of pancreatic fistula after pancreaticoduodenectomy: an updated meta-analysis of randomized controlled trials[J].Ann Surg,2015,261:882-887. |
 2016, Vol. 37
2016, Vol. 37


