肾细胞癌是泌尿系统常见肿瘤,约占所有恶性肿瘤的2%~3%[1],约1/4的患者就诊时已有转移。局限性肾癌患者术后预后良好,而转移性肾癌对于化疗和放疗均不敏感,免疫治疗、靶向治疗效果也不理想,预后较差。肾细胞癌转移的影响因素复杂,转移相关蛋白与其相关[2]。趋化因子受体CXCR4 (CXC chemokine receptor 4)与肿瘤转移密切相关,其在细胞核内迁移表达与肾癌细胞高侵袭性和转移性相关[3],但目前对其在肾癌病理组织中的表达情况尚不清楚。本研究拟观察肾癌组织CXCR4的表达情况,并分析其核定位表达与肾癌患者临床病理指标的相关性,为后续研究奠定基础。
1 资料和方法 1.1 一般资料2011年3月至2012年11月,第二军医大学长海医院泌尿外科收治的肾癌患者413例,男233例,女180例,年龄27~77岁,平均(56.8±10.9)岁,平均体质指数(24.4±3.2) kg/m2。术前均未行放疗和化疗。413例患者术后肾癌病理组织学分类:透明细胞癌355例、肾乳头状细胞癌29例、嫌色细胞癌26例、肉瘤样肾细胞癌3例,其中23例伴肾静脉和(或)下腔静脉癌栓、13例伴区域淋巴结转移、20例伴远处器官转移(肺、骨、肝脏等)。随访时间截至2014年4月15日。本研究经第二军医大学长海医院医学伦理委员会审批通过。患者入院时即签署知情同意书,同意术后肿瘤标本用于科学研究。
1.2 免疫荧光染色法测定肾癌组织CXCR4表达将肾癌石蜡标本以石蜡切片机制取4 μm切片,蜡片贴附于多聚赖氨酸处理过的载玻片上;60℃烘片,二甲苯脱蜡,梯度乙醇水化,枸橼酸液修复抗原;PBS浸洗、透膜剂透膜、滴加封闭血清;滤纸擦去封闭液,加入CXCR4抗体4℃过夜;次日PBS充分洗涤3次,加FITC标记的二抗,室温孵育15 min,PBS洗3次,每次5 min以上;加入DAPI染色3 min后,PBS冲洗1次;50%甘油封片,荧光显微镜下观察。
1.3 结果判定制取切片,抗体包埋后,免疫荧光显微镜下观察并拍照,由两位病理科医师双盲判定。判定标准为:(1)每例肾癌病理组织石蜡标本制取4片切片,对每个切片单独评分。(2)镜下观察到癌细胞核内有CXCR4定位,则此切片评定为CXCR4核定位阳性,记1分;反之,评定为阴性,记0分。(3)对4张切片结果汇总,分数总和。总和为0~1分为CXCR4核定位阴性;2~4分为核定位阳性。
1.4 肾癌组织CXCR4核转移表达与临床病理指标及预后的相关性分析根据免疫荧光染色结果将患者分为核定位阳性组及核定位阴性组,比较两组患者的临床病理指标及预后情况。
1.5 统计学处理采用PASW Statistics 18.0软件进行统计分析,组间比较采用Pearson χ2检验或Mann-Whitney检验,生存率比较采用Kaplan-Meier检验,检验水准(α)为0.05。
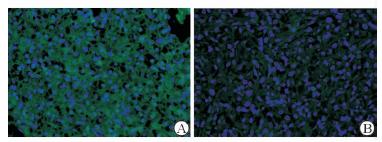
2 结 果 2.1 肾癌组织CXCR4的表达定位情况免疫荧光显微镜下蓝色荧光、椭圆形的是细胞核,绿色荧光、絮状的是CXCR4蛋白。413例肾癌组织中170例核内CXCR4阳性表达(图 1A),243例核内CXCR4阴性表达(图 1B)。
|
图 1 免疫荧光显微镜下观察肾癌组织CXCR4的表达 A: CXCR4核定位阳性表达;B: CXCR4核定位阴性表达. Original magnification:×400 |
相关性分析结果(表 1)表明:两组患者基线资料类似,差异无统计学意义;两组患者Furhman分级差异无统计学意义(P=0.169);与核定位阴性表达组相比,核定位阳性表达组Robson分期高、癌栓发生率高、淋巴结转移率高、远处转移率高,差异均有统计学意义(P<0.01)。
|
|
表 1 两组患者基线资料的对比 |
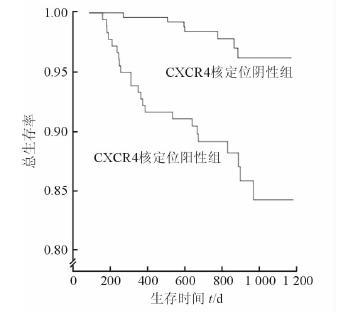
随访结果(图 2)表明:核转移阳性表达组生存率为86.5%(147/170),低于核转移阴性表达组97.1%(236/243),差异有统计学意义(P<0.001)。
|
图 2 两组患者总生存曲线的对比 |
趋化因子受体CXCR4是趋化因子CXCL12的唯一生理性受体,二者共同表达于心、脑、肾、肺、肝等组织,相互作用构成了与细胞信息传递、 迁移密切相关的CXCL12/CXCR4 生物轴,在肿瘤、炎症、HIV感染[4, 5]等多种生理、病理过程中发挥重要作用。近年来,CXCL12/CXCR4轴被发现在多种肿瘤的转移中扮演重要角色,与乳腺 癌、胃癌、肺癌等肿 瘤的转移 密切相关[6, 7, 8, 9, 10, 11, 12]。 进一步的CXCR4亚细胞定位研究表明,CXCR4的核转移定位表达与结直肠癌[13]、肝癌[14]等的转移及预后密切相关。
目前关于CXCL12/CXCR4轴在肾癌中的作用研究较少。我们的前期研究对97例肾癌标本进行分析,检测原发灶、癌旁组织及转移灶CXCR4的表达,发现转移灶CXCR4表达最高,其次是原发灶,癌旁组织最少,并且CXCR4高表达提示患者预后差[15]。进一步应用RNA干扰技术降低肾癌A498细胞株CXCR4基因表达水平,细胞体外侵袭力明显受抑[16];通过不同浓度CXCL12β刺激体外培养的肾癌A498细胞,进行免疫荧光染色原位观察,发现经过CXCL12β的刺激,出现CXCR4向细胞核内迁移的现象,并且这种细胞株侵袭能力明显增高[3]。这些研究结果提示肾癌组织CXCR4核转移定位表达可能与肾癌转移及侵袭相关。
本研究中肾癌组织CXCR4总表达率为92.0%,CXCR4核定位占61.0%,胞质定位占37.5%,与既往文献[15]报道相符。统计分析显示,肾癌组织CXCR4核定位与Robson分期、淋巴结转移、癌栓形成、远处转移都有关;生存率随访显示,CXCR4核定位与低的总体生存率相关。本研究结果提示CXCR4入核后,肾癌分期、转移性、侵袭性增加,预后变差,但其具体的分子机制尚无明确结论。后续研究主要关注于以下几个问题:(1)核定位的CXCR4来源问题。它与肿瘤细胞胞膜、胞质内的CXCR4是否同一来源,如果是同一来源,入核是由什么机制诱导?(2)核定位的CXCR4在核内是否与特异性DNA片段或蛋白结合,可能的片段或位点是什么?(3)核定位的CXCR4在核内是否激活了其他信号转导通路?
综上所述,本研究结果表明,CXCR4核定位与肾癌Robson分期、静脉癌栓发生、肿瘤淋巴转移、肿瘤远处转移相关,并且提示预后较差;CXCR4肾癌细胞核定位可能是肾癌患者预后的潜在判断指标;对CXCL12/CXCR4轴的阻断,可能成为肾癌靶向治疗的新策略。
| [1] | Jemal A, Siegel R, Xu J, Ward E. Cancer statistics, 2010[J].CA Cancer J Clin,2010,60:277-300. |
| [2] | Cohen H T, McGovern F J. Renal-cell carcinoma[J].N Engl J Med,2005,353:2477-2490. |
| [3] | Wang L, Wang L, Yang B, Yang Q, Qiao S, Wang Y, et al. Strong expression of chemokine receptor CXCR4 by renal cell carcinoma cells correlates with metastasis[J].Clin Exp Metastasis,2009,26:1049-1054. |
| [4] | Feng Y, Broder C C, Kennedy P E, Berger E A. HIV-1 entry cofactor: functional cDNA cloning of a seven-transmembrane, G protein-coupled receptor[J].Science,1996,272:872-877. |
| [5] | Müller A, Homey B, Soto H, Ge N, Catron D, Buchanan M E, et al. Involvement of chemokine receptors in breast cancer metastasis[J].Nature,2001,410:50-56. |
| [6] | Balkwill F. The significance of cancer cell expression of the chemokine receptor CXCR4[J].Semin Cancer Biol,2004,14:171-179. |
| [7] | Chu Q D, Panu L, Holm N T, Li B D, Johnson L W, Zhang S. High chemokine receptor CXCR4 level in triple negative breast cancer specimens predicts poor clinical outcome[J].J Surg Res,2010,159:689-695. |
| [8] | Chu Q D, Holm N T, Madumere P, Johnson L W, Abreo F, Li B D.Chemokine receptor CXCR4 overexpression predicts recurrence for hormone receptor-positive, node-negative breast cancer patients[J]. Surgery, 2011,149:193-199. |
| [9] | Otsuka S, Klimowicz A C, Kopciuk K, Petrillo S K, Konno M, Hao D, et al. CXCR4 overexpression is associated with poor outcome in females diagnosed with stage Ⅳ non-small cell lung cancer[J].J Thorac Oncol, 2011,6:1169-1178. |
| [10] | Chen G, Wang Z, Liu X Y, Liu F Y. High-level CXCR4 expression correlates with brain-specific metastasis of non-small cell lung cancer[J].World J Surg,2011,35:56-61. |
| [11] | Ying J, Xu Q, Zhang G, Liu B, Zhu L. The expression of CXCL12 and CXCR4 in gastric cancer and their correlation to lymph node metastasis[J].Med Oncol,2012,29:1716-1722. |
| [12] | Feil C, Augustin H G. Endothelial cells differentially express functional CXC-chemokine receptor-4 (CXCR-4/fusin) under the control of autocrine activity and exogenous cytokines[J].Biochem Biophys Res Commun,1998,247:38-45. |
| [13] | Wang S C, Lin J K, Wang H S, Yang S H, Li A F, Chang S C. Nuclear expression of CXCR4 is associated with advanced colorectal cancer[J]. Int J Colorectal Dis,2010,25:1185-1191. |
| [14] | 向作林,曾昭冲,汤钊猷,樊 嘉,孙惠川,吴伟忠,等.趋化因子受体4核阳性以及血管内皮生长因子C和细胞角蛋白19的表达水平与肝细胞癌淋巴结转移风险的关系[J].中华肿瘤杂志,2010,32:344-349. |
| [15] | Wang L, Chen W, Gao L, Yang Q, Liu B, Wu Z, et al. High expression of CXCR4, CXCR7 and SDF-1 predicts poor survival in renal cell carcinoma[J].World J Surg Oncol,2012,10:212. |
| [16] | 王林辉,黄 霆,杨 庆,陈 伟,吴震杰,孙颖浩.稳定沉默CXCR4表达的肾癌A498细胞株的构建[J].第二军医大学学报,2011,32:1103-1107. Wang L H, Huang T, Yang Q,Chen W,Wu Z J, Sun Y H.Establishment of a renal carcinoma cell line A498 with CXCR4 stably silenced[J]. Acad J Sec Mil Med Univ,2011,32:1103-1107. |
 2015, Vol. 36
2015, Vol. 36


