2. 第二军医大学长海医院胸心外科, 上海 200433
2. Department of Cardiac Surgery, Changhai Hospital, Second Military Medical University, Shanghai 200433, China
心脏手术患者术前心功能差会导致对血流动力学变化不耐受,使术后急性肾损伤(acute kidney injury,AKI)的发病率增加。脑钠肽(brain natriuretic peptide,BNP)是心力衰竭患者常见且公认的血清标记物,多个研究表明,术前BNP及其前体水平与心脏手术术后的并发症、住院时间和病死率密切相关[1, 2]。AKI是心脏手术术后常见且严重的并发症,依据AKI不同的诊断标准,其发病率为15%~51%[3],且研究表明,即使是轻度肾损伤也和预后不良相关[4]。目前对BNP和AKI之间关系的研究甚少,本研究旨在观察心脏手术患者术前BNP水平和术后AKI之间的关系。 1 资料和方法 1.1 一般资料
收集2012年1月至2013年1月在第二军医大学长海医院胸心外科行心脏手术的患者的病例资料182例,手术方式包括冠状动脉旁路移植术(CABG)、瓣膜置换术、联合手术(瓣膜置换+CABG)。为提高检出率,入选患者是AKI的高风险患者,符合以下标准任一项或多项:(1)基础肾脏病,基线血肌酐>15 mg/L(132 μmol/L);(2)心功能3~4级;(3)年龄>70岁;(4)糖尿病。排除标准:术前肌酐>354 μmol/L或透析患者。本研究经第二军医大学伦理委员会批准后实施,患者均签署知情同意书。 1.2 方法
采用术前末次静脉血测量BNP水平,应用Triage检测仪(Biosite,美国),以酶联免疫法检验数值。估算的肾小球滤过率(eGFR)应用MDRD 公式计算。心功能分级应用纽约心脏病协会(NYHA)[5] 的心力衰竭分级标准,分为Ⅰ~Ⅳ 级。AKI分级应用最新改善全球肾脏病预后 (Kidney Disease: Improving Global Outcomes,KDIGO)指南[6](表 1)进行评估。 共入选182例,按术前BNP水平升序五分位法进行分组[7],共分5组,其中3组每组36例,2组每组37例。
|
|
表 1 KDIGO指南[6]AKI分级 |
应用SPSS 18.0软件进行统计学分析,正态分布数据采用x±s 表示,非正态分布数据用中位数和四分位数表示。多组正态分布数据之间的比较应用单因素方差分析(one-way ANOVA),率的比较应用χ2检验,多组构成比的比较应用Pearson χ2检验,有序多分类变量的比较应用多组有序资料的秩和检验中的Kruskal-Wallis检验。检验水准(α)为0.05。 2 结 果 2.1 一般情况
共入选 182例,平均年龄(68.6±8.9)岁,其中男性占65.9%(120/182);手术方式:CABG 45.0%(82/182),瓣膜手术31.3%(57/182),联合手术23.6%(43/182);术前肾功能:肌酐(92.3±39.4)μmol/L,eGFR(70.0±20.5)mL/min。分为5组,按BNP水平升序排列入各组后,患者年龄、基础肾功能和术前BNP水平差异有统计学意义(P<0.05,表 2)。性别构成、糖尿病、手术方式构成差异无统计学意义。
|
|
表 2 入选患者一般情况 |
患者术后AKI发生率达33.5%(61/182),按照KDIGO标准,5组术后AKI的发生率如表 3所示,AKI的发生率随BNP水平的升高而逐渐增加,且1级(轻度AKI)和总AKI的发生率在趋势上差异有统计学意义(P<0.05)。
|
|
表 3 患者术后AKI发生率与BNP的相关性 |
以术前BNP水平预测术后AKI发生率,绘制ROC曲线图(图 1),曲线下面积(AUC)为0.687 (95% CI: 0.607~0.768)。取其灵敏度和特异度之和最大为界值(cut-off点),则BNP水平为79.5 pg/mL时,灵敏度为0.55,特异度为0.742。可见术前BNP水平预测术后AKI发生率有一定的价值,但预测强度中等偏下。
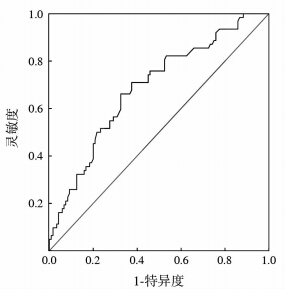 | 图 1 以术前BNP水平预测术后AKI发生率的ROC曲线图 BNP: 脑钠肽; AKI: 急性肾损伤;ROC: 受试者工作特征 |
BNP又称B型利钠肽,来源于心室,具有促进排钠、利尿及较强的舒血管作用,可对抗肾素-血管紧张素-醛固酮系统的缩血管作用,同心房利钠肽一样是人体抵御容量负荷过重及高血压的一个重要内分泌激素。心功能障碍能够刺激利钠肽系统,心室负荷重会增加BNP的释放。BNP一直被用来评估患者心功能情况以及心脏病的预后[8]。心脏手术患者术前由于基础病的原因心功能欠佳,所以对手术、体外循环、术后血流动力学的改变尤为敏感,术前BNP水平和术后并发症、住院时间、病死率密切相关[1, 2]。
依据诊断标准的不同,AKI发病率差别很大。2012年KDIGO组织发布新的AKI诊断标准,与以往标准相比,此诊断标准在急性肾损伤网络(acute kidney injury network,AKIN) 的基础上仍然延续了48 h内血肌酐升高>0.3 g/L(26.5 μmol/L)的早期诊断,又增加了7 d内血肌酐上升>1.5倍的时间概念,这样的标准与预后的相关性更好[3]。
心脏手术术后AKI一直受到心脏外科和肾脏病科医生的密切关注,其发病率及病死率高,危险因素与术前患者基本情况、术中及术后并发症密切相关。术前的危险因素多考虑与年龄、基础肾功能密切相关[9]。Doddakula等[10]的研究显示,体外循环时间是术后AKI发生的独立危险因素;Parolari等[11]研究显示当体外循环过程中保持血流速度在1.8~2.2 L/(min·m2)、灌注压在50~70 mmHg(1 mmHg=0.133 kPa)可以维持组织所需要的氧供,体外循环心脏手术中应尽可能缩短大动脉阻断时间。在术后危险因素分析中,Suen等[12]研究证明,术后低血压(收缩压低于90 mmHg)超过1 h是术后AKI的危险因素;Mangano等[13]证实在CABG术后因低心排使用经皮主动脉内气囊反搏(IABP)的患者发生AKI的危险增加7倍。
在本研究中,在BNP不同组别中,分析术前各种基础疾病时,基础肾功能和年龄的差别导致AKI的发生率更高,而糖尿病患者存在血管内皮的损伤,理论上可能与AKI的发生率有密切关系。Patel等[7]研究也表明糖尿病与AKI的发生率有密切相关性,本研究中各组患者糖尿病构成比无差异,可能与样本量不够大、糖尿病发病率较国外低等因素相关。本研究中手术方式的构成也无统计学差异,可能与患者虽然经历不同的手术、但体外循环时间较为类似有关,因为AKI的发生可能与体外循环时间有关[10]。BNP作为心衰的主要生物标记物,意味着心功能不全患者对手术中和手术后血流动力学改变更为敏感,更易造成心源性休克或低心排综合征,就更易造成肾血流量减少,从而造成AKI的发生。依据KDIGO标准,本研究中AKI的发生率在不同的BNP组分别为19.4%、22.2%、33.3%、40.5%、51.3%。BNP水平越高AKI发生率越高,且在每组中,多以KDIGO分级中1级占多数,说明多数心脏术后的AKI是可逆的,1级AKI和总AKI的发生率在趋势上差异有统计学意义(P<0.05),与国外报道[13]一致。本研究以术前BNP水平预测AKI发生率绘制ROC曲线,AUC达0.687,虽然不能够成为诊断标记物,但在心脏手术中,可以作为较好的危险分层的生物标记物。
综上所述,心脏手术术后发生AKI是由多种因素造成的,至今发生率仍然较高,也预示早期评价和早期诊断的体系仍不完善。BNP可作为一种较好的危险分层指标。
| [1] | Attaran S, Sherwood R, Desai J, Langworthy R, Mhandu P, John L, et al. Brain natriureticpeptide a predictive marker in cardiac surgery[J]. Interact Cardiovasc Thorac Surg,2009, 9:662-666. |
| [2] | Nozohoor S, Nilsson J, Algotsson L, Sjogren J. Postoperative increase in B-type natriuretic peptide levels predicts adverse outcome after cardiac surgery[J]. J Cardiothorac Vasc Anesth,2011,25:469-475. |
| [3] | Sampaio M C, Máximo C A, Montenegro C M, Mota D M, Fernandes T R, Bianco A C, et al. Comparsison of diagnostic criteria for acute kidney injury in cardiac surgery [J].Arq Bras Cardiol, 2013,101:18-25. |
| [4] | Coca S G, Peixoto A J, Garg A X, Krumholz H M, Parikh C R. The prognostic importance of a small acute decrement in kidney function in hospitalized patients: a systematic review and meta-analysis[J].Am J Kidney Dis,2007, 50:712-720. |
| [5] | Apostolakis E, Akinosoglou K. Reexamining the New York Heart association functional classification of heart failure[J].Am J Cardiol,2007,100:911-912. |
| [6] | Kidney Disease: Improving Global Outcomes (KDIGO) Acute Kidney Injury Work Group. KDIGO clinical practice guideline for acute kidney injury[J]. Kidney Int Suppl,2011,2:1-138. |
| [7] | Patel U D, Garg A X, Krumholz H M, Shlipak M G, Coca S G, Sint K,et al.Preoperative serum brain natriuretic peptide and risk of acute kidney injury after cardiac surgery[J]. Circulation, 2012,125:1347-1355. |
| [8] | Fox A A, Nascimben L, Body S C, Collard C D, Mitani A A, Liu K Y, et al. Hemoglobin and B-type natriuretic peptide preoperative values but not inflammatory markers, are associated with postoperative morbidity in cardiac surgery: a prospective cohort analytic study[J]. Anesthesiology, 2013,119:284-294. |
| [9] | Li S Y, Chen J Y, Yang W C, Chuang C L. Acute kidney injury network classification predicts in-hospital and long-term mortality in patients undergoing elective coronary artery bypass grafting surgery[J]. Eur J Cardiothorac Surg,2011,39:323-328. |
| [10] | Doddakula K,AI-Sarraf N,Gately K, Hughes A, Tolan M, Young V, et al.Predictors of acute renal failure requiting renal replacement therapy post cardiac surgery in patients with preoperatively normal renal function[J].Interact Cardiovasc Thorac Surg,2007,6:314-318. |
| [11] | Parolari A, Alamanni F, Gherli T, Bertera A, Dainese L, Costa C,et al.Cardiopulmonary bypass and oxyen consumption: oxygen delivery and hemodynamics[J].Ann Thorac Surg, 1999, 67:1320-1327. |
| [12] | Suen W S,Mok C K,Chiu S W, Cheung K L, Lee W T, Cheung D,et al. Risk factors for development of acute renal failure(ARF), requiring dialysis in patients undergoing cadiac surgery[J].Angiology,1998,49:789-800. |
| [13] | Mangano C M,Diamondstone L S,Ramsay J G,Aggarwal A, Herskowitz A, Mangano D T. Renal dysfunction after myocardial revascularization:risk factors,adverse outcomes,and hospital resourceutilization.The Multicenter Study of Perioperalive Ischemia Reasearch Group[J].Ann Intern Med,1998,128:194-203. |
 2015, Vol. 36
2015, Vol. 36


