2. 第二军医大学药学院药物分析学教研室, 上海 200433;
3. 上海市药物(中药)代谢产物研究重点实验室, 上海 200433
2. Department of Pharmaceutical Analysis, School of Pharmacy, Second Military Medical University, Shanghai 200433, China;
3. Shanghai Key Laboratory for Pharmaceutical (Chinese Materia Medica) Metabolite Research, Shanghai 200433, China
透析技术是近年发展起来的一项活体取样技术,它以透析原理作为基础,试验时将半透膜插入目的组织中,待测药物可以沿浓度梯度到达半透膜另一侧透析液中,然后测定透析中药物浓度,并通过探针回收率计算组织内的游离药物浓度。微透析技术在基本不干扰体内正常生命过程的情况下进行在体取样,与传统的取样技术相比,具有活体取样、动态观察、定量分析、采样量小、组织损伤轻等优点[1, 2]。微透析系统主要是由微量灌流泵、探针、导管和样品收集器组成。在微透析系统中,探针是最关键的部分,目前常用的探针类型有:同心圆探针(主要用于脑部和血液)、柔性探针(主要用于血液)、线性探针(主要用于肌肉、皮肤等)和分流探针[3, 4]。因此,微透析技术可在动物各脏器组织中进行活体、实时、在线、微量取样分析,对于药物在各个作用部位的真实含量、分布及代谢变化有着重要的意义,广泛的应用于药代动力学、药效动力学以及药动学—药效学拟合等研究领域[5, 6, 7, 8]。
罗库溴铵是一种新型非去极化神经肌肉阻滞剂,给药后起效快、可控性好、无组胺释放、体内蓄积作用极小,临床上主要作为肌松药应用于术前肌肉松弛和快速诱导气管内插管的肌肉松弛,为目前起效最快的非去极化肌松药[9]。为了进一步探讨微透析技术在罗库溴铵体内过程研究中的应用价值,有必要测定罗库溴铵体内回收率来评价其体内微透析采样的可行性。微透析探针回收率是微透析试验的关键环节,它关系到体内物质的计算,因此稳定的微透析探针回收率是进行微透析试验的前提[10, 11, 12]。本实验基于微透析探针制备技术[13, 14],采用自制的同心圆探针和线性探针进行罗库溴铵体外与在体微透析回收率实验,考察影响微透析探针回收率的主要因素,为体内试验研究提供稳定可靠的自制探针和实验条件。
1 仪器、试药及方法 1.1 仪器SHIMADZU 8040液相色谱-质谱联用仪(岛津公司),包括LC-20AD高压泵、SIL-20A HT自动进样器、DGU-20A 3R脱气机、CTO-20A柱温箱、CBM-20A控制器、SPD-M20A PDA检测器、LCMS-8040质谱仪、Labsolutions工作站。
美国BAS公司生产的微透析设备,包括灌流注射器推进泵(Baby Bee Syringe Drive,MD-1001)、灌注器(1 mL Bee Stinger Gastight Syringe,MDN-0100)、灌注器架(3-Syringe Bracket for Baby Bee,MDD-1002)、流速控制器(Work Bee Controller,MD-1000,MD-1020)。微透析探针为自制的同心圆探针(膜长10 mm)和线性探针(膜长20 mm),截留相对分子质量大小5 000,灌流液为去离子水,探针连接管(从膜到出口)死体积4 μL。
S0200-230V-EU涡旋混合器(美国Labnet公司),Thermo Fisher CR3i冷冻离心机(美国ThermoFisher公司)。XS205Du十万分之一电子天平(瑞士METTLER TOLEDO集团公司),SK7200H超声仪(上海科导超声仪器有限公司),Hi-Tech水纯化系统(18.2 MΩ,上海和泰仪器有限公司)。
1.2 试药罗库溴铵化学对照品,批号X1-130101,含量99.3%,由浙江奥默医药技术有限公司提供。苯海拉明化学对照品,批号SM-130905,含量98.5%,由上海市药物(中药)代谢产物研究重点实验室提供。甲醇为德国Merck公司生产的色谱纯试剂,醋酸铵为江苏强盛功能化学股份有限公司制造的分析纯试剂,水为自制去离子水。
1.3 色谱条件色谱柱为DIONEX C18柱(5 μm,50 mm×2.1 mm),柱温35℃;流动相为甲醇∶5 mmol/L乙酸铵水溶液=70∶30(V/V),等度洗脱,流速0.2 mL/min,分析时间为2.5 min,进样量为5 μL;所有分析样品均加入相同体积(10 μL) 20 ng/mL 苯海拉明溶液作为内标物质,混匀待测。
1.4 质谱条件采用ESI离子源,正离子检测,MRM模式进行质谱分析。质谱检测工作参数如下:DL 250℃;Nebulizing 3 L/min;Heat Block 400℃;Dry Gas 15 L/min;针位-1 mm。用于定量的离子通道分别为m/z 529→487(罗库溴铵)和m/z 256→167(苯海拉明)。
1.5 标准曲线制备精密称取罗库溴铵化学对照品10.04 mg,用70%甲醇溶解并定容于10 mL量瓶中,混合均匀,即得质量浓度为1.004 mg/mL的标准贮备液。取上述罗库溴铵标准贮备液适量,并用70%甲醇稀释成质量浓度为1.004、2.008、5.02、10.04、50.2、100.4、401.6、502 ng/mL的标准工作液,按照质量浓度从低到高依次进样,以罗库溴铵与苯海拉明两者的峰面积的比值(As/Ai,Y)为纵坐标,相应的质量浓度(X)为横坐标,绘制标准曲线,罗库溴铵的标准曲线按(1/X)加权线性回归,标准曲线的相关系数0.999以上。最低检测限的定义为信噪比大于3,最低定量限定为信噪比大于10。
1.6 精密度和准确度取浓度为2.008、50.2、401.6 ng/mL的 低、中、高3种不同质量浓度的罗库溴铵标准溶液,在1 d内连续进样5次,另在连续5 d内每天进样1次,考察日内精密度和日间精密度。另取低、中、高3种不同质量浓度的罗库溴铵标准溶液,各浓度分别配置5份,每份样品测定1次,经标准曲线计算样品浓度,并测定方法准确度。
1.7 体外微透析试验在微透析试验中,由于探针透析膜外部的药物浓度未知,一般通过反透析法测定药物经过半透膜时的流失量来反映动态过程中透析膜的透过量,从而间接计算探针的回收率。 药物在探针中的回收率等于其释放率是利用反透析法测定其回收率的前提,但不是所有药物的释放率总等于其回收率,所以在将反透析法作为罗库溴铵微透析探针回收率的测定方法之前,我们需要通过实验证明反透析法测得的结果与其真实回收率是否一致。体外微透析试验对增量法(反映真实的回收率)和减量法(反映反透析法测得的回收率)测得的回收率进行了比较,为进一步利用微透析进行罗库溴铵体内研究提供依据[15]。
1.7.1 不同流速对探针回收率的影响采用增量法和减量法研究流速对探针回收率的影响。增量法即正透析法,是将微透析探针浸入浓度为200 ng/mL的罗库溴铵溶液中,以0.5、1.0、2.0、3.0、4.0 μL/min灌注空白去离子水,每次更换流速时须平衡30 min,使探针处于稳定状态,待平衡后每隔20 min收集一份透析液,每个流速收集3份,待测。减量法即反透析法,是将微透析探针浸入空白去离子水中,以不同流速0.5、1.0、2.0、3.0、4.0 μL/min灌注罗库溴铵溶液(200 ng/mL),待平衡30 min后每隔20 min收集一份透析液,每个流速收集3份,待测。增量法探针回收率(RR)和减量法探针回收率(RL)分别按公式计算: RR(%)=Cs/C0×100%,RL(%)=(C0-Cs)/C0×100%,其中,C0表示罗库溴铵溶液的初始浓度,Cs表示所测得的透析液中罗库溴铵浓度。
1.7.2 不同药物浓度对回收率的影响采用增量法研究不同质量浓度的罗库溴铵对微透析探针回收率的影响,将探针浸入浓度为(50、200、500 ng/mL)的罗库溴铵溶液中,以2.0 μL/min的流速灌流空白去离子水,每改变一次药物浓度需平衡30 min,待平衡后每隔20 min收集1份透析液,共3份,待测。罗库溴铵的回收率按增量法公式计算。
1.7.3 微透析探针回收率的稳定性采用增量法研究微透析探针回收率的稳定性,将探针浸入浓度为200 ng/mL的罗库溴铵溶液中,以2.0 μL/min的流速灌流空白去离子水,在收集样品之前,先平衡30 min,使探针处于一个较稳定状态,然后每隔20 min收集一份透析液,若收集8 h。分别测定样品,计算回收率。
1.8 在体回收率测定 1.8.1 血液微透析探针植入手术雄性SD大鼠来自上海斯莱克实验动物有限公司,许可证号为SCXK(沪)2012-0002,体质量为190~220 g,按1.25 g/kg的剂量腹腔注射20%乌拉坦麻醉,将大鼠置于恒温(37℃)加热板上。 仰位固定,颈部两侧剪开皮肤分离暴露颈静脉,用手术线结扎颈静脉远心端防止出血;将引导管向心插入颈静脉,再将微透析探针沿引导管插入颈静脉,移除引导管,结扎固定微透析探针。整个操作过程中灌流空白去离子水保持探针膜处于湿润状态。探针植入手术完成后,以去离子水为灌流液,灌流速度2 μL/min。灌流平衡1 h左右,使插管周围局部血流量恢复正常。之后收集空白样品3份,时间间隔为20 min,作为阴性干扰试验样品。
1.8.2 血液微透析探针回收率测定采用反透析法测定同心圆微透析探针的在体回收率,验证体外与体内环境下探针的回收率是否相近。取6只雄性SD大鼠,体质量在190~220 g,将微透析探针植入大鼠血管中,连接蠕动泵,以质量浓度100 ng/mL的罗库溴铵溶液为灌流液,灌流速度2 μL/min。收集样品之前先平衡30 min,使探针处于一个较稳定状态,待平衡后每隔20 min收集一份透析液,收集3份。体内反透析法探针回收率按减量法公式计算。
1.8.3 肌肉微透析探针植入手术雄性SD大鼠,体质量在190~220 g,按1.25 g/kg的剂量腹腔注射20%乌拉坦麻醉,将大鼠置于恒温(37℃)加热板上。仰位固定,将穿刺针针头平行插入其一侧后肢肌肉,然后将线性探针沿穿刺针针头平行植入肌肉,取出穿刺针针头将线性透析探针膜留于大鼠肌肉组织中,并将探针结扎固定。以去离子水为灌流液,灌流速度2 μL/min。灌流平衡1 h左右,使插管周围局部血流量恢复正常。之后收集空白样品3份,时间间隔为20 min,作为阴性干扰试验样品。
1.8.4 肌肉微透析探针回收率测定采用反透析法测定线性微透析探针的在体回收率,验证体外与体内环境下探针的回收率是否相近。 取6只雄性SD大鼠,体质量在190~220 g,将微透析探针植入大鼠肌肉中,连接蠕动泵,以质量浓度100 ng/mL的罗库溴铵溶液为灌流液,灌流速度2 μL/min。收集样品之前,先平衡30 min,使探针处于一个较稳定状态,待平衡后每隔20 min收集一份透析液,收集3份。体内反透析法探针回收率按减量法公式计算。
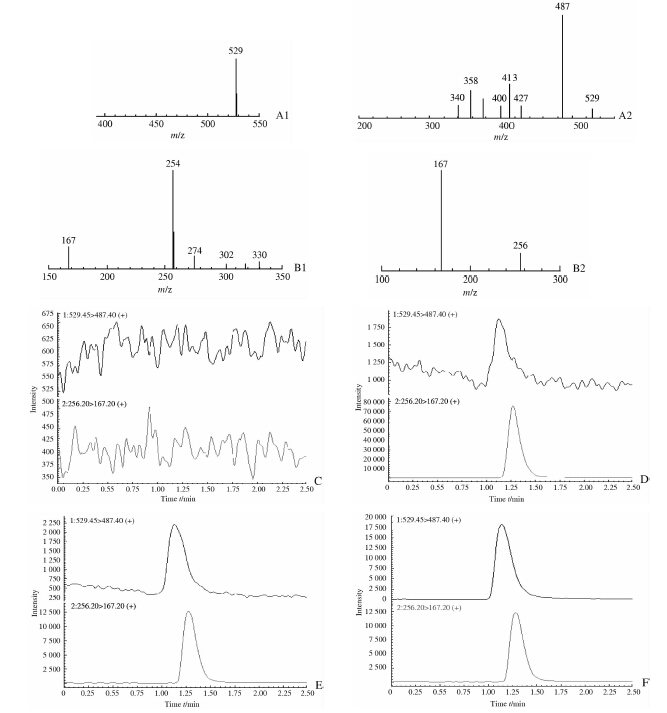
2 结 果 2.1 透析液样品的LC-MS/MS分析 采用LC-MS/MS方法测定透析液样品中罗库溴铵浓度,罗库溴铵和内标苯海拉明分析特异性强,分离效能高,典型色谱图见图 1。 本实验条件下罗库溴铵的保留时间约为1.1 min,苯海拉明的保留时间约为1.3 min,通道之间没有串扰,相应色谱峰理论塔板数均大于5 000,LLOQ定量信噪比大于10。定量分析标准曲线方程为: Y=0.028 11X-0.016 88(r2=0.999 7),线性范围为1.004~502 ng/mL。罗库溴铵最低定量限为1.004 ng/mL(S/N>10)。2.008、50.2、401.6 ng/mL的罗库溴铵标准溶液日内精密度RSD分别为1.56%、1.42%、1.83%,日间精密度RSD分别为3.61%、1.31%、1.58%,均小于5%,表明方法精密度良好。2.008、50.2、401.6 ng/mL的罗库溴铵标准溶液的准确度分别为102.07%、100.94%、99.30%,RSD分别为2.39%、1.57%、1.39%,标准偏差均小于5%,表明方法准确度良好。
|
图 1 LC-MS/MS分析典型色谱图 Fig 1 Typical chromatogram of rocuronium and diphenhydramine by LC-MS/MS Channel 1 is for internal standard and channel 2 is for rocuronium; A1: First class mass spectrum of rocuronium; A2: Second order mass spectrum of rocuronium; B1: First class mass spectrum of diphenhydramine; B2:Second order mass spectrum of diphenhydramine; C: Microdialysis blank sample; D:Internal standard(IS) solution; E:Rocuronium lower limit of quantitation (1 ng/mL) and IS (10 ng/mL); F:Rocuronium medium concentration quality control (50 ng/mL) and IS (10 ng/mL) |
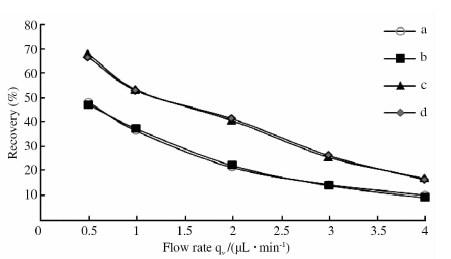
同时应用增量法和减量法考察不同流速(0.5、1.0、2.0、3.0、4.0 μL/min)对同心圆探针和线性探针回收率影响。结果随着流速的增大罗库溴铵的回收率呈下降趋势(图 2)。在同一流速条件下,同一探针增量法和减量法所测得的探针回收率基本一致,这为反透析法测定罗库溴铵体内探针回收率提供了依据。
|
图 2 流速对探针回收率的影响 Fig 2 The influence of flow rate on the probe recovery a: Concentric cannula probe,incremental; b: Concentric cannula probe,reduction; c: Linear probe,incremental; d: Linear probe,reduction |
采用增量法考察50、200、500 ng/mL的罗库溴铵标准溶液,同心圆探针回收率分别为(23.53±2.33)%、(25.09±3.62)%、(21.78±0.92)%;线性探针的回收率分别为(44.31±1.25)%、(42.47±1.86)%、(43.20±1.01)%。
结果表明,当以2 μL/min的流速灌注微透析探针时,在3种不同药物浓度的透析媒介中,同心圆探针和线性探针的回收率均保持相对稳定,表明在一定的浓度范围内探针的回收率与浓度无关。
2.4 试验过程中微透析探针回收率稳定性考察结果表明,灌流速度为2.0 μL/min时同心圆探针和线性探针的回收率在8 h内保持稳定,平均回收率分别为23.16%、42.79%,RSD%分别为4.75%、4.41%,具有良好的稳定性。
2.5 微透析探针在体回收率的测定结果结果显示同心圆探针和线性探针在SD大鼠体内的回收率分别为(18.45±0.35)%、(42.96±0.75)%。采用反透析法测定罗库溴铵体内与体外探针回收率差别不大,这一结果为反透析法作为测定罗库溴铵体内探针回收率提供了重要的实验依据。
3 讨 论探针的回收率测定是将微透析技术应用于药物动力学研究的一个关键问题。影响探针回收率的因素有很多,包括细胞外几何结构、透析膜、对流因素、温度、灌流速度、探针植入等;就探针本身而言,透析膜和灌流速度是主要影响因素。因此,对于微透析取样技术,有必要对探针的回收率及重要的影响因素进行校正。
灌流速度的大小直接影响到探针回收率的高低,灌流速度越快,其流经半透膜时膜内外药物的平衡时间就越短,导致回收率降低。在体内微透析试验中,体内探针回收率的测定只能通过减量法(反透析法)实现,而体内药物浓度的测定是通过增量法进行的。同时采用增量法与减量法考察不同流速对同心圆探针和线性探针回收率的影响是很有必要的。
体内微透析试验持续的时间往往比较长,同一根探针常常需要连续取样几个小时,如果在长时间取样过程中探针回收率发生较大的变化,那就会失去微透析技术本身的意义,有必要考察罗库溴铵探针回收率的稳定。
由于动物体内的药物实际浓度是未知的,所以探针真正的体内回收率是无从测得的。体外回收率实验已经证明,相同条件下,增量法(正透析)与减量法(反透析)测得的探针回收率相差不大,说明反透析法测得的回收率可以代替增量法进行体内校正。但是体内微透析探针所处的环境一般比较复杂,减量法测得的回收率并不一定与体外测得的相近[16]。需要进一步采用反透析法对同心圆探针和线性探针在SD大鼠血管和肌肉内的回收率进行研究。
本文基于自制同心圆探针和线性探针,通过对微透析探针体外回收率和在体回收率主要影响因素的研究,说明了体外回收率的测定可用于验证罗库溴铵微透析回收率的浓度无关性,这是微透析探针应用于在体取样测定药物真实浓度的前提条件;体外微透析试验增量法(反映真实的回收率)和减量法(反映反透析法测得的回收率)测得回收率结果的一致性,反映了反透析法测定药物体内回收率的可行性及合理性;通过反透析法证实罗库溴铵体内探针回收率与体外探针回收率的相似性,由此可以推断在体实际药物浓度。
本实验对灌流速度、采样量及采样时间等微透析参数进行了初步的研究,结果表明,流速与回收率成反比,但是最佳的流速取决于最佳的取样量,不应单纯提高回收率而选择低流速,过低的流速需要较长的采样时间,将会导致丢失部分浓度变化的详细信息。综合考虑回收率、流速、取样体积等因素,本研究在体外实验中最终选择了2 μL/min的流速、20 min的取样时间间隔,样品收集量为40 μL。这些参数可作为罗库溴铵血液和肌肉微透析参数选择的参考,但其最佳值还要根据具体的体内研究结果才能最终确定。
| [1] | Plock N, Kloft C. Microdialysis-theoretical background and recent implementation in applied life-sciences[J]. Eur J Pharm Sci,2005,25:1-24. |
| [2] | 徐 铭, 李范珠. 微透析取样技术及其在体内药物分析中的应用[J]. 药物分析杂志,2006,26:1030-1034. |
| [3] | Höcht C, Opezzo J W, Taira C. Validation of a new intraarterial microdialysis shunt probe for the estimation of pharmacokinetic parameters[J]. J Pharm Biomed Anal,2003,31:1109-1117. |
| [4] | Davies M I, Cooper J D, Desmond S S, Lunte C E, Lunte S M. Analytical considerations for microdialysis sampling[J]. Adv Drug Deliv Rev,2000,45(2-3):169-188. |
| [5] | 吴兆恩,王丹巧. 多位点微透析技术在药代动力学研究中的应用[J]. 中国中药杂志,2010:1765-1768. |
| [6] | Brunner M, Derendorf H, Muller M. Microdialysis for pharmacokinetic/pharmacodynamic characterization of anti-infective drugs[J]. Curr Opin Pharmacol,2005,5:495-499. |
| [7] | Delacher S, Derendorf H, Hollenstein U, Brunner M, Joukhadar C, Hofmann S, et al. A combined in vivo pharmacokinetic-in vitro pharmacodynamic approach to simulate target site pharmacodynamics of antibiotics in humans[J]. J Antimicrob Chemother,2000,46:733-739. |
| [8] | Höcht C, Opezzo J A W, Taira C A. Applicability of reverse microdialysis in pharmacological and toxicological studies[J]. J Pharmacol Toxicol Methods,2007,55:3-15. |
| [9] | 邱 飞, 严 慧, 刁 勇. 罗库溴铵的合成工艺研究[J]. 海峡药学,2011(7):213-215. |
| [10] | 王 丹, 石力夫, 胡晋红. 微透析技术探针回收率的影响因素研究进展[J]. 国际药学研究杂志,2008,35:261-266. |
| [11] | 徐红燕, 汤 湛, 王 俏, 张望刚. 川芎嗪体内外微透析回收率实验研究[J]. 中国药学杂志,2012(21):1750-1753. |
| [12] | 马 博, 孙桂波, 李 明, 孙晓波. 钩藤碱微透析探针回收率测定及影响因素研究[J]. 中国新药杂志,2012(20):2371-2375. |
| [13] | Wang C, Li S, Tang Y J, Wang S W, Zhang Y L, Fan G R, et al. Microdialysis combined with liquid chromatography-tandem mass spectrometry for the determination of levo-tetrahydropalmatine in the rat striatum[J]. J Pharm Biomed Anal,2012,64-65:1-7. |
| [14] | Sun N,Wen J, Lu G C, Hong Z Y, Fan G R,Wu Y T,et al. An ultra-fast LC method for the determination of iodiconazole in microdialysis samples and its application in the calibration of laboratory-made linear probes[J]. J Pharm Biomed Anal,2010,51:248-251. |
| [15] | 晏亦林, 叶 勇, 周莉玲, 林晓珊. 磷酸川芎嗪微透析体外回收率的研究[J]. 中药新药与临床药理,2008,19:117-119. |
| [16] | 王利胜, 石宗丰, 郭 琦, 刘宏伟, 赖宝林. 川芎嗪、阿魏酸微透析体外回收率及体内稳定性的研究[J]. 中成药,2011(2):304-308. |
 2015, Vol. 36
2015, Vol. 36


