2. 重庆医科大学附属第二医院药剂科, 重庆 400010
2. Department of Pharmacy, Second Affiliated Hospital of Chongqing Medical University, Chongqing 400010, China
溴新斯的明(neostigmine bromide,NB)是一种可逆性的抗胆碱酯酶药,可抑制乙酰胆碱酯酶(AChE)的活性而发挥完全拟胆碱作用,对骨骼肌及胃肠道平滑肌兴奋作用较强[1],NB还可用于对抗竞争性神经肌肉阻滞药过量时的毒性反应[2]。临床主要用于治疗重症肌无力、手术后功能性肠胀气及尿潴留等,但NB生物利用度低、半衰期短,长期频繁给药导致体内血药浓度波动大,容易发生不良反应。
多囊脂质体(multivesicular liposomes,MVLs)是英国Skyepharma PLC公司于1983年研制的一种新型脂质体,采用Depofoam技术(DepofoamTM)主要将亲水性药物包封于多个不连续的囊泡中,药物从其中一个囊泡破裂释放而其他囊泡仍维持完整结构包封药物,从而使药物具有缓释长效的作用,同时能够克服药物生物利用度低、半衰期短等缺点[3, 4],多用于注射给药。我们前期将NB制备成溴新斯的明多囊脂质体(neostigmine bromide multivesicular liposomes,NB-MVLs)[5],使药物具有缓释长效的作用,以延长药物半衰期,减少给药次数,提高药物生物利用度,减少不良反应的发生,提高患者顺应性。目前尚无对NB-MVLs药代动力学的相关报道,本研究考察其在大鼠体内的药代动力学特征,为NB-MVLs的进一步研究提供参考依据。 1 材料和方法 1.1 材料 1.1.1 药品与试剂
NB-MVLs(自制[5],含量为22.98 mg/L);NB注射剂(自制,含量为22.98 mg/L); NB对照品(武汉远城科技发展有限公司,纯度≥99.6%);溴吡斯的明(武汉远城科技发展有限公司,纯度≥99.6%);乙腈、庚烷磺酸钠为色谱纯,其余试剂均为分析纯。 1.1.2 仪器与设备
LC-2010A HT 液相色谱仪(日本岛津公司);PHS-3C型PH测定仪(上海精科仪器有限公司);TGL-16B高速台式离心机(江苏省金坛市大地自动化仪器厂);TDL80-2B离心机(上海安亭科学仪器厂)。 1.1.3 动物
12只健康SD大鼠,雌雄各半,体质量(220±20)g,购自重庆医科大学实验动物管理中心 [许可证号:SYXK(渝)2012-0001]。 1.2 给药方法
将12只健康SD大鼠随机平均分成受试组和参比组,2组均于实验前禁食12 h,并在给药前取空白血样,受试组大鼠经皮下注射NB-MVLs受试制剂,参比组大鼠经皮下注射等量的NB参比制剂,给药剂量均为0.15 mg/kg。 1.3 样品的收集
受试组和参比组于给药后 5 min、30 min、1 h、2 h、4 h、6 h、8 h、12 h、24 h、36 h、 48 h、72 h从大鼠眼底取血0.3 mL,将收集的血液样品分别置于事先装有适量肝素的2 mL离心管内,(2 390.6 ×g)离心10 min,离心结束后收集上层血浆备用。 1.4 样品的处理和制备
精密吸取100 μL血浆样品,依次加入苦味酸氢氧化钠溶液 (0.1 mol/L,pH 7.0) 50 μL、水饱和二氯甲烷适量、磷酸二氢钠溶液 (0.1 mol/L) 40 μL、溴吡斯的明溶液(320 mg/L)10 μL,混匀,离心10 min (597.7×g),取有机相置离心管中,加入三丁基氯化铵溶液(0.1 mol/L)100 μL混匀后离心2 min (597.7×g),取水相挥干,加50 μL流动相再次溶解,溶解完全后取20 μL于高效液相色谱仪分析。 1.5 RP-HPLC色谱条件[6]
溴吡斯的明为内标;色谱柱选用Lichrospher C18 (250 mm×4.6 mm,5 μm);庚烷磺酸钠缓冲液(磷酸调节pH至3.0)-乙腈(77∶23)为流动相;柱温为30℃;进样量为20 μL;流速为1.0 mL/min;紫外检测波长为260 nm。 1.6 数据处理和统计学方法
根据所测得的NB血药浓度-时间数据,绘制血药浓度-时间曲线。分别采用药动学软件DAS 2.1.1和统计矩法将实验数据进行拟合,计算房室模型和非房室模型时NB-MVLs和NB的主要药动学参数,根据公式F(相对生物利用度)=AUC(test)/AUC(reference)×100%计算NB-MVLs的生物利用度。达峰时间 (peak time,Tmax)和峰浓度 (peak concentration,Cmax) 采用实测值。 2 结 果 2.1 方法学考察
分别精密吸取空白血浆100 μL,精密量取NB对照品适量,分别配制成NB浓度为0.05、0.1、0.5、1、2、5、8 mg/L的系列标准溶液。按1.4项下条件操作,记录色谱图。以标准溶液浓度C为横坐标,以待测药物与内标溶液峰面积的比值A(Ax/As)为纵坐标进行线性回归,得回归方程A=0.033 2C + 0.076 3,r=0.999 2(n=5),结果表明,NB在血浆中的浓度在0.05~8 mg/L范围内峰面积比A(Ax/As)与浓度C呈良好的线性关系。
低(0.05 mg/L)、中(2.08 mg/L)、高(7.96 mg/L)3个浓度样品溶液的日内精密度(RSD)分别为3.65%、2.26%、1.19%,日间RSD分别为2.55%、1.69%、1.33%,RSD均小于5%,符合含量测定要求。
低(0.05 mg/L)、中(2 mg/L)、高(8 mg/L)3个浓度的方法回收率分别为(89.73±2.29)%、(96.57±2.47)%、(97.67±0.80)%,提取回收率分别为(88.73±2.49)%、(90.57±1.58)%、(93.67±1.87)%,方法回收率与提取回收率均大于85%,表明该方法精密度高、准确度好,能满足分析要求。
血浆样品在室温下放置2 h、6 h及-20℃下放置3 d、7 d内测定NB含量的RSD均小于5%,表明样品在室温下放置6 h和-20℃放置7 d均稳定。 2.2 大鼠体内药动学结果 2.2.1 平均血药浓度-时间曲线的绘制
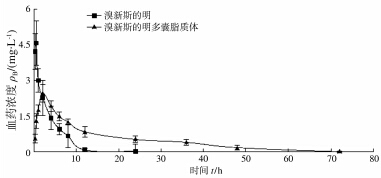
SD大鼠单剂量注射NB注射剂和NB-MVLs后,以药物浓度对时间作图,即得血药浓度-时间曲线,见图 1。
|
图 1 溴新斯的明多囊脂质体及溴新斯的明注射后药时曲线图 n=6,x±s |
由图 1看出,SD大鼠分别注射NB和NB-MVLs后,参比试剂NB在大鼠体内无吸收过程,只有分布和消除过程,在药物快速分布达平衡后消除开始,药物经时过程中血药浓度波动大且呈下降趋势,在约12 h后大鼠体内的血药浓度接近于0。受试制剂NB-MVLs 在大鼠体内平稳缓慢地释放药物,在约2 h内药物完成分布过程,血药浓度上升至峰值(约2.5 mg/L),在此后NB-MVLs仍在持续缓慢地释放药物,药物浓度波动较小,在12 h左右药物浓度约为0.8 mg/L。 2.2.2 主要药动学参数
首先计算非房室模型参数,药代数据采用统计矩法计算非房室模型,非房室模型主要药动学参数见表 1。NB-MVLs非房室模型的Tmax、Cmax与房室模型的Tmax、Cmax一致,MRT0-∞是NB的6.18倍,NB-MVLs和NB的AUC0-∞分别为(40.62±8.96) mg·h/L和 (16.01±5.21) mg·h/L,计算得到NB-MVLs的相对生物利用度是NB的253.72%。
|
|
表 1 溴新斯的明多囊脂质体及溴新斯的明的药动学参数 |
根据Akaike’s information criterion(AIC)最小原则和R2拟合度结果判断最优房室模型,以AIC最小和R2拟合度越接近1的拟合模型为优。拟合结果显示NB-MVLs与NB均符合二室模型,房室模型主要药动学参数见表 1。NB-MVLs和NB经注射给药后,NB-MVLs的Tmax是NB的5.33倍,Cmax是NB的一半左右,t1/2是NB的8.46倍,AUC0-∞分别为(41.21±7.82) mg·h·L-1和(18.11±5.72) mg·h·L-1,计算得到NB-MVLs的相对生物利用度是NB的227.55%。表 1结果表明,采用房室模型和非房室模型分析药动学主要参数所得结果基本一致。 2.2.3 生物等效性分析
AUC0-t、AUC0-∞及Cmax采用DAS 2.1.1软件拟合经对数转换后进行双单侧t检验和[1-2α] 90%可信区间考察。结果NB-MVLs的AUC0-t和AUC0-∞经对数转换后[1-2α] 90%可信区间不在等效标准80%~125%范围内;的Cmax对数转换后[1-2α] 90%可信区间不在等效标准70%~143%范围内;Tmax采用实测值,对Tmax进行Wilcoxon非参数检验,结果表明NB-MVLs和NB有统计学差异(P<0.05),但受试周期和受试个体之间的差异无统计学意义。按照生物等效性标准判定,NB-MVLs与NB不具有生物等效性。 3 讨 论
MVLs是新型的脂质体,它的结构为非同心囊结构,有较大粒径,给药途径多为局部注射给药,而普通脂质体多为血管内给药。NB为亲水性药物,但普通脂质体对亲水性药物包封率低,而MVLs内部含有大量的水相能够克服NB包封率低的缺点。与普通脂质体相比,MVLs有更高的包封率、更好的稳定性及更长的缓释时间,更能提高药物的生物利用度,具有长效缓释作用[7, 8]。因此将NB制成NB-MVLs可以克服NB包封率低、生物利用度低、半衰期短的缺点。
NB-MVLs注射给药后在大鼠体内的Tmax约为2.40 h,是NB的5.33倍,Cmax约为2.49 mg/L,是NB的一半左右,t1/2约15.14 h,约是NB的8.46倍,说明NB-MVLs延长了Tmax、延长了t1/2、降低了Cmax。NB只有分布和消除过程,在药物快速分布达平衡后消除开始,药物血药浓度波动大,药物浓度维持时间短,而NB-MVLs约2 h完成分布过程,达到峰浓度后能够以高浓度长时间维持并缓慢释放药物,NB-MVLs的包封率高,在大鼠体内处置慢,清除率低,使得NB-MVLs具有明显的长效缓释作用,能够平稳缓慢地释放药物,从而可以减少给药次数,有利于提高患者顺应性,体内血药浓度波动较小可以避免因Cmax过高引起的不良反应。
本研究采用房室模型与非房室模型两种拟合方法计算药动学参数,结果表明,NB与NB-MVLs采用房室模型和非房室模型计算得到的主要药动学参数基本一致。经生物等效性分析,NB-MVLs与NB不具有生物等效性,NB-MVLs的生物利用度高于NB。本研究由房室模型和非房室模型的药动学参数计算NB-MVLs的相对生物利用度分别为227.55%和253.72%,熊华蓉等[9]研究发现,NB缓释片在家兔体内的相对生物利用度为115.4%,结果表明NB-MVLs比NB缓释片的相对生物利用度提高得更多。文献报道多囊脂质体可使盐酸纳曲酮和胸腺五肽具有长效缓释作用和提高生物利用度[10, 11]。本实验对NB-MVLs的药动学进行了初步研究,为NB-MVLs的体内研究提供了参考依据。
| [1] | 李 荣.药理学[M].2版.北京:人民卫生出版社,2005:233-236. |
| [2] | Lorenzutti A M, Martin-Flores M,Baldivieso J M, Himelfarb M A, Litterio N J. Evaluation of neostigmine antagonism at different levels of vecuronium-induced neuromuscular blockade in isoflurane anesthetized dogs[J].Can Vet J,2014,55:156-160. |
| [3] | Angst M S, Drover D R. Pharmacology of drugs formulated with Depofoam:a sustained release drug delivery system for parenteral administration using multivesicular liposome technology[J].Clin Pharmacokinet,2006,45:1153-1176. |
| [4] | Davidson E M, Barenholz Y, Cohen R, Haroutiunian S, Kagan L, Ginosar Y. High-dose bupivacaine remotely loaded into multivesicular liposomes demonstrates slow drug release without systemic toxic plasma concentrations after subcutaneous administration in humans[J]. Anesth Analg,2010,110:1018-1023. |
| [5] | 罗 文,赵春景,熊华蓉,李 艺,张景勍.紫外分光光度法测定溴新斯的明多囊脂质体的包封率[J].激光杂志,2013,34:52-53. |
| [6] | 罗 文,谭群友,熊华蓉,赵春景,张景勍.溴新斯的明缓释片的药动学和相对生物利用度研究[J].中国药学杂志,2011,46:1349-1352. |
| [7] | 王晓梅,唐 星,何海冰.多囊脂质体的研究进展[J].中国新药杂志,2006,15:1243-1246. |
| [8] | Mantripragada S.A lipid based depot (DepoFoam technology) for sustained release drug delivery[J].Prog Lipid Res,2002,41:392-406. |
| [9] | 熊华蓉,谭群友,刘碧林,罗 文,张景勍.溴新斯的明缓释片的药动学及相对生物利用度[J].四川大学学报:医学版,2011,42:657-660. |
| [10] | Sun L,Wang T,Gao L,Quan D,Feng D.Multivesicular liposomes for sustained release of naltrexone hydrochloride:design,characterization and in vitro/in vivo evaluation[J].Pharm Dev Technol,2013,18:828-833. |
| [11] | Zuo J,Gong T,Sun X,Huang Y,Peng Q,Zhang Z.Multivesicular liposomes for the sustained release of thymopentin:stability,pharmacokinetics and pharmacodynamics[J].Pharmazie,2012,67:507-512. |
 2015, Vol. 36
2015, Vol. 36


