近年来随着经济发展和生活方式的改变,我国糖尿病发病率不断增加[1],糖尿病主要危害在于各种慢性并发症。其中,糖尿病视网膜病变(diabetic retinopathy,DR)是最常见的糖尿病慢性并发症之一,病理改变主要体现在基底膜增厚、微血管瘤形成、内皮细胞增生、新生血管增殖等,其致盲率极高,严重威胁糖尿病患者的生活质量乃至生命安全[2, 3]。目前,尚未揭示其致病机制,且临床DR治疗手段十分有限,探讨DR的危险因素并早期采取预防措施显得十分必要。因此,本研究着重探讨尿微量白蛋白(urine microalbuminuria,U-ALB)排出量及血纤维蛋白原(fibrinogen,Fb)和血红蛋白(hemoglobin,Hb)在DR发生过程中的可能意义,为后续研究奠定基础。 1 资料和方法 1.1 一般资料
2010年1月至2014年9月我院收治的101例2型糖尿病(T2DM)患者,其中男67例,女34例;平均年龄(48.62±6.51)岁;平均糖尿病病程(16.93±5.08)年。所有病例均符合WHO 1999年的糖尿病诊断标准,DR的诊断及分期依据2002年悉尼国际眼科学术会议制定的糖尿病性视网膜病变国际临床分级标准,排除高血压、青光眼、眼外伤等疾病引起的眼底病变。所有患者均为慢性糖尿病,排除原发性肾脏疾病、肿瘤或自身免疫性疾病、急性感染性疾病、严重心脑血管疾病等。所有入选患者均无糖皮质激素和免疫抑制剂应用史。所有患者均使用胰岛素控制血糖浓度。记录所有患者临床一般资料,包括年龄、病程、吸烟史、身高、体质量、血压等。 1.2 患者分组
根据患者视网膜病变病情分组:无并发症组49例,其中男26例,女23例,平均(53.6±8.34)岁,空腹血糖水平为(7.51±1.57) mmol/L;2型糖尿病并发DR组52例(单纯期38例,增殖期14例),所有患者均经临床确诊,其中男31例,女21例,平均年龄(54.1±7.98)岁,空腹血糖水平为(8.17±2.43)mmol/L。此外还设有正常对照组,健康人50例,其中男27例,女23例,平均年龄(55.2±6.93)岁,对照组所有人员均无心脏病、高血压,临床检测排除糖尿病,所有研究对象均无明确心、肝、肺及肾脏等疾病,无传染病或恶性肿瘤等。3组间年龄、性别等参数差异无统计学意义,具有可比性。 1.3 观察指标的测定 1.3.1 血压及体质指数的检测
记录3组受试者年龄、病程,并均安排测体质量、身高、体质指数(BMI),BMI=体质量(kg)/身高的平方(m2)。测定3组受试者右上肢血压2次,记录收缩压和舒张压,取平均值。 1.3.2 U-ALB水平测定
受试者在收集标本之前避免运动,收集尿液,采用免疫透射法测定尿中U-ALB水平(Nephlometer 100 analyser仪)。 1.3.3 血中Fb、Hb水平测定
抽取3组受试者静脉血,抗凝处理,离心或静置后分离血浆,1份采用全自动生化分析仪(美国雅培公司)和配套试剂、质控产品检测Hb水平;另1份用于检测Fb的表达水平,采用Clauss方法,在Sysmex-CA530血液凝固仪上检测,所用试剂来自美国DadeBehring公司。 1.3.4 血清中脂联素和肿瘤坏死因子α水平检测
采用ELISA试剂盒(Market公司,美国)标准程序检测血清脂联素(adiponectin,APN)和肿瘤坏死因子α (TNF-α)的表达水平,所用酶标仪为SLT.Spectra产品。 1.4 统计学处理
采用SPSS 17.0软件进行分析,计量资料采用 x±s 表示,组间比较采用独立样本t检验,Spearman相关分析U-ALB、Fb、Hb与DR发生是否存在相关性,检验水准(α)为0.05。 2 结 果 2.1 3组受试者临床指标的比较
结果(表 1)表明:空腹条件下,糖尿病患者血糖浓度高于正常对照组,差异有统计学意义(P<0.05);糖尿病患者收缩压和舒张压均高于正常对照组,差异有统计学意义(P<0.05);但是BMI在3组受试者间差异无统计学意义。糖尿病患者血TNF-α水平明显高于正常对照组,而并发DR组患者表达水平远高于无并发症组,差异均具有统计学意义(P<0.05);而血清APN水平随疾病进展逐渐下降,差异均具有统计学意义(P<0.05)。
| 表 1 3组受试者临床指标的比较 Tab 1 Comparison of clinical indices between 3 groups |
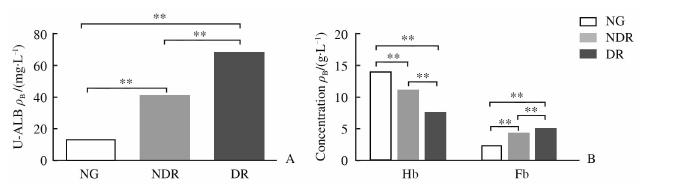 | 图 1 3组受试者U-ALB及血Fb、Hb水平的比较 Fig 1 Comparison of urine U-ALB level and blood Fb and Hb levels in the 3 groupsNG: Normal group (n=50); NDR: Non-diabetic retinopathy (n=49); DR: Diabetic retinopathy (n=52). Hb: Haemoglobin; Fb:Fibrinogen; U-ALB: Urine microalbuminuria. **P<0.01 |
为探讨尿U-ALB及血Fb、Hb水平是否对DR进展有影响,进一步比较了它们在单纯期DR患者和增殖期DR患者体内水平。结果(表 2)表明:尿U-ALB含量和血Fb水平在增殖期DR组高于单纯期DR组,差异均有统计学意义(P<0.01);而Hb水平在单纯期DR组高于增殖期DR组,差异有统计学意义(P<0.01)。
| 表 2 增殖期DR及单纯期DR患者U-ALB及血Fb、Hb的比较 Tab 2 Comparison of urine U-ALB and blood Fb and Hb levels in PDR and NPDR patients |
相关性分析结果(表 3)显示:DR患者尿U-ALB及血Fb、Hb水平与TNF-α、 APN表达均正相关(P<0.05),而与其他临床参数无明显相关(表 3)。
| 表 3 DR患者尿U-ALB及血Fb、Hb水平与临床参数相关性分析 Tab 3 Correlation of urine U-ALB and blood Fb and Hb levels with clinical parameters in DR patients |
T2DM是由基因和环境等多因素间相互作用而导致的一种慢性疾病,该病特点是患者胰岛B细胞功能失调,对胰岛素不敏感进而导致血糖水平失调。临床2型糖尿病患者多发各种并发症,其中DR是最为常见的一种合并症。尽管随着科学技术的进步,在其诊断和治疗上已取得很大进展,但因它极高的致盲率使得2型糖尿病合并DR不仅对患者自身、家庭甚至社会都是一种沉重的负担[2]。DR的发生发展是由糖代谢、脂代谢、细胞因子、炎症反应、遗传背景等多因素的共同作用所致,各因素间可能存在共同的发病基础,也可能相互影响。探讨与DR相关的高危因素,对于临床早期诊断、治疗和提高患者生活质量有着重要意义。
T2DM合并视网膜病变患者往往伴随尿 U-ALB 排泄异常现象,且其异常与DR发生及进展程度之间有相关性。Mohan等[4]研究发现,尿U-ALB在T2DM患者中含量与DR存在相关性,其含量越高预示着DR进展越严重。本研究发现,尿U-ALB在糖尿病患者中含量高于健康对照组,合并DR的T2DM患者显著高于未合并患者;且DR合并组患者中,U-ALB在增殖期DR组患者尿中水平显著高于单纯期DR组。结果提示尿U-ALB含量与DR发生密切相关。
糖尿病是一种慢性炎症疾病,糖尿病的发生会引起Fb表达水平改变,进而改变机体凝血系统,损伤血液纤溶系统功能,最终导致血管硬化和视网膜病变进展[5]。本研究发现,Fb在糖尿病患者体内表达水平高于健康对照组,且合并DR组患者水平高于未合并组,增殖期患者水平高于单纯期患者,提示糖尿病患者血Fb水平与DR发生、进展密切相关。
糖尿病患者多伴随贫血症状,而导致该现象的主要因素是促红细胞生成素和铁含量不足。既往研究[6, 7, 8]表明,在肝受损程度相同的情况下,糖尿病患者贫血发病率比非糖尿病患者高1~2倍,而合并DR的糖尿病患者贫血状态更加严重。本研究结果显示,2型糖尿病患者体内Hb水平低于正常对照组,且合并DR组患者体内Hb水平显著低于无并发症组患者,而在增殖期DR组患者体内,Hb水平下降趋势更明显,提示Hb水平下降与DR发生、发展密切相关。本研究中,DR患者尿U-ALB含量及血Fb、Hb水平与血APN和TNF-α均正相关,提示这3种因子可能协同参与了DR的发生及进展[9]。
综上所述,2型糖尿病患者尿U-ALB含量及血Fb、Hb含量均发生显著变化,在DR合并或增殖期患者体内,这一变化趋势更加明显。动态检测2型糖尿病患者尿U-ALB含量及血Fb、Hb水平,可以为临床预防2型糖尿病合并DR的发生、发展提供重要的指导意义。 4 利益冲突
所有作者声明本文不涉及任何利益冲突。
| [1] | 胡媛媛,曾 臻,潘发明,段振华,冯大洋,李桂兴. 2型糖尿病住院患者心理健康状况及影响因素分析[J].安徽医药, 2010, 14: 1416-1418. |
| [2] | 何斌斌,魏 丽,韩俊峰,李 鸣,刘宇翔,包玉倩.2型糖尿病患者视网膜病变与贫血的关系[J].上海医学, 2012, 35: 20-22. |
| [3] | Lunetta M, Infantone L, Calogero A E. Increased urinary albumin excretion is a matter of risk for retinopathy and coronary heart disease in patients with type 2 diabetes mellitus [J]. Diabetes Res Clin Pract, 1998, 40: 45-51. |
| [4] | Mohan V K, Nithyanandam S, Idiculla J. Microalbuminuria and low hemoglobin as risk factors for the occurrence and increasing severity of diabetic retinopathy [J]. Indian J Ophthalmol, 2011, 59: 207-210. |
| [5] | Le D S, Miles R, Savage P T, Cornell E,Tracy R P,Knowler W C. The association of plasma fibrinogen concentration with diabetic microvascular complications in young adults with early-onset of type 2 diabetes [J]. Diabetes Res Clin Pract, 2008, 82: 317-323. |
| [6] | Terry F C, Loukaci V, Green R F. Cooperative influence of genetic polymorphism on interleukin 6 transcriptional regulation [J]. J Biol Chem, 2000, 275: 18138-18144. |
| [7] | Lunetta M, Infantone L, Calogero A E, Infantone E. Increased urinary albumin excretion is a marker of risk for retinopathy and coronary heart disease in patients with type 2 diabetes mellitus[J].Diabetes Res Clin Pract,1998,40:45-51. |
| [8] | Adamis A P. Is diabetic retinopathy an inflammatory disease?[J]. Br J Ophalmol, 2002, 86: 363-365. |
| [9] | Lampropoulou I T, Stangou M, Papagianni A, Didangelos T, Iliadis F, Efstratiadis G. TNF-α and microalbuminuria in patients with type 2 diabetes mellitus[J].J Diabetes Res,2014,2014:394206. |
 2015, Vol. 36
2015, Vol. 36


