2. 贵州省人民医院心内科, 贵阳 550002
2. Department of Cardiovasology, Guizhou Provincial People's Hospital, Guiyang 550002, Guizhou, China
随着临床永久性起搏器植入数量的攀升,常规右心室起搏后心力衰竭成为临床上一个常见的难题,其解决方法之一是将常规心脏起搏器升级为心脏再同步化治疗(cardiac resynchronization therapy,CRT)[1, 2]。然而,起搏器升级手术不仅是简单的更换脉冲发生器,手术更加复杂,每个细节的处理都关系到手术的成败。本研究入选了6例第二军医大学长海医院心内科起搏器术后心力衰竭升级为CRT的患者,分析其临床资料、手术过程中囊袋和原电极的处理、左心室电极的植入方法和术后随访资料,进而探讨常规心脏起搏器升级的手术时机、手术策略和操作技巧,以提高手术成功率,减少并发症。 1 资料和方法 1.1 一般资料
入选2009年3月至2014年2月在第二军医大学长海医院心内科住院的6例常规起搏器术后心力衰竭患者,男3例,女3例,年龄51~83岁,平均(71.63±12.62)岁,常规心脏起搏器植入术后3~9年,平均(6.50±2.07)年,平均右心室起搏比例80.5%,均属起搏器依赖。其中术前诊断Ⅲ度房室传导阻滞2例,病态窦房结综合征4例;单腔起搏器2例,双腔起搏器4例;原起搏器囊袋位于左侧2例,位于右侧4例;右心室电极均为被动翼状电极,位于右室心尖部,所有患者入院前均已给予最优化的抗心力衰竭药物治疗。入院后完善术前常规检查,平均QRS波群宽度(179.50±9.95) ms,平均左室舒张末期内径(53.12±3.82) mm,左室射血分数(LVEF)为(38.50±4.89)%,纽约心脏病学会(NYHA)心功能分级Ⅲ级4例,Ⅳ级2例。所有患者均符合我国CRT升级适应证[3]。 1.2 方 法
所有患者均给予最优化的抗心力衰竭药物治疗,积极纠正酸碱失衡和电解质紊乱,NYHA Ⅳ级患者至少能平卧2 h以上。术前综合分析患者临床资料,制定手术方案。手术过程:第一步,植入左心室电极。左心室导线植入途径:4例囊袋位于右胸患者2例选择右颈内静脉、2例选择左锁骨下静脉,2例囊袋位于左胸患者选择左锁骨下静脉。切开局部皮肤及皮下组织,穿刺成功后沿钢丝送入冠状静脉窦长鞘,交换冠状窦电极导管进行引导性插管,将长鞘送至冠状窦内。送入经皮冠状动脉腔内成形术(PTCA)导丝及造影球囊逆行造影,寻找合适靶静脉,在左心室电极推送系统的帮助下植入左心室电极于侧静脉或后侧静脉。测试电极起搏阈值、感知、阻抗合格后通过保护袖套固定。第二步,处理原囊袋和电极。小心切开囊袋,避免损伤原电极导线,检测原右心房、右心室电极,功能良好者予留用,参数不合格者予以拔除,植入新电极,并连接至三腔起搏器相应插孔。对起搏器依赖患者术中使用异丙肾上腺素维持或连接起搏器测试仪并起搏,防止出现阿斯综合征。第三步,接入左心室电极。若左心室电极植入血管并不在原囊袋附近,需建立皮下隧道。自左心室电极穿刺处至起搏器囊袋处建立皮下隧道,将左心室电极通过皮下隧道牵引至原起搏器囊袋处,接入三腔起搏器,若无右心房电极,用堵头堵住右心房电极插孔。放入囊袋包埋,逐层缝合,对皮,生物胶水粘合伤口,沙袋压迫囊袋处4~6 h。术后对患者行起搏器参数优化。术中、术后常规使用抗生素24~48 h (头孢拉定2 g,2次/d,静脉滴注)。术后3 d及3个月行心电图、心脏超声、BNP检查,再次评定NYHA心功能分级。 1.3 统计学处理
采用SPSS 17.0软件,计量资料以 x±s表示,计数资料用百分率表示,对升级术前、术后的随访指标数据采用配对t检验,检验水准(α)为0.05。
2 结 果
6例患者中单腔起搏器2例,双腔起搏器4例,原 起搏器囊袋位于左侧2例,位于右侧4例。按照术前制定的手术策略,升级时左心室电极植入途径为右颈内静脉2例,均走行于右颈内静脉至右胸前皮下隧道(图 1A);植入途径为左锁骨下静脉4例,其中2例走行于左锁骨下静脉至右胸前皮下隧道(图 1B),2例于穿刺处直接连接脉冲发生器。原电极导线一共10根,拔除2根,续用8根。所有患者均成功完成升级手术,无手术相关并发症。
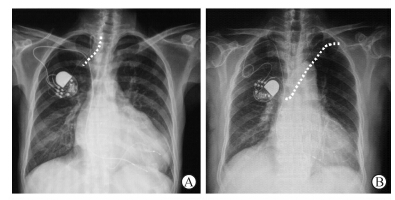 | 图 1 术后胸片显示左心室电极走行于皮下隧道 A:左心室电极走行于右侧颈内静脉至右胸前皮下隧道(白色虚线所示);B:左心室电极走行于左锁骨下静脉至右胸前皮下隧道(白色虚线所示) |
术后随访显示,与入院时相比,术后3 d QRS波时限缩短(P<0.05),BNP降低(P<0.05),左室舒张末期内径、LVEF和NYHA心功能分级无明显变化;术后3个月,QRS波时限缩短(P<0.05),左室舒张末期内径缩小(P<0.05),LVEF改善(P<0.05),NYHA心功能分级平均提高一个等级,BNP降低(P<0.05)。详见表 1。
|
|
表 1 升级治疗前后心功能相关指标比较 |
多项研究表明,对于心力衰竭或心脏失同步化患者,CRT可通过双心室起搏,再同步左右心室起搏顺序,逆转左心室重构,延缓心脏功能的恶化,降低心力衰竭住院率和死亡率,并且随着CRT植入时间的延长,这种益处可持续存在或继续增加[4, 5, 6, 7]。因此,为恢复常规起搏器术后心力衰竭患者的左右心室同步及左心室内收缩同步,有必要将常规右心室心尖起搏升级为CRT。2008年中华医学会心电生理和起搏分会CRT工作组会议纪要[3]提出,出现以下情况应该尽早升级为双心室起搏:(1)慢性心力衰竭,心功能Ⅲ~Ⅳ级,LVEF≤35%;(2)心室依赖起搏;(3)超声检查发现心脏收缩不同步。在原起搏器电池耗竭时考虑升级为双心室起搏:(1)心功能Ⅱ级;(2)LVEF降低;(3)心室收缩不同步;(4)一般情况尚可,预计存活期较长。2012年美国和欧洲心力衰竭器械治疗指南则认为,在最优化药物治疗的基础上,LVEF≤35%、心室起搏比例>40%的患者可植入CRT或升级为CRT。而对于心力衰竭合并房颤患者,目前各类指南均更加强调LVEF≤35%和术后双室起搏比例接近100%,而较少关注NYHA心功能分级。对不能保证双室起搏比例的房颤患者建议先行房室结消融,造成人为的Ⅲ度房室传导阻滞,或采用药物控制自身心室率,以保证术后双心室起搏比例接近100%。
起搏器升级不是简单的更换脉冲发生器,而是涉及术前、术中、术后护理等方面的系统工程[8],其中左心室电极的植入是升级手术的难题。电极植入血管途径理论上可以和原电极导线共用,但在一项研究中发现,131例患者植入起搏器电极,随访44个月后32.9%患者出现静脉阻塞(DSA造影显示管腔狭窄>60%定义为阻塞),导致原电极拔除和新的电极导线植入困难[9]。因此术中必要时可保留原电极导线,重新选择新的血管途径植入新电极。本研究的6例患者,升级时左心室电极走行于右颈内静脉2例,均走行于右颈内静脉至右胸前皮下隧道;走行于左锁骨下静脉4例,其中2例走行于左胸至右胸皮下隧道,2例于穿刺处直接连接脉冲发生器,植入过程均顺利。10根原电极经测试8根功能良好,予以续用,2根由于测试起搏阈值较高,予以拔除,未发生相关并发症。
在常规起搏器术后心力衰竭升级为CRT过程中,需要重点把握以下几个问题:(1)左心室电极的植入路径。右侧锁骨下静脉途径因为血管路径转折较多,不利于电极输送鞘的送达,不便采用。左颈内静脉途径容易在颈部遗留瘢痕,影响美观,同时术后患者颈部运动幅度较大,加上衣领摩擦,可能会出现电极植入部位皮肤磨损引起感染等后果,不是首选。因此首选途径为左侧头静脉或左锁骨下静脉,该途径自穿刺部位至靶血管路径血管呈“C”形或半圆型弯曲,利于冠状静脉窦电极导管和冠状静脉窦长鞘送达。(2)建立皮下隧道。若原囊袋位于左侧且无囊袋感染,如左心室电极从左侧头静脉或锁骨下静脉植入顺利,则不需要制作皮下隧道,可直接将左心室电极连接脉冲发生器。若囊袋位于右侧,采用右颈内静脉途径植入左心室电极,则需要制作沿右颈内静脉穿刺处至囊袋处皮下隧道。若原囊袋位于右侧且采用左侧头静脉或左锁骨下静脉植入途径,则需要制作从左胸前至右侧囊袋处皮下隧道,将左心室电极牵引至右侧囊袋。另外,若右侧囊袋感染,一般需要更换囊袋位置、弃用原电极并予以拔除,重新在左侧制作新囊袋并从左侧静脉植入左心室电极。(3)原电极导线和囊袋的处理。如发生非脉冲发生器原因的起搏失夺获、导线阈值升高、脱位或存在电极相关并发症时应该拔除原电极;对拔除困难者,或拔除出现并发症可能性大、囊袋及导线周围瘢痕严重难以剥离拟拔除导线者予以保留;由于电池耗竭等原因导致起搏阈值增高但仍在可接受范围可续用[10]。需要说明的是,由于数根电极导线在囊袋附近固定缠绕,加上瘢痕的生长,术中原囊袋的切开相对麻烦,可在术前透视留影,尽量在远离电极位置切开分离囊袋,这些原则对于起搏器升级和更换都是一致的。拔除电极最常见的并发症是心肌或血管损伤,甚至心脏穿孔,需要手术医师熟练掌握电极拔除的技巧。
本研究中6例患者经升级后,随访观察发现QRS时限缩短,BNP表达降低,左心室舒张末期内径减小,LVEF提高,心功能改善,活动耐力提高,左心房大小无明显变化,显示升级CRT为常规起搏器术后心力衰竭治疗的有效手段。这与国外报道[1, 2, 4, 5, 11]相一致。Rickard等[12]研究发现,QRS时限缩小率是预测升级起搏器升级后有无反应的独立预测因子。在我们的研究中,对比术前,术后即刻QRS波群时限即缩短,提示CRT治疗可以立即改善左右心室收缩不同步,使心脏运动更加协调,提高做功效率,减少刺激神经内分泌激活的因素,阻断“心功能恶化—神经内分泌激活—心脏重构—心功能恶化”的恶性循环,发挥延缓和逆转心脏重构的作用。
总之,对于具备起搏器术升级CRT手术适应证的患者,熟练掌握手术的策略和术中操作技巧是将常规起搏器升级为CRT成功的关键。升级术后能显著提高左右心室收缩的同步性,改善心功能,提高生活质量。
4 利益冲突
所有作者声明本文不涉及任何利益冲突。
| [1] | De Sisti A, Márquez M F, Tonet J, Bonny A, Frank R, Hidden-Lucet F. Adverse effects of long-term right ventricular apical pacing and identification of patients at risk of atrial fibrillation and heart failure[J]. Pacing Clin Electrophysiol, 2012, 35:1035-1043. |
| [2] | Cleland J G, Daubert J C, Erdmann E, Freemantle N, Gras D, Kappenberger L, et al. The effect of cardiac resynchronization on morbidity and mortality in heart failure[J]. N Engl J Med, 2005, 352:1539-1549. |
| [3] | 陈柯萍, 黄德嘉, 张 澍, 王方正.常规起搏适应证的患者何时需要升级为双心室起搏——中华医学会心电生理和起搏分会心脏再同步治疗工作组会议纪要[J]. 中华心律失常学杂志, 2008, 12: 159-160. |
| [4] | Moss A J, Hall W J, Cannom D S, Klein H, Brown M W, Daubert J P, et al. Cardiac-resynchronization therapy for the prevention of heart-failure events[J]. N Engl J Med, 2009, 361:1329-1338. |
| [5] | Goldenberg I, Hall W J, Beck C A, Moss A J, Barsheshet A, McNitt S, et al. Reduction of the risk of recurring heart failure events with cardiac resynchronization therapy: MADIT-CRT (Multicenter Automatic Defibrillator Implantation Trial With Cardiac Resynchronization Therapy)[J]. J Am Coll Cardiol, 2011, 58:729-737. |
| [6] | Cleland J G, Daubert J C, Erdmann E, Freemantle N, Gras D, Kappenberger L, et al. Longer-term effects of cardiac resynchronization therapy on mortality in heart failure [the CArdiac REsynchronization-Heart Failure (CARE-HF) trial extension phase][J]. Eur Heart J, 2006, 27:1928-1932. |
| [7] | Akerström F, Pachón M, Puchol A, Jiménez-López J, Segovia D, Rodríguez-Padial L, et al. Chronic right ventricular apical pacing: adverse effects and current therapeutic strategies to minimize them[J]. Int J Cardiol, 2014, 173:351-360. |
| [8] | 沈法荣, 张 澍. 起搏器更换或升级:经验与指南[J]. 中华心律失常学杂志, 2012, 16: 166-167. |
| [9] | Oginosawa Y, Abe H, Nakashima Y.The incidence and risk factors for venous obstruction after implantation of transvenous pacing leads[J]. Pacing Clin Electrophysiol, 2002, 25:1605-1611. |
| [10] | 沈法荣, 王志军, 黄抒伟, 陈建明, 凌 锋.心脏再同步治疗起搏器更换时原左心室导线的处理[J]. 中华心律失常学杂志, 2007, 11: 249-251. |
| [11] | Fröhlich G, Steffel J, Hürlimann D, Enseleit F, Lüscher T F, Ruschitzka F, et al. Upgrading to resynchronization therapy after chronic right ventricular pacing improves left ventricular remodelling[J]. Eur Heart J, 2010, 31:1477-1485. |
| [12] | Rickard J, Cheng A, Spragg D, Cantillon D, Chung M K, Tang W H, et al. QRS narrowing is associated with reverse remodeling in patients with chronic right ventricular pacing upgraded to cardiac resynchronization therapy[J]. Heart Rhythm, 2013, 10:55-60. |
 2015, Vol. 36
2015, Vol. 36


