外阴阴道假丝酵母菌病(vulvovaginal candidiasis,VVC)是妇科常见的局部感染性疾病,有70%~75%的育龄期妇女一生中至少罹患1次VVC[1]。VCC发病率高且容易复发,在1年内发作4次以上且有临床症状的即为复发性外阴阴道假丝酵母菌病(RVVC)[2]。RVVC发病率为5%~8%[3],严重影响女性的身心健康。环吡酮胺阴道乳膏是治疗VVC的新型制剂,既往研究显示该药对RVVC有明显的疗效且复发率低[4],但迄今鲜见大样本的研究报道,特别是论证强度高的临床试验。为此,我们采用随机对照试验,研究环吡酮胺阴道乳膏对VVC的疗效及用药后复发情况,以期对临床治疗有所助益。
1 对象和方法 1.1 研究对象 1.1.1 病例来源本研究经第四军医大学西京医院医学伦理委员会批准。2012年1月至2013年10月在我院妇科门诊收集VVC病例。向所有VVC患者告知试验方案,同意接受者列入研究病例。
1.1.2 纳入标准依据患者的临床症状和体征,以及阴道分泌物镜下检查或培养的结果,见到芽孢及菌丝即明确诊断。年龄18~70周岁,既往病程不足1个月至1年以上,单纯性VVC和复杂性VVC均可入选。患者来院前没有接受其他抗真菌药物治疗,且血常规、尿常规、肝肾功能和血糖均正常。
1.1.3 排除标准有糖尿病史者;妊娠期、哺乳期及口服避孕药的妇女;近2周内连续应用抗生素者、合并心肺肾疾病、重度贫血、肝功能异常者;已知对抗真菌药物有不良反应者、阴道及宫颈畸形者以及盆腔恶性病变者;来院前应用过环吡酮胺的各种制剂、硝酸咪康唑栓或其他抗真菌阴道及口服制剂治疗者;有手脚真菌及阴道滴虫感染者。
1.1.4 剔除标准治疗过程中有性生活者或观察期间性生活未使用避孕套者退出试验;自行口服抗真菌药物者退出试验;剔除支原体、衣原体培养阳性者;以及依从性差,不按试验方案完成试验者。
1.2 研究方法连续入选的病例由专人按随机数字表分组;各位经治的主治医师对患者的实际分组及其用药不知情,并且不参与后期的统计学处理。由专人按分组情况将环吡酮胺阴道乳膏(78 g/支,含环吡酮胺0.78 g/支;意大利多帕药业有限公司,批准文号: H20090920)及硝酸咪康唑栓(200 mg/粒;西安杨森制药有限公司,国药准字H10930214)分别放入不透明的纸质袋。患者按药物说明自行使用。试验组应用环吡酮胺阴道乳膏每次5 g(含环吡酮胺0.05 g),对照组每次应用硝酸咪康唑栓1粒(含硝酸咪康唑200 mg);两组用药均置入阴道深处,均为每日1次,连用7 d。所有入选患者固定由1位副主任医师评估疗效。该医师对患者的具体用药不知情、不询问,分别于停药后1周及1、3、6个月各复查白带常规1次,并记录患者的临床症状和体征的改善情况及其不良反应。所有患者用药期间至停药后1周内禁止性生活,观察期间性生活时全程使用避孕套。
1.3 疗效评价疗效判断标准[5]:疗效分为治愈、有效和无效。治愈:VVC临床症状及体征完全消失,真菌镜检为阴性;有效:VVC症状及体征好转,真菌镜检为阴性;无效:VVC症状及体征无减轻或加重,真菌镜检为阳性。复发指治愈后在随访期间再次发作VVC的症状,并且阴道真菌学检查为阳性。
1.4 统计学处理使用SAS 6.21软件进行统计学处理。计量资料的比较采用两样本均数比较的t检验,计数资料的比较采用χ2检验。检验水准(α)为0.05。
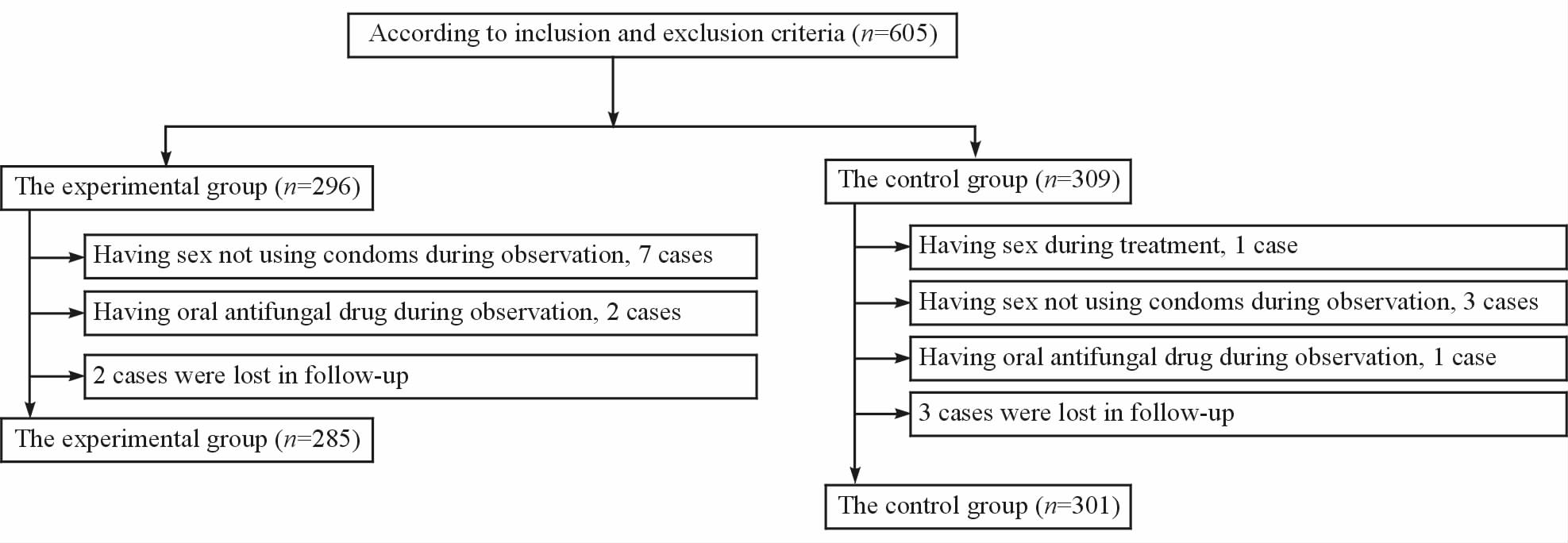
2 结 果 2.1 一般资料按纳入、排除标准,共有605例入选本试验,依随机数字表分成两组。后有19例患者因观察期间性生活时未使用避孕套、口服抗真菌药物、未按试验方案使用药物等原因被剔除,最终共有586例完成试验(图 1)。两组年龄、孕产次、婚姻状况、既往病程等各项参数差异无统计学意义(P>0.05,表 1),对研究结果无影响。
|
图 1 病例筛选流程图 Fig 1 Flow chart of case selecting |
|
|
表 1 两组一般情况的比较 Tab 1 Comparison of general information of the two groups |
在阴道用药的24 h内,试验组有78.25%(223/285)的患者外阴瘙痒症状得到了明显缓解,而对照组有41.86%(126/301)的患者症状得到缓解,两组比较差异有统计学意义(χ2=80.46,P<0.01)。停药1周后随访,其中试验组治愈204例,有效58例,总有效率为91.93%(262/285);而对照组治愈205例,有效51例,总有效率为85.05%(256/301),两组差异有统计学意义(χ2=6.75,P<0.01)。详见表 2。
|
|
表 2 两组治疗后的疗效比较 Tab 2 Comparison of clinical outcomes of the two groups after treatment |
试验组治愈的204例患者中,在停药后1个月随访时未见复发病例,停药后3个月随访1例复发,停药后6个月8例复发。对照组治愈的205例患者中,在停药后1个月随访时有1例复发,停药后3、6个月分别有15例和29例复发。两组3个月和6个月的复发率差异有统计学意义(χ2分别为12.68和12.99,P<0.01)。
2.3 不良反应本研究治疗期间部分患者有阴道局部烧灼不适感,其中试验组13例,对照组17例。上述症状均在停药后消失。本研究治疗期短,患者依从性良好。
3 讨 论VVC分为单纯性VVC和复杂性VVC,目前的治疗仍是在消除诱因的基础上局部或全身应用抗真菌药。单纯性VVC的致病菌为白色假丝酵母菌,治疗主要以局部短程药物为主,吡咯类药物依然是首选。其中,硝酸咪康唑为高效、安全、广谱的抗真菌药,其栓剂在临床上已经应用多年。该药治疗VVC的短期疗效尚可,但停药后容易复发。其原因可能与假丝酵母菌谱变迁,菌株基因型变异及毒力变化等因素相关。而复杂性VVC的致病菌为非白色假丝酵母菌,常规药物治疗的疗效欠佳。本研究主要目的是对比环吡酮胺乳膏和硝酸咪康唑栓2种阴道给药的不同疗效,在研究对象的选取上未区分单纯性VVC和复杂性VVC,后期研究中将会考虑单纯性VVC和复杂性VVC在临床上治疗方案的差异性。
本研究结果显示:环吡酮胺乳膏和硝酸咪康唑栓治疗VVC用药24 h内的症状缓解率分别为78.25%(223/285)和41.86%(126/301),差异有统计学意义(P<0.01); 停药1周后总有效率分别为91.93%(262/285)和85.05%(256/301),前者更佳(P<0.01)。停药后两组的复发率随着时间的延长均有所增加,试验组在停药后的3、6 个月的复发率分别为0.49%和3.92%,而对照组相应的复发率分别为7.32%和14.15%,试验组的复发率显著低于对照组(P<0.01)。可见在迅速缓解临床症状和预防复发方面,环吡酮胺阴道乳膏明显优于硝酸咪康唑栓。硝酸咪康唑则通过抑制真菌细胞膜固醇的合成,使得膜的通透性增加,真菌体内的重要成分如蛋白质、氨基酸、磷脂及核苷酸等渗漏出膜外,导致真菌死亡[6]。其短期疗效肯定,本研究显示总有效率为85.05%。但近年来非白假丝酵母菌感染有上升趋势,非白假丝酵母菌的比例在VVC患者中增高[7, 8],对该药逐渐产生耐药性,复发率较高,且治疗效果差[9, 10]。因此,临床上需要新的抗真菌药物提高疗效,减少复发。环吡酮胺是合成的广谱抗真菌药,由环吡酮和乙醇胺结合而成,具有完全不同于传统咪唑类或三唑类药物的化学结构。其作用机制包括改变真菌细胞膜的稳定性,引起细胞膜内物质外流,并阻断蛋白质前体物质的摄取,导致真菌细胞死亡。该药毒性低,渗透力强,对霉菌、酵母菌、放射菌和其他真菌有较强的杀菌和抑菌作用。既往研究显示,环吡酮胺在治疗皮肤真菌感染方面收到很好临床疗效[11]。另外,VVC患者往往是包括真菌在内的复合感染,而环吡酮胺对其他病原体如细菌、支原体、衣原体、毛滴虫也有抑制作用。加之,本研究应用的环吡酮胺在剂型上有优势,在阴道放药的同时可涂抹外阴及肛周,杀灭局部病菌避免再次感染。
应当注意的是,本研究中环吡酮胺的疗效好与本地区既往很少应用该药治疗VVC不无关系。随着日后用药病例的增多,病菌耐药性的变化,该药的疗效如何还值得进一步观察。本试验根据临床流行病学原理设计,采用随机分组、盲法对照,有严格的纳入、排除标准,对可能影响研究结果的因素进行了均衡性检验。鉴于随机对照试验的论证强度高,结果较可靠,我们认为环吡酮胺的疗效肯定、复发率低,可依临床实际情况适当选用。
| [1] | Mikamo H, Matsumizu M, Nakazuru Y, Okayama A, Nagashima M. Efficacy and safety of a single oral 150 mg dose of fluconazole for the treatment of vulvovaginalcandidiasis in Japan[J].J Infect Chemother,2015,21:520-526. |
| [2] | Workowski K A, Berman S; Centers for Disease Control and Prevention (CDC).Sexually transmitted diseases treatment guidelines, 2010[J]. MMWR Recomm Rep,2010,59(RR-12):1-110. |
| [3] | Ugwa E A. Vulvovaginal Candidiasis in Aminu Kano Teaching Hospital, North-West Nigeria: Hospital-Based Epidemiological Study[J]. Ann Med Health Sci Res,2015,5:274-278. |
| [4] | 何 叶,曾定元,李晶晶.环吡酮胺治疗复发性外阴阴道念珠菌病的疗效[J].实用医学杂志,2012,28:4164-4165. |
| [5] | 中华妇产科学分会感染性疾病协作组. 外阴阴道念珠菌病诊治规范(草案)[J].中华妇产科杂志,2004,39:430-431. |
| [6] | 武 璁,樊尚荣. 复发性外阴阴道念珠菌病的药物治疗研究进展[J].中国全科医学,2011,14:1990-1992. |
| [7] | Täuber A, Müller-Goymann C C. Comparison of the antifungal efficacy of terbinafine hydrochloride and ciclopirox olamine containing formulations against the dermatophyte Trichophyton rubrum in an infected nail plate model[J]. Mol Pharm,2014,11:1991-1996. |
| [8] | Aguin T J, Sobel J D. Vulvovaginal candidiasis in pregnancy[J].Curr Infect Dis Rep,2015,17:462. |
| [9] | Li J,Jiang Y, Sun T,Ren S. Fast and simple method for assay of ciclopirox olamine by micellar electrokinetic capillary chromatography[J].J Pharm Biomed Anal,2008,47(4-5):929-933. |
| [10] | Beghini J, Giraldo P C, Linhares I M, Ledger W J, Witkin S S. Neutrophil gelatinase-associated lipocalin concentration in vaginal fluid: relation to bacterial vaginosis and vulvovaginal candidiasis[J]. Reprod Sci,2015,22:964-968. |
| [11] | Täuber A, Müller-Goymann C C. In vitro permeation and penetration of ciclopirox olamine from poloxamer 407-based formulations-comparison of isolated human stratum corneum, bovine hoof plates and keratin films[J]. Int J Pharm,2015,489(1-2):73-82. |
 2015, Vol. 36
2015, Vol. 36


