2. 贵州省人民医院心内科, 贵阳 550002
2. Department of Cardiology, Guizhou Provincial People's Hospital, Guiyang 550002, Guizhou, China
心房纤颤(房颤)的主要不良后果是引起脑卒中,对于非瓣膜性房颤患者,约90%的血栓栓子来源于左心耳[1]。因此,左心耳封堵术这一闭合“血栓窝点”的疗法可以预防血栓形成。然而目前的外科手段和经导管技术虽然取得可喜的进展,但皆有其局限性。为进一步推动左心耳封堵的治疗技术,我们与上海形状记忆合金材料有限公司合作,研制了“酒杯状”镍钛合金左心耳反向封堵器,拟尝试通过胸腔镜进行左心耳封堵。本研究通过在离体犬心脏标本上进行初步的体外封堵实验,探讨该封堵器与左心耳解剖的匹配度和经胸左心耳反向封堵的可行性,为下一步经胸左心耳反向封堵技术的动物实验奠定基础。
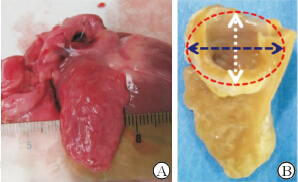
1 材料和方法 1.1 犬左心耳应用解剖取健康杂交犬[体质量(140±15)g]心脏标本10只,保留左心耳周围组织,生理盐水反复冲洗后,先观察左心耳的外形及毗邻组织关系,将标本置于操作台上,沿左室流出道剪开心室,暴露主动脉瓣结构,再沿房间隔中线纵向剪开,暴露左心耳口、左房室瓣及肺静脉。测量:(1)左心耳开口的长径、短径、周长(图1);(2)左心耳开口边缘与左上、下肺静脉开口及左房室瓣环的最短距离。
|
图 1 实验犬左心耳新鲜(A)及固定标本(B) Fig 1Fresh (A) and fixed (B) left atrial appendage specimens of canine |
委托上海形状记忆合金材料有限公司制作“酒杯状”镍钛合金左心耳封堵器,在封堵器心外盘面、腰部及心耳盘面缝上涤纶膜以阻挡血流,两侧盘面均为不锈钢铆并凹陷,以保证盘面平整。心外盘面不锈钢铆有螺纹可与推送杆连接。按照实验犬左心耳解剖参数设计封堵器心耳口盘面尺寸及腰部高度。
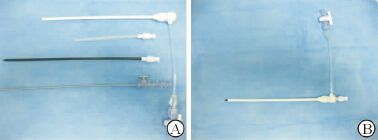
1.3 输送系统输送系统包括9F输送鞘及匹配的扩张鞘、预载鞘及推送杆。输送鞘上有刻度可把握进入左心耳长度,扩张鞘头端为平滑过渡设计,插入输送鞘后头端仅露出约0.8 cm以免损伤心脏内部结构(图2)。
|
图 2 输送系统 Fig 2 Delivery system A: Delivery system including delivery sheath, expanding sheath, preloading sheath, pushing rod; B: The head of the expanding sheath emerges from delivery sheath about 0.8 cm |
取健康杂种犬心脏标本10只,置于操作台上,左侧朝上以充分暴露左心耳,直视下选择左心耳上中1/3正中作为穿刺点,围绕穿刺点用4-0 Prolene线制作缝合荷包,用穿刺针穿刺荷包中央,用短泥鳅导丝建立左心耳外-穿刺点-左心房-左心室半轨道,沿泥鳅导丝将输送鞘送入左心耳内,保留输送鞘头端1.5~2.0 cm位于左心耳及左心房内,将载有封堵器的预载鞘与输送鞘尾端连接,送入封堵器,待封堵器心耳内盘面释放后回拉推送杆,感觉有阻力提示盘面与左心耳口紧密贴合,稍后退输送鞘,释放心耳外盘面,逆时针旋转以断开推送杆,将荷包缝合,完成封堵过程。随后解剖心脏观察封堵器位置及毗邻组织是否受到影响。
2 结 果 2.1 犬左心耳大体解剖参数左心耳是左心房前侧壁上部向外突出的狭长盲端腔,腔内面分布较多肌小梁样结构,凹凸不平。左心耳开口位于左上、左下肺静脉口的下方,左房室瓣的上方,其开口长径、短径、心耳上中1/3处厚度(定义为心耳口中心至心耳外侧上中1/3横径中点的距离)、左心耳开口边缘距离左上、下肺静脉及左房室瓣的距离(表1)。
|
|
表 1 实验犬左心耳大体解剖学参数 Tab 1 Anatomical data of left atrial appendage (LAA) of experimental canines |
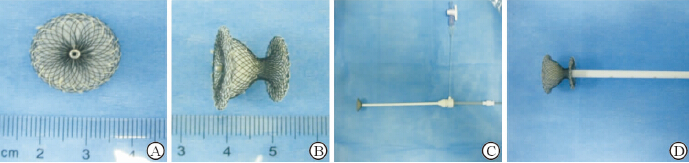
左心耳外观整体呈“酒杯状”,2个盘面及腰部共缝有3层涤纶膜以阻挡血流,心耳内侧盘面直径有16 mm、18 mm、20 mm共3种型号,每种型号分别有腰高8 mm、10 mm两种,心耳外侧盘面尺寸固定,均为16 mm。体外实验证实,封堵器可以顺利经9F鞘管收入、输送和释放 (图3)。
|
图 3 “酒杯状”封堵器的外观及体外输送、释放 Fig 3 The appearance, delivery and release of a glass-shaped occluder A: LAA occluder outer disk view; B: LAA occluder side view; C: The LAA occluder released the LAA opening disk by delivery system; D:The LAA occluder released the LAA outside disk by delivery system. LAA: Left atrial appendage |
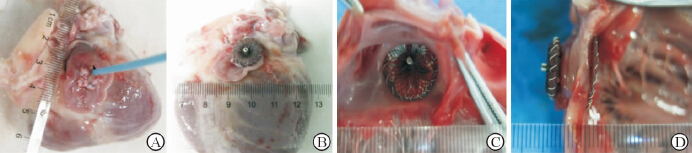
10只离体犬心脏中9例体外封堵实验均获得成功,封堵完成后心耳口盘面稳定置于心耳口正中,与左下、左上肺静脉开口及左房室瓣距离均在5 mm以上,不影响左上、左下肺静脉的血液回流和左房室瓣的功能。穿刺点位于左心耳外长轴上中1/3处,术后撤去封堵器见穿刺点位置正对于左心耳开口中央(图4)。其中1例因穿刺点位置不佳,封堵器释放后行牵拉实验见封堵器心耳口盘面也进入心耳腔内,心耳口面观见封堵器盘面与心耳口平面不重合,大部分盘面在心耳腔内,撤去封堵器,见穿刺点靠近心耳体下半部分,位置过低(图5)。
|
图 4 左心耳封堵器体外封堵实验 Fig 4 LAA reverse occluding animal experiments in vitro A: Select the puncture site at the middle of upper 1/3 LAA; around the puncture site suture with 4-0 Prolene suture purse cables; and after puncturing the femoral artery expand with a 5F sheath expansion sheath; B: Exchange delivery sheath into LAA, convey the occluder, release two disk one by one, then suture the purse-string, and complete the occlusion process; C: After the occlusion process LAA lateral view, the occluder location is good, the distances from LAA opening edge to left superior pulmonary vein, left inferior pulmonary vein and mitral valve edge are all >3 mm, and blood flow was not affected; D: LAA side view, it is visible that the occlude waist-high matches with the thickness of the LAA. LAA: Left atrial appendage |
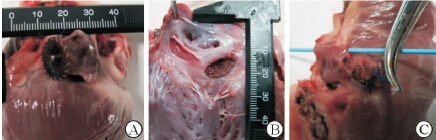
|
图 5 左心耳封堵器体外封堵失败实验 Fig 5 A failed LAA reverse occluding animal experiment in vitro A: LAA outer disk view, the occlude is into the LAA cavity in deep position during the traction experiment after the occluder released; B: LAA opening view, the LAA opening disk of the occlude does not coincide with the LAA opening, the LAA opening disk is lateral in the LAA cavity (not an ideal position); C: Withdrawing the occluder, the puncture position is close to the lower part of LAA body, the position is too low, and the correct puncture site is the middle of upper 1/3 of LAA, or the blue bar through site. LAA: Left atrial appendage |
左心耳是妊娠3个月胚胎时期左心房发育过程中残留的原始左心房,作为左心房的一部分,其收缩和舒张功能与左心房一致,但收缩舒张能力较弱,类似于左心房的一个“蓄水池”。心耳内有大量肌小梁,凹凸不平,形成许多小窝,在房颤的病理状态下,心房内血流淤滞,容易形成血栓,一旦脱落则随血流至全身动脉引起栓塞,尤以“卒中”引起的后果最为严重。正是由于左心耳上述的解剖学特征和生理病理学特点,非瓣膜性房颤的血栓90%在左心耳形成,而风湿性瓣膜病房颤患者57%的血栓形成与心耳有关[1]。因此,封堵左心耳这一“血栓窝点”可以减少房颤患者的卒中发生率。这为预防卒中而对房颤患者的左心耳行切除、缝合分离、经胸腔镜套扎和经导管封堵等治疗方法提供了理论基础。
然而外科切除左心耳创伤大、恢复慢,只适合在心脏外科手术时同期进行,而且切除后常遗留左心耳残根[2,3,4,5,6]。缝合分离方法的短期和长期失败率均较高,且缝合失败后形成血栓的风险反而会上升。经胸腔镜左心耳套扎术使用辅助器械,提高了左心耳闭合的成功率,但操作复杂,且术后会有一定的松解率,临床应用受限[7,8,9]。经导管左心耳封堵术的原理主要有两种,一种是“活塞式”,以Watchman封堵器[10,11]和PLATTO装置[12,13]为代表,对于弯曲度较大(如鸡翅样)和内腔较小(如菜花样)的左心耳不易封堵成功。另一种是“覆盖式”,以Amplatzer Cardiac Plug(ACP)装置[14]和国产LAmbre封堵器[15,16]为代表,对于开口狭长的心耳,要选择较大的封堵器以完全覆盖开口,这样势必会增加封堵盘的覆盖面,影响毗邻结构,如肺静脉、左房室瓣等。此外,各封堵器皆可能出现倒钩损伤心耳、慢性穿孔、压迫回旋支等问题,且对于内腔浅(呈脸盆状)的左心耳则由于无合适“锚定区”(landing zone)皆不能封堵。同时,经导管途径的封堵器皆是由金属材料编织而成,金属异物永久存留心脏的安全性,如随心脏不停跳动是否磨损、侵蚀周围组织还缺乏长期的随访资料。
因此,将外科手段(如胸腔镜技术)和内科经导管技术结合起来,可以开创一种左心耳封堵的新方法,即经胸左心耳反向封堵术。本研究对这种方法的可行性进行了初步探索。首先,对实验犬的左心耳应用解剖进行研究,根据解剖参数设计出经胸左心耳反向封堵器,根据左心耳开口大小设计心耳口盘片直径,心耳上中1/3处厚度设计腰高,并通过离体心脏犬标本行体外实验证实封堵的可行性。
考虑到封堵器要与左心耳的解剖相匹配,本研究设计的封堵器整体类似于酒杯状,心耳口盘面主要起封堵心耳开口的作用,其直径设计了3个数值,分为16 mm、18 mm、20 mm。腰部设计为从内侧盘面到外侧盘面由粗至细缓慢过渡,保证封堵器腰部与心耳腔由开口到远端逐渐缩小的特点,根据心耳上中1/3处厚度,腰高设计为8 mm和10 mm两种。心耳外侧盘面在封堵器释放以后能够紧密贴合在心耳外缘,防止封堵器移位或脱落,盘面直径固定在16 mm。
体外实验共纳入10只犬心脏标本,其中9例获得成功,结果显示封堵器的形态可以较好地吻合左心耳形态。在封堵完成以后解剖心脏发现,封堵器心耳口盘面不是覆盖于心耳口,而是少许进入心耳内利用盘面的支撑力将心耳口适度撑开,这样位置稳定,同时可以避免盘面影响左上、下肺静脉和左房室瓣。而腰部高度比心耳相应部位厚度稍小,可以将心耳上1/3部分适度“压紧”,保证封堵器不会移位,在植入封堵器后并不占据额外空间。心耳外侧盘面设计为一固定值16 mm,实验中可以看到外侧盘面紧紧贴附于心耳上1/3外表面而不超过其横径。这样的设计可以保证植入术后在心脏不停的跳动中,减少封堵器和周围组织摩擦的机会,可能会减少术后远期侵蚀周围组织导致严重并发症。
结合体外实验结果,展望下一步的经胸左心耳反向封堵技术,可能涉及的技术要点主要包括3个:(1)选择合适的切开位置以充分暴露左心耳,一般来说,在左侧第4~5肋间靠近脊柱侧做1个5 cm的切口,可以充分暴露左心耳,但还需要下一步的动物实验去摸索,在开胸封堵实验取得成功以后,再考虑经胸腔镜的手术入路。(2)由于左心房的容积空间有限,输送鞘管进入左心耳内不能过深,以免伤及心内组织。后续的动物实验中我们发现,使用带刻度的输送鞘,在输送鞘进入心脏内1.5 cm后,宜固定鞘管位置,不宜送入过深或过浅,过浅可能易于滑出,滑出难以再次寻找穿刺点,因为出血后局部视野模糊,时间过长可能会导致出血过多甚至死亡。(3)穿刺点位置的选择。本研究中1例封堵不成功,解剖见封堵器心耳口盘片与心耳口平面没有重合,盘面“侧卧”在心耳腔内,其原因就在于穿刺点过于靠下。结合9例成功的经验,我们的体会是,穿刺点位于左心耳外长轴上中1/3处比较理想,荷包应该围绕这一点来制作,术后撤去封堵器见穿刺点位置正对于左心耳开口中央。荷包的缝线有两个方面的功能,一是在送入封堵鞘的过程中可以反向提拉,协助鞘管顺利送入;二是在封堵器释放完毕后结扎,起到止血效果。
本中心曾经于2012年进行过类似的经胸左心耳封堵实验[17],本实验与之比较,存在以下两点不同。(1)封堵器的形态有所区别:先前实验封堵器心耳内盘片与腰部连接处呈圆锥状,腰部较细长,心耳外侧盘片较薄且略微向心房侧弯曲。本实验封堵器盘片与腰部连接处呈酒杯状,腰部较短,过渡自然,心耳外侧盘片相对较厚且边缘圆钝向心房侧有较明显的弧度,更有利于与心耳外侧贴合紧密;(2)输送系统有所区别:本实验输送系统较之前实验有所改进,输送鞘上有刻度可把握进入左心耳长度,扩张鞘头端为平滑过渡设计,插入输送鞘后头端仅露出约0.8 cm以防损伤心脏内部结构,提高了安全性,更有利于操作导管进入深度,减少了不必要的并发症。
综上所述,体外实验证实了经胸左心耳反向封堵是可行的,可以开展下一步的动物实验研究。事实上,我们已经完成了经胸小切口左心耳反向封堵的动物实验研究,并取得良好结果。相对于经皮左心耳封堵术,经胸左心耳反向封堵术的优点就在于,几乎对于任何形态的左心耳皆可实现封堵,且封堵器不会脱落,封堵器心耳口盘面通过过度撑开心耳口,不影响肺静脉回流和左房室瓣的功能。而相对于其他外科手段来说,胸腔镜下左心耳反向封堵术创伤小,恢复快,值得进一步研究以应用于临床。
| [1] | Blackshear J L, Odell J A. Appendage obliteration to reduce stroke in cardiac surgical patients with atrial fibrillation[J].Ann Thorac Surg,1996,61:755-759. |
| [2] | Madden J L. Resection of the left auricular appendix; a prophylaxis for recurrent arterial emboli[J].J Am Med Assoc,1949,140:769-772. |
| [3] | Leonard F C, Cogan M A. Failure of ligation of the left auricular appendage in the prevention of recurrent embolism[J].N Engl J Med,1952,246:733-735. |
| [4] | Healey J S, Crystal E, Lamy A, Teoh K, Semelhago L, Hohnloser S H, et al. Left Atrial Appendage Occlusion Study (LAAOS): results of a randomized controlled pilot study of left atrial appendage occlusion during coronary bypass surgery in patients at risk for stroke[J].Am Heart J,2005,150:288-293. |
| [5] | Katz E S, Tsiamtsiouris T, Applebaum R M, Schwartzbard A, Tunick P A, Kronzon I. Surgical left atrial appendage ligation is frequently incomplete: a transesophageal echocardiograhic study[J].J Am Coll Cardiol,2000,36:468-471. |
| [6] | Kanderian A S, Gillinov A M, Pettersson G B, Blackstone E, Klein A L. Success of surgical left atrial appendage closure: assessment by transesophageal echocardiography[J].J Am Coll Cardiol,2008,52:924-929. |
| [7] | Blackshear J L, Johnson W D, Odell J A, Baker V S, Howard M, Pearce L, et al. Thoracoscopic extracardiac obliteration of the left atrial appendage for stroke risk reduction in atrial fibrillation[J].J Am Coll Cardiol,2003,42: 1249-1252. |
| [8] | Ailawadi G, Gerdisch M W, Harvey R L, Hooker R L, Damiano R J Jr, Salamon T, et al. Exclusion of the left atrial appendage with a novel device: early results of a multicenter trial[J].J Thorac Cardiovasc Surg,2011, 142: 1002-1009. |
| [9] | Stone D, Byrne T, Pershad A. Early results with the LARIAT device for left atrial appendage exclusion in patients with atrial fibrillation at high risk for stroke and anticoagulation[J].Catheter Cardiovasc Interv,2015, 86: 121-127. |
| [10] | Holmes D R, Reddy V Y, Turi Z G, Doshi S K, Sievert H, Buchbinder M, et al. Percutaneous closure of the left atrial appendage versus warfarin therapy for prevention of stroke in patients with atrial fibrillation: a randomised non-inferiority trial[J].Lancet, 2009,374:534-542. |
| [11] | Reddy V Y, Holmes D, Doshi S K, Neuzil P, Kar S. Safety of percutaneous left atrial appendage closure: results from the Watchman Left Atrial Appendage System for Embolic Protection in Patients with AF (PROTECT AF) clinical trial and the Continued Access Registry[J].Circulation,2011,123:417-424. |
| [12] | Block P C, Burstein S, Casale P N, Kramer P H, Teirstein P, Williams D O, et al. Percutaneous left atrial appendage occlusion for patients in atrial fibrillation suboptimal for warfarin therapy: 5-year results of the PLAATO (Percutaneous Left Atrial Appendage Transcatheter Occlusion) Study[J].JACC Cardiovasc Interv,2009,2:594-600. |
| [13] | Bayard Y L, Omran H, Neuzil P, Thuesen L, Pichler M, Rowland E, et al. PLAATO (Percutaneous Left Atrial Appendage Transcatheter Occlusion) for prevention of cardioembolic stroke in non-anticoagulation eligible atrial fibrillation patients: results from the European PLAATO study[J].EuroIntervention,2010,6:220-226. |
| [14] | Park J W, Bethencourt A, Sievert H, Santoro G, Meier B, Walsh K, et al. Left atrial appendage closure with Amplatzer Cardiac Plug in atrial fibrillation: initial European experience[J].Catheter Cardiovasc Interv,2011, 77: 700-706. |
| [15] | Lam Y Y, Yan B P, Doshi S K, Li A, Zhang D, Kaya M G, et al. Preclinical evaluation of a new left atrial appendage occluder (Lifetech LAmbreTM Device) in a canine model[J].Int J Cardiol,2013,168:3996-4001. |
| [16] | Lam Y Y. A new left atrial appendage occluder (Lifetech LAmbreTM Device) for stroke prevention in atrial fibrillation[J].Cardiovasc Revasc Med,2013,14:134-136. |
| [17] | 崔 婷.经皮和经胸植入左心耳封堵器的动物实验研究[D].上海:第二军医大学,2013. |
 2015, Vol. 36
2015, Vol. 36


