2. 泸州医学院附属医院核医学科, 泸州 646000
2. Department of Nuclear Medicine, Affiliated Hospital of Luzhou Medical College, Luzhou 646000, Sichuan, China
阿奇霉素(azithromycin) 是新一代氮杂内酯类抗生素,是在红霉素化学结构上修饰后得到的一种广谱抗生素[1],临床上主要对各种革兰阴性细菌、厌氧菌及其他病原体如支原体、衣原体有很强的活性,主要用于呼吸道、皮肤和软组织感染[2]。但是口服阿奇霉素治疗往往伴有胃肠道的各种不良反应,如腹部绞痛、腹泻、恶心、呕吐以及导致心脏活动异常或有潜在性致命心律不齐和容易诱发耐药性等缺点[3]。因此,提高其疗效,降低毒副反应及耐药性对临床应用有着重要的意义。泡囊或非离子型的表面活性剂泡囊,是非离子型表面活性剂的混合烷基或二烷基酯的聚甘油醚类和胆固醇在含水介质中水化形成的层状结构。在生命科学中,由于其能作为细胞膜最好的模拟体系,受到了人们的广泛关注。药物被包封于泡囊中主要被网状内皮系统的巨噬细胞所吞噬,在肺、肝、脾等网状内皮细胞较丰富的器官内集中,而使药物在心肾中累积量比游离药物明显降低,从而降低毒副作用。本实验将制备阿奇霉素泡囊,根据阿奇霉素泡囊和阿奇霉素在动物体内的吸收特征和变化规律,以Loo-Riegelman法计算体内吸收分数、反卷积分法计算输入函数,分析阿奇霉素泡囊体外释放与体内吸收的相关性,为临床用药提供依据。
1 材 料 1.1 仪器安捷伦1100型高效液相色谱仪(美国Agilent公司);UV-VIS3150型紫外可见分光光度仪(日本岛津公司);分析电子天平(瑞士Mettler Toledo公司);透析袋(Mw=8 000~14 000,美国联合碳化物公司);激光粒度仪(英国Malvern公司);QL-901 型旋涡混合器(海门市其林贝尔仪器制造有限公司);TGL-16B高速台式离心机(江苏省金坛市大地自动化仪器厂)。
1.2 药品与试剂
阿奇霉素 (上海现代制药股份有限公司,批号:20101126);阿奇霉素标准品(效价:952 U/mg,中国生物制品检定所);胆固醇(广州天马精细化工厂);吐温-80(上海申宇医药化工有限公司);十八胺(上海南翔试剂有限公司);甲醇、乙腈、异丙醇为色谱纯,其余试剂均为分析纯,水为重蒸馏水。
1.3 动物
健康SD大鼠,雌雄各半,体质量(230 ± 20)g,重庆医科大学实验动物中心提供,动物生产许可证号:SCXK(渝)2011-0001。
2 方法和结果2.1 阿奇霉素泡囊的制备方法
采用薄膜分散法制备泡囊[4]。将阿奇霉素、十八胺、胆固醇、吐温80加入圆底烧瓶中,再加入适量氯仿溶解,减压蒸发至瓶内壁上形成一层薄膜,加入磷酸盐缓冲液和玻璃珠若干,水浴常压下搅拌分散混悬,使薄膜溶胀水合,得到混悬液,于4℃冰箱保存备用。
2.2 阿奇霉素泡囊的粒径分布和zeta电位取适量阿奇霉素泡囊,用蒸馏水稀释20倍后,用激光粒度仪测定其粒径和zeta电位。经激光粒度仪测定其粒径为(907.4 ± 0.10) nm,多分散指数(PDI)为0.230,zeta电位为(14.6 ± 0.02) mV。
2.3 体外分析方法的建立精密称取适量105℃干燥至恒质量的阿奇霉素对照品,用少量无水乙醇溶解后,转移至容量瓶中,再用pH 7.4磷酸盐缓冲溶液定容,作为对照品贮备溶液。精密量取适量对照品贮备溶液并用pH 7.4的磷酸盐缓冲溶液稀释成24、48、72、96、120 μg/mL系列浓度。再分别取上述溶液5 mL加入5 mL 75%硫酸溶液混匀显色,室温冷却后在482 nm波长处测定光密度(D)值。以D对相应的浓度(C)进行线性回归,得回归方程D= 0.014 4C-0.0701,r=0.999 6 (n=3)。结果表明,阿奇霉素浓度在24~120 μg/mL范围内与光密度呈良好的线性关系,平均回收率为99.12%,RSD为0.52% (n=3)。
2.4 阿奇霉素泡囊体外释放度测定采用动态膜透析法测定体外释放度。取阿奇霉素泡囊混悬液2 mL(相当于阿奇霉素约2 mg)和阿奇霉素溶液2 mL,置于经蒸馏水浸泡处理过的透析袋中,将含药透析袋置于盛有20 mL pH 6.8磷酸盐缓冲溶液为释放介质的溶出瓶中,温度为(37 ± 0.5)℃,转速为100转/分,定时从袋外取出1 mL,立即补加等量同质同温释放介质。按2.3项下方法测定含量,计算累积释放百分率Y。结果可知,在0.5、1、2、4、6、8、12、24、36、48 h时药物体外累积释放大约为(20.26± 2.28)%、(39.25±2.60)%、(61.67±0.93)%、(75.77±3.76)%、(82.23±5.51)%、(85.92±2.42)%、(88.56±2.43)%、(91.20±4.19)%、(98.18±3.42)%,表明该制剂在体外具有明显的缓释效果。
2.5 体内分析方法的建立色谱条件:伊利特 C18 色谱柱(250 mm×4.6 mm,5 μm);柱温:40℃;流动相为乙腈∶异丙醇∶0.004 mol/L的磷酸氢二钠= 60∶15∶25(V/V/V),流速为1 mL/min;检测波长:210 nm,进样量为40 μL。
血液样品的处理方法:取空白血浆300 μL于具塞离心管中,加入内标 (20 μg/mL罗红霉素) 10 μL,涡旋,加入0.2 mol/L的氢氧化钠溶液80 μL涡旋振荡混匀,再加入乙醚2 mL,涡旋。完毕后3 187.5×g离心10 min,提取乙醚层,40℃真空干燥,加甲醇200 μL复溶涡旋,12 750×g离心10 min,取上清液40 μL进样分析。
标准曲线的建立:分别取空白血浆300 μL,加入不同浓度的阿奇霉素标准溶液配制成的系列浓度血浆样品,按照血浆样品处理方法操作后进样,分别以阿奇霉素和内标(罗红霉素)峰面积之比(A)对阿奇霉素浓度(C)进行线性回归。阿奇霉素体内血浆样品的标准曲线回归方程为:A= 19.26C-52.69,r=0.999 0(n=3),结果表明在1.0 ~50.0 μg/mL范围内浓度与峰面积比呈良好线性关系。配制阿奇霉素低、中、高3个质量浓度(5、15、25 μg/mL)的血浆样品,按血浆样品的处理后进样,1 d内连续进样检测5次,连续5 d考察其日间和日内精密度。高、中、低3个浓度的溶液中阿奇霉素的绝对回收率分别为97.80%、99.51%、98.43%;内标的绝对回收率为97.21%、98.66%、100.7%。将血浆样品中阿奇霉素峰面积与直接相应浓度阿奇霉素溶液的峰面积进行比较,测得萃取回收率为82.31%、88.49%、90.24%,回收率较高,说明采用该方法处理阿奇霉素血浆样品合适。
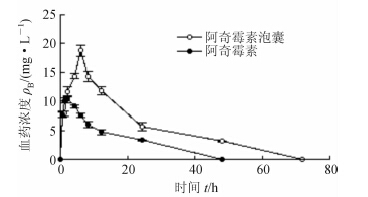
2.6 体内实验设计采用交叉设计单剂量给药方案,给药剂量为每只大鼠200 mg/kg(以阿奇霉素计)。将6只SD大鼠随机分为2组,每组3只。实验前禁食12 h,全程不禁水。分别于给药后0.5、1、2、4、6、8、12、24、48、72 h用乙醚麻醉大鼠,采用眼底取血的方法采集血样,至肝素浸润过的离心管中,6 375×g离心10 min,吸取上层血浆,置于-20℃冰箱中保存待测。间隔1周后交叉给药。单剂量口服阿奇霉素混悬液或阿奇霉素泡囊后的血浆样品的结果见图 1。
|
图 1 单剂量口服阿奇霉素泡囊和阿奇霉素后的血药浓度与时间关系
n=6,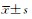
|
分别采用室模型依赖法[5]和反卷积分[6]进行体内外相关性的研究。
2.7.1 室模型依赖法[5]将血药浓度数据用DAS 2.1软件进行拟合并以赤池信息量准则(AIC)、拟合度R2为判断依据,结果表明阿奇霉素泡囊在大鼠体内药动学符合二室模型。因此采用Loo-Reigelma方程计算各时间点体内药物吸收百分数,并与相应时间点体外药物累积释放百分数进行线性回归考察体内外相关性,计算公式如下:
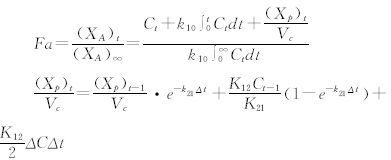
其中,Fa为t时药物吸收百分数,XA为体内吸收的药物总量,Ct是t时体内血药浓度,k10是药物从中央室消除的一级速率常数,Vc是中央室表观分布容积,Xp是周边室药物量,K21和K12为中央室与周边室之间的转运速率常数。
由图 1可知,单剂量口服阿奇霉素泡囊后,血药浓度6 h后达峰,因此按照上述公式计算0.5、1、2、4、6 h的体内吸收分数Fa,如表 1。以0.5~6 h体外累积释放百分率为自变量Y,体内吸收百分数为因变量Fa,得线性回归方程Fa=0.981 8Y + 1.083 1,r=0.956 5,根据相关系数临界表r(3,0.01)=0.958 7,r小于相关系数临界值,表明阿奇霉素泡囊体外累积释放百分数与体内吸收百分数无相关性。
2.7.2 反卷积分法[6] 采用卷积-反卷积理论进行体内外相关性研究的对象是稳定的线性系统,缓控释药物可以使用此法对其进行描述。根据质量守恒原则,药物在体内的浓度可用以下卷积分方程表示:
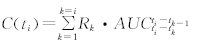
式中设测定的时间间隔点为t0、t1、t2……ti;相应阿奇霉素泡囊血药浓度数据分别为:C0、C1、C2……Ci;时间间隔为ti-1~ti的平均药物输入分别为R1、R2……Ri(输入函数);AUC为阿奇霉素各个时间段药时曲线下面积,以输入函数R相对应时间点的体外累积释放度进行线性回归,考察阿奇霉素泡囊的体内外相关性,如表 1。以输入函数R为因变量,体外累积释放百分数Y为自变量,得回归方程R=0.763 5Y-15.699,r=0.862 7,临界值r(3,0.01)=0. 958 7,r小于相关系数临界值,结果表明阿奇霉素泡囊无体内外相关性。
| 表 1 阿奇霉素泡囊在体内的吸收分数和输入函数 |
3 讨 论
缓释制剂体内外相关性实验的主要目的在于预测药物在体内的作用特征,从而减少体内研究数量,降低新药研发成本[7]。药物在体外释放特征与体内作用特征之间的定量关系能够指导和优化处方设计,合理调整和选择制剂和工艺,对于药物制剂特别是缓控释制剂的研究开发具有重要的指导意义。
评价体内外相关性时,国内最常用的方法为模型法。如果药物在体内的药动学特征符合一室模型,吸收分数采用Wagner-Nelson法计算,如果药物在体内的药动学特征符合多室模型,则采用Loo-Riegelman法计算。但是Loo-Reieglman法计算公式复杂,吸收分数的计算引入了消除速率常数Ke,由于缓控释制剂的体内滞留时间较长,药物从制剂中释放速度较慢,尾段数据常混杂有吸收相,给尾段数据分析带来较大的误差。反卷积分法不需使用模型,而是直接根据实验数据得到关于药物体内动态的情况,适用于房室模拟困难的药物与缓控释制剂的体内外相关性研究[8]。
本实验同时采用了Loo-Reieglman法和反卷积分法研究了阿奇霉素泡囊的体内外相关性,反卷积分法由于采用数据较少,因而相关性系数也稍低。结果均表明阿奇霉素泡囊的体外释放和体内吸收没有相关性。
4 利益冲突
所有作者声明本文不涉及任何利益冲突。
| [1] | Zhang L, Chai X, Wang B, Yu S, Hu H, Zou Y, et al.Design, synthesis and biological evaluation of azithromycin glycosyl derivatives as potential antibacterial agents[J].Bioorg Med Chem Lett, 2013, 23:5057-5060. |
| [2] | Shorr A F, Zilberberg M D, Kan J, Hoffman J, Micek S T, Kollef M H.Azithromycin and survival in Streptococcus pneumoniae pneumonia: a retrospective study[J].BMJ Open, 2013, 3:e002898. |
| [3] | Giudicessi J R, Ackerman M J.Azithromycin and risk of sudden cardiac death: guilty as charged or falsely accused?[J].Cleve Clin J Med, 2013, 80:539-544. |
| [4] | Ruckmani K, Sankar V.Formulation and optimization of Zidovudine niosomes[J].AAPS Pharm Sci Tech, 2010, 11:1119-1127. |
| [5] | Honório Tda S, Pinto E C, Rocha H V, Esteves V S, dos Santos T C, Castro H C, et al.In vitro-in vivo correlation of efavirenz tablets using GastroPlus®[J].AAPS Pharm Sci Tech, 2013, 14:1244-1254. |
| [6] | Bose A, Wui W T.Convolution and validation of in vitro-in vivo correlation of water-insoluble sustained-release drug (domperidone) by first-order pharmacokinetic one-compartmental model fitting equation[J].Eur J Drug Metab Pharmacokinet, 2013, 38:191-200. |
| [7] | Prasanna R I, Sankari K U.Design, evaluation and in vitro-in vivo correlation of glibenclamide buccoadhesive films[J].Int J Pharm Investig, 2012, 2:26-33. |
| [8] | The United States Pharmacopeial Convention.USP 28-NF23, General Chapters:〈1088〉In vitro and In vivo evaluation of dosage forms[S/OL].Atlanta:2005[2013-10-29].http://www.usp.org/ |
 2014, Vol. 35
2014, Vol. 35


