对于局限性肾癌患者,肾癌根治术虽然能完整切除肿瘤,但也使得患者术后肾功能受损,术后肾功能不全的风险明显增加[1]。随着技术成熟,腹腔镜下肾部分切除术既能够完整切除肿瘤,又不影响肿瘤预后[2]。因此在2010年的欧洲泌尿外科肾癌指南[3]中,已经推荐对于局限性的肾癌患者在技术允许的情况下实施肾部分切除术,以保留肾功能。
微创是泌尿外科发展的趋势。随着腹腔镜技术的发展,单孔腹腔镜肾部分切除术作为既微创、美容,又最大限度保存肾功能的手术方法早在2009年就被报道[4],随后该技术在世界各地推广。我们在积累了丰富的单孔腹腔镜操作经验的基础上,于2009年8月完成国内第1例经脐单孔腹腔镜肾部分切除术[5],并进行了经验总结。肾部分切除术对于术中操作要求高,既要求完整切除肿瘤,确切缝合止血,还必须尽可能减少肾缺血时间[6],而单孔腹腔镜由于自身存在的“筷子效应”,使得单孔腹腔镜肾部分切除术难度进一步加大。
2013年我科完成了国内首例经腹3D单孔腹腔镜肾切除术[7]。3D腹腔镜是通过特殊的腹腔镜系统、影像采集和显示系统,使得术中能够获得三维立体的影像,从而使得手术操作更加精确。我们在积累了丰富的单孔腹腔镜操作经验的基础上,精心准备,并联合Olympus公司新研发生产的末端可弯的3D腹腔镜尝试进行单孔多通道经腹3D腹腔镜猪肾部分切除术,探讨该手术的可行性和安全性,总结操作经验,并对该动物模型的优缺点进行探讨。
1 材料和方法 1.1 实验动物及手术器械
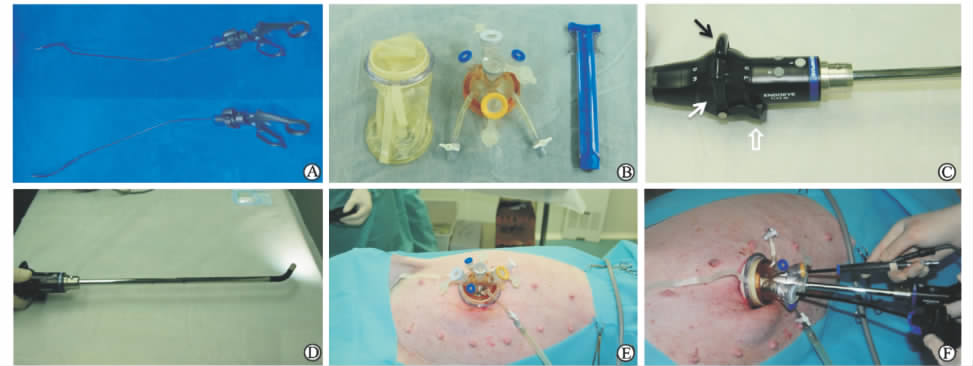
1岁雄性香猪1只,由上海汇智赢华医疗科技研发有限公司提供,体质量35 kg。手术操作于2014年1月2日在汇智赢华医疗科技研发有限公司动物实验中心(上海)完成。手术器械:5 mm无损伤抓钳、分离钳、剪刀、持针器、吸引器;5 mm电钩,5 mm可拆卸的预弯抓钳、分离钳、剪刀(图 1A)。单孔多通道组合套件:QuadPort单孔腹腔镜通道系统(QuadPort,OlympusTM),如图 1B所示。该通道由两部分组成:一部分为皮肤肌肉牵开器,包括1个内环和2个外环,由双层圆形塑料胶反折包裹;另一部分为多通道装置,包括1个12 mm套管、2个10 mm套管、2个5 mm的套管、1个独立进气通道及1个独立排气通道。3D腹腔镜手术系统(Olympus 3D System),包括3D摄像主机,型号22204011-114;5 mm末端可弯Olympus 0°3D腹腔镜(图 1C、1D);32 inch(1 inch=2.54 cm) 3D监视器;普通300 W氙灯光源)。
|
图 1 手术器械、手术体位及Port安置 Fig 1 Instruments of operation,operation positioning and port placement A:5 mm pre-curved instruments (OlympusTM); B: QuadPort (OlympusTM); C,D: Flexible 3D laparoscopy(OlympusTM); E,F:Positioning and port placement. The black and white arrows show the up and down angulation control lever,respectively; the white hollow arrow shows the angulation lock |
对实验猪实施全身麻醉(丙泊酚+维库溴铵+芬太尼)后,行气管插管术。取完全平卧位,四肢用束缚带固定,向左侧旋转手术床,使其与水平面成30°。常规消毒铺单后,取第四乳头平面,经右侧腹直肌行3.5 cm纵行手术切口,依次切开皮下、腹直肌鞘,钝性分离腹直肌约2~3 cm以适合Olympus QuadPort置入并具有较好的气密性,切开后鞘及腹膜进入腹膜腔,按Olympus QuadPort的器械使用说明置入单孔多通道组合套件(图 1E)。连接气腹机,以14 mmHg(1 mmHg=0.133 kPa)压力持续充气,充气满意后置入5 mm Olympus 末端可弯0°3D腹腔镜(图 1F)。 1.2.2 手术操作
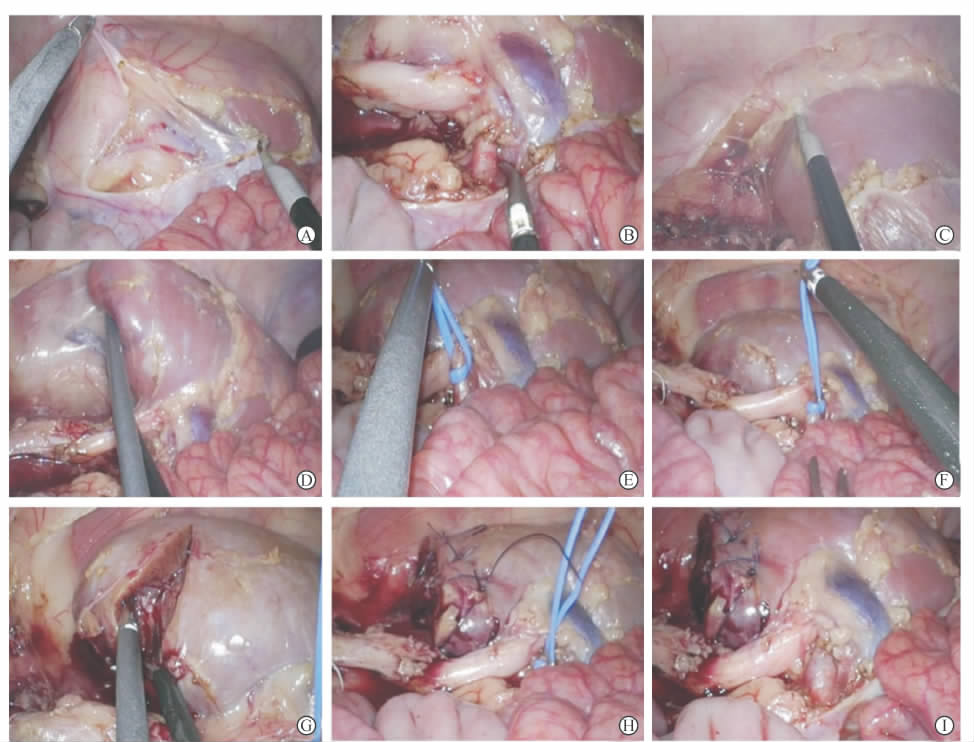
操作原则与常规经腹腹腔镜下右肾下极部分切除术相同。先用电钩分离并从肾蒂腹侧小心地打开肾周筋膜(图 2A),显露右肾蒂。用电钩或分离钳、吸引器小心剥离肾蒂周围脂肪,游离出右肾动脉(图 2B)。继续游离肾周腹侧面(图 2C)及下极背侧面,完全游离整个右肾下极(图 2D)。用蓝色橡皮带及钛夹阻断肾动脉(图 2E、2F)后,用剪刀锐性切除肾下极(图 2G)。更换5 mm持针器,用2-0薇乔可吸收线全层“8”字缝合肾脏创面(图 2H)。开放血流后肾脏创面未见明显渗血(图 2I)。标本用EndoCatchTM标本袋取出。
|
图 2 单孔3D腹腔镜肾部分切除术术中操作 Fig 2 Intra-operative maneuvers of transperitoneal 3D laparoendoscopic single-site partial nephrectomy A: Dissect peri-renal fascia to renal pedicle; B: Exposure of renal artery; C: Dissection of peri-renal fascia lateral to the right kidney; D: Expose the space dorsal to right kidney; E: Control of renal artery; F: Block the right renal artery; G: Resection of lower renal pole; H: Figure-8 sutures were used to close the wound; I: The wound of kidney after artery unclamping |
手术顺利,总手术时间为47 min,其中动脉阻断时间21 min,肾下极切除时间5 min,缝合时间为16 min。术中出血少,出血约20 mL,开放血流后未见明显渗血。无任何术中并发症。术毕,动物存活良好,生命体征平稳,由动物实验中心进行后续处理。
3 讨 论
单孔腹腔镜技术将泌尿外科微创推向了一个新的领域,而3D腹腔镜技术的引入,为腹腔镜下的视野提供了更加精确的景深,三维立体的图像使得腹腔镜操作视野如同开放手术一样。虽然早在1992年3D腹腔镜手术就应用于临床[8],但由于当时器械水平的限制,并未得到有效推广。真正大范围、成规模应用于临床始于近5年。2012年,北京协和医院完成了国内首例3D普通腹腔镜手术[9]。此后3D腹腔镜技术在国内得到了较好的推广。2013年,我们团队在积累了丰富的单孔腹腔镜操作经验的基础上,尝试性开展了国内首例单孔多通道经腹3D腹腔镜肾切除术[7]。此次,我们通过动物实验,探讨单孔多通道经腹3D腹腔镜下肾部分切除术的可行性、安全性,并初步尝试联合末端可弯3D腹腔镜,总结使用体会及手术经验。
单孔腹腔镜肾部分切除术开展难度大,对术者要求高,主要体现在术中精确操作上,不论是肾蒂血管显露、肾肿瘤精确切除,还是肾创面缝合止血,都需要精确操作。而单孔腹腔镜由于器械“打架”的问题,使得这些精确操作更难。3D腹腔镜可以给术者带来近乎真实的立体视觉,有效帮助术者进行纵深的判断,有助于术中的精确操作。本次操作中,肾脏切除时间5 min,缝合时间16 min,肾动脉总阻断时间21 min,接近普通腹腔镜肾部分切除术的操作。3D腹腔镜系统发展至今,在国际上已经形成了几大系统,如Karl Storz、 Olympus、Viking、贝朗等。目前随着显像技术的进步,3D腹腔镜已经由原来的标清进入了高清时代,这使得手术显示更加清晰,更加逼真。
我们曾探讨了3D腹腔镜在视野、操作等方面的优缺点[7]。在此,我们主要结合本研究的特点进行讨论。
(1) 猪作为3D单孔腹腔镜肾部分切除术动物模型主要的优缺点:国内高新课题组[10]曾进行单孔腹腔镜猪动物训练模型的构建,其中进行单孔肾部分切除术,成功率达80%。我们认为猪作为3D单孔腹腔镜肾部分切除术动物模型的优点如下:与兔、犬等其他动物相比,猪个体较大,腹腔解剖结构较接近人体。猪作为实验动物,较易获得。猪肾周解剖较简单,没有结肠覆盖,肾周脂肪少,易显露,适合于手术培训使用。然而猪肾周的解剖层次和结构与人体有一定差别,在猪进行的手术操作经验不能直接完全照搬到人体。另外,猪作为培训模型,费用较贵,且需要专门的麻醉人员、麻醉器械等进行配合。
(2) 末端可弯3D腹腔镜的使用:如图 1C、1D所示,该腹腔镜有3个机关控制可弯末端。实心黑白箭头示,通过前后运动,各自控制末端的上、下以及左右的弯曲。空心箭头所示机关用于锁定镜头末端弯曲状态。单孔腹腔镜虽然创伤小,瘢痕小,但由于单孔腹腔镜本身的原因,各个通道距离太近,普通腹腔镜器械操作近乎平行,常导致术中器械碰撞,产生干扰。本研究中采用末端可弯腹腔镜系统,可以巧妙避开器械“打架”的问题,通过可弯的末端,重建“三角关系”,在手术中取得满意视野。末端可弯3D腹腔镜有如下优点:5 mm实现高清成像,无需占用10 mm的通道;末端可弯,对于单孔腹腔镜的视野显露、防止器械“打架”等有明显帮助;利于狭小空间操作,甚至可以绕过组织观察组织背面的情况。然而它的缺点也很明显,末端可弯的软头容易损坏,弯曲时易受到组织的碰撞,进出通道时也要注意保护;由于末端可弯,视角的调整和适应需要一定过程;术中不能通过常规硬式腹腔镜的经验来判断进器械的角度。
(3) 3D单孔腹腔镜肾部分切除动物模型的体会:单孔腹腔镜肾部分切除术对精确操作要求高,要求术者在较短时间内完成切除、缝合,以减少肾脏缺血,保护肾功能。该动物模型可以为临床开展单孔腹腔镜肾部分切除术积累经验。除了3D腹腔镜的立体视野帮助,预弯或者可弯器械的使用也会对手术带来有效的帮助。在本次研究中,我们使用了Olympus新型可拆卸的预弯抓钳、分离钳及剪刀。该可拆卸的预弯器械可以通过拆卸后重新组装来调整左右,以便适合左、右手的使用。研究中预弯器械的使用能给单孔腹腔镜的操作带来便利,但需要术者适应预弯器械,熟悉器械的形状,防止在腹腔内意外损伤周围器官。该动物模型还可以让术中更好适应3D腹腔镜带来的立体视觉,积累3D腹腔镜立体视觉下解剖标识识别的经验。当然本模型尚存在一定局限,由于是正常肾脏,无法培训临床中真实肿瘤切除的情况,更无法培训术中超声对肿瘤切缘的定位等操作。
(4) 本研究的局限性:首先,本研究例数少,仅为1例,具有一定的局限性,仅作为经腹单孔多通道联合末端可弯3D腹腔镜行猪肾部分切除术的初步尝试,为后续建立规范化动物训练模型积累经验。其次,本研究选择动物的右肾下极进行手术,由于没有动物模型模拟肾脏“肿块”,故进行下半肾脏切除。因此和临床中肾脏肿瘤的肾部分切除术具有较大差异,无法训练肾脏肿瘤剥离、确保肿瘤切缘阴性等问题。再次,虽然本研究选择猪的右肾进行手术,但在实际操作中,由于猪的脾脏较大,对左肾操作可能会有一定影响。建议采用“金手指”拉钩通过单孔Port的一个通道进行牵拉,暴露术野。最后,由于猪的解剖和人的差异,腹膜后脂肪少,腹膜后间隙较难分离,容易导致腹膜破裂,猪的腹腔镜训练模型常采用经腹腹腔镜操作进行练习。
综上所述,本研究初步证实单孔多通道经腹3D腹腔镜下肾部分切除术总体可行、安全。联合末端可弯3D腹腔镜,使得手术图像立体感强,手术操作精确度高,能有效降低单孔器械“打架”及手眼协调难度。应用猪作为动物模型进行单孔多通道联合末端可弯3D腹腔镜肾部分切除术可以让外科医生有效积累手术经验及技巧。本研究中单孔3D腹腔镜猪肾部分切除术是国内单孔3D腹腔镜手术临床应用研究的一个突破,希望通过3D与单孔腹腔镜优势的结合,降低单孔腹腔镜肾部分切除术的难度,减少手术创伤,减少术中肾脏缺血时间,最大限度地保留肾脏功能,提高术中精确缝合、止血等操作的准确性、有效性,为临床应用积累经验,为手术规范培训积累经验。
4 利益冲突
所有作者声明本文不涉及任何利益冲突。
| [1] | Porpiglia F,Fiori C,Bertolo R,Morra I,Russo R,Piccoli G,et al.Long-term functional evaluation of the treated kidney in a prospective series of patients who underwent laparoscopic partial nephrectomy for small renal tumors[J].Eur Urol,2012,62:130-135. |
| [2] | Margulis V,Tamboli P,Jacobsohn K M,Swanson D A,Wood C G.Oncological efficacy and safety of nephron-sparing surgery for selected patients with locally advanced renal cell carcinoma[J].BJU Int,2007,100:1235-1239. |
| [3] | Ljungberg B,Cowan N C,Hanbury D C,Hora M,Kuczyk M A,Merseburger A S,et al. EAU guidelines on renal cell carcinoma: the 2010 update[J].Eur Urol,2010,58:398-406. |
| [4] | Aron M,Canes D,Desai M M,Haber G P,Kaouk J H,Gill I S.Transumbilical single-port laparoscopic partial nephrectomy[J].BJU Int,2009,103:516-521. |
| [5] | 刘冰,王林辉,杨印辉,罗文彬,罗睿,杨波,等.经脐单孔多通道腹腔镜下肾部分切除术的初步应用[J].第二军医大学学报,2010,31:1349-1352. Liu B,Wang L H,Yang Y H,Luo W B,Luo R,Yang B,et al.Transumbilical laparoendoscopic single-site partial nephrectomy: an initial clinical experience of 2 cases[J].Acad J Sec Mil Med Univ,2010,31:1349-1352. |
| [6] | Colombo J R Jr,Haber G P,Gill I S.Laparoscopic partial nephrectomy in patients with compromised renal function[J].Urology,2008,71:1043-1048. |
| [7] | 王林辉,刘冰,王志向,杨庆,叶华茂,鲍一,等.中国首例单孔多通道经腹3D腹腔镜肾切除术[J].第二军医大学学报,2013,34:1116-1120. Wang L H,Liu B,Wang Z X,Yang Q,Ye H M,Bao Y,et al.Transperitoneal 3D laparoendoscopic single-site (LESS) nephrectomy: the first clinical case in China[J].Acad J Sec Mil Med Univ,2013,34:1116-1120. |
| [8] | Becker H,Melzer A,Schurr M O,Buess G.3-D video techniques in endoscopic surgery[J].Endosc Surg Allied Technol,1993,1:40-46. |
| [9] | 李汉忠,张玉石,张学斌,徐维锋,李永强,纪志刚,等.3D腹腔镜系统在泌尿外科手术中的应用[J].中华泌尿外科杂志,2013,34:325-328. |
| [10] | 温星桥,黄文涛,郑骏明,司徒杰,张淑璇,孙其鹏,等.单孔腹腔镜猪动物训练模型的建立体会[J].中华腔镜泌尿外科杂志:电子版,2011,5:10-12. |
 2014, Vol. 35
2014, Vol. 35


