原发性肝癌是全球最常见的第五大肿瘤,且位居肿瘤致死病因的第三位[ 1 ]。在我国,其发病率居恶性肿瘤的第四位,在肿瘤致死病因中则位居第二[ 2 ]。原发性肝癌以肝细胞癌(hepatocellular carcinoma,HCC)为主,同时伴发肝炎、肝硬化。到目前为止,肝癌的发生机制仍不能完全明确,有关肝炎、肝硬化与肝癌之间转归的争议一直存在。20世纪80年代以来,一些学者就肝癌组织与不同质地肝组织之间的胶原差异性分布进行了分析[ 3,4 ],但尚欠缺深入研究的相关报道。本实验拟通过建立大鼠肝癌模型,动态观察大鼠肝脏历经炎症、硬化、癌变过程中胶原纤维的变化情况,并总结其规律,为肝癌的进一步防治研究提供参考。
1 材料和方法 1.1 实验动物及分组SPF级雄性Wistar大鼠50只,体质量80~120 g,由南方医科大学实验动物中心提供,许可证号:SCXK(粤)2011-00015。大鼠每笼4只,饲养在25℃恒温SPF级层流室,标准化光照(12 h光照和12 h黑暗交替),自由摄取鼠粮、蒸馏水,隔日更换垫料,适应环境1周。全部大鼠按照随机数字表法分为模型组及对照组。
1.2 肝癌模型的建立肝癌大鼠模型的建立参照Park等[ 5 ]报道的方法并稍加改进。模型组经腹腔注射二乙基亚硝胺(DEN,Sigma-Aldrich公司产品)溶液(50 mg/kg,加生理盐水至0.1 mL,超声振荡溶解),2次/周,连续4周后改为同样剂量1次/周,至14周停止。正常对照组腹腔注射生理盐水0.1 mL,2次/周,连续4周后改为同样剂量1次/周,至14周停止。
1.3 取材于诱癌开始前及诱癌后第2、4、8、12、14、18周,分批处死大鼠,模型组和对照组各时间点处死的大鼠数均为3只。 剖腹取肝脏,观察肝脏外观(包括大小、色泽、质地、有无结节形成等),出现癌灶者取肉眼癌灶及距癌灶边缘1 cm癌旁组织,未出现癌灶者随机取部分肝组织,均用10%甲醛溶液固定,用于病理石蜡切片制备,所取组织块大小约0.5 cm×0.5 cm。其余标本置-80℃冰箱冷冻保存。
1.4 肝组织病理学观察对大鼠肝组织标本按常规进行H-E染色。 采用Masson染色法对肝组织中胶原进行染色,嗜银染色(网状染色)对网状纤维进行染色,具体操作按试剂盒说明书进行。染色后于光镜下观察肝组织病理学改变。
1.5 肝组织胶原含量动态观察采用荧光定量PCR技术检测肝组织Ⅰ、Ⅲ型胶原mRNA含量,观察胶原含量随肝癌进展过程的动态变化。 1.6 肝组织基质金属蛋白酶(MMP)含量检测
采用明胶酶谱法检测肝组织中MMP-2、MMP-9含量。 1.7 统计学处理
使用SPSS 13.0统计软件对实验数据进行统计分析。不同时间点两组间比较采用独立样本t检验,同一时间点组内不同组织间的比较采用配对t检验,不同时间点多组间比较采用单因素方差分析。检验水准(α)为0.05。 2 结 果 2.1 肝组织病理学变化
本模型中肝脏的病理变化以肝脏炎性反应、胶原纤维沉积、肝硬化结节形成、肝癌形成为主要特点。主要分为3个阶段。 2.1.1 肝细胞损伤、肝纤维化阶段(0~4周)
从肝脏大体外观来看,第2周肝脏边缘略钝,第4周肝表面粗糙。光学显微镜下观察,2周时炎性反应较重,淋巴细胞浸润明显,4周时可见桥接坏死,但肝小叶结构尚完整。组织内胶原主要沉积在汇管区结缔组织、中央静脉以及窦周,无纤维隔形成,可见透明细胞病灶形成(图 1A)。
2.1.2 肝硬化形成阶段(5~12周)第8周取材时发现肝硬化形成(3/3),肝脏体积明显增大,肝质地变硬,表面凹凸不平。光学显微镜下观察,中央静脉周围坏死、塌陷,胶原纤维沉积形成完整的纤维隔,包绕再生肝实质,形成大小不等的肝硬化结节,肝小叶结构完全被破坏,透明细胞灶增多增大,Masson、嗜银染色可见大量纤维沉积,并见纤维桥接坏死(图 1B~1D)。 2.1.3 肝癌形成阶段(14周以后)
肝脏体积较前稍增大,色泽晦暗,肝表面布满粗颗粒结节,并可见癌结节(1~2个/只),至18周时,癌结节增多、增大(2~10个/只),有的癌结节伴有出血坏死,呈暗紫色(图 1E)。光学显微镜下观察,癌结节多与周围肝组织界限清楚,胶原纤维沉积较周围组织减轻,癌细胞核多较大,形态不规则,核分裂像易见,后期可见血管内癌栓(图 1F)。

|
图 1 模型组诱癌不同时间肝组织病理或大体观察 Fig 1 Pathological or macroscopic observation of liver tissues at different time points of hepatocellular carcinoma (HCC) induction A: Hepatitis-hepatic fibrosis(4 weeks,H-E staining); B: Hepatic cirrhosis(12 weeks,Masson staining); C: Hepatic cirrhosis(12 weeks,Ag staining); D: Hepatic cirrhosis(12 weeks,H-E stainning); E: Liver cancer with hemorrhage(18 weeks); F: Tumor thrombus formation(18 weeks,H-E staining). Original magnification: ×100(A),×200(B,D,F) |
诱癌2周时,模型组肝组织内Ⅰ型胶原mRNA含量较诱癌前差异无统计学意义;4周以后均较2周时明显增加(P<0.01),表达量由低至高依次为4周<8周<12周<14周<18周(均P<0.01)。14周及18周时,肝癌组织中Ⅰ型胶原mRNA含量均较癌周肝组织减少,差异有统计学意义(P<0.05);比较癌组织内Ⅰ型胶原mRNA含量,18周时较14周时减少,差异有统计学意义(P<0.05)。具体数据见表 1。 2.2.2 Ⅲ型胶原mRNA含量
诱癌2周时,模型组Ⅲ型胶原mRNA含量较诱癌前增加,差异有统计学意义(P<0.05),4周时较2周时显著增加(P<0.01),8周时较4周时显著增加(P<0.01),12周时较8周时显著增加(P<0.01),但14周时较12周时差异无统计学意义(P>0.05),18周时较14周时显著增加(P<0.01)。14周、18周时,癌组织内Ⅲ型胶原mRNA含量均较癌周组织减少,差异有统计学意义(P<0.05);比较癌组织内Ⅲ型胶原mRNA含量,18周时较14周时减少,差异有统计学意义(P<0.05)。具体数据见表 1。
|
|
表 1 肝组织中胶原mRNA含量的动态变化
Tab 1 Expression levels of collagen type Ⅰ and type Ⅲ mRNA at different time points of hepatocellular carcinoma (HCC) induction n=3,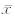 ±s ±s
|
采用明胶酶谱法检测肝组织中MMP-2、MMP-9含量,结果见表 2。正常肝组织MMP-2 和MMP-9酶原形式均有表达,但表达量较低,而其活性形式均未检测到。4周时,上述两种酶原的表达增加,活性形式仍未能检测到;8周时,两种酶原表达进一步增加;12周以后能检测到MMP-2活性形式;14周后癌灶形成,癌组织内MMP-2、MMP-9、活性MMP-2表达较前进一步增高。
|
|
表 2 肝组织中金属蛋白酶含量的动态变化
Tab 2 Relative expression levels of matrix metalloproteinases (MMP)-2 and MMP-9 at different time points of hepatocellular carcinoma (HCC) induction n=3,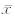 ±s ±s
|
肝癌是全球常见的恶性肿瘤之一,死亡率位列所有癌症的第3位[ 1 ],世界上每年新诊断的病例约60万例。据统计,2007年我国城市居民肝癌死亡率
占所有恶性肿瘤的第2位(25.47/10万),在农村居民中,肝癌死亡率甚至达到了28.72/10万[ 6 ]。虽然肝癌外科治疗技术日益完善,但许多肝癌患者就诊时病情已至中、晚期,客观上导致术后复发率居高不下,严重影响患者预后[ 7 ]。因此,肝癌的预防和早期诊断至关重要。我国肝癌患者多伴发肝硬化,肝硬化甚至被看作是肝癌的前期病变[ 8,9 ]。目前研究较多的肝癌癌前病变包括肝硬化基础上肝细胞的不典型增生、腺瘤样增生、变异肝细胞结节等[ 10 ]。但是,各地区病理学家在交界性病变的评价上仍存在争议,如边界不清晰的异形增生结节(DNs)在西方病理学家看来诊断为高级别的异形增生结节(HGDNs),在日本却认为是早期高分化的HCC(eWDHCC)[ 11 ]。这种争议在未来仍会存在,并将影响肝癌的治疗。正如英国病理学会百年纪念日大会上所说:“未来人类许多癌症的一系列评估指标将作为常规形态学上评估预后指标的参考。当我们到达一个存在有效的治疗手段的时期,精确的肿瘤分类对于治疗还是非常重要,外科病理将无疑继续占有一个中心地位” [ 12 ]。
肝硬化作为肝脏的常见疾病,主要是由于肝细胞受损后肝内胶原纤维过度沉积所致。肝癌与肝硬化的转归关系备受重视,很多学者进行了相关研究,其中肝癌组织与硬化肝组织之间的胶原差异,自20世纪80年代以来陆续有学者进行了分析 [ 3,4 ] ,但进展缓慢。肝脏胶原纤维是细胞外基质的主要组成成分,不仅对细胞和组织器官起着机械支持作用,还能调节和控制细胞增生、迁移、极性和分化。迄今已确定了19种不同基因的胶原类型[ 13,14 ]。肝脏中主要有5类胶原[ 15 ],分为间质性胶原(Ⅰ、Ⅲ、Ⅴ、Ⅵ)及基底膜胶原(Ⅳ)。肝硬化时Ⅰ、Ⅲ、Ⅳ型胶原的分布与正常肝一致,但含量均增加。正常人肝脏胶原约占肝质量的2%,肝硬化时上升至8%~10%,以Ⅰ型胶原显著增加为特征,使肝内Ⅰ/Ⅲ型胶原比例倒置[ 16 ]。
本实验进一步证实了肝脏硬化过程中,组织内Ⅰ、Ⅲ型胶原沉积持续增加;肝癌组织内Ⅰ、Ⅲ型胶原含量较癌旁组织降低,至本实验结束,癌灶组织内胶原量持续减少,MMP含量异常增加。以往资料提示癌组织内胶原合成是比较活跃的[ 17,18 ],结合本实验结果,我们考虑导致癌组织内胶原减少的原因可能是胶原的降解较胶原合成更为活跃。而癌灶内胶原降解与合成的平衡可能与肝癌的预后有关,有研究指出相对于胶原降解程度高的肝癌组织,降解程度低的癌组织分化程度较高[ 4 ]。 癌组织内胶原降解活跃可能跟肿瘤细胞自身产生MMP并刺激宿主细胞产生此酶有关[ 19,20 ],这与我们的实验结果一致。癌组织胶原被降解,局部形成溶解区构成肿瘤移动的通道,通过细胞黏附分子、播散因子等作用,促使肿瘤转移,这被认为在肿瘤的浸润和转移中发挥重要作用[ 21,22 ]。我们的实验结果进一步验证了大鼠肝脏癌变前后Ⅰ、Ⅲ型胶原沉积及MMP含量的变化特点,成癌的时间在12周至14周之间,随着实验的进行,癌灶呈多发、直径增大的趋势,这与临床观察的肝癌进展特点相符,而癌灶内胶原持续减少,很可能是导致这种现象的原因之一。下一步我们将深入观察该时间区间内肝组织胶原变化特点,并引入药物拮抗,探讨影响肝癌进展过程的可能。
4 利益冲突
所有作者声明本文不涉及任何利益冲突。
| [1] | Verslype C,Van Cutsem E,Dicato M,Arber N,Berlin J D,Cunningham D,et al.The management of hepatocellular carcinoma.Current expert opinion and recommendations derived from the 10th World Congress on Gastrointestinal Cancer,Barcelona,2008[J].Ann Oncol,2009,20 Suppl 7:vii1-vii6. |
| [2] | 曹广文.以社区为基础的群体医学在恶性肿瘤预防和控制中的重要意义[J].第二军医大学学报,2014,35:1-7. Cao G W.Significance of community-based population medicine in prevention and control of malignant diseases [J].Acad J Sec Mil Med Univ,2014,35:1-7. |
| [3] | Yamamoto M,Sumiyoshi H,Nakagami K,Tahara E. Distribution of collagen types Ⅰ,Ⅲ,and Ⅴ in fibrotic and neoplastic human liver[J].Acta Pathol Jpn,1984,34:77-86. |
| [4] | 王要军,孙自勤.人肝细胞癌及癌旁肝组织Ⅰ、Ⅲ型胶原的定量研究[J].医学理论与实践,1996,9:53,59. |
| [5] | Park D H,Shin J W,Park S K,Seo J N,Li L,Jang J J,et al.Diethylnitrosamine (DEN) induces irreversible hepatocellular carcinogenesis through overexpression of G1/S-phase regulatory proteins in rat[J].Toxicol Lett,2009,191(2-3):321-326. |
| [6] | 中华人民共和国卫生部.2008中国卫生统计年鉴[M].北京:中国协和医科大学出版社,2008: 232,269. |
| [7] | Llovet J M,Burroughs A,Bruix J.Hepatocellular carcinoma[J].Lancet,2003,362:1907-1917. |
| [8] | Simonetti R G,Cammà C,Fiorello F,Politi F,D'Amico G,Pagliaro L.Hepatocellular carcinoma.A worldwide problem and the major risk factors[J].Dig Dis Sci,1991,36:962-972. |
| [9] | Fattovich G,Stroffolini T,Zagni I,Donato F.Hepatocellular carcinoma in cirrhosis: incidence and risk factors[J].Gastroenterology,2004,127(5 Suppl 1):S35-S50. |
| [10] | 杨拥军.肝细胞性肝癌癌前病变形态学特点及分子生物学研究进展[J].中国肿瘤,2008,17: 41-44. |
| [11] | Kojiro M.Diagnostic discrepancy of early hepatocellular carcinoma between Japan and West [J].Hepatol Res,2007,37 Suppl 2:S121-S124. |
| [12] | Hall P A,Wright N A.Understanding Disease.A Centenary Celebration of the Pathological Society of Great Britain and Ireland[M].Chicester: John Wiley & Sons Ltd,2006:207-216. |
| [13] | 陈惠黎.生物大分子的结构和功能[M].上海:上海医科大学出版社,1999:113-123. |
| [14] | Friedman S L.Molecular regulation of hepatic fibrosis,an integrated cellular response to tissue injury[J].J Biol Chem,2000,275:2247-2250. |
| [15] | Aycock R S,Seyer J M.Collagens of normal and cirrhotic human liver[J].Connect Tissue Res,1989,23:19-31. |
| [16] | Elsharkawy A M,Mann D A.Nuclear factor-kappaB and the hepatic inflammation-fibrosis-cancer axis[J].Hepatology,2007,46:590-597. |
| [17] | Liotta L A,Thorgeirsson U P,Garbisa S.Role of collagenases in tumor cell invasion[J].Cancer Metastasis Rev,1982,1:277-288. |
| [18] | Bramhall S R.Stromal degradation by the malignant epithelium in pancreatic cancer and the therapeutic potential of proteolytic inhibition[J].J Hepatobiliary Pancreat Surg,1998,5:392-401. |
| [19] | Del Bigio M R,Seyoum G.Effect of matrix metalloproteinase inhibitors on rat embryo development in vitro[J].Cells Tissues Organs,1999,165:67-73. |
| [20] | Mäkelä M,Larjava H,Pirilä E,Maisi P,Salo T,Sorsa T,et al.Matrix metalloproteinase 2 (gelatinase A) is related to migration of keratinocytes[J].Exp Cell Res,1999,251:67-78. |
| [21] | Legrand C,Gilles C,Zahm J M,Polette M,Buisson A C,Kaplan H,et al.Airway epithelial cell migration dynamics.MMP-9 role in cell-extracellular matrix remodeling[J].J Cell Biol,1999,146:517-529. |
| [22] | Zeng Z S,Cohen A M,Guillem J G.Loss of basement membrane type Ⅳ collagen is associated with increased expression of metalloproteinases 2 and 9 (MMP-2 and MMP-9) during human colorectal tumorigenesis[J].Carcinogenesis,1999,20:749-755. |
 2014, Vol. 35
2014, Vol. 35


