欧洲泌尿外科学会《肾细胞癌诊疗指南》推荐保留肾单位手术为cT1期肾肿瘤的标准治疗方式[1]。对于肾部分切除术而言,除肿瘤大小外,肿瘤空间位置也是影响手术安全和疗效的重要因素。2009年,Kutikov等[2]率先提出了基于肾脏肿瘤空间位置的半定量评分系统R.E.N.A.L.,包括: 肿瘤最大径R(Radius)、肿瘤内外生比例E(exophytic/endophytic properties)、肿瘤与集合系统或肾窦距离N(nearness of the tumor to the collecting system or sinus)、肿瘤位于腹侧或背侧A(anterior/posterior)、肿瘤在冠状位上与上下极线及中线的位置关系L(location relative to the polar lines),以及肿瘤是否累及肾脏动静脉主干H(hilar),其中A和H作为定性描述,其余4个参数均以1~3分描述并计算总分。根据R.E.N.A.L.评分系统,总分得分为4~6分的肾肿瘤为低度复杂程度,7~9分为中度复杂程度,10~12分为高度复杂程度。这一评分系统客观、全面描述了肾脏肿瘤的空间解剖位置特点,大大提高了来自不同单位文献报道之间的可比性,同时也为肾部分切除术适应证的界定提供了新的方法。本研究旨在运用R.E.N.A.L.评分系统分析2012年3月至2013年9月 第二军医大学长海医院泌尿外科同一术者连续完成的70例达芬奇机器人辅助腹腔镜肾部分切除术中的肿瘤特点及手术疗效,并探讨这一术式的临床应用价值。 1 资料和方法 1.1 一般资料
2012年3月至2013年9月第二军医大学长海医院泌尿外科收治的70例患者,男性47例、女性23例,年龄(52.8±10.3)岁,体质指数(body mass index, BMI)为(24.8±3.25) kg/m2,麻醉评分(American Society of Anesthesiologists Score, ASA)为(2.0±0.4)分,Charlson全身合并症评分(age-weighted)为(0.7±1.03)分。左侧肿瘤38例(其中孤立肾肾肿瘤1例),右侧肿瘤32例(其中孤立肾肾肿瘤1例),肿瘤均为单发,肿瘤最大径(3.7±1.31) cm;R.E.N.A.L.评分(8.1±1.31)分;腹侧肿瘤24例,背侧31例,难以区分15例,肾门型即累及肾脏动静脉主干肿瘤5例。 术前估算的肾小球滤过率(estimated glomerular filtration rate,eGFR)为(97.8±23.1) mL/(min·1.73 m2)。 1.2 手术方法 手术入路选择经腹腔途径或经后腹腔途径,主要根据肿瘤位置、患者肥胖程度、有无既往腹腔手术史等确定。具体手术步骤参照文献[3],与传统腹腔镜肾部分切除术相似。对于完全内生的肿瘤,术中需借助内镜下超声定位进行准确切除(图 1)。
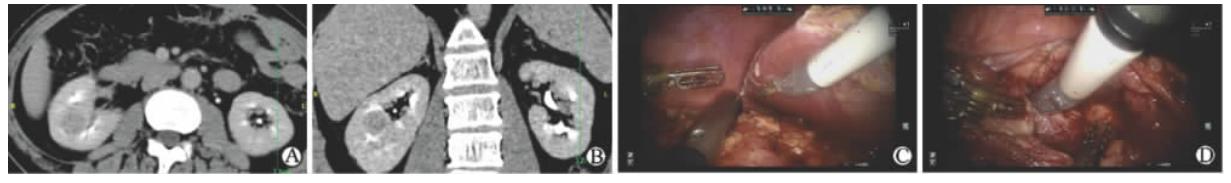 | 图 1 达芬奇机器人辅助腹腔镜右肾部分切除术 Fig 1 da Vinci robot-assisted laparoscopic right partial nephrectomy A, B: Complete endophytic tumor in the right kidney, R.E.N.A.L. score 1+3+3+X+3=10X; C: Tumor orientation with laparoscopic ultrasound probe; D: Tumor excision |
根据肾肿瘤R.E.N.A.L.评分系统得分高低,分为低度复杂程度组(4~6分)6例,中度复杂程度组(7~9分)55例和高度复杂程度组(10~12分)9例。收集并比较各组患者的手术时间、术中出血量、缺血时间、术中输血情况、术中并发症、切缘阳性率,术后住院时间、术后输血情况、术后并发症、病理学结果和随访情况(随访时间、肿瘤复发转移、估算肾功能情况下降比例),同时比较患者术前术后肾功能变化。术后并发症严重程度按照Clavien分级标准[4]评定。应用SPSS 16.0软件处理数据。连续变量以 ±s表示,组间比较采用Wilcoxon符号秩检验或Jonckheere-Terpstra非参数检验;分类变量采用频数或百分数表示,组间比较采用Pearson χ2检验。检验水准(α)为0.05。 2 结 果 2.1 手术疗效
70例手术中,1例因术中出血中转开放手术完成,其余手术均顺利完成,无中转根治手术。手术时间(230±48.3) min。 术中出血量(154±135.9) mL。术中1例未阻断肾蒂完成,1例高选择性阻断肾分支动脉完成,其余均阻断肾动脉主干完成,阻断时间(23.0±9.30) min。术后住院时间(11.4±4.44) d。总体输血率8.57%(6/70)。总体手术并发症发生率17.1%(12/70),术中并发症发生率1.43%(1/70),术后并发症发生率15.7%(11/70),其中Clavien Ⅰ~Ⅱ级10例,Clavien Ⅳ级1例。 2.2 术后病理及随访
病理学检查提示: 手术切缘均为阴性,组织学类型为肾细胞癌58例 (透明细胞癌51例, 乳头状细胞癌1例, 嫌色细胞癌6例),血管平滑肌脂肪瘤4例,肾囊肿及囊肿性病变4例,嗜酸细胞腺瘤、后肾腺瘤、炎性病变和瘢痕样组织增生各1例。术后随访1~18个月,均未见肿瘤复发或转移。末次随访eGFR为(90.8±22.3) mL/(min·1.73 m2),与术前比较差异有统计学意义(P=0.003)。 2.3 不同复杂程度患者临床资料对比
根据肾肿瘤R.E.N.A.L.评分系统得分分组,组间各参数比较结果(表 1)显示: 低、中、高复杂程度(R.E.N.A.L.评分)组间各参数之间,在前10例中完成的例数(50.0% vs 10.9% vs 11.1%, P=0.033)、手术时间[(213±35.5) vs (225±48.9) vs (269±31.7) min, P=0.008]、术中出血量 [(86±31.3) vs (158±148.5) vs (172±66.7) mL, P=0.032]和缺血时间 [(18.9±7.54) vs (22.2±8.88) vs (30.4±9.76) min, P=0.019]差异有统计学意义。 3 讨 论
近年来,保留肾单位手术在可选择适应证患者中的获益被进一步阐明,对于局限性尤其是T1期肾癌,肾部分切除术可提高患者术后生活质量,并延长患者生存时间[5,6]。同时,微创外科的快速发展使我们可以拥有更多技术完成肾部分切除术,比如: 传统腹腔镜技术、单孔腹腔镜技术以及达芬奇机器人腹腔镜技术等。因此,仅凭肿瘤大小作为肾部分切除术临床决策或适应证界定的唯一依据并不全面。R.E.N.A.L.评分系统的创立者通过分析1966年至2008年有关肾脏肿瘤手术的所有文献,建立了全面衡量肾肿瘤空间解剖位置的可量化评分系统,为手术适应证的界定提供了一种更实用的方法[2]。
| 表 1 机器人腹腔镜肾部分切除术低、中、高复杂程度(R.E.N.A.L. 评分)组间疗效比较Tab 1 Comparison of surgical outcomes of robotic laparoscopic partial nephrectomy between groups with different R.E.N.A.L. scores |
本研究运用R.E.N.A.L.评分系统分析了同一术者1年半以来连续完成的70例达芬奇机器人腹腔镜肾部分切除术中的肿瘤特点,发现这一术式在适应证选择方面有以下特点: (1)中度复杂程度(R.E.N.A.L.评分7~9分)的T1期肾肿瘤是其主要的适应证,缺血时间可以控制在25 min以内,在前10例中即可顺利完成。(2)低度复杂程度(R.E.N.A.L.评分4~6分)的T1期肾肿瘤所占比例较小,且50.0%的病例在前10例中完成,这一方面说明了对于有丰富传统腹腔镜肾部分切除手术经验的医生,在开始使用达芬奇机器人腹腔镜完成肾部分切除术时仍应选择难度较小的病例,确保患者安全和手术成功;另一方面,虽然缺血时间多可控制在20 min甚至10 min以内,但机器人辅助腹腔镜尚未成为这一类肾肿瘤手术的主流技术,这可能与机器人腹腔镜手术较昂贵的手术费用以及用传统腹腔镜技术亦可取得不错疗效有关。(3)高度复杂程度(R.E.N.A.L.评分10~12分)的肾肿瘤在本研究中所占比例不高,且多在第10例手术后完成,说明机器人辅助腹腔镜肾部分切除术在这一部分肿瘤中的学习曲线较长。但是,结果显示缺血时间多可控制在30 min左右,且无任何手术并发症,无输血病例,这很好地证实了机器人腹腔镜技术在完成复杂高难度肾部分切除术时的优势,在手术安全性、手术疗效方面是传统腹腔镜技术难以比拟的。
此外,本研究还对各组的手术效果进行了比较,发现肿瘤复杂程度的高低可能与手术时间、术中出血和缺血时间有关。R.E.N.A.L.评分能否预测手术结果,国外文献报道并不一致,有研究发现R.E.N.A.L.评分与缺血时间、手术并发症等相关[7, 8],也有报道两者并无关联[9]。R.E.N.A.L.评分系统创立者的本意并非用该系统预测手术结果,而旨在全面、客观描述肾肿瘤空间位置特点,促进并提高学术交流的质量[2]。我们认为缺血时间、并发症风险等与肿瘤复杂程度有一定联系,但是两者在多大程度上关联仍需进一步研究,本研究由于样本量较小未作进一步亚组分析。总体上说,机器人辅助腹腔镜肾部分切除术安全性高,虽有一定并发症发生率,但绝大多数属低级别Clavien分级;肾功能损害较小,总体eGFR下降比例多在10%以内;短期肿瘤控制效果确切,但仍需进一步随访观察。
达芬奇机器人辅助腹腔镜肾部分切除术安全、可行、有效,尤其在处理复杂程度较高的肾肿瘤时优势明显。应充分通过R.E.N.A.L.评分系统术前评估手术的复杂难度,并根据自己的手术经验来确定手术,指导达芬奇机器人腹腔镜技术在临床的合理应用,始终把手术质量和患者安全放在第一位。 4 利益冲突
所有作者声明本文不涉及任何利益冲突。
| [1] | Ljungberg B, Cowan N C, Hanbury D C, Hora M, Kuczyk M A, Merseburger A S, et al.EAU guidelines on renal cell carcinoma:the 2010 update[J].Eur Urol, 2010, 58:398-406. |
| [2] | Kutikov A, Uzzo R G.The R.E.N.A.L.nephrometry score:a comprehensive standardized system for quantitating renal tumor size, location and depth[J].J Urol, 2009, 182:844-853. |
| [3] | 王林辉, 叶华茂, 徐 斌, 刘 冰, 纪家涛, 肖 亮, 等.机器人辅助腹腔镜下肾部分切除术12例报告[J].中华泌尿外科杂志, 2012, 33:814-817. |
| [4] | Dindo D, Demartines N, Clavien P A.Classification of surgical complications:a new proposal with evaluation in a cohort of 6 336 patients and results of a survey[J].Ann Surg, 2004, 240:205-213. |
| [5] | MacLennan S, Imamura M, Lapitan M C, Omar M I, Lam T B, Hilvano-Cabungcal A M, et al.Systematic review of oncological outcomes following surgical management of localised renal cancer[J].Eur Urol, 2012, 61:972-993. |
| [6] | MacLennan S, Imamura M, Lapitan M C, Omar M I, Lam T B, Hilvano-Cabungcal A M, et al.Systematic review of perioperative and quality-of-life outcomes following surgical management of localised renal cancer[J].Eur Urol, 2012, 62:1097-1117. |
| [7] | Rosevear H M, Gellhaus P T, Lightfoot A J, Kresowik T P, Joudi F N, Tracy C R.Utility of the RENAL nephrometry scoring system in the real world:predicting surgeon operative preference and complication risk[J].BJU Int, 2012, 109:700-705. |
| [8] | Altunrende F, Laydner H, Hernandez A V, Autorino R, Khanna R, White M A, et al.Correlation of the RENAL nephrometry score with warm ischemia time after robotic partial nephrectomy[J].World J Urol, 2013, 31:1165-1169. |
| [9] | Mufarrij P W, Krane L S, Rajamahanty S, Hemal A K.Does nephrometry scoring of renal tumors predict outcomes in patients selected for robot-assisted partial nephrectomy?[J].J Endourol, 2011, 25:1649-1653. |
 2014, Vol. 35
2014, Vol. 35


