扩展功能
文章信息
- 邱红, 邹立, 张民生, 朱超祁, 贾永刚
- QIU Hong, ZOU Li, ZHANG MinSheng, ZHU ChaoQi, JIA YongGang
- 南海北部油气缓释环境沉积物脂类化合物组成特征
- Compositions of Lipid Compounds in the Oil and Gas Releasing Sediments in the Northern South China Sea
- 沉积学报, 2019, 37(2): 416-423
- ACTA SEDIMENTOLOGICA SINCA, 2019, 37(2): 416-423
- 10.14027/j.issn.1000-0550.2018.137
-
文章历史
- 收稿日期:2017-12-25
- 收修改稿日期: 2018-05-15
2. 中国海洋大学海洋环境与生态教育部重点实验室, 山东青岛 266100;
3. 中国海洋大学山东省海洋环境地质工程重点实验室, 山东青岛 266100
2. Education Key Laboratory for Marine Environment and Ecology, Ocean University of China, Qingdao, Shandong 266100, China;
3. The Shandong Provincial Key Laboratory of Marine Environment and Geological Engineering, Ocean University of China, Qingdao, Shandong 266100, China
南海(South China Sea,SCS)作为我国最大边缘海,总面积约为350×104 km2,其北部受欧亚板块和太平洋板块的影响,复杂的地质作用,强烈的岩浆活动和频繁的构造运动,形成了以陆架、陆坡和深海盆地为主的地貌类型,控制了沉积物的分布和沉积相的特征[1]。南海沉积物有机碳分布受陆源输入影响显著,其中北部海域在中新世以来,平均沉积速率高达54.2 cm/ka,在陆坡形成巨厚的海相沉积,汇集了丰富的陆源输入,有机碳含量平均高达0.81%[2]。该区域甲烷流体活动带沉积物中有机碳含量介于0.11%~0.97%,泥质区有机碳含量较高[3]。随着埋藏深度增加,沉积环境由氧化转向还原条件,有机碳含量逐渐降低,埋藏更深沉积物中有机碳含量变化较小[4]。油气主要通过有机碳发生一系列的化学反应转化而来,只要沉积速率大于30 m/Ma,有机碳含量达到0.5%,即可满足水合物形成所需的生物成因甲烷[5]。南海北部发育着南海最高沉积速率堆积体,全新世时期沉积速率达到89~819 m/Ma,有机碳含量大于0.7%,可以满足天然气水合物形成的气源条件[6]。
海洋油气形成与多种因素相关,其中有机碳在特定条件下的沉积和矿化是关键过程。降解过程是海洋沉积有机质早期成岩作用的基础。在早期成岩过程中,结构不同脂肪酸的被降解能力依次为:不饱和脂肪酸>支链脂肪酸>饱和脂肪酸;饱和脂肪酸中,短链脂肪酸的降解速率是长链脂肪酸的6~7倍[7]。由于结合态脂类化合物的生物有效性较低,其降解程度低于游离态[8]。研究表明,不同来源有机碳生成油气的能力差别很大,其中脂类含量高的碳源生油潜能大,陆生高等植物碳源以产气为主[9]。因此,脂类化合物的结构与形态不仅反映了脂类物质的矿化和成岩速度,还预示着油气的生成能力和种类。脂类化合物在海洋沉积物中广泛分布,它们与沉积物中大分子物质、矿物质、腐殖质等物质键合,主要以有机—无机复合脂类形式存在[10],常规的索式提取法和超声萃取法只能提取出游离态脂类化合物;只有采用先碱解再酸解的处理方法,有效地提取了结合态的脂类物质,才能认识沉积物中脂类物质的全貌[11]。已有研究通过脂类化合物,认识南海沉积物有机质的来源[12]、分布和保存[13],以及重建古海洋环境信息[14]等,而对油气环境中脂类化合物的早期成岩过程研究却少有报导。
本文以南海北部油气缓释沉积环境为研究背景,以不同形态脂类化合物为指征,研究有机碳的赋存特点,阐述生源脂类有机碳的转化特征,为深入辨析南海油气形成的早期成岩过程提供理论依据。
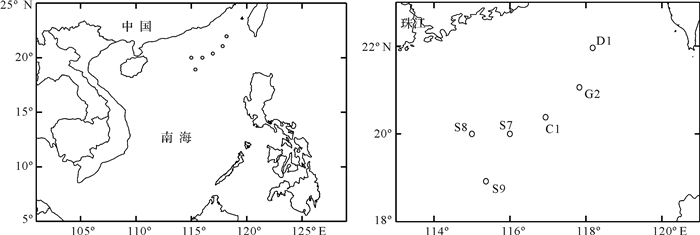
1 材料与方法 1.1 站位设置与样品采集南海表层沉积物样品采集于2016年5月“东方红2号”的“基金委南海东北部及吕宋海峡共享航次”。研究区域位于南海北部的NE—SW走向陆坡,水深610~2 603 m,是天然气水合物的多发区[6]。沿北部陆坡设置6个采样站位,记为D1、G2、C1、S7、S8和S9(图 1)。沉积物以箱式采泥器采集后,取0~3 cm表层沉积物于样品袋,冷冻避光保存,直至实验室分析。
|
| 图 1 2016年5月份南海北部采样站位分布图 Figure 1 Study area and sampling stations in the northern South China Sea, May, 2016 |
粒度分析参照GB/T12763.8—2007,取少量样品以双氧水去除有机质,加3 mL HCl (10%)进一步去除有机质和钙质。以六偏磷酸钠分散后,用激光粒度仪(Rise—2002)进行分析,测量相对偏差为0.71%。
1.2.2 有机碳及其稳定同位素分析沉积物样品以HCl (10%)去除无机碳,低温干燥后,用锡杯包裹待测。有机碳含量(Organic carbon, OC)以元素分析仪(PE2400Ⅱ型)分析测试,测试相对偏差为0.03%;碳稳定同位素(δ13C)采用元素分析仪—质谱仪联用仪(EA-IRMS)分析测试,测试相对偏差为0.3‰。
1.2.3 脂类化合物分析脂类化合物分为游离态(Free, FR)、碱性水解态(Base hydrolytic, BH)和酸性水解态(Acid hydrolytic, AH)三种形态。样品提取方法参照彭溶(2012)的脂类分析方法[15]。取5 g湿样先以有机溶剂提取FR组分;剩余残渣经KOH-甲醇溶液皂化后,用有机溶剂提取BH组分;AH组分为提取BH组分后残渣,经HCl-HF酸化,进一步提取获得。FR、BH和AH组分提取液先以正己烷提取中性脂类组分,在酸性条件下(pH < 2)提取脂肪酸类组分。中性脂类组分以BSTFA转化为三甲基硅脂(N-TMS),脂肪酸类组分以三氟化硼—甲醇溶液酯化为脂肪酸甲脂(FAME)。
中性脂类组分和脂肪酸类组分均以气相色谱质谱连用仪(安捷伦7890A/5975C, GC-MS)定量和定性。7890A/5975C使用毛细管色谱柱为DB-5 (30 m × 0.25 mm × 0.25 μm),载气为高纯氦气,检测器为FID,升温程序为:在50 ℃时保持1 min,以4 ℃/min升温至300 ℃,并在300 ℃时保持20 min。用内标法定量,脂肪酸内标为正构十九碳脂肪酸甲酯(252.02 mg/L, Sigma-Algrich),中性脂内标为5α-胆甾烷(124.90 mg/L, Sigma-Algrich),测试结果用“μg/g,干重”表示。
2 结果与讨论 2.1 粒度、有机碳含量及其碳稳定同位素丰度研究区域表层沉积物中值粒径(d50)、有机碳含量及其稳定同位素丰度结果如表 1所示。沉积物均为黏质粉砂,d50分布在2.44~9.85 μm之间。有机碳含量范围为0.22%~0.66%,有机碳与中值粒径并无明显相关性(n=6,r=0.093 81),可能与研究区域沉积物粒度差异较小,以及样品数量少有关。有机碳稳定同位素分布在-20.88‰~-22.93‰之间,表现为显著的海源特征[16]。
| 站位 | D1 | G2 | C1 | S7 | S8 | S9 |
| 水深/m | 980 | 1 039 | 610 | 1 248 | 735 | 2 603 |
| d50/μm | 6.21 | 8.01 | 6.62 | 4.89 | 9.85 | 2.44 |
| OC/% | 0.65 | 0.28 | 0.22 | 0.66 | 0.60 | 0.47 |
| δ13C/ ‰ | -22.30 | -22.93 | — | -21.34 | -20.99 | -20.88 |
研究区域表层沉积物中共检测出21种脂肪酸,碳数分布区间为12~26,包括饱和直链和支链脂肪酸、单和多不饱和脂肪酸。总脂肪酸(Total fatty acids, TFAs)范围为12.57~40.27 μg/g,呈现两侧高中间低的趋势,并且随着离岸距离的增加TFAs含量降低;这与有机碳分布规律相似,TFAs与有机碳相关分析结果表明,二者呈现显著正相关(n=6, r=0.942 8)。共检测出6种脂肪醇,总脂肪醇含量范围为5.03~8.98 μg/g,碳数小于20,以18-OH为主,占总脂肪醇的95%以上;各站位间脂肪醇含量相差较小。共检测出8种甾醇,总甾醇含量范围为0.15~3.75 μg/g,碳数分布区间为27~30;各站位间甾醇含量差别较大,较高甾醇含量约是较低甾醇含量的3~40倍,其总体分布特征与有机碳和TFAs相似。植醇含量变化也较大,范围为0.01~3.99 μg/g,分布规律与有机碳、脂肪酸和甾醇相似,其含量与总甾醇含量呈现显著正相关(n=6, r=0.985 3)。
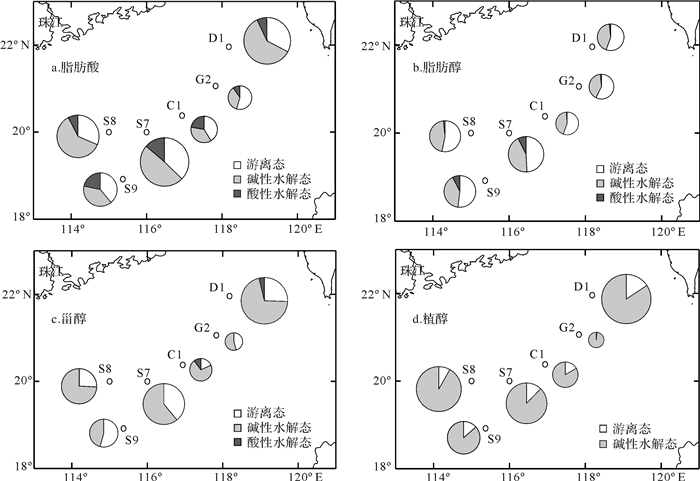
总脂肪酸中FR、BH和AH组分分别占31.48~54.64%(平均39.41%)、35.67%~60.96%(平均46.94%)和6.86%~22.28%(平均13.64%),表明脂肪酸类化合物以FR和BR为主,BH略高于FR,AH贡献较低(图 2)。总脂肪醇以FR组分为优势,约占49.16%~57.26%,BH组分仅次之,约占40.44%~45.00%,AH组分贡献较小,仅占1.13%~7.60%。甾醇主要以BH形式存在,约占45.67%~74.20%,FR次之,约占18.27%~54.33%,AH < 15%,并且在G2、S7、S8和S9中未检出。植醇以BH为绝对优势,约占83.39%~98.37%,其次为FR形式存在,约占1.63%~16.61%,未检出AH植醇。
|
| 图 2 南海北部表层沉积物不同结构类型的脂类生物标志物含量和形态组成 Figure 2 Compositions and forms of lipid biomarkers in the surface sediments of the northern South China Sea |
脂类化合物分子由于具有结构上的相对稳定性和生源特异性,是有机碳溯源、指征环境和过程的有效手段[17]。特征脂类分子的潜在来源如表 2所示,计算不同来源脂肪酸分子的相对百分比结果如图 3所示。脂肪酸分子以混合来源为主,占54.26%~61.18%;特征脂肪酸中,以海洋微藻源为优势脂肪酸,其贡献率为21.18%~33.78%,细菌源贡献率次之,为11.02%~15.64%,陆生高等植物源贡献低于5%。C27甾醇是含量最丰富的甾醇,具有多种来源,占总甾醇的32.91%~68.42%。特征甾醇中,陆源甾醇(C29甾醇)贡献率为11.07%~24.87%,藻源甾醇(C28+C30甾醇)贡献率为20.51%~42.22%。综上所述,南海北部表层沉积物有机质呈现混合源特征,其中自生源(浮游生物和海洋细菌)为主,异地源(陆源)贡献较少。

|
| 图 3 南海北部表层沉积物中不同来源脂类物质的相对含量 Figure 3 Relative contents of functional lipid groups in the surface sediments of the northern South China Sea |
研究区域沉积物中藻源有机质含量丰富,其藻源脂肪酸和甾醇平均含量约是中间海域的1.8倍和4.1倍。珠江口邻近海域和台湾海峡海域都拥有较高的现场初级生产力,叶绿素a含量均高于1 mg/m3[21-22],为该区沉积环境提供较为丰富的藻源有机碳输送。本研究结果显示(图 2),相应区域的植醇含量较高,佐证了沉积物留存丰富的藻源有机碳。海洋细菌行为与有机质的物源输入有关,研究区域靠近台湾海峡和珠江口沉积物中,细菌源脂肪酸含量相当,约是中间区域的2.7倍;其在TFAs中所占比例也相当,约为14%。研究区域细菌源脂肪酸含量约是微藻源脂肪酸的50%。黄、渤海海域、黄河口潮滩和南沙海域沉积环境脂肪酸均显示藻源为主,细菌源其次,但是藻源与细菌源相对贡献不同[12, 23-24]。研究区域藻源脂肪酸和细菌脂肪酸对TFAs的贡献率及其相对比例,与黄河口潮滩沉积环境现场脂类生产的状况更为接近。推测研究区域细菌再生产活动相对较弱,使得陆源和现场生产有机碳降解较慢,在研究区域得到较好的留存,从而为油气形成提供物质基础。
2.4 脂类分子的形态组成与早期成岩特征有机质降解是早期成岩作用的基础,脂类物质中FR组分活性较高,较容易被氧化和被微生物降解;BH和AH组分由于与沉积颗粒结合紧密,化学性质相对稳定[25]。研究区域沉积物中脂类物质的形态组成,表征其在沉积环境中的相对稳定性和留存特征,对比脂类分子间的含量和形态组成发现,具有相似结构特征的脂类分子呈现较为一致的分布规律。
2.4.1 脂肪酸分子如图 4所示,细菌源的支链脂肪酸a/i-C15:0和奇数碳脂肪酸C15:0、微藻源的单不饱和脂肪酸C18:1n9和多不饱和脂肪酸C18:2n6与含量最高的短链偶数碳C16:0具有相似的形态组成和分布,其在表层沉积物中以FR和BH为主,AH较低。单不饱和脂肪酸C18:1n9是脂肪酸中仅次于C16:0的优势种类,约占TFAs的18.64%~31.28%,多不饱和脂肪酸C18:2n6含量与a/i-C15:0和C15:0相当,是C18:1n9的8.20%~13.09%;可见研究区域存留丰富的海洋微藻源脂类物质,不饱和脂肪酸分子由于其含有双键结构,比饱和脂肪酸分子更加活跃,双键越多越容易被降解。长链脂肪酸对研究区域TFAs贡献较低,所占比例仅为0.94%~3.82%,其中C22:0占长链脂肪酸的25.53%~36.88%。其来自于陆源高等植物,在由河到海的长距离输送过程中,比海源脂肪酸分子经历了更长的降解过程,因此长链脂肪酸不仅含量低,而且形态组成中以BH占绝对优势(除C1站位);C1站位C22:0更是以AH占绝对优势,是FR和BH之和的2.0倍。

|
| 图 4 南海北部表层沉积物中不同结构脂类分子的含量和形态组成 Figure 4 Contents and form compositions of lipid molecules in the surface sediments of the northern South China Sea (FR. free form; BH. base hydrolytic form; AH. acid hydrolytic form) |
海洋中植醇主要来源于浮游植物,可以用来指征海洋初级生产力状况。研究区域靠近台湾海峡和珠江口海域的沉积物中植醇含量是中部区域的37.4倍和9.5倍。植醇仅以FR和BH形态存在,其中BH占绝对优势,约为83.39%~98.37%。浙江近海沉积物中的植醇形态组分,也是以BH为主[8]。说明FR植醇不稳定很容易被降解,转化为BH形态后相对稳定,在成岩过程中得以留存。脂肪醇18-OH、C28甾醇和C30甾醇主要来源于海洋生物,相对于C29甾醇(主要来源于陆生高等植物)具有较高的FR组分(图 4),由于海洋自生源有机质与水体中的悬浮物物及沉积物相互作用的时间相对较短,结合程度较弱,所以FR组分相对较高。根据C28甾醇和C30甾醇的硅、甲藻来源特征,研究区域C28甾醇/C30甾醇比值为2.26~14.90,表明南海东北部浮游植物群落以硅藻为优势种群,其中远离珠江口和台湾海峡的站位由于陆源输入减少,上覆水体中现场生源物质贡献增大,硅藻优势更显著;这一结果与该区域生物硅的分布趋势一致[26]。
2.5 细菌与脂类物质早期成岩的关系有机质降解是海洋沉积环境中生物地球化学过程的能量来源和动力源泉,微生物作为有机质降解主要媒介,其种类与丰度对有机质降解速率有重要影响。在油气渗漏区的沉积物中硫代谢菌含量丰富,这些微生物对海洋沉积有机质生物降解过程中起到重要作用。在厌氧的沉积环境中,硫酸盐还原菌(SRB)可以通过降解一系列不同的有机基质实现有机质的再加工[27]。研究表明,海洋沉积物中50%的有机质矿化归因于SRB[28]。除了SRB的独立作用,其与某种古菌综合体也可以完成一半以上的有机质的硫酸盐氧化降解[29]。脂肪酸是细胞重要的能量物质和结构成分,与细菌新陈代谢有着极为密切的关系[30]。支链脂肪酸i/a-C15:0和i/a-C17:0在需氧和厌氧细菌活动中都能检出,海洋沉积物中i/a-C15:0和i/a-C17:0脂肪酸分子主要来源于SRB[27]。研究区域各站位间沉积物支链脂肪酸i/a-C15:0和i/a-C17:0含量(TSRB)差异较大,最低的中部海域沉积物TSRB仅为0.16 μg/g,最高的位于靠近珠江口海域,TSRB高达1.79~2.62 μg/g,占TFAs的5.14~6.50%,表明着该区域有机质受硫酸盐还原菌的分解活动较强。同期通过基因测序得到,靠近珠江口海域站位的古菌群落中,直接与硫酸盐还原过程相关的基因丰度为5.71%[31]。这一结果与细菌特征脂肪酸分子组成相一致。
3 结论南海蕴藏着丰富的油气资源,油气的形成与沉积环境有机碳的留存和来源状况密切相关。本文研究南海北部珠江口盆地及其邻近海域沉积环境脂类化合物的组成特征,得到以下结论:
(1) 南海北部表层沉积有机碳含量为0.22%~0.66%,靠近珠江口和台湾海峡海域有机碳含量较高;有机碳稳定同位素分布在-20.88‰~-22.93‰之间,表现为显著的海源特征。
(2) 沉积物中共检测出21种脂肪酸、6种脂肪醇、8种甾醇和1种植醇;脂肪酸、甾醇和植醇的分布规律与有机碳相似,脂肪醇含量分布则较为均匀。
(3) 脂类化合物组分以FR和BR形态为主,AH贡献较低;其中脂肪酸BH组份略高于FR,脂肪醇FR组分略高于BH,植醇和甾醇则呈现明显的BH优势,并且植醇未检出AH组分。
(4) 脂肪酸与甾醇潜在来源分析表明,研究区域脂类有机物以海洋微藻和细菌相对贡献为主,海洋微藻脂肪酸贡献率为21.18%~33.78%,约是细菌贡献率的2倍,陆源贡献较少,低于5%。
(5) 潜在硫酸盐还原菌来源的支链脂肪酸分布与沉积物中古菌分布基本一致。
| [1] |
苏广庆, 罗又郎, 邱传珠, 等. 南海东北部沉积环境和沉积演化模式的初步研究[J]. 海洋学报, 1987, 9(3): 335-343. [ Su Guangqing, Luo Youlang, Qiu Chuanzhu, et al. Preliminary exploration of sedimentary environment and evolution model in the northeastern South China Sea[J]. Acta Oceanologica Sinica, 1987, 9(3): 335-343.] |
| [2] |
陈芳, 庄畅, 周洋, 等. 南海东北部陆坡天然气水合物钻探区生物地层与沉积速率[J]. 地球科学, 2016, 41(3): 416-424. [ Chen Fang, Zhuang Chang, Zhou Yang, et al. Calcareous nannofossils and foraminifera biostratigraphy on the northeastern slope of the South China Sea and variation in sedimentation rates[J]. Earth Science, 2016, 41(3): 416-424.] |
| [3] |
于晓果, 金肖兵, 姚旭莹, 等. 甲烷流体活动与沉积物中碳、氮同位素组成响应:南海东北部海洋Ⅳ号地区研究[J]. 海洋学研究, 2013, 31(3): 1-7. [ Yu Xiaoguo, Jin Xiaobing, Yao Xuying, et al. The stable isotopic composition of sediments in methane fluid flowing area, Haiyang IV, the northern part of South China Sea[J]. Journal of Marine Sciences, 2013, 31(3): 1-7. DOI:10.3969/j.issn.1001-909X.2013.03.001] |
| [4] |
茅晟懿, 朱小畏, 孙永革, 等. 南海北部神狐海域现代沉积物正构脂肪酸来源:加权平均碳同位素的建立与应用[J]. 海洋地质前沿, 2014, 30(8): 1-15. [ Mao Shengyi, Zhu Xiaowei, Sun Yongge, et al. Source of saturated fatty acids in modern sediments in Shenhu area, northern South China Sea and implications:application of n-weighted average carbon isotope[J]. Marine Geology Frontiers, 2014, 30(8): 1-15.] |
| [5] |
Thena T, Mohan K. Estimation of pore space methane hydrate in marine sediments of Cascadia margin[J]. Journal of Natural Gas Science and Engineering, 2016, 35: 956-963. DOI:10.1016/j.jngse.2016.09.046 |
| [6] |
吴能友, 邬黛黛, 叶瑛, 等. 南海东北部东沙海域沉积物烃类有机地球化学研究及其意义[J]. 南海地质研究, 2007(1): 1-14. [ Wu Nengyou, Wu Daidai, Ye Ying, et al. Hydrocarbon geochemical study of sediments from Dongsha area, Northeast South China Sea and their significances[J]. Gresearch of Eological South China Sea, 2007(1): 1-14.] |
| [7] |
Haddad R I, Martens C S, Farrington J W. Quantifying early diagenesis of fatty acids in a rapidly accumulating coastal marine sediment[J]. Organic Geochemistry, 1992, 19(1/2/3): 205-216. |
| [8] |
王江涛, 杨庶, 谭丽菊, 等. 浙江南部近海沉积物柱状样中脂类生物标志物的组成及形态分布[J]. 海洋学报, 2011, 33(5): 83-90. [ Wang Jiangtao, Yang Shu, Tan Liju, et al. Composition and form distribution of lipids biomarkers in a sediment core from southern coastal area of Zhejiang province[J]. Acta Oceanologica Sinica, 2011, 33(5): 83-90.] |
| [9] |
Tissot B P, Pelet R, Ungerer P. Thermal history of sedimentary basins, maturation indices, and kinetics of oil and gas generation[J]. American Association of Petroleum Geologists Bulletin, 1987, 71(12): 1445-1466. |
| [10] |
Brinis A, Mejanelle L, Momzikoff A, et al. Phospholipid ester-linked fatty acids composition of size-fractionated particles at the top ocean surface[J]. Organic Geochemistry, 2004, 35(11/12): 1275-1287. |
| [11] |
Stefanova M, Disnar J R. Composition and early diagenesis of fatty acids in lacustrine sediments, lake Aydat (France)[J]. Organic Geochemistry, 2000, 31(1): 41-55. DOI:10.1016/S0146-6380(99)00134-5 |
| [12] |
段毅, 崔明中, 罗斌杰, 等. 我国海洋沉降颗粒物质的有机地球化学研究:Ⅰ.有机质通量及烃类化合物和脂肪酸分布特征[J]. 中国科学(D辑):地球科学, 1997, 27(5): 442-446. [ Duan Yi, Cui Mingzhong, Luo Binjie, et al. Organic geochemical studies of sinking particulate material in China sea area(Ⅰ):organic matter fluxes and distributional features of hydrocarbon compounds and fatty acids[J]. Science China (Seri.D):Earth Sciences, 1997, 27(5): 442-446.] |
| [13] |
曹梦莉, 马倩倩, 吴莹, 等. 南海北部和海南岛附近海域表层沉积物中有机质的分布和降解状态的差异[J]. 海洋与湖沼, 2017, 48(2): 258-265. [ Cao Mengli, Ma Qianqian, Wu Ying, et al. Difference in organic matter distribution and degradation in surface sediment between northern South China Sea and Hainan Island[J]. Oceanologia et Limnologia Sinica, 2017, 48(2): 258-265.] |
| [14] |
赵美训, 赵晓晨, 陈建芳, 等. 南海表层沉积物生物标志物的分布特征及古生产力重建意义[J]. 热带海洋学报, 2009, 28(3): 45-53. [ Zhao Meixun, Zhao Xiaochen, Chen Jianfang, et al. Distribution of phytoplankton biomarkers in surface sediments from the South China Sea and its implication for paleoproductivity reconstruction[J]. Journal of Tropical Oceanography, 2009, 28(3): 45-53. DOI:10.3969/j.issn.1009-5470.2009.03.008] |
| [15] |
彭溶.应用脂类化合物研究北黄海沉积物有机碳的埋藏特征[D].青岛: 中国海洋大学, 2012. [Peng Rong. Sedimentary of organic carbon in the sediments of North Yellow Sea: Indicated by lipid compounds[D]. Qingdao: Ocean University of China, 2012.] http://cdmd.cnki.com.cn/Article/CDMD-10423-1012504212.htm
|
| [16] |
Jia G D, Peng P A. Temporal and spatial variations in signatures of sedimented organic matter in Lingding Bay (Pearl estuary), southern China[J]. Marine Chemistry, 2003, 82(1/2): 47-54. |
| [17] |
Volkman J K. A review of sterol markers for marine and terrigenous organic matter[J]. Organic Geochemistry, 1986, 9(2): 83-99. DOI:10.1016/0146-6380(86)90089-6 |
| [18] |
Volkman J K, Jeffrey S W, Nichols P D, et al. Fatty acid and lipid composition of 10 species of microalgae used in mariculture[J]. Journal of Experimental Marine Biology and Ecology, 1989, 128(3): 219-240. DOI:10.1016/0022-0981(89)90029-4 |
| [19] |
Volkman J K. Sterols and other triterpenoids:source specificity and evolution of biosynthetic pathways[J]. Organic Geochemistry, 2005, 36(2): 139-159. DOI:10.1016/j.orggeochem.2004.06.013 |
| [20] |
Peng X Z, Zhang G, Mai B X, et al. Tracing anthropogenic contamination in the Pearl River estuarine and marine environment of South China Sea using sterols and other organic molecular markers[J]. Marine Pollution Bulletin, 2005, 50(8): 856-865. DOI:10.1016/j.marpolbul.2005.02.031 |
| [21] |
黄良民, 陈清朝, 尹健强, 等. 珠江口及邻近海域环境动态与基础生物结构初探[J]. 海洋环境科学, 1997, 16(3): 1-7. [ Huang Liangmin, Chen Qingchao, Yin Jianqiang, et al. Basic organism composition and environment status of the Zhujiang estuary and adjacent waters[J]. Marine Environmental Science, 1997, 16(3): 1-7.] |
| [22] |
康建华, 陈兴群, 黄邦钦. 台湾海峡及其邻近海域表层水叶绿素a含量时空变化特征[J]. 台湾海峡, 2010, 29(1): 34-41. [ Kang Jianhua, Chen Xingqun, Huang Bangqin. Study on the spatial and temporal variation of surface chlorophyll a in Taiwan Strait and its adjacent waters[J]. Journal of Oceanography in Taiwan Strait, 2010, 29(1): 34-41.] |
| [23] |
高寒凌.黄渤海沉积物有机碳的运输和矿化特征研究[D].青岛: 中国海洋大学, 2016. [Gao Hanling. Study on the transport and mineralization of organic carbon in the Yellow Sea and Bohai Sea[D]. Qingdao: Ocean University of China, 2016.]
|
| [24] |
于文涛.黄河三角洲潮间带有机碳的地球化学研究[D].青岛: 中国海洋大学, 2014. [Yu Wentao. The geochemical research of organic carbon in the intertidal zone of the Yellow River Delta[D]. Qingdao: Ocean University of China, 2014.] http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=D547550
|
| [25] |
Ding H B, Sun M Y. Biochemical degradation of algal fatty acids in oxic and anoxic sediment-seawater interface systems:effects of structural association and relative roles of aerobic and anaerobic bacteria[J]. Marine Chemistry, 2005, 93(1): 1-19. |
| [26] |
周鹏, 李冬梅, 刘广山, 等. 南海东北部和南部海域表层沉积物生物硅研究[J]. 热带海洋学报, 2010, 29(4): 40-47. [ Zhou Peng, Li Dongmei, Liu Guangshan, et al. Biogenic silica in surface sediments of the northeastern and southern South China Sea[J]. Journal of Tropical Oceanography, 2010, 29(4): 40-47. DOI:10.3969/j.issn.1009-5470.2010.04.007] |
| [27] |
Londry K L, Jahnke L L, Marais D J D. Stable Carbon isotope ratios of lipid biomarkers of sulfate-reducing bacteria[J]. Applied and Environmental Microbiology, 2004, 70(2): 745-751. DOI:10.1128/AEM.70.2.745-751.2004 |
| [28] |
Taylor J, Parkes R J. Identifying different populations of sulphate-reducing bacteria within marine sediment systems, using fatty acid biomarkers[J]. Journal of General Microbiology, 1985, 131(3): 631-642. |
| [29] |
Boetius A, Ravenschlag K, Schubert C J, et al. A marine microbial consortium apparently mediating anaerobic oxidation of methane[J]. Nature, 2000, 407(6804): 623-626. DOI:10.1038/35036572 |
| [30] |
张国赏, 吴文鹃, 潘仁瑞. 气相色谱-质谱法检测细胞脂肪酸及其在细菌鉴定上的应用[J]. 合肥联合大学学报, 2000, 10(4): 92-96. [ Zhang Guoshang, Wu Wenjuan, Pan Renrui. Determination of fatty acids in cells by GC-MS and its application in bacterium identification[J]. Journal of Hefei Union University, 2000, 10(4): 92-96.] |
| [31] |
陈烨, 张玉, 甄毓, 等. 南海东北部珠江口盆地沉积物中古菌群落垂向分布研究[J]. 海洋环境科学, 2017, 36(5): 735-740. [ Chen Ye, Zhang Yu, Zhen Yu, et al. Vertical profile of archaeal community in the sediments of Pearl River Mouth Basin in the northeastern South China Sea[J]. Marine Environmental Science, 2017, 36(5): 735-740.] |
 2019, Vol. 37
2019, Vol. 37


