扩展功能
文章信息
- 肖良, 漆亚玲, 马文忠, 李相传, 郭俊锋, 孙楠, 姚肖永
- XIAO Liang, QI YaLing, MA WenZhong, LI XiangChuan, GUO JunFeng, SUN Nan, YAO XiaoYong
- 吐哈盆地北缘中侏罗世植物化石稳定碳同位素的古环境意义
- Stable Carbon Isotope of Middle Jurassic Plant Fossils in the North Edge of Turpan-Hami Basin, Xinjiang and Their Palaeoenvironmental Implications
- 沉积学报, 2017, 35(3): 489-498
- ACTA SEDIMENTOLOGICA SINCA, 2017, 35(3): 489-498
- 10.14027/j.cnki.cjxb.2017.03.007
-
文章历史
- 收稿日期:2016-11-15
- 收修改稿日期: 2016-12-30
2. 中国石油长庆油田分公司勘探开发研究院, 西安 710018;
3. 中国科学院南京地质古生物研究所现代古生物学和地层学国家重点实验室, 南京 210008
2. Research Institute of Petroleum Exploration and Development, PetroChina Changqing Oilfield Company, Xi'an 710018, China;
3. State Key Laboratory of Palaeobiology and Stratigraphy, Nanjing Institute of Geology and Palaeontology, Chinese Academy of Sciences, Nanjing 210008, China
古气候和古环境的研究已成为地球演化研究的一项重要内容,一直受到学术界和社会的普遍关注[1],多种地质记录都已被科学家尝试用来了解古环境变化。目前,利用树木年轮[2]、冰芯[3]、湖泊沉积物[4]和海洋沉积物[5]、生物化石[6]、古植被[7-8]和古土壤[9]等参数重建地质历史时期的古环境变化已取得了明显进展。其中碳、氢、氧等稳定同位素在该领域研究中的应用日益广泛[10],尤其是碳同位素,包括土壤有机质、土壤碳酸盐、植物硅酸体和动物牙齿化石的珐琅质等已在古生态与古气候研究中取得了重要进展[11]。在陆相生境中,植物叶片化石一直被作为重建古气候的一个重要材料,不过以前的研究主要利用植物群组合、叶相特征、气孔参数恢复古环境变化[12-13]。近年来,随着生物地球化学的发展,现代植物叶片的稳定碳同位素对环境变化响应的研究已引起越来越多的重视,但是植物化石稳定碳同位素的研究却很少[1]。由于植物化石中包含的碳直接从大气中合成而来,因此其碳源可以作为一个有效的材料重建古大气的变化[14]。目前,部分研究已经证明植物化石叶片稳定碳同位素可以揭示植物对古环境响应的生理信息变化[15-17]。
侏罗纪是中国西北最重要的聚煤期,很多大型煤田含矿地层都集中在这个时期,如此丰富的煤炭资源必然代表了当时具有繁盛的植被面貌。通过古土壤中碳酸盐的碳同位素值以及碳平衡模型已经知道侏罗纪的CO2浓度可以达到1 000 mL/m3以上,比现在的CO2浓度(约400 mL/m3)高出很多。与现代气候相比,侏罗纪处于明显的温室环境中。而在如此高的CO2浓度下植物如何生长,它们的生理特征是否与现代植物相似?这些问题的了解对于我们预测未来的植被,甚至整个生物圈,在即将到来的温室环境下如何生长发育具有很好的启迪作用。而植物叶片的稳定碳同位素研究为了解侏罗纪时期的植物生理过程提供了可行的方法。但是,至今西北侏罗纪植物化石叶片稳定碳同位素的研究鲜见报道,仅有甘肃窑街盆地的植物化石进行过详细的稳定碳同位素研究[18-19]。新疆吐哈盆地北缘的三道岭煤矿为一大型煤田,其中植物化石丰富,以银杏类和真蕨类植物为主[20],大部分都为压型化石,为分析化石叶片的稳定碳同位素提供了丰富而可靠的材料。前人对三道岭煤田植物化石的研究主要侧重于属种的鉴定及植物群特征研究,古气候古环境的定量研究很少见。肖良等[21]通过该地区银杏类和茨康类叶片化石的气孔参数已重建出中侏罗世吐哈盆地的CO2浓度为1 770 mL/m3,与其他资料中显示的CO2值相当,显示出当时该地区处于强烈的温室效应中。本次研究选择三道岭植物群中的优势属种分析它们的稳定碳同位素值,包括似银杏属(Ginkgoites)、拟刺葵属(Phoenicopsis)、枝脉蕨属(Cladophlebis)以及一种推测为银杏类的繁殖器官——斯堪尼狭轴穗(Stenorachis),比较中侏罗世不同植物间的稳定碳同位素差异,探讨不同植物的生理差异,了解在中侏罗世温室效应下植物的生理过程,进而讨论化石植物稳定碳同位素对古环境的指示。
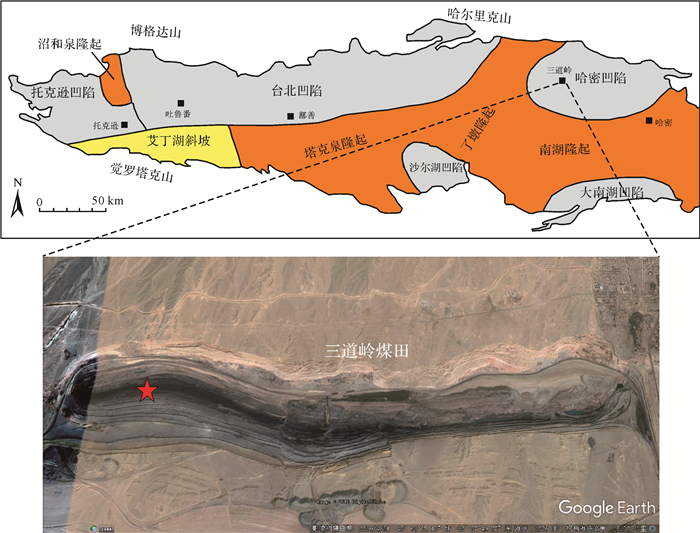
1 区域地质背景吐哈盆地位于新疆北部东天山地区,是新疆地区三大沉积盆地之一,北以博格达山脉为界,南为觉罗塔格山所限,东西两端分别被哈尔里克山和卡拉乌成山所围[22],盆地中发育石炭系—第四系,是一从古生代末开始发育的中、新生代大型内陆山间盆地[23]。在早中侏罗世,吐哈盆地处于伸展盆地发育阶段[24],主要发育冲击扇、三角洲、湖泊等沉积体系[25-26]。按侏罗纪的沉积环境及构造特征,吐哈盆地主要构造单元可以划分为托克逊凹陷、艾丁湖斜坡、台北凹陷、哈密凹陷、沙尔湖凹陷、大南湖凹陷及塔克泉隆起、了墩隆起和南湖隆起等(图 1)[27]。位于盆地东北缘的三道岭煤田在构造单元上归属于哈密凹陷,该地区的主要含煤地层为西山窑组(J2x)。
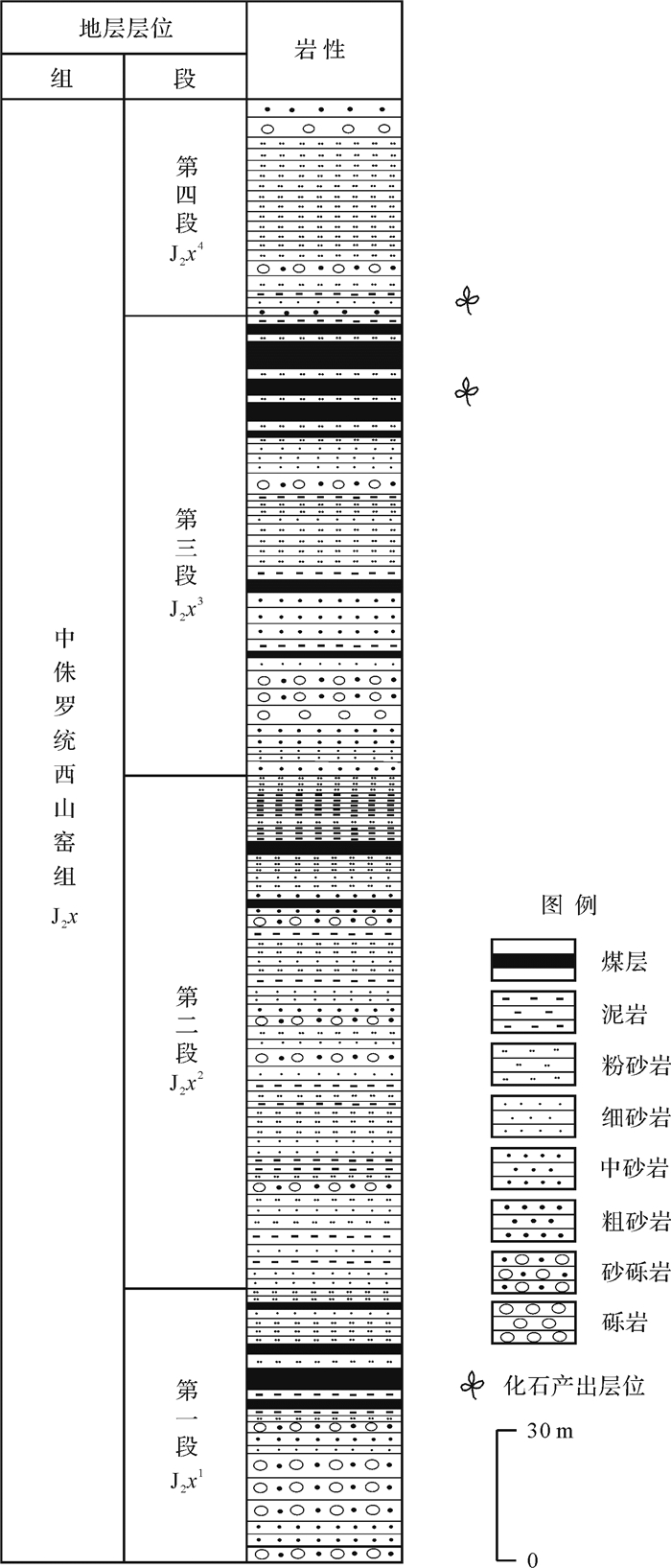
西山窑组是指整合于三工河组之上、头屯河组之下的一套湖沼相含煤碎屑岩沉积,其岩性为灰、灰绿色、灰黄色砂岩、石英砂岩、灰黑色泥岩、炭质泥岩夹煤层及薄菱铁矿层等,并以含煤岩系而区别于其上、下地层,时代为中侏罗世[28-29]。吴伯林等[30]进一步据地层结构及岩性岩相等特征进一步将西山窑组分为四个岩性段(图 2),分别是:第一岩性段(J2x1),由砾岩—砂岩—泥岩及煤层组成良好的韵律层及较典型的二元结构,为辫状河相含煤碎屑岩建造,顶部为厚煤层;第二岩性段(J2x2),主要由泥岩和砂岩组成韵律层,为河流三角洲相沉积,顶部具有多层薄煤层及煤线;第三岩性段(J2x3)为河流—沼泽相含煤碎屑岩建造,下部为辫状河相含砾粗砂岩,砂质砾岩,上部为两层煤夹一层砂岩;第四岩性段(J2x4)以厚层泥岩为主夹砂岩,不含煤层,以河流三角洲相沉积为主。
植物化石采自东距哈密约90 km的三道岭露天煤矿(图 1)。商平等[20]从三道岭煤矿的植物化石中鉴定出43属86种,认为该植物组合属于中国北方温带植物地理区Coniopteris-Phoenicopsis植物群的典型组合,通过与其他植物群的对比,推断三道岭煤矿该地层时代应为中侏罗世早期的阿连期到巴柔期(Aalenian-Bajocian)。本次研究采集的植物化石经过初步鉴定主要为真蕨类和银杏类,植物群归属于Coniopteris-Phoenicopsis组合[21]。吴伯林等[30]通过吐哈盆地的古植物化石数据,认为J2x1~J2x2的标志性化石为Sphenozamites,J2x3的古植物组合主要为苏铁类和松柏类,J2x4时期的植物化石组合主要为真蕨类和银杏类。结合西山窑组的古植物和岩石组合特征,推断本次研究所采的植物化石可能来自西山窑组第三岩性段的上部以及第四岩性段(J2x3和J2x4)(图 2)。此次,我们挑选三道岭植物群中优势属种的叶片和繁殖器官进行稳定碳同位素分析,包括似银杏(Ginkgoites)、拟刺葵(Phoenicopsis)、枝脉蕨(Cladophlebis)以及斯堪尼狭轴穗(繁殖器官,Stenorachis)(图 3)。

|
| 图 3 西山窑组4类植物化石(图中的比例棒均为1 cm) a.Ginkgoites; b.Phoenicopsis; c.Cladophlebis; d.Stenorachis Figure 3 Four plant fossils in the Xishanyao Formation |
选取11个植物化石标本和1个现生植物标本进行稳定碳同位素分析。在分析之前,需要对样品进行预处理。对于现生样品,需要进行以下步骤:1) 在蒸馏水中浸泡叶片30 min,以去除尘土;2) 将叶片放置在烘箱中50℃恒温烘干12小时;3) 将现生叶片用剪刀剪碎,混合其茎和叶,放入研钵中研磨,使样品均一化;4) 放置在烘箱中50℃恒温烘干12小时后取出。而对于化石样品,则需要进行不同的步骤:1) 用解剖刀从岩石上剥离出角质层,放入蒸馏水中浸泡约1小时,以去除附着的沉积物;2) 将样品转移入10%的盐酸中,浸泡约12小时,以充分去除碳酸盐岩;3) 稀释至中性后,将样品转移入50%的氢氟酸中,浸泡约12小时,以充分去除硅质沉积物;4) 稀释至中性后,放置在烘箱中50℃恒温烘干12小时。
经过预处理的角质层送至中国科学院地球环境研究所开展稳定碳同位素实验。取10mg样品转入石英管内,加入氧化铜(1~2 cm),红色的铜(1 cm左右)和箔金丝1根,抽好真空后熔封,放入真空的高温反应炉内,在850℃条件下恒温灼烧;在真空系统中用酒精—液氮冷阱分离纯化CO2气体,最后在MAT251型同位素质谱仪上测定CO2的δ13C值,标样采用国家标准物质GBW04407,分析误差 < ±0.1‰,结果以VPDB标准表示,δ13C=(Rsample/Rstandard-1)×1000‰(R代表13C/12C比率)。
3 结果与讨论 3.1 三道岭化石植物的δ13C值从三道岭植物群中选择三种优势物种作为分析稳定碳同位素的化石材料,分别为银杏类、茨康类和蕨类植物,包括9块叶片化石和2块繁殖器官化石。叶片经过鉴定分别为银杏类中的似银杏、茨康类中的拟刺葵以及蕨类中的枝脉蕨,而繁殖器官化石经过与其他同时期的标本进行比较确定为斯堪尼狭轴穗(Stenorachis)[31],采取孙革等[32]提出的观点,认为Stenorachis可能与银杏类的雄性生殖器官有密切关系,应归于银杏类。为了对比,2013年从西安的长安大学校园里采集现生银杏(Ginkgo biloba)叶片分析其稳定碳同位素值。此次共分析了12个样品的稳定碳同位素,其值见表 1。
| 样品编号 | 属种名称 | δ13C(‰, VPDB) | 平均值 | ||
| 化石植物 | SDL-3 | Ginkgoites | -23.26 | -23.55 | |
| SDL-4 | -23.83 | ||||
| SDL-25 | Phoenicopsis | -21.66 | -22.18 | ||
| SDL-23 | -22.7 | ||||
| SDL-9 | Cladophlebis | -23.01 | -23.37 | ||
| SDL-12 | -23.76 | -23.15 | |||
| SDL-41 | -23.26 | ||||
| SDL-43 | -23.2 | ||||
| SDL-42 | -23.63 | ||||
| SDL-24 | Stenorachis | -20.88 | -20.91 | ||
| SDL-34 | -20.94 | ||||
| 现生植物 | YX2014-1 | Ginkgo biloba | -26.96 | -26.96 | |
植物的稳定碳同位素主要由其采用的光合途径决定,现代植物包含3种类型:C3、C4和CAM。不同光合途径因光合羧化酶(RuBP羧化酶和PEP羧化酶)和羧化时空上的差异对13C具有不同的识别和排斥能力,导致了C3、C4和CAM具有显著不同的δ13C值。C3植物的δ13C值为-20‰~-35‰(平均值为-26‰),主要包括乔木、灌木、寒冷地区的草本;C4植物为-7‰~-15‰(平均为-12‰),主要包括热带草本;而CAM植物为-10‰~-22‰(平均为-16‰),主要为沙漠中肉质植物和热带附生植物[33]。当前研究的植物化石叶片的δ13C值分布在-21.66‰~-23.83‰(平均值为-23.15‰),属于典型的C3植物。
分析了银杏类植物的繁殖器官—斯堪尼狭轴穗的稳定碳同位素值,为-20.91‰,比所有分析的化石叶片的δ13C值高。前人研究已经证实不同器官间碳同位素值不同,果实和种子往往比叶片更能富集13C[34],这主要是因为繁殖器官在形成过程中会产生碳同位素的分馏效应,从而导致其δ13C值偏高。本次研究中斯堪尼狭轴穗的δ13C值比似银杏的高2.64‰,与Xiao et al.[16]分析的枫香叶片及其繁殖器官间的稳定碳同位素差异相似,说明银杏类植物的繁殖器官具有相似的同位素分馏效应。为了进一步检验碳同位素结果的可靠性,同一个化石属种均分析了两个及以上的样品(表 1),发现同一种甚至同一属内的δ13C差异均小于1‰,进一步说明这些碳同位素值是可信的。然而,在比较不同属种间稳定碳同位素的差异发现,拟刺葵的δ13C值最高(-22.18‰),枝脉蕨和似银杏的δ13C值相似,分别为-23.37‰和-23.55‰,指示似银杏和拟刺葵间δ13C差异较大。而二者均来自同一地点、同一套地层,因此环境因素和成岩作用对其稳定碳同位素的影响应该是一致的。二者δ13C的差异可能是由于植物本身的生理和遗传因素决定的,因为不同植物属种间的稳定碳同位素值往往具有差异,即Species-specific或者Genus-specific。以前根据叶片外形和角质层微细特征,将茨康类植物当作已灭绝的银杏类成员,但是随着茨康类植物繁殖器官的进一步研究,对其归属提出了疑问,认为和银杏类的关系实际上比较疏远[35],其瓣状蒴果显示出演化上的重大进步①。本文中似银杏和拟刺葵间稳定碳同位素间的差异也支持了银杏类和茨康类植物亲缘关系疏远的观点,与肖良等[21]根据似银杏和拟刺葵的气孔指数推测的结果一致。
① 苗雨雁. 新疆准噶尔盆地西部中侏罗世银杏类和茨康类植物[D].长春:吉林大学博士学位论文,2006.
侏罗纪作为一个重要的成煤期,在我国西北已发现很多侏罗系的煤层,而侏罗系中则以中侏罗统发育最为普遍[31],同样的情况也出现在欧洲[36]。在这些中侏罗统的地层中均埋藏有丰富的植物化石,而且部分已进行过稳定碳同位素研究[18-19, 36-37]。甘肃窑街中侏罗统窑街组中的银杏属植物(Ginkgo)的平均δ13C值为-26.6‰[18],似管状叶属植物(Solenites murrayana)的平均δ13C值为-26.82‰[19];甘肃华亭中侏罗统延安组中拟刺葵的δ13C值为-24.6‰[37]。而欧洲中侏罗世的部分地层中银杏类和茨康类植物的稳定碳同位素值也已分析,英国Yorkshire的Ginkgo huttonii和Solenites vimineus的δ13C值分别为-24.1‰和-23.7‰,瑞典Scania的Ginkgoites regnellii的δ13C值为-23.8‰[36]。Ginkgoites和Phoenicopsis的δ13C值分别为-23.55‰和-22.18‰。对于银杏类植物,西山窑组Ginkgoites的δ13C值比甘肃窑街组Ginkgo的高出约3‰,与欧洲中侏罗世的Ginkgo和Ginkgoites的值相当;而对于茨康类植物,西山窑组Phoenicopsis的δ13C值比甘肃华亭延安组Phoenicopsis的高2.42‰,比甘肃窑街组和欧洲中侏罗世的Solenites的δ13C值分别高出4.64‰和1.52‰。综合以上的对比发现,本文获得的银杏类和茨康类植物化石的稳定碳同位素值与欧洲同时期同类植物化石的值更加接近,窑街组比其他地方中侏罗世植物化石的稳定碳同位素值均偏负许多,这可能是由于进行碳同位素分析的窑街组植物化石产出层位中含有大量油页岩的原因[19],而其余地方的岩性均没有油页岩。
3.2 中侏罗世大气CO2稳定碳同位素组分(δ13Ca)植物的稳定碳同位素除了主要受遗传因素的控制,同时还要受到诸多外界环境因素的影响[38-39]。Farquhar et al. [40]建立了植物稳定碳同位素(δ13Cp)和大气CO2碳同位素(δ13Ca)以及一些植物生理参数间的关系公式:
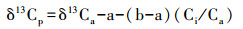 (1)
(1)
式中,a代表CO2扩散到气孔时产生的分馏效应,约为4.4‰,b为光合羧化酶RUBP对碳同位素的分馏效应,约为27‰;Ci表示细胞间CO2分压,Ca表示大气中CO2分压。
从公式1可以看出,植物稳定碳同位素值的一个重要影响因素是δ13Ca。虽然,现代植物稳定碳同位素的研究已讨论了多种环境因素对其产生的影响[33],但是由于当今大气CO2的δ13Ca保持近似恒定[38],因此这些研究往往没有讨论δ13Ca对植物稳定碳同位素的影响。而在地质历史时期,δ13Ca一直发生着变化[41],因此在研究化石植物稳定碳同位素时,需要了解当时大气CO2的稳定碳同位素变化,也是古环境重建的一个重要参数[42]。Arens et al.[43]和Gröcke[44]分析了大量现生植物和大气CO2的稳定碳同位素值以及对应的大气CO2浓度,发现植物体δ13Cp变化主要是由大气CO2的稳定碳同位素改变引起,约占90%,而大气CO2水平仅占次要地位,同时也据此建立了δ13Cp和δ13Ca之间的回归方程,见公式2:
 (2)
(2)
将获得的现生和化石叶片的稳定碳同位素值代入公式2,计算出现在和中侏罗世大气CO2的δ13Ca(表 2)。现生银杏叶片的稳定碳同位素值为-26.96‰,据公式2获得的δ13Ca值为-7.54‰,与直接测量出的2013年大气CO2的值相似(-8.3‰)(表 2),这说明银杏叶片可以作为重建大气δ13Ca的可靠材料。Beerling et al.[45]曾根据海洋碳酸钙质化石恢复出中侏罗世早期大气CO2的δ13Ca为-5.6‰。而此次根据三道岭化石中3类植物叶片和1种繁殖器官稳定碳同位素获得的δ13Ca中,由似银杏和枝脉蕨叶片化石得到的δ13Ca值相似,分别为-4.43‰和-4.27‰,这两个值与利用海洋碳酸钙获得的δ13Ca相近。这不但说明本文所测的银杏类叶片化石的稳定碳同位素结果可靠,受成岩作用的影响较小,而且表明公式2也适用于银杏类化石叶片重建δ13Ca。由此可以判断,银杏类叶片是重建地质历史时期大气CO2稳定碳同位素值的一个可靠化石,为今后研究中生代—新生代δ13Ca变化提供了一个有效的方法。此外,根据枝脉蕨化石叶片也获得了可靠的中侏罗世δ13Ca,但是没有分析其他地质时期枝脉蕨叶片化石与δ13Ca的关系,因此需要进一步研究以待确认。
| 属种名称 | δ13Cp | δ13Ca(据植物)a | δ13Ca(据海洋碳酸钙或直接测量)b | Δ13C(‰)c | Ci/Ca |
| Ginkgoites | -23.55 | -4.43 | -5.6 | 17.95 | 0.60 |
| Phoenicopsis | -22.18 | -3.19 | 16.58 | 0.54 | |
| Cladophlebis | -23.37 | -4.27 | 17.77 | 0.59 | |
| Stenorachis | -20.91 | -4.07 | -5.6 | ||
| Ginkgo biloba | -26.96 | -7.54 | -8.3 | 18.66 | 0.63 |
| 注:a表示将植物叶片的δ13C代入公式2计算获得δ13Ca;b表示中侏罗世的δ13Ca根据海洋碳酸钙质化石获得,而2013年的δ13Ca来自于NOAA(美国国家海洋大气管理局)的测量数据(见http://www.esrl.noaa.gov/gmd/ccgg/globalview/co2/co2_intro.html);c表示获取Δ13C的δ13Ca来自于b的数据。 | |||||
稳定同位素技术常用的两个分析指标是同位素比值(isotope ratio, δ)和同位素判别值(isotope discrimination, Δ),前文已经详细讨论过三道岭植物化石的碳同位素比值,但是没有涉及同位素判别值。Δ也称为植物的13C分辨能力,结果越大表示分辨能力越强,相应植物样品的13C丰度越低,δ13C的值越小。Farquhar et al. [40, 46]根据C3植物的生理过程已经建立了Δ的关系公式:
 (3)
(3)
将公式1和公式3结合处理得到公式4:
 (4)
(4)
公式3和公式4中各符号指示的意义见公式1中的说明。
从公式3可知,Δ值已经将δ13Ca考虑进去。由于不同地质历史时期的δ13Ca不同,因而,在比较不同地质历史时期植物的δ13C值时,最好将稳定碳同位素值都转换成稳定碳同位素辨别值,这样可以排除δ13Ca的干扰。同样,根据公式4可以获得Ci/Ca比值,也能够排除δ13Ca的影响。Ci/Ca比值是一重要的植物生理生态特征值,主要由气孔导度和光合速率决定[33]。这两个生理参数除了在不同物种间存在差异,还受环境因素的影响,比如光照、水分、营养、大气CO2浓度和温度等[47],因而可以利用Ci/Ca的变化了解地质历史时期环境的演变。所有化石叶片的稳定碳同位素值都转换为Δ值,进而计算成Ci/Ca比值(表 2)。Ehleringer et al.[48]曾分析不同植物的Ci/Ca变化,发现Ci/Ca比率在不同植物间是不同的,这是因为气孔导度的变化或者叶绿体对CO2需求的变化,又或者两者都有,总之代表了一个整体多因素的影响结果。对于三道岭化石叶片的Ci/Ca值,似银杏的Ci/Ca值与狭叶拟刺葵的差距较大,进一步从植物生理生态特征方面支持了似银杏与拟刺葵亲缘关系较远的结论。Chakraborty et al.[49]研究印度白垩纪植物化石Ci/Ca的变化发现,在合适的条件下,植物往往会保持一个恒定或近似恒定的Ci/Ca比率,从而使它们的同化作用速率达到最优。当Ci/Ca比值较高时(>0.7),反映了植物采用的是非节约型水分利用方式。在一些热带雨林物种中,其Ci/Ca比值均较高,缺乏水分节约策略[50]。本次分析的现生银杏和3类化石叶片的Ci/Ca比值均低于0.7,说明这些植物均具有一定的水分节约策略,从稳定碳同位素方面指示了三道岭植物群的气候类型为非热带湿润型,间接支持了商平等[20]根据古植被类型推测该地区中侏罗世气候为北温带型。该方法提供了一种相对简单的途径来确定某一化石植物群的气候类型。
为了与三道岭中侏罗世植物化石的Ci/Ca进行比较,也分析了似银杏属植物的现存对应种——银杏的Ci/Ca。从表 2可知,似银杏化石的Ci/Ca值为0.60,西安现生银杏的值为0.63,二者相似。虽然西安的现代气候为暖温带半湿润型,但是由于本次分析的现生西安银杏人工种植于大学校园内,并不缺少水分,因此其所处的小生境应该归为湿润型,从而与三道岭地区中侏罗世温带潮湿型气候相似。Ehleringer et al.[48]的研究已经表明,不同植物的Ci/Ca对CO2浓度增高的响应不同,一些物种的Ci/Ca保持恒定,而另一些物种的Ci/Ca发生变化,但是其Ci保持稳定。这是因为不同植物间气孔导度以及自身叶绿体对CO2需要的差异。Tu et al.[51]曾经研究不同CO2浓度下栎属植物碳同位素分馏值的变化,发现栎属植物的Ci/Ca一直保持稳定,说明栎属植物对CO2的变化比较敏感,是恢复地史时期古CO2浓度的良好指示植物。因此,一些学者已经利用栎属植物的气孔参数重建出新近纪的古CO2变化[51]。银杏植物的气孔参数一直被认为对CO2浓度的变化比较敏感,是重建古CO2浓度的一个重要且使用广泛的物种[52]。但是,银杏植物的生理特征对CO2浓度增高的响应却鲜见报道。当大气CO2浓度增加时,植物通过降低气孔密度来保持一个稳定的或近稳定的Ci/Ca值,这也是利用气孔参数恢复CO2浓度的生理机制。肖良等[21]已根据银杏类植物化石的气孔参数重建出三道岭地区中侏罗世的古CO2浓度为1 770 mL/m3,比现今390 mL/m3的CO2浓度高出约4.5倍。CO2浓度的增加已被证明是引起温室效应的重要气体,McElwain et al.[53]据此建立了CO2和温度之间的关系式:ΔT=4.0×ln(RCO2),ΔT表示不同CO2水平下全球平均大气表面温度间的差异。肖良等[21]在前期研究中,已经获得该地区西山窑组中Ginkgoites的RCO2为5.9,据以上公式计算出ΔT为7.1℃。而现在全球平均大气表面温度的背景值为14℃[19],因此推断出三道岭地区中侏罗世的古平均温度为21.1℃,而此次现生银杏采集地——西安的年均温为13.7℃。本次研究的中侏罗世似银杏的Ci/Ca与现生银杏的相似,中侏罗世Ca的增加同时意味着Ci的提高,中侏罗世银杏植物的高Ci值可能反映了植物当时具有高的光合速率[49, 54]。同时也说明,随着温度升高,银杏类植物的光合速率会随之增加。这从生理方面解释了银杏植物Ci/Ca保持恒定的机制。而恒定的Ci/Ca值则指示了银杏植物的气孔参数对CO2的变化比较敏感,其气孔参数可作为重建CO2浓度的良好指示剂。因此,本次研究为判断一种植物是否可用来重建古CO2浓度提供了一个简便的方法,即如果发现某种植物在不同CO2水平下,其Ci/Ca保持恒定的话,那么这种植物的气孔参数对CO2的变化比较敏感,是重建古CO2浓度的良好指示物。
4 结论(1) 似银杏属(Ginkgoites)、拟刺葵属(Phoenicopsis)和枝脉蕨属(Cladophlebis)三种叶片化石的δ13C分别为-23.55‰、-22.18‰和-23.37‰,属于典型的C3植物。斯堪尼狭轴穗(Stenorachis)银杏类繁殖器官的δ13C为-20.91‰,比叶片化石的δ13C偏正,说明果实比叶片更能富集13C。
(2) 根据化石Ginkgoites和现生Ginkgo biloba的稳定碳同位素组分获得的大气CO2的δ13Ca分别为-4.43‰和-7.54‰,与据海洋碳酸钙和直接测量的δ13Ca相似,表明银杏类叶片的稳定碳同位素比值是重建地质历史时期大气CO2稳定碳同位素值的一个可靠材料。
(3) 化石Ginkgoites的Ci/Ca比率为0.60,而现生Ginkgo biloba的Ci/Ca为0.63,二者相似,从而推断银杏植物的Ci/Ca在地史时期不同CO2水平下能够保持恒定,指示了银杏植物气孔参数对CO2变化比较敏感,其气孔参数可作为重建CO2浓度的良好指示物。这也为判断一种植物能否用来恢复古CO2浓度提供了一种简便而有效的检测方法。
致谢: 感谢编辑老师和审稿专家对论文提出的宝贵意见。| [1] | 刘贤赵, 张勇, 宿庆, 等. 现代陆生植物碳同位素组成对气候变化的响应研究进展[J]. 地球科学进展, 2014, 29 (12): 1341–1354. [ Liu Xianzhao, Zhang Yong, Su Qing, et al. Research progress in responses of modern terrestrial plant carbon isotope composition to climate change[J]. Advances in Earth Science, 2014, 29(12): 1341–1354. ] |
| [2] | Chen F, Yuan Y, Wei W. Climatic response of Picea crassifolia tree-ring parameters and precipitation reconstruction in the western Qilian Mountains, China[J]. Journal of Arid Environments, 2011, 75(11): 1121–1128. DOI: 10.1016/j.jaridenv.2011.06.010 |
| [3] | Petit J R, Jouzel J, Raynaud D, et al. Climate and atmospheric history of the past 420, 000 years from the Vostok ice core, Antarctica[J]. Nature, 1999, 399(6735): 429–436. DOI: 10.1038/20859 |
| [4] | Wang Huanye, Dong Hailiang, Zhang Chuanlun, et al. Deglacial and Holocene archaeal lipid-inferred paleohydrology and paleotemperature history of Lake Qinghai, northeastern Qinghai-Tibetan Plateau[J]. Quaternary Research, 2015, 83(1): 116–126. DOI: 10.1016/j.yqres.2014.10.003 |
| [5] | 袁子能, 邢磊, 张海龙, 等. 生物标志物稳定氢同位素研究进展及在海洋古环境重建中的应用[J]. 地球科学进展, 2012, 27 (3): 276–283. [ Yuan Zineng, Xing Lei, Zhang Hailong, et al. Progress of biomarker stable hydrogen isotope and its application to marine paleoenvironmental reconstruction[J]. Advances in Earth Science, 2012, 27(3): 276–283. ] |
| [6] | 李明涛, 孙柏年, 肖良, 等. 浙东中新世Betula mioluminifera Hu et Chaney的发现及古气候重建[J]. 地球科学进展, 2008, 23 (6): 651–658. [ Li Mingtao, Sun Bainian, Xiao Liang, et al. Discovery of Betula mioluminifera Hu et Chaney from the Miocene in eastern Zhejiang and reconstruction of palaeoclimate[J]. Advances in Earth Science, 2008, 23(6): 651–658. ] |
| [7] | Spicer R A, Yang Jian, Herman A B, et al. Asian Eocene monsoons as revealed by leaf architectural signatures[J]. Earth and Planetary Science Letters, 2016, 449: 61–68. DOI: 10.1016/j.epsl.2016.05.036 |
| [8] | Sun Jimin, Xu Qinghai, Liu Weiming, et al. Palynological evidence for the latest Oligocene-early Miocene paleoelevation estimate in the Lunpola Basin, central Tibet[J]. Palaeogeography, Palaeoclimatology, Palaeoecology, 2014, 399: 21–30. DOI: 10.1016/j.palaeo.2014.02.004 |
| [9] | Kelly E F, Blecker S W, Yonker C M, et al. Stable isotope composition of soil organic matter and phytoliths as paleoenvironmental indicators[J]. Geoderma, 1998, 82(1/2/3): 59–81. |
| [10] | Schatz A K, Zech M, Buggle B, et al. The late Quaternary loess record of Tokaj, Hungary: reconstructing palaeoenvironment, vegetation and climate using stable C and N isotopes and biomarkers[J]. Quaternary International, 2011, 240(1/2): 52–61. |
| [11] | 郑淑霞, 上官周平. 陆生植物稳定碳同位素组成与全球变化[J]. 应用生态学报, 2006, 17 (4): 733–739. [ Zheng Shuxia, Shangguan Zhouping. Terrestrial plant stable carbon isotope composition and global change[J]. Chinese Journal of Applied Ecology, 2006, 17(4): 733–739. ] |
| [12] | Sun Bainian, Wang Qiujun, Konrad W, et al. Reconstruction of atmospheric CO2 during the Oligocene based on leaf fossils from the Ningming formation in Guangxi, China[J]. Palaeogeography, Palaeoclimatology, Palaeoecology, 2016, 467: 5–15. |
| [13] | Yang Jian, Wang Yufei, Spicer R A, et al. Climatic reconstruction at the Miocene Shanwang Basin, China, using leaf margin analysis, CLAMP, coexistence approach, and overlapping distribution analysis[J]. American Journal of Botany, 2007, 94(4): 599–608. DOI: 10.3732/ajb.94.4.599 |
| [14] | Hesselbo S P, Morgans-Bell H S, McElwain J C, et al. Carbon-cycle perturbation in the Middle Jurassic and accompanying changes in the terrestrial paleoenvironment[J]. Journal of Geology, 2003, 111(3): 259–276. DOI: 10.1086/373968 |
| [15] | Kürschner W M. Carbon isotope composition of fossil leaves-revealing ecophysiological responses to past environmental change[J]. New Phytologist, 2002, 155(2): 199–201. DOI: 10.1046/j.1469-8137.2002.00461_2.x |
| [16] | Xiao Liang, Yang Hong, Sun Bainian, et al. Stable isotope compositions of recent and fossil sun/shade leaves and implications for palaeoenvironmental reconstruction[J]. Review of Palaeobotany and Palynology, 2013, 190: 75–84. DOI: 10.1016/j.revpalbo.2012.10.002 |
| [17] | Lockheart M J, Poole I, van Bergen P F, et al. Leaf carbon isotope compositions and stomatal characters: important considerations for palaeoclimate reconstructions[J]. Organic Geochemistry, 1998, 29(4): 1003–1008. DOI: 10.1016/S0146-6380(98)00168-5 |
| [18] | Xie Sanping, Sun Bainian, Yan Defei, et al. Leaf cuticular characters of Ginkgo and implications for paleoatmospheric CO2 in the Jurassic[J]. Progress in Natural Science, 2006, 16(S): 258–163. |
| [19] | Yan Defei, Sun Bainian, Xie Sanping, et al. Response to paleoatmospheric CO2 concentration of Solenites vimineus (Phillips) Harris (Ginkgophyta) from the Middle Jurassic of the Yaojie Basin, Gansu Province, China[J]. Science in China Series D: Earth Sciences, 2009, 52(12): 2029–2039. DOI: 10.1007/s11430-009-0181-1 |
| [20] | 商平, 付国斌, 侯全政, 等. 新疆吐哈盆地中侏罗世植物化石[J]. 现代地质, 1999, 13 (4): 403–407. [ Shang Ping, Fu Guobin, Hou Quanzheng, et al. Middle Jurassic fossil plants from Turpan-Hami Basin, Xinjiang, Northwest China[J]. Geoscience, 1999, 13(4): 403–407. ] |
| [21] | 肖良, 李勇, 周建仁, 等. 新疆吐哈盆地中侏罗世古大气CO2重建[J]. 兰州大学学报:自然科学版, 2014, 50 (2): 154–160. [ Xiao Liang, Li Yong, Zhou Jianren, et al. Paleoatmospheric CO2 level of the Middle Jurassic in Turpan-Hami Basin, Xinjiang[J]. Journal of Lanzhou University: Natural Sciences, 2014, 50(2): 154–160. ] |
| [22] | 陈建平, 黄第藩, 李晋超, 等. 吐哈盆地侏罗纪煤系油气主力源岩探讨[J]. 地质学报, 1999, 73 (2): 140–152. [ Chen Jianping, Huang Difan, Li Jinchao, et al. Main source rocks of petroleum from Jurassic coal-bearing strata in the Turpan-Hami Basin, Northwest China[J]. Acta Geologica Sinica, 1999, 73(2): 140–152. ] |
| [23] | 陶明信. 吐—哈盆地大地构造环境分析——兼论大陆板内盆地与造山带的成因关系[J]. 沉积学报, 1994, 12 (4): 40–50. [ Tao Mingxin. Tectonic environmental analysis of Turpan-Hami Basin on the genetic relationship between basin and orogenic belt of continental inner plate[J]. Acta Sedimentologica Sinica, 1994, 12(4): 40–50. ] |
| [24] | 曹代勇, 邵龙义, 张鹏飞. 吐哈盆地早、中侏罗世聚煤期古构造[J]. 古地理学报, 1999, 1 (2): 46–52. [ Cao Daiyong, Shao Longyi, Zhang Pengfei. Palaeotectonics in the early and Middle Jurassic coal-forming periods of the Turpan-Hami Basin[J]. Journal of Palaeogeography, 1999, 1(2): 46–52. ] |
| [25] | 张元, 李树新, 郭翔, 等. 吐哈盆地台北凹陷侏罗系高分辨率层序地层学研究[J]. 石油地球物理勘探, 2005, 40 (Suppl.1): 102–107. [ Zhang Yuan, Li Shuxin, Guo Xiang, et al. High resolution sequence stratigraphy of Jurassic Taibei sag, Turpan-Hami Basin[J]. Oil Geophysical Prospecting, 2005, 40(Suppl.1): 102–107. ] |
| [26] | 赵虹, 党犇, 陈永胜, 等. 吐哈盆地台北凹陷侏罗系储层砂体发育及其岩石学特征[J]. 西安科技大学学报, 2007, 27 (3): 386–391. [ Zhao Hong, Dang Ben, Chen Yongsheng, et al. Sandstone-bodies and their petrology characteristics of Jurassic reservoirs in Taibei depression of Turpan-Hami Basin[J]. Journal of Xi'an University of Science and Technology, 2007, 27(3): 386–391. ] |
| [27] | 邵龙义, 高迪, 罗忠, 等. 新疆吐哈盆地中、下侏罗统含煤岩系层序地层及古地理[J]. 古地理学报, 2009, 11 (2): 215–224. [ Shao Longyi, Gao Di, Luo Zhong, et al. Sequence stratigraphy and palaeogeography of the Lower and Middle Jurassic coal measures in Turpan-Hami Basin[J]. Journal of Palaeogeography, 2009, 11(2): 215–224. ] |
| [28] | 新疆维吾尔自治区地层表编写组. 西北地区区域地层表:新疆维吾尔自治区分册[M]. 北京: 地质出版社, 1981: 6-233. [ Regional Stratigraphic Scale of Xinjiang. Regional stratigraphic table of Northwest China: Xinjiang province volume[M]. Beijing: Geological Publishing House, 1981: 6-233. ] |
| [29] | 蔡土赐, 孙巧缡, 缪长泉, 等. 新疆维吾尔自治区岩石地层[M]. 武汉: 中国地质大学出版社, 1999: 120-126. [ Cai Tuci, Sun Qiaoli, Miao Changquan, et al. Stratigraphy (lithostratic) of Xinjiang Uygur Autonomous Region[M]. Wuhan: China University of Geosciences Press, 1999: 120-126. ] |
| [30] | 吴伯林, 徐高中. 吐哈盆地西南缘水西沟群古气候演变特征及其层序地层学意义[J]. 东华理工学院学报, 2004, 27 (2): 135–140. [ Wu Bolin, Xu Gaozhong. Evolution feature of palaeoclimate and significance of sequence stratigraphy in Suixigou Group in the southwest edge of Turpan-Hami Basin[J]. Journal of East China Institute of Technology, 2004, 27(2): 135–140. ] |
| [31] | 张泓, 李恒堂, 熊存卫, 等. 中国西北侏罗纪含煤地层与聚煤规律[M]. 北京: 地质出版社, 1998: 1-316. [ Zhang Hong, Li Hengtang, Xiong Cunwei, et al. Jurassic coal-bearing strata and coal accumulation in Northwest China[M]. Beijng: Geological Publishing House, 1998: 1-316. ] |
| [32] | 孙革, 郑少林, DilcherD L, 等. 辽西早期被子植物及伴生植物群[M]. 上海: 上海科技教育出版社, 2001: 7-227. [ Sun Ge, Zheng Shaolin, Dilcher D L, et al. Early angiosperms and their associated plants from western Liaoning, China[M]. Shanghai: Shanghai Scientific and Technological Education Publishing House, 2001: 7-227. ] |
| [33] | 马晔, 刘锦春. δ13C在植物生态学研究中的应用[J]. 西北植物学报, 2013, 33 (7): 1492–1500. [ Ma Ye, Liu Jinchun. Applications of δ13C in plant ecological research[J]. Acta Botanica Boreali-Occidentalia Sinica, 2013, 33(7): 1492–1500. ] |
| [34] | Martinelli L A, Almeida S, Brown I F, et al. Stable carbon isotope ratio of tree leaves, boles and fine litter in a tropical forest in Rondônia, Brazil[J]. Oecologia, 1998, 114(2): 170–179. DOI: 10.1007/s004420050433 |
| [35] | 周志炎. 中生代银杏类植物系统发育、分类和演化趋向[J]. 云南植物研究, 2003, 25 (4): 377–396. [ Zhou Zhiyan. Mesozoic ginkgoaleans: phylogeny, classification and evolutionary trends[J]. Acta Botanica Yunnanica, 2003, 25(4): 377–396. ] |
| [36] | Bocherens H, Friis E M, Mariotti A, et al. Carbon isotopic abundances in Mesozoic and Cenozoic fossil plants: palaeoecological implications[J]. Lethaia, 1993, 26(4): 347–358. DOI: 10.1111/let.1993.26.issue-4 |
| [37] | 丁素婷, 孙柏年, 吴靖宇, 等. 甘肃华亭侏罗系Phoenicopsis(Phoenicopsis)angustifolia Heer的表皮构造与碳同位素特征[J]. 兰州大学学报:自然科学版, 2010, 46 (1): 14–21. [ Ding Suting, Sun Bainian, Wu Jingyu, et al. Cuticular composition and carbon isotope characteristics of Jurassic Phoenicopsis (Phoenicopsis) angustifolia Heer from Huating in Gansu province, China[J]. Journal of Lanzhou University: Natural Sciences, 2010, 46(1): 14–21. ] |
| [38] | 冯虎元, 安黎哲, 王勋陵. 环境条件对植物稳定碳同位素组成的影响[J]. 植物学通报, 2000, 17 (4): 312–318. [ Feng Huyuan, An Lizhe, Wang Xunling. A review on effect of environmental factors on stable carbon isotope composition in plants[J]. Chinese Bulletin of Botany, 2000, 17(4): 312–318. ] |
| [39] | 何春霞, 李吉跃, 孟平, 等. 树木叶片稳定碳同位素分馏对环境梯度的响应[J]. 生态学报, 2010, 30 (14): 3828–3838. [ He Chunxia, Li Jiyue, Meng Ping, et al. Changes in leaf stable carbon isotope fractionation of trees across climatic gradients[J]. Acta Ecologica Sinica, 2010, 30(14): 3828–3838. ] |
| [40] | Farquhar G D, O'Leary M H, Berry J A. On the relationship between carbon isotope discrimination and the intercellular carbon dioxide concentration in leaves[J]. Australian Journal of Plant Physiology, 1982, 9(2): 121–137. DOI: 10.1071/PP9820121 |
| [41] | Du Baoxia, Sun Bainian, Zhang Mingzhen, et al. Atmospheric palaeo-CO2 estimates based on the carbon isotope and stomatal data of Cheirolepidiaceae from the Lower Cretaceous of the Jiuquan Basin, Gansu province[J]. Cretaceous Research, 2016, 62: 142–153. DOI: 10.1016/j.cretres.2015.07.020 |
| [42] | Jahren A H, Arens N C, Harbeson S A. Prediction of atmospheric δ13CO2 using fossil plant tissues[J]. Reviews of Geophysics, 2008, 46(1): RG1002. |
| [43] | Arens N C, Jahren A H, Amundson R. Can C3 plants faithfully record the carbon isotopic composition of atmospheric carbon dioxide?[J]. Paleobiology, 2000, 26(1): 137–164. DOI: 10.1666/0094-8373(2000)026<0137:CCPFRT>2.0.CO;2 |
| [44] | Gröcke D R. The carbon isotope composition of ancient CO2 based on higher-plant organic matter[J]. Philosophical Transactions of the Royal Society A: Mathematical, Physical and Engineering Sciences, 2002, 360(1793): 633–658. DOI: 10.1098/rsta.2001.0965 |
| [45] | Beerling D J, Lake J A, Berner R A, et al. Carbon isotope evidence implying high O2/CO2 ratios in the Permo-Carboniferous atmosphere[J]. Geochimica et Cosmochimica Acta, 2002, 66(21): 3757–3767. DOI: 10.1016/S0016-7037(02)00901-8 |
| [46] | Farquhar G D, Ehleringer J R, Hubick K T. Carbon isotope discrimination and photosynthesis[J]. Annual Review of Plant Physiology and Plant Molecular Biology, 1989, 40: 503–537. DOI: 10.1146/annurev.pp.40.060189.002443 |
| [47] | Grein M, Roth-Nebelsick A, Wilde V. Carbon isotope composition of middle Eocene leaves from the Messel Pit, Germany[J]. Palaeodiversity, 2010, 3: 1–7. |
| [48] | Ehleringer J R, Cerling T E. Atmospheric CO2 and the ratio of intercellular to ambient CO2 concentrations in plants[J]. Tree Physiology, 1995, 15(2): 105–111. DOI: 10.1093/treephys/15.2.105 |
| [49] | Chakraborty S, Jana B N, Bhattacharya S K, et al. Carbon isotopic composition of fossil leaves from the Early Cretaceous sediments of western India[J]. Journal of Earth System Science, 2011, 120(4): 703–711. DOI: 10.1007/s12040-011-0098-x |
| [50] | González-Rodríguez A M, Morales D, Jiménez M S. Gas exchange characteristics of a Canarian laurel forest tree species (Laurus azorica) in relation to environmental conditions and leaf canopy position[J]. Tree Physiology, 2001, 21(14): 1039–1045. DOI: 10.1093/treephys/21.14.1039 |
| [51] | Tu T T N, Kürschner W M, Schouten S, et al. Leaf carbon isotope composition of fossil and extant oaks grown under differing atmospheric CO2 levels[J]. Palaeogeography, Palaeoclimatology, Palaeoecology, 2004, 212(3/4): 199–213. |
| [52] | Sun Bainian, Dilcher D L, Beerling D J, et al. Variation in Ginkgo biloba L. leaf characters across a climatic gradient in China[J]. Proceedings of the National Academy of Sciences of the United States of America, 2003, 100(12): 7141–7146. DOI: 10.1073/pnas.1232419100 |
| [53] | McElwain J C, Beerling D J, Woodward F I. Fossil plants and global warming at the Triassic-Jurassic boundary[J]. Science, 1999, 285(5432): 1386–1390. DOI: 10.1126/science.285.5432.1386 |
| [54] | Beerling D J. Ecophysiological responses of woody plants to past CO2 concentrations[J]. Tree Physiology, 1996, 16(4): 389–396. DOI: 10.1093/treephys/16.4.389 |
 2017, Vol. 35
2017, Vol. 35