扩展功能
文章信息
- 高有红, 李卓仑, 韩朗, 李若兰
- GAO YouHong, LI ZhuoLun, HAN Lang, LI RuoLan
- 阿拉善沙漠植物钙质根管:形态特征、分类及其环境指示意义
- Calcareous Root Tubes in the Alashan Deserts: morphological characteristics, classification and environmental significance
- 沉积学报, 2017, 35(1): 75-84
- ACTA SEDIMENTOLOGICA SINCA, 2017, 35(1): 75-84
- 10.14027/j.cnki.cjxb.2017.01.008
-
文章历史
- 收稿日期:2016-02-02
- 收修改稿日期: 2016-05-09
植物钙质根管是陆生植物形成的次生碳酸盐结壳,其广泛分布于季节性土壤水分亏损的石灰质土壤或风成沉积地层中,如地中海地区[1-3]、澳大利亚中西部[4]、美国中西部[5]、印度西南部[6]等。因其在古环境研究中具有极高的潜力和价值,得到了国内外学者的广泛关注,先后开展了植物钙质根管的分类[7-8]、形态学[9]、年代学[10-11]、生物标志化合物研究[12]、同位素组成[10, 13]及环境指示意义[14-18]等方面的研究。上述研究为植物钙质根管的形成机制、环境指示意义等研究提供了有益的参考。
在植物钙质根管的形态学及其形成机制方面的研究中,Klappa[7],Barta[8]先后给出了植物钙质根管的定义,并对每一个子类别的植物钙质根管形态进行了描述。但由于命名规则的不一致以及植物钙质根管形态特征的差别,导致了对植物钙质根管的定义、命名和分类等在不同的研究中仍存在区别和混淆的情况。譬如, hypocoating[8],rhizocretion[7]都表示植物钙质根管子类中的绕根结核;而子类root cast被Klappa[7]定义为由于碳酸盐或沉积物将根模具填充而形成的根状结核,但在Cramer et al.[4]的研究中,则将root cast描述为由于根系和根围微生物的共同作用而形成的管状碳酸盐胶结,即将root cast定义为绕根结核,等同于Klappa[7]的rhizocretion。虽然上述研究在一定程度上给出了植物钙质根管的定义和形态描述,但由于命名的不一致性,导致了其基本概念仍然相对模糊,不同的概念指示同一种根管形态,不同的根管形态被同一个概念指代[4, 7-8]。例如,国内学者在古气候研究中使用的表示植物钙质根管概念的名词主要有:植物根管[14],根状结核[15],钙质根套[16],植物根套[19],蚀余钙质根管[17],植物钙质根管[18]等。这些概念是否指示同一种根管形态还是有一定的差异,目前尚未见具体的研究和论述。同时,对于植物钙质根管的形成原因及其环境指示意义仍然存在一定分歧,以阿拉善沙漠植物钙质根管为例,杨小平认为植物根管是大气降水在沙丘中的淋滤作用产生的碳酸盐胶结[14],Li et al.[11], 李卓仑等[18]认为气候相对湿润及土壤发育是制约植物钙质根管形成的重要因素,高尚玉等通过对腾格里沙漠广泛分布的钙质根套的14C测年研究认为钙质根套是砂质古土壤的蚀余堆积,可以指示全新世最适宜期古土壤曾在腾格里沙漠广泛发育[16]。上述研究均表明植物钙质根管的形成指示了相对湿润的气候条件[11, 14, 16, 18];而陈建生等[15]发现根状结核主要分布于干涸古湖泊,并认为根状结核是由地下水重结晶作用形成的。上述对植物钙质根管形成机制的分歧,是否是由于未对其进行形态学分类以及不同类型的植物钙质根管,其形成过程是否具有一定的差异,这些差异是否具有不同的环境指示意义,均尚需进一步的研究。
基于上述,本文拟通过形态学研究,进一步明晰植物钙质根管的基本概念及其形成机制。在此基础上对阿拉善沙漠的26组根管样品进行形态学分类,并探讨不同类型植物钙质根管在阿拉善沙漠的时间分布特征及其环境指示意义。这些问题的解决将进一步明晰植物钙质根管的形成机制及其环境指示意义,为其成为可靠的古环境研究代用指标提供新的证据。
1 区域概况阿拉善沙漠位于我国北方中部沙区,由巴丹吉林沙漠、腾格里沙漠和乌兰布和沙漠组成,面积约8×104 km2(图 1)。巴丹吉林沙漠位于雅布赖山以西、北大山以北、弱水以东、拐子湖以南,面积为5.2×104 km2,为我国第二大沙漠[20]。年降水量40~120 mm,自东南向西北减少,年平均蒸发量约为1 000 mm[21-22]。中部有密集的高大沙山,高约200~300 m,最高可达500 m,以复合型沙山为主。沙山之间的洼地分布有许多大小不等的咸水湖,而淡水湖甚少,仅见于沙漠东南部边缘。沙丘上植物较少,仅于沙丘下部或丘间低地生长有稀疏灌木、半灌木。腾格里沙漠位于阿拉善高原东南部,介于贺兰山、祁连山与雅布赖山之间,面积约为4.27×104 km2,是中国第四大沙漠[23],年降水量125~160 mm,年潜在蒸发量2 600 mm[24]。沙漠内部沙丘、湖盆、山地、平地交错分布,其中沙丘占71 %,以流动沙丘为主,沙漠内大小湖盆多达422个。植被以沙生灌木、半灌木为主。乌兰布和沙漠位于阿拉善高原东北部,北至狼山,东北与河套平原相邻。东近黄河,南至贺兰山北麓,西至吉兰泰盐池,面积为1×104 km2。年均降水量102.9 mm,年均蒸发为2 957 mm[24]。整个沙漠地势都低于黄河水面,有引黄灌溉的条件,浅水资源丰富。植被由沙生、旱生、盐生类灌木组成。

|
| 图 1 研究区植物钙质根管采样点分布图 Figure 1 Study area and distribution of the calcareous root tubes |
Klappa[7]将高等植物根系形成的生物沉积结构定义为根迹化石(Rhizoliths),包括碳酸盐和沉积物在植物根系周围沉淀并胶结形成的或者根细胞内部发生钙化形成的根状结构,即本文所提及的植物钙质根管。同时,Klappa强调了根迹化石是由高等植物根系所形成的,并根据其不同形态进行了分类并对其子类进行了命名。虽然根迹化石这一定义在后续的研究中被广泛采用[25-27],但对于其子类的命名,有待进一步统一。譬如,Barta[10]将碳酸钙注入土壤基质的空洞中形成的结构定义为绕根结核(hypocoating)(图 2a);Cramer[4]将碳酸盐胶结物定义为根状结核(Root cast)(图 2b),并指出原先存在于这种胶结物内部的根系的位置往往被更软的碳酸盐胶结占据。Barta和Cramer所定义的绕根结核和根状结核均对应于Klappa对根迹化石分类中的绕根结核(rhizocretion)(图 2c)。而国内学者的研究,则未细分到其子类。为明晰上述概念及分类,本文将植物钙质根管定义为陆生植物形成的次生碳酸盐结壳,亦即Klappa文章中提及的根迹化石(Rhizoliths),并参考其分类,将植物钙质根管分成五个子类:①钙质根套(calcareous sheath):由碳酸盐胶结粗质沙砾构成的简单硬质外壳。在较为疏松的风成沉积物或风积沙中,植物根系分泌物与根系微生物分泌物将根系周围松散沉积物或沙砾黏结聚集(图 2d),随着根围水分的蒸发,植物呼吸作用和微生物活动产生大量的CO2,导致碳酸盐在根围沉淀并将松散沉积物或沙砾胶结形成钙质根套(calcareous sheath)(图 2e)[28]。②绕根结核(rhizocretion):硬质外壳内部胶结有白色碳酸盐而形成的双层结构或者由碳酸盐胶结粗质沙砾或完全由碳酸盐胶结形成的实心根状结构(图 2c)。其形成是由于钙质根套的形成阻碍了根系吸收水分和养分,导致根系逐渐死亡,伴随着水分在钙质根套内部的淋滤,根系快速腐烂所产生的蛋白质和糖类导致根围的pH值增加变为碱性,白色的碳酸盐沉淀或碳酸盐裹挟着周围的沙砾逐步填充原先根系占据的空间,形成了绕根结核[2]。③根模具(root mould):土壤中的根系腐烂后保留下来的疏松管状孔洞(图 2f)。植物根系插入质地坚硬的土壤或沉积物当中,当根系腐烂后,由原先根系所占据的位置形成多孔而具渗透性的质地疏松的管状孔洞[7]。④根导管(root tubule):根模具被碳酸盐进一步胶结而成的管体(图 2g)。根模具一旦形成即成为水分下行的导管,含钙水溶液沿着导管不断淋滤,随着水分的不断蒸发,根模具内的含钙水溶液达到饱和,碳酸盐不断积累,将疏松的根模具胶结成质地坚硬的管体,即根导管[7](Klappa,1980)。⑤根状结核(root cast):根导管内部被碳酸盐或沉积物填充而形成的根状结构(图 2h)。当含钙水溶液继续沿着根导管内壁淋滤,水分的蒸发使裹挟着沉积物颗粒的碳酸盐在管壁内不断积累胶结形成白色或灰色的沉淀而将管壁进一步填充,最终形成根状结核(root cast)[2]。可见,上述5个子类的形成过程有较为明显的差异,其中,前两种子类的形成与植物的生长及其根围的微生物活动密切相关,而根模具、根导管和根状结核则是在植物根系完全腐烂之后由于水分的蒸发形成的[2, 7]。

|
| 图 2 植物钙质根管的分类 图片来自文献[4, 7-8]。a. Barta定义的绕根结核[8];b. Cramer定义的根状结核[4];c. Klappa定义的绕根结核[7];d.植物根系分泌物与微生物分泌物将根系周围松散沉积物或沙砾黏结聚集形成的结构;e.钙质根套;f.根模具;g.根导管;h.根状结核 Figure 2 Classification of the calcareous root tubes The figures cited from [4, 7-8].a. rhizocretion defined by Barta[8]; b. root cast defined by Cramer[4]; c. rhizocretion defined by Klappa[7]; d. the structure formed by loose sediments or sand which was gathered by root exudates and secretion secreted from microorganisms; e. calcareous sheath; f. root mould; g. root tubule; h. root cast |
上述植物钙质根管的5种子类在形态上亦有一定的差异。钙质根套和根导管均为空心管体;绕根结核和根状结核则是碳酸盐胶结形成的双层结构或由粗质沙砾、沉积物等填充形成的实心结构;根模具仅是土壤中疏松的管状空心孔洞[7]。因此,可以通过形态学特征并结合有无微生物活动参与其形成过程来区分上述5种子类。
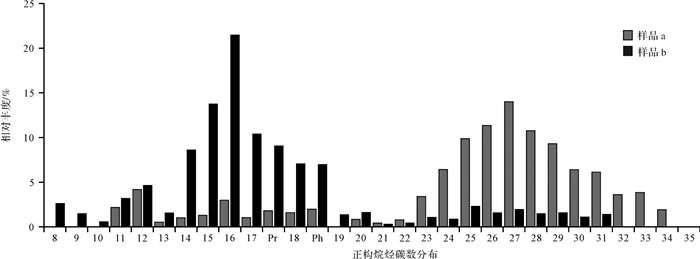
3 阿拉善高原植物钙质根管的分类及其形态学特征尽管根据前人的研究成果[7-8]可以将植物钙质根管分为五个子类,但不同地区的植物钙质根管会因其形成途径的不同而形成不同的子类。植物钙质根管中的正构烷烃可作为判断其形成途径的依据。Ficken et al.[28-30]研究发现,细菌、藻类等微生物对短链正构烷烃(碳数小于20)的贡献较大,而对26组阿拉善沙漠植物钙质根管样品中的正构烷烃研究发现,绝大多数样品中均存在短链正构烷烃,其中颜色呈灰白色且存在明显分层的根管样品的短链正构烷烃相对丰度较高(图 3),个别样品甚至其主峰碳数小于20;颜色呈棕黄色且分层不明显的根管样品短链正构烷烃的丰度稍低(图 3),说明阿拉善沙漠的植物钙质根管在形成的过程中受到根围微生物活动的深刻影响,而非在植物根系完全腐烂之后形成。综上,根据前述根管的两种形成途径,阿拉善沙漠的植物钙质根管的形成应当是由植物生长和根围微生物活动引起的,可形成两种类型的植物钙质根管,即钙质根套和绕根结核。
|
| 图 3 植物钙质根管中正构烷烃的相对丰度 a.采样点坐标为(39°30′31.1″ N,105°38′40.4″ E);b.采样点坐标为(38°47′14.5″ N,104°17′8.9″ E) Figure 3 Abundance of n-alkanes in the calcareous root tubes a.sample point coordinates is (39°30′31.1″ N, 105°38′40.4″ E); b.sample point coordinates is (38°47′14.5″ N, 104°17′8.9″ E) |
通过对26个采样点(图 1)的植物钙质根管样品的颜色,长度,管径,有无分层等形态学特征的统计,结果显示(表 1):26个采样点中,绝大多数采样点这两种类型的植物钙质根管均有分布,每种类型的植物钙质根管的形态特征归纳如下:
| 地区 | 采样点位置 | cal yr B.P. (2σ)* | 颜色 | 短链正构烷烃相对丰度 | 根管总数/个 | 钙质根套百分比 | 绕根结核百分比 | |
| 纬度(N) | 经度(E) | |||||||
| 腾格里沙漠 | 38°46′42.1″ | 105°14′28.9″ | 2 259 (2 061~2 457) | 棕黄色 | 较低 | 34 | 76% | 24% |
| 38°44′30.4″ | 105°16′7.4″ | 3 150 (2 971~3 328) | 棕黄色 | 较低 | 8 | 50% | 50% | |
| 38°45′22.2″ | 105°05′13.1″ | 3 573 (3 455~3 691) | 棕黄色 | 较低 | 20 | 75% | 25% | |
| 38°47′14.5″ | 104°17′8.9″ | 4 192 (3 980~4 404) | 棕黄色 | 较低 | 20 | 90% | 10% | |
| 37°54′59.9″ | 104°52′13.0″ | 4 630 (4 438~4 821) | 棕黄色 | 较低 | 14 | 86% | 14% | |
| 38°24′1.7″ | 104°34′50.3″ | 5 462 (5 326~5 597) | 灰白色 | 较低 | 20 | 10% | 90% | |
| 38°48′58.9″ | 104°56′43.3″ | 5 523 (5 333~5 712) | 棕黄色 | 较低 | 10 | 60% | 40% | |
| 38°48′53.5″ | 104°16′24.5″ | 6 154 (6 004~6 305) | 灰白色 | 较高 | 10 | 40% | 60% | |
| 38°12′48.4″ | 104°34′50.3″ | 6 829 (6 670~6 988) | 棕黄色 | 较高 | 17 | 29% | 71% | |
| 乌兰布和沙漠 | 39°34′28.7″ | 105°52′23.3″ | 3 570 (3 448~3 692) | 灰白色 | 较高 | 6 | 100% | 0% |
| 39°50′18.5″ | 106°39′14.1″ | 3 879 (3 698~4 060) | 灰白色 | 较高 | 16 | 75% | 25% | |
| 39°41′36.5″ | 106°33′7.1″ | 4 137 (3 929~4 345) | 灰白色 | 较低 | 10 | 0% | 100% | |
| 39°52′51.6″ | 106°32′6.3″ | 4 617 (4 420~4 813) | 灰白色 | 较高 | 25 | 96% | 4% | |
| 40°17′29.7″ | 106°35′25.7″ | 4 631(4 440~4 821) | 灰白色 | 较高 | 5 | 0% | 100% | |
| 39°34′40.4″ | 105°50′30.6″ | 4 791 (4 617~4 964) | 棕黄色 | 较低 | 26 | 62% | 38% | |
| 39°39′1.8″ | 105°53′17.9″ | 6 382 (6 280~6 483) | 灰白色 | 较高 | 26 | 31% | 69% | |
| 40°10′41.2″ | 106°40′58.4″ | 6 451 (6 301~6 601) | 灰白色 | 较高 | 23 | 74% | 26% | |
| 39°30′31.1″ | 105°38′40.4″ | 6 534 (6 404~6 604) | 灰白色 | 较高 | 22 | 18% | 82% | |
| 39°59′59.8″ | 106°37′34.5″ | 7 102 (6 946~7 257) | 灰白色 | 较高 | 25 | 0% | 100% | |
| 巴丹吉林沙漠 | 39°51′27.13″ | 102°05 ′15.44″ | 2 553(2 378~2 728) | 灰白色 | 较低 | 15 | 73% | 27% |
| 39°46′29.41″ | 102°10 ′42.45″ | 3 237(3 083~3 391) | 棕黄色 | 较高 | 47 | 79% | 21% | |
| 39°46′7.9″ | 102°28′34.8″ | 5 256 (5 062~5 449) | 灰白色 | 较高 | 30 | 33% | 67% | |
| 39°56′13.9″ | 102°36′20.1″ | 6 353 (6 218~6 488) | 灰白色 | 较高 | 11 | 82% | 18% | |
| 39°57′19.4″ | 101°50′17.12″ | 31 190 (30 902~31 478) | 黑褐色 | 较低 | 20 | 0% | 100% | |
| 39°39′14.2″ | 102°09′26.3″ | 33 276 (32 708~33 843) | 黑褐色 | 较高 | 25 | 64% | 36% | |
| 39°39′12.6″ | 102°09′26.2″ | 34 084 (33 652~34 515) | 黑褐色 | 较低 | 16 | 56% | 44% | |
| 注:*年代结果引自文献[11]。 | ||||||||
(1)钙质根套,是由碳酸盐胶结粗质沙砾构成的简单硬质外壳,内部没有白色碳酸盐胶结物,无分层现象,有的仅在管壁内部有一层白色碳酸盐薄层(图 4a);部分钙质根套内部发现有未被分解的根系残体(图 4b);钙质根套的颜色以棕黄色和灰白色为主,仅有一组测年结果显示为深海氧同位素3阶段晚期(MIS 3a)的钙质根套[11]呈黑褐色(图 4c);钙质根套的平均长度在3~10 cm之间,管壁平均厚度在0.2~0.7 cm之间。

|
| 图 4 阿拉善沙漠植物钙质根管形态特征 a.钙质根套,内部无碳酸盐胶结,外附白色碳酸盐薄层;b.内部残留根毛的钙质根套;c.外表呈黑褐色的钙质根套;d.双层结构的绕根结核,管体内部存在较厚的碳酸盐胶结;e.由沙砾胶结而成的实心绕根结核,外表呈黑褐色;f.完全由碳酸盐胶结而成的实心绕根结核。 Figure 4 Morphological characteristics of calcareous root tubes from the Alashan Desert a. calcareous sheath without carbonate cementation in it but with the carbonate thin layer attached outside; b. calcareous sheath with remnant root hair; c. calcareous sheath with brown-black appearance; d. rhizocretion with double-layer structure and thick carbonate cementation within it; e. brown-black and solid rhizocretion cemented by sand gravel; f. solid rhizocretion cemented by carbonate completely, arrow points to the circular holes. |
(2)绕根结核,可分为两种不同的形态:第一种形态可分为内外两层,外层为由碳酸盐胶结粗质沙砾构成的硬质外壁,内层为细腻的白色碳酸盐胶结层(图 4d);第二种形态为实心的根状结构,大部分的绕根结核由碳酸盐胶结的粗质沙砾构成(图 4e),个别绕根结核完全由碳酸盐胶结而成,且横截面可观察到圆形小孔(图 4f)。绕根结核的颜色以灰白色为主,部分采样点存在棕黄色,仅有两个测年结果显示为MIS 3a阶段的绕根结核[11]呈黑褐色;绕根结核的平均长度在3~8 cm之间,管壁平均厚度在0.2~0.7 cm之间。
4 阿拉善沙漠植物钙质根管的时间分布特征及其环境指示意义 4.1 阿拉善沙漠植物钙质根管的时间分布特征本文选取的26组植物钙质根管样品主要分布于全新世中期(7~5 cal kyr B.P.)和晚期(4~0 cal kyr B.P.),少量分布于MIS 3a阶段(3组样品)。巴丹吉林沙漠7组样品中,2组分布于全新世中期,2组分布于全新世晚期,3组分布于MIS 3a阶段;腾格里沙漠9组样品中,4组分布于全新世中期,5组分布于全新世晚期;乌兰布和沙漠10组样品中,4组分布于全新世中期,6组分布于全新世晚期(表 1)。由于MIS 3a阶段的植物钙质根管样品量较少且主要集中分布于巴丹吉林沙漠,因此,本文将主要讨论阿拉善沙漠全新世植物钙质根管的时间分布特征。就各个沙漠来看(图 5),腾格里沙漠的5组全新世中期的植物钙质根管样品中绕根结核数量百分比明显高于钙质根套,而4组全新世晚期的植物钙质根管样品中两种类型的数量分布则与全新世中期恰好相反(图 5a);乌兰布和沙漠的4组全新世中期的植物钙质根管样品中两种类型的数量百分比与腾格里沙漠同时期的植物钙质根管的数量分布特征相同,而6组全新世晚期的植物钙质根管样品中有4组样品钙质根套的数量百分比明显高于绕根结核,另外2组样品全部为绕根结核(图 5b),有两个因素可能导致上述结果:一是采样点的总样品量过少,无法给出钙质根套和绕根结核数量百分比的准确数据;二是相对湿润的局地环境使得绕根结核广泛发育,从而影响了全新世晚期的钙质根套和绕根结核的数量分布特征的判断[24];尽管巴丹吉林沙漠采集到的全新世的植物钙质根管的样品量较少,但在全新世晚期钙质根套的数量百分比同样明显高于绕根结核,而在全新世中期的个别样品钙质根套的数量百分比较高可能是由于样品量较少或者受到局地环境的影响(图 5c)。综上,在阿拉善沙漠分布于全新世中期的植物钙质根管样品中绕根结核的数量百分比明显高于钙质根套;而分布于全新世晚期的植物钙质根管样品中钙质根套的数量百分比明显高于绕根结核。

|
| 图 5 阿拉善沙漠植物钙质根管绕根结核数量百分比 a.腾格里沙漠;b.乌兰布和沙漠;c.巴丹吉林沙漠 Figure 5 The percentage of rhizocretion of calcareous root tubes in the Alashan Desert a.Tengger Desert; b.Ulan Buh Desert; c.Badain Jaran Desert |
阿拉善沙漠植物钙质根管包括钙质根套和绕根结核两种类型。本研究结果显示,在阿拉善沙漠,钙质根套和绕根结核往往存在伴生现象(图 5),即同一采样点既存在钙质根套又存在绕根结核。Alonso-Zarza et al.[2]研究指出,钙质根套进一步形成绕根结核需受到如下两个条件的共同控制:一是有含钙水溶液沿着钙质根套内部产生淋滤;二是根系腐烂分解释放CO2并产生蛋白质和糖类导致根围的pH值增加变为碱性。换言之,单纯的含钙水溶液的淋滤但根系已完全腐烂无法分解释放CO2,亦或是根系腐烂释放大量CO2而没有含钙水溶液的淋滤作用,绕根结核均无法形成。因此,绕根结核的存在表明其必然受到含钙水溶液的淋滤作用。此外,绕根结核是伴随着植物根系的腐烂分解形成的,说明其形成所需的时间远远小于一般次生碳酸盐[10],表明在千年尺度上,同一采样点钙质根套与绕根结核可以认为是同一时期形成的。
前人的研究表明[14-15, 18],阿拉善沙漠植物钙质根管的形成受到了有效湿度的控制,形成于相对湿润的气候条件。在全新世中期(7~5 cal kyr B.P.),已有的研究结果显示,阿拉善沙漠地区气候较为湿润,是全新世气候最适宜期,钙质根管大量分布[24]。其中,巴丹吉林沙漠湖泊水位明显高于全新世晚期[31]、腾格里沙漠也显示了湿润的气候[32]、沙漠西北部湖泊水位在全新世中期达到最高值[33],乌兰布和沙漠也显示了较为湿润的气候特征[24],上述研究均表明,在阿拉善沙漠地区,全新世中期气候明显湿润。而全新世晚期(4~0 cal kyr B.P.),巴丹吉林沙漠湖泊水位相较于全新世中期明显下降[22, 31],腾格里沙漠植物钙质根管中低Sr/Ca比值揭示了气候相对干旱的特征[32]、红水河剖面总孢粉浓度显著降低也反映了气候由湿向干转变[34];乌兰布和沙漠亦呈现干旱特征[35],上述研究均反映出该区域气候由湿润向干旱转变的特点。本研究表明,绕根结核需要含钙水溶液的淋滤作用方能形成[2]。从阿拉善沙漠全新世不同类型的植物钙质根管的时间分布来看(图 5),分布于较为湿润的全新世中期(7~5 cal kyr B.P.)的植物钙质根管颜色以灰白色为主,显示了较高的碳酸盐含量,绕根结核的数量百分比明显高于钙质根套;而分布于较为干旱的全新世晚期(4~0 cal kyr B.P.)的植物钙质根管颜色则以棕黄色和灰白色为主,且钙质根套数量百分比明显高于绕根结核。因此,有效湿度较高时,钙质根套内部含钙水溶液淋滤作用较强,更易与根系腐烂产生CO2及根围变为碱性的条件相结合,产生大量碳酸盐沉淀而形成绕根结核;有效湿度较低时,钙质根套内部含钙水溶液淋滤作用相对较弱,与根系腐烂产生CO2及根围变为碱性的条件相结合较为困难,从而形成较少的绕根结核。可见,绕根结核的数量百分比较高指示了植物钙质根管形成时期较高的有效湿度,而钙质根套的数量百分比较高则指示了植物钙质根管形成时期较低的有效湿度。
5 结论通过形态学对阿拉善沙漠的植物钙质根管进行了分类。植物钙质根管是陆生植物形成的次生碳酸盐结壳,在阿拉善沙漠主要存在钙质根套和绕根结核两个子类,是在植物生长和微生物活动的影响下形成的。钙质根套是由碳酸盐胶结粗质沙砾或沉积物构成的简单硬质外壳,绕根结核则是硬质外壳内部胶结有白色碳酸盐形成的双层结构或者由沙砾、沉积物填充形成的实心根状结构。
由于绕根结核的形成同时受控于含钙水溶液的淋滤和根系腐烂产生CO2及根围变为碱性的控制,使得钙质根套和绕根结核在阿拉善沙漠普遍存在伴生现象,但二者的数量百分比的高低则指示了有效湿度的高低,绕根结核的数量百分比较高指示了植物钙质根管形成时期有效湿度较高,而钙质根套的数量百分比较高则指示了植物钙质根管形成时期有效湿度较低。
致谢: 感谢审稿专家对本文提出了宝贵的修改意见,谨致谢忱!| [1] | Wright V P, Platt N H, Marriott S B, et al. A classification of rhizogenic (root-formed) calcretes, with examples from the Upper Jurassic-Lower Cretaceous of Spain and Upper Cretaceous of southern France-reply[J]. Sedimentary Geology, 1997, 110(3/4): 305–307. |
| [2] | Alonso-Zarza A M, Genise J F, Cabrera M C, et al. Megarhizoliths in Pleistocene aeolian deposits from Gran Canaria (Spain):ichnological and palaeoenvironmental significance[J]. Palaeogeography, Palaeoclimatology, Palaeoecology, 2008, 265(1/2): 39–51. |
| [3] | Jaillard B, Guyon A, Maurin A F. Structure and composition of calcified roots, and their identification in calcareous soils[J]. Geoderma, 1991, 50(3): 197–210. DOI: 10.1016/0016-7061(91)90034-Q |
| [4] | Cramer M D, Hawkins H J. A physiological mechanism for the formation of root casts[J]. Palaeogeography, Palaeoclimatology, Palaeoecology, 2009, 274(3/4): 125–133. |
| [5] | Liutkus C M. Using petrography and geochemistry to determine the origin and formation mechanism of calcitic plant molds; rhizolith or tufa?[J]. Journal of Sedimentary Research, 2009, 79(12): 906–917. DOI: 10.2110/jsr.2009.093 |
| [6] | Hendry D A. Silica and calcium carbonate replacement of plant roots in tropical dune sands, SE India[J]. Geological Society, London, Special Publications, 1987, 35(1): 309–319. DOI: 10.1144/GSL.SP.1987.035.01.21 |
| [7] | Klappa C F. Rhizoliths in terrestrial carbonates:classification, recognition, genesis and significance[J]. Sedimentology, 1980, 27(6): 613–629. DOI: 10.1111/sed.1980.27.issue-6 |
| [8] | Barta G. Secondary carbonates in loess-paleosoil sequences:a general review[J]. Central European Journal of Geosciences, 2011, 3(2): 129–146. |
| [9] | Barta G. Paleoenvironmental reconstruction based on the morphology and distribution of secondary carbonates of the loess-paleosol sequence at Süttö, Hungary[J]. Quaternary International, 2014, 319: 64–75. DOI: 10.1016/j.quaint.2013.08.019 |
| [10] | Gocke M, Pustovoytov K, Kühn P, et al. Carbonate rhizoliths in loess and their implications for paleoenvironmental reconstruction revealed by isotopic composition:δ13C, 14C[J]. Chemical Geology, 2011, 283(3/4): 251–260. |
| [11] | Li Zhuolun, Wang Nai'ang, Cheng Hongyi, et al. Formation and environmental significance of late Quaternary calcareous root tubes in the deserts of the Alashan Plateau, northwest China[J]. Quaternary International, 2015, 372: 167–174. DOI: 10.1016/j.quaint.2014.11.021 |
| [12] | Gocke M, Kuzyakov Y, Wiesenberg G L B. Rhizoliths in loess-evidence for post-sedimentary incorporation of root-derived organic matter in terrestrial sediments as assessed from molecular proxies[J]. Organic Geochemistry, 2010, 41(11): 1198–1206. DOI: 10.1016/j.orggeochem.2010.08.001 |
| [13] | Gallant C E, Candy I, Van Den Bogaard P, et al. Stable isotopic evidence for Middle Pleistocene environmental change from a loess-paleosol sequence:Kärlich, Germany[J]. Boreas, 2014, 43(4): 818–833. DOI: 10.1111/bor.12065 |
| [14] | 杨小平. 近3万年来巴丹吉林沙漠的景观发育与雨量变化[J]. 科学通报, 2000, 45 (4): 428–434. [ Yang Xiaoping. Landscape evolution and precipitation changes in the Badain Jaran Desert during the last 30000 years[J]. Chinese Science Bulletin, 2000, 45(4): 428–434. ] |
| [15] | 陈建生, 赵霞, 汪集旸, 等. 巴丹吉林沙漠湖泊钙华与根状结核的发现对研究湖泊水补给的意义[J]. 中国岩溶, 2004, 23 (4): 277–282. [ Chen Jiansheng, Zhao Xia, Wang Jiyang, et al. Meaning of the discovery of lacustrine tufa and root-shaped nodule in Badain Jaran Desert for the study on lake recharge[J]. Carsologica Sinica, 2004, 23(4): 277–282. ] |
| [16] | 高尚玉, 陈渭南, 靳鹤龄, 等. 全新世中国季风区西北缘沙漠演化初步研究[J]. 中国科学(B辑), 1993, 23 (2): 202–208. [ Gao Shangyu, Chen Weinan, Jin Heling, et al. Preliminary study on Holocene sand desert evolution in the northwestern fringe of China's monsoon region[J]. Science in China (Series B), 1993, 23(2): 202–208. ] |
| [17] | 闫满存, 王光谦, 李保生, 等. 巴丹吉林沙漠高大沙山的形成发育研究[J]. 地理学报, 2001, 56 (1): 83–91. [ Yan Mancun, Wang Guangqian, Li Baosheng, et al. Formation and growth of high megadunes in Badain Jaran Desert[J]. Acta Geographica Sinica, 2001, 56(1): 83–91. ] |
| [18] | 李卓仑, 邵孔兰, 宁凯, 等. 阿拉善高原沙漠地区植物钙质根管的矿物组成特征[J]. 中国沙漠, 2015, 35 (6): 1483–1488. [ Li Zhuolun, Shao Konglan, Ning Kai, et al. Mineral composition characteristics of calcareous root tubes in the deserts of the Alxa Plateau, NW China[J]. Journal of Desert Research, 2015, 35(6): 1483–1488. ] |
| [19] | 孙庆峰, 陈发虎, 李孝泽. 巴丹吉林沙漠第四纪研究评述与讨论[J]. 干旱区研究, 2008, 25 (2): 304–310. [ Sun Qingfeng, Chen Fahu, Li Xiaoze. Review and discussion about the progress of Quaternary research of the Badain Jaran Desert, China[J]. Arid Zone Research, 2008, 25(2): 304–310. DOI: 10.3724/SP.J.1148.2008.00304 ] |
| [20] | 朱金峰, 王乃昂, 陈红宝, 等. 基于遥感的巴丹吉林沙漠范围与面积分析[J]. 地理科学进展, 2010, 29 (9): 1087–1094. [ Zhu Jinfeng, Wang Nai'ang, Chen Hongbao, et al. Study on the boundary and the area of Badain Jaran Desert based on remote sensing imagery[J]. Progress in Geography, 2010, 29(9): 1087–1094. ] |
| [21] | Yang Xiaoping, Ma Nina, Dong Jufeng, et al. Recharge to the inter-dune lakes and Holocene climatic changes in the Badain Jaran Desert, western China[J]. Quaternary Research, 2010, 73(1): 10–19. DOI: 10.1016/j.yqres.2009.10.009 |
| [22] | Yang Xiaoping, Scuderi L, Paillou P, et al. Quaternary environmental changes in the drylands of China-A critical review[J]. Quaternary Science Reviews, 2011, 30(23/24): 3219–3233. |
| [23] | 朱震达, 吴正, 刘恕, 等. 中国沙漠概论[M]. 北京: 科学出版社, 1980: 68-76. [ Zhu Zhenda, Wu Zheng, Liu Shu, et al. Introduction to the Desert in China[M]. Beijing: Science Press, 1980: 68-76. ] |
| [24] | Li Zhuolun, Wang Nai'ang, Li Ruolan, et al. Indication of millennial-scale moisture changes by the temporal distribution of Holocene calcareous root tubes in the deserts of the Alashan Plateau, northwest China[J]. Palaeogeography, Palaeoclimatology, Palaeoecology, 2015, 440: 496–505. DOI: 10.1016/j.palaeo.2015.09.023 |
| [25] | Hong Wang, Ambrose S H, Fouke B W. Evidence of long-term seasonal climate forcing in rhizolith isotopes during the last glaciation[J]. Geophysical Research Letters, 2004, 31(13): L13203. |
| [26] | Gocke M, Peth S, Wiesenberg G L B. Lateral and depth variation of loess organic matter overprint related to rhizoliths-revealed by lipid molecular proxies and X-ray tomography[J]. Catena, 2014, 112: 72–85. DOI: 10.1016/j.catena.2012.11.011 |
| [27] | Liutkus C M, Wright J D, Ashley G M, et al. Paleoenvironmental interpretation of lake-margin deposits using δ13C and δ18O results from early Pleistocene carbonate rhizoliths, Olduvai Gorge, Tanzania[J]. Geology, 2005, 33(5): 377–380. DOI: 10.1130/G21132.1 |
| [28] | Calvet F, Pomar L, Esteban M. Las rizocreciones del Pleistoceno de Mallorca[J]. Instituto de Investigaciones Geológicas de la Universidad de Barcelona, 1975, 30: 35–60. |
| [29] | Ficken K J, Li B, Swain D L, et al. An n-alkane proxy for the sedimentary input of submerged/floating freshwater aquatic macrophytes[J]. Organic Geochemistry, 2000, 31(7/8): 745–749. |
| [30] | Robinson N, Cranwell P A, Finlay B J, et al. Lipids of aquatic organisms as potential contributors to lacustrine sediments[J]. Organic Geochemistry, 1984, 6: 143–152. DOI: 10.1016/0146-6380(84)90035-4 |
| [31] | Yang Xiaoping, Scuderi L A. Hydrological and climatic changes in deserts of China since the late Pleistocene[J]. Quaternary Research, 2010, 73(1): 1–9. DOI: 10.1016/j.yqres.2009.10.011 |
| [32] | 李若兰, 李卓仑, 宁凯, 等. 腾格里沙漠植物钙质根管Sr/Ca比值揭示的全新世千年尺度有效湿度变化[J]. 第四纪研究, 2016, 36 (2): 379–387. [ Li Ruolan, Li Zhuolun, Ning Kai, et al. Holocene millennial-scale effective moisture changes revealed by Sr/Ca ratios from calcareous root tubes in the Tengger Desert[J]. Quaternary Sciences, 2016, 36(2): 379–387. ] |
| [33] | 王乃昂, 李卓仑, 程弘毅, 等. 阿拉善高原晚第四纪高湖面与大湖期的再探讨[J]. 科学通报, 2011, 56 (17): 1367–1377. [ Wang Nai'ang, Li Zhuolun, Cheng Hongyi, et al. High lake levels on Alxa Plateau during the Late Quaternary[J]. Chinese Science Bulletin, 2011, 56(17): 1367–1377. ] |
| [34] | Long Hao, Lai Zhongping, Wang Nai'ang, et al. Holocene climate variations from Zhuyeze terminal lake records in East Asian Monsoon margin in arid northern China[J]. Quaternary Research, 2010, 74(1): 46–56. DOI: 10.1016/j.yqres.2010.03.009 |
| [35] | Chen Fahu, Li Guoqiang, Zhao Hui, et al. Landscape evolution of the Ulan Buh Desert in northern China during the late Quaternary[J]. Quaternary Research, 2014, 81(3): 476–487. DOI: 10.1016/j.yqres.2013.08.005 |
 2017, Vol. 35
2017, Vol. 35


