纳米与生物技术的快速发展为身体域的分子通信研究提供了强有力的基础.笔者总结了细菌分子通信领域的最新研究进展,介绍了细菌接合传输和细菌分泌传输2种机制以及相关的实验和仿真结果.基于细菌分子通信,讨论了身体域纳米网络相关的中继组网技术,阐述了纳米生物技术的发展趋势和所面临的挑战.
The rapid development of nano and biology technologies pave the way to the research of molecular communication within the body area. The article surveys the recent advents of the bacteria-based molecular communication, in which the bacteria conjugation and bacteria paracrine transmission mechanisms are elaborated, and the related experiment and simulation are presented. Accordingly, the body-area nano-network based on bacteria molecular communication is discussed, and the corresponding relay networking technology is presented. Finally, the future open issues and challenges are discussed.
面对即将到来的信息化爆炸时代以及纳米技术的快速发展,纳米物联网成为研究关注的焦点[1],其中尤以生物医学领域的体域纳米网最具发展应用前景[2, 3]. 学术界将可执行简单感知、数据存储以及驱动的纳米尺度元件定义为纳米机器,它的尺寸一般在1~100nm之间,这就导致个体纳米机器仅能在有限空间内执行相对简单的工作. 然而,若要在相当于大尺度异构通信网络的人体内执行复杂的监测、治疗等任务,则需纳米机器间互连以形成身体域纳米网络以提高整体的执行能力. 因此,身体域纳米网络中纳米机器间的通信以及如何智能组网一直是业界研究难点和重点问题.
人体内有大量天然的纳米机器(如细胞),它们可以通过分子的传递来实现信息的交换,从而形成稳定高效的生物纳米网络. 这种天然的纳米机器为人类开发新型纳米机器以及身体域纳米网络提供了参考模型,也为构造复杂的身体域纳米网络提供了天然的基准组件. 业界普遍认为基于生物启发的分子通信是实现身体域纳米网络的最为可行的技术方案之一[4].
目前,基于分子通信的身体域纳米网络研究仍处于起步阶段,已有研究成果主要集中于物理层的信道传输机制以及调制编码技术,对于纳米网路的组网理论研究还较少. 然而,对于身体域纳米网络的相关应用,如对病情的早期诊断和微创治疗、智能给药[5]以及对免疫系统的支持[6]等,均需要基于分子通信的身体域纳米网络的组网理论予以支持. 因此,身体域纳米组网理论和相关技术亟需突破,以促进智能健康发展,满足人们对智慧医疗的需求.
为了探索身体域纳米网络的特征,揭示与传统无线通信的差异及关键因素的影响,笔者总结了细菌分子通信及对应的身体域纳米组网的最新研究进展,探讨了未来技术发展及可能的瓶颈,以促进身体域纳米网络理论和技术的成熟.
1 基于细菌的分子通信分子通信是一种通过分子的交换来实现收发器间信息传递的通信技术. 根据信息分子的传输方式不同,可将分子通信分为被动传输通信与主动传输通信两种类型;而根据信息分子传输距离的不同,可将分子通信分为短距(nm~μm)通信、中距(μm~mm)、长距(mm~m)通信[7]. 其中,自由扩散是一种最为普遍的短距被动传输方式,其本质上是流体介质内信息分子通过布朗运动而向任意方向进行传播的广播通信方式. 由于纯粹的布朗运动所承载的信息传递速度非常慢,研究人员希望找到一种主动传输机制,以加速信息的传递并扩展通信的范围. 细菌马达就是这样一种主动传输方式,其机理是通过细菌的趋化性,诱导细菌进行定向运动,并通过细菌的接合过程实现遗传物质(如质粒)的交换. 由于细菌的自主运动机制和细菌菌群的协作感知,基于细菌分子通信的身体域纳米网络已成为目前业界关注的热点和焦点,具有广阔的发展前景.
通过细菌来进行纳米网络通信的概念最早由Gregori等[8]提出,它通过DNA的腺嘌呤A、胸腺嘧啶T、胞嘧啶C和鸟嘌呤G来进行四进制编码,并将编码完成的信息DNA链注入到细菌的质粒中,通过细菌的承载来实现通信. 更进一步,Cobo等[9]提出了基于细菌的纳米网络架构,详细论述了身体域纳米网络的通信步骤,包括编码、封装、传播、解封装、中继和解码;分析和评估了多个网络性能,包括通信范围、端到端时延以及网络容量.
基于Cobo等[9]的研究成果,Gao等[10]提出了关于细菌引诱剂调度的概念,从而优化系统的端到端时延. Lio等[11]提出了纳米网络通信过程中细菌间接合以进行编码DNA信息交换的概念,并将其运用到细菌多跳传输中,有效地提高了系统的时延性能和通信范围. 然而,由于细菌接合时所构建的物理连接过于脆弱,在外界机械力和化学物质的压力下极易断裂,从而造成信息的不完整传输,最终在接收器端,信息无法进行解码,导致系统整体通信性能的降低. 针对这一现象,Petrov等[12]提出了一种前向和反向结合的信息编码方案,即将信息分段,并分别从正向和反向进行编码,可有效提高系统的信息成功解码率. 然而,当多个细菌同时与同一接收器或细菌相接合时,会产生干扰现象,Islam等[13]利用一种叫最大加权双向匹配的图论方法分析了接收侧冲突模型的最大可获得吞吐量.
总结近年来有关细菌纳米网络的文献,细菌的传输机制主要有两种,其一为上述的细菌马达传输机制;其二为细菌分泌传输机制[14],它本质上也是一种基于自由扩散传输机制的广播通信方式,主要依靠细菌间的协作感知来进行信息的编码、解码工作,是自由扩散机制的一种较为可行的实施方案. 为了进一步描述基于细菌的传输机制,下面将对细菌的特性进行详细阐述.
1.1 细菌特性细菌最重要的特性是在流体媒介中可以自主运动,这一特性使得通过细菌进行纳米网络的分子通信比单纯的扩散方式更具吸引力. 具体来说,细菌的运动能力源于鞭毛的快速旋转,当鞭毛进行逆时针旋转时,细菌的所有鞭毛会扭合在一起形成一个束,束的高速旋转推动细菌做直线运动,即细菌的游泳运动;而当鞭毛进行顺时针旋转时,细菌的鞭毛会分散开来,导致细菌在原地进行翻滚运动,从而改变其运动的方向. 根据细菌的记忆机制,细菌可比较当前环境的化学引诱剂浓度等级来调整运动的方向. 在没有化学引诱剂浓度差异变化的情况下,细菌的运动是随机的,即采取直线运动和翻滚以改变运动方向相接合的运动方式,然而当细菌感知到周围的化学引诱剂浓度有差异梯度时,翻滚频率会相应上升,从而朝着化学引诱剂浓度升高的方向运动,从数学的角度来看,这是一个修正的皮尔 森- 瑞利随机游走过程[15].
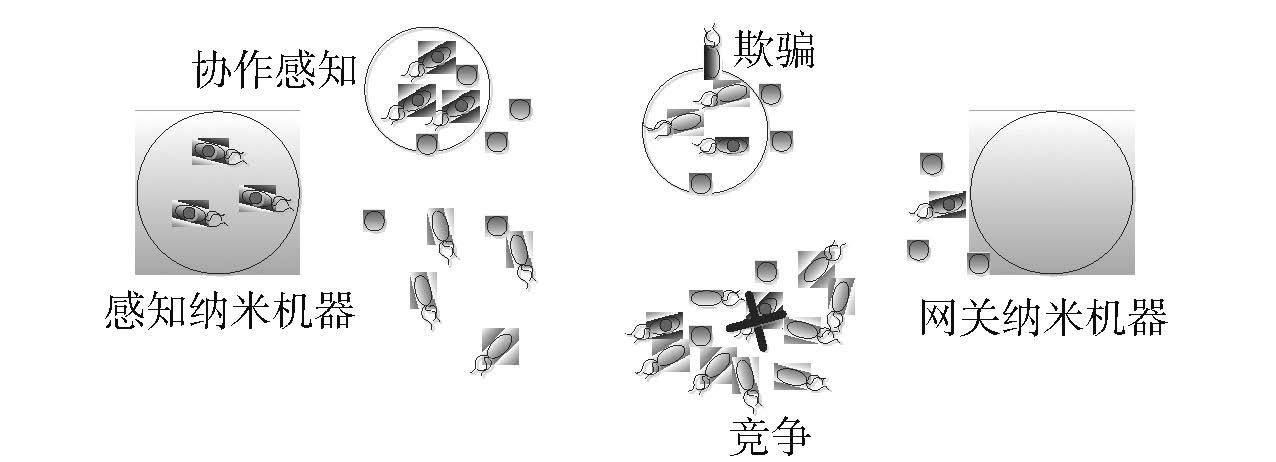
与传统的通信系统不同,由于细菌本身是活体生物,因此基于细菌的分子通信(后面简称细菌分子通信)必须要考虑细菌本身的社会行为属性(如协作、竞争等)[16],这些行为属性既有可能有益于通信的可靠性(协作行为),同时也有可能成为确保通信可靠性的障碍(非协作行为),如图 1所示.
协作感知是细菌最为重要的一种协作社会行为属性,较为典型的例子是细菌具有趋化性. 当单个细菌检测到周围的营养物质浓度较高时,它会向外部空间排放类食物分子以吸引其他细菌朝它游动;反之,若周围的营养物质浓度较低时,它会向外部空间排放排斥分子以驱赶其他细菌远离自己的方位,从而表现为细菌的一致趋化性. 另一个例子是细菌的群体感知,它为细菌间协作完成复杂任务以及探查细菌本身的种群浓度提供了基础.
其他的协作社会行为还包括:①协作分层组织,即通过形成菌落来集体抵抗外界的抗体以及环境恶化;②觅食,即通过形成较为复杂结构的群落以最大化细菌群落的摄食能力;③保护,即在营养匮乏的情况下限制细菌种群的繁殖以确保每个细菌的营养供给;④记忆与学习,即细菌群落可根据以往的经验对现有情况作出最优判断,如在抗生素的压力下,细菌群落会通过改变细菌的集群模式来稀释抗生素的影响.
细菌间的协作行为有益于整体细菌群落的存活以及繁殖,然而仍然存在部分细菌不愿参与协作行为而想窃取群体协作行为所带来的增益,典型的非协作社会行为包括欺骗与竞争. 欺骗表现为菌群协作完成某项工作(如生物膜的形成)时,部分细菌选择自私的行为以获得相应的个体收益. 然而,这种非协作的行为会对菌群执行的工作造成恶劣影响. 以生物膜的建立为例,如果执行非协作行为的细菌多于执行协作行为的细菌,将导致整体生物膜结构的全面崩溃. 另外,细菌的学习能力对其执行欺骗行为有一定的促进作用. 例如,如果某个细菌感知到周围环境中细菌的整体密度相对较高,则该细菌有可能选择非协作的行为,因为它认为该改变不会被菌群检测到.
竞争表现为资源(如营养物质)受限情况下,细菌间对资源的不公平占用. 非协作的细菌可以获得更多的资源并相应降低其他个体的资源获取,这种自私的资源占用将降低细菌菌群整体的资源利用. 当营养物质严重不足时,为了自身的存活,细菌间的竞争尤为猛烈. 例如,大肠杆菌会产生并分泌一种叫作大肠杆菌素的毒素,它可以抑制其他细菌的生长速率,甚至杀死其中大肠杆菌素敏感的菌株.
1.2 细菌分子通信的传输机制细菌分子通信方式大体可以划分为细菌马达传输机制和细菌分泌传输机制.
1.2.1 细菌马达传输机制细菌马达传输机制主要有3种表现形式. 第1种称为接合通信[17],也是最为基础的一种细菌分子通信方式,它通过在细菌间形成物理连接来进行质粒的交换;第2种称为纳米管道通信[18],这种纳米管道会在固体表面上形成,不同于接合通信,细菌可通过纳米管道同时进行质粒或者离子和蛋白质的交换;第3种称为噬菌体通信[19],可简述为通过噬菌体携带有用信息,并依靠噬菌体依附细菌的特性,利用细菌进行信息的承载和传输,该方法可提高信息的可到达率,并扩大通信的范围,目前有两种方案,一种为细菌静止而仅排放噬菌体,另一种为细菌移动而将噬菌体排放在一个固定的范围内.
然而,由于纳米管道通信所需要的通信环境相对苛刻,噬菌体通信的扩散与接合过程较复杂,因此,这里主要讨论基于细菌接合方式的细菌马达传输机制. 具体以大肠杆菌为例,当两个细菌距离非常近时,一个叫作配对形成的多蛋白复合物会引发供体细菌产生细胞外枝,即纤毛,并与受体细菌相连. 在两细菌通过纤毛相连之后,另一个多蛋白复合物DNA松弛小体会在转移起点区域进行切割,在质粒中切割下来的相应单链DNA被送入受体细菌后,两细菌间的物理连接会被中断,这时接合过程结束,DNA信息在两细菌间得到传递.
利用细菌接合的传输机制,可以通过细菌承载编码的DNA数据来实现纳米网络的通信. 这里主要涉及3种性质,其一是细菌通过质粒存储信息;其二是细菌可通过转化过程捕获媒介中游离的编码DNA链[20];其三是细菌的趋化性运动,即通过化学诱导剂的诱导可使细菌定向地传输到接收纳米机器处. 身体域纳米网络研究中最常用的一个细菌品种是大肠杆菌,因为人类已经知道它的完整基因组序列[21],信息编码更容易掌握,且它可对一些特定的诱导剂产生趋化性运动[22]. 下面简要介绍基于细菌接合传输机制的单跳通信步骤[9],如图 2所示,由编码、封装、传播、解封装、解码等步骤组成.
1) 编码
感知纳米机器收集外界信息,并将其编码在质粒之中,即一个环形的双链DNA,它可以通过细菌的转化过程和接合过程来进行自我复制和自我转移. 这个质粒由3部分构成,分别为转移区、路由区和信息区. 其中,转移区是典型的质粒中本身就存在的区域,它包含负责质粒进行自我复制和转移的基因和结构. 路由区负责区分空白细菌(不含有用信息)和负载细菌,具体可表现为以下几点:①禁止细菌对发射器的趋化性,并表现为对接收器的趋化性;②抑制细菌的复制以降低载有相同信息的指数性增长,这种细菌复制会严重增强接收器的负载;③使能一个可编程的死亡期限,这可以用来消除游离在系统中时间较长的细菌以避免传输中的干扰和细菌的基因便车现象,并可确定信息的重传机制;④添加抵制抗生素相关的基因,以方便在网关节点处消除非法细菌,减轻干扰. 信息区包含目的接收器的网络地址和信息的有效载荷. 考虑到质粒中编码的信息DNA序列可能会被表达,并引起相关蛋白质的合成,导致信息传输的干扰,因此,需要抑制质粒中编码信息的基因表达,即将其编码为非活性DNA,但这是以降低每个碱基对的信息量为代价的.
2) 封装
信息在被编码到质粒中之后,需要转移到细菌载体中. 发射器将同时排放质粒与传输引诱剂(TA,transmission attractant),排放TA的目的是吸引周围的空白细菌聚集过来,并与这些游离的质粒相接合,在吸收这些质粒的过程中,质粒会解链为单链DNA并以这种形式整合到空白细菌的质粒中,这称为转化过程. 此时,转移DNA中的活性基因将被表达,细菌将受到接收器引诱剂(RA,reception attractant)的吸引.
3) 传播
在传播阶段,细菌受到RA的吸引,将在发射器与接收器间进行传播. 在整个传播过程中,载体细菌有可能会与其他空白细菌接合,从而增大系统的信息成功到达率以及通信的距离. 由于受到质粒活性基因的表达,细菌会在传播中执行一个固定的生存时间,以限制细菌在通信过程中的时延. 当超过一定延时后,信息将被认定为丢失,这时信道内的相关细菌将被消除并执行信息的重传.
4) 解封装
当载体细菌传输到接收器时,细菌内的信息将卸载到接收器内. 当系统中有多个节点时,每个节点的化学引诱剂均不相同,然而还是会有载体细菌与错误的接收器相接合,这时需要接收器具有对载体细菌承载信息进行判定的能力,若检测到信息的物理地址与正确的发射器不匹配,则该信息将被舍弃.
5) 解码
接收器对所接收质粒的DNA链的核苷酸序列进行排序,从而可以得到解码后信息并进行相应的反应和处理.
文献[9]中给出了一些重要的系统特性的推导以及性能分析,如传播时延、容量以及通信范围. 其中,系统时延被分解为编码、封装、传播、解封装和解码时延5部分,且传播时延在系统时延占比最大;系统容量根据信息的误码率和丢失率进行求解,而每一跳的通信范围则是根据引诱剂排放的浓度梯度进行求解. 另外,文献[9]将细菌的运动过程假设为一个线性时不变的系统,通过它的脉冲响应和引诱剂的浓度变化的卷积计算,可推导出针对不同引诱剂排放浓度下细菌具体的游动和翻滚的运动特性.
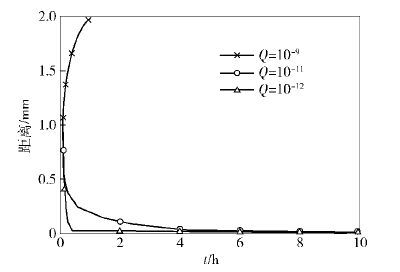
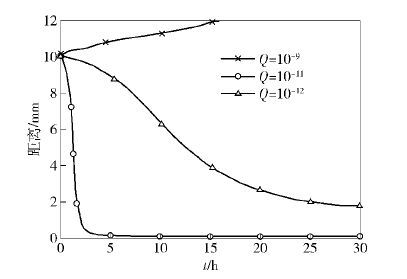
如图 3~图 5所示,不同通信距离(1mm、10mm、100mm)所需引诱剂的排放速率Q不同,越长的通信距离需要越高的排放速率;而且,当通信距离超过一定长度时,需要分阶段使用不同的引诱剂排放速率才能较好地完成通信.
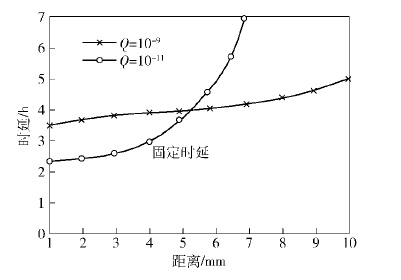
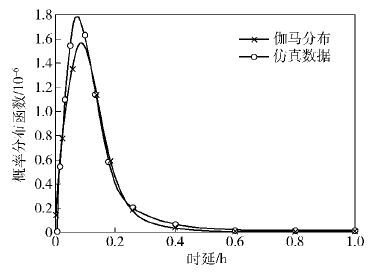
另外,如图 6所示,不同引诱剂排放速率和通信距离会引发不同的时延. 值得注意的是,相同通信距离下并不一定是排放速率高系统时延低,这说明了不同的引诱剂排放速率有其特定的最佳通信距离. 而且,如图 7所示,传播时延的概率特性可近似为伽马分布.
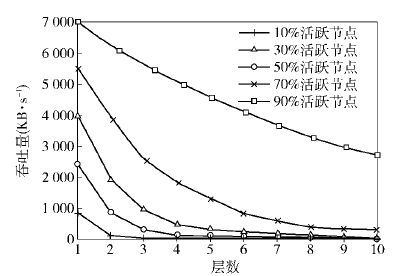
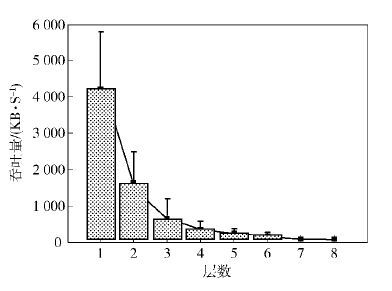
与此同时,文献[9]针对四进制编码给出了每跳容量结果,并证明了基于细菌接合通信的容量远高于其他分子通信方式. 而文献[13]对接收端多接合冲突情况下的最大可获得吞吐量进行了详细研究,并给出了最大可获得吞吐量相关性质与变化规律. 具体而言,利用图论理论,将所有节点分为n层,每层有一定的活跃节点,源端在最左边一层,目的地端在最右边一层. 如图 8所示,吞吐量随每层活跃节点比例增加提高明显,且层数增加会降低系统吞吐量,即通信的跳数或距离的增加会降低系统的吞吐量. 更进一步,如图 9所示,当不确定每一层活跃节点的先验比例时,即对活跃节点进行随机分配下,可以得到吞吐量随层数(通信跳数或距离)近似指数递降的结论.
1.2.2 细菌分泌传输机制
细菌间的分泌通信类似于自由扩散传输机制,主要应用于细菌间的协作感知. 在自体诱导剂的扩散范围内,细菌会独立感知某个参数或接收信号的浓度,并形成本地的自我认知,通过群体感知,相关参数信息将在该范围内所有细菌间进行传播,从而这些细菌将同时对这个信息达成一致的评估.
信息的形成(共识的达成)过程可分为两类:有反馈分泌和无反馈分泌. 对于有反馈分泌,若细菌感知到周围的分子浓度高于预期值,会提高其产生和分泌分子的速率,这与现实中细菌的特性是相一致的. 而对于无反馈分泌,细菌被设定仅依靠它们自己的评估来产生和分泌分子,并且相应的分泌速率将维持不变直到整个过程趋于稳定,这类信息的形成过程可通过移除细菌内负责正反馈的基因来实现. 比较两类形成过程,基于反馈的方式可以得到更快的收敛结果,然而这种方式也会增大信息误报率;相反,无反馈方式以时延为代价换取了较高的信息准确率. 由于无反馈方式更加便于仿真的控制与性能的计算,目前研究更多的是关于无反馈方式的应用.
1.3 细菌分子通信的实验与仿真平台为方便对纳米网络进行直接测试并动态测量相关的网络通信参数,如时延或噪声干扰等,利用微流体设备建立实验平台非常必要. 微流体设备广泛使用于对生物学的分析中,具有设备体积小、试剂使用量低以及实验并行处理等优点. 目前,对于身体域纳米网络的细菌分子通信,文献[23]和文献[24]先后建立了针对细菌群体感知通信的微流体设备,以此来探索细菌的群体感知反应过程.
研究人员已经提出了各种细菌仿真平台以精确描述纳米网络中细菌复杂的物理和生化过程,大体可以分为两类:一类为单细胞级仿真;另一类为群体级仿真. 针对细菌分子通信的仿真算法主要有3种,分别为Gillespie随机仿真算法(SSA,stochastic simulation slgorithm)、随机微分方程(SDE,stochastic differential equations)算法和混合多尺度算法. SSA跟踪每一个反应使得它仅能仿真小尺度的单细胞级系统,文献[25]中的NFSim就是利用SSA建立的仿真平台. 为了克服SSA的不足以加速系统的仿真速度,从而适应群体级的仿真,SDE算法应运而生,它是SSA的一种近似,可以提高仿真速度,但也会引入严重的噪声. 混合多尺度算法是前两种算法的有机结合,即对关键的噪声评估使用SSA,而其他非关键因素使用SDE算法,从而综合权衡了仿真速度和噪声性能. Wei等[26]提出了名为NBSim的仿真平台,整合了上述3种仿真算法,研究人员可以动态地进行算法的选择.
2 基于细菌分子通信的身体域纳米网络利用细菌分子通信,可以形成身体域纳米网络,它是医疗健康互联网的重要组成,对人类的健康保护、疾病诊断和治疗等有着颠覆性的改变. 身体域纳米网络的核心组件是纳米机器,它有多种类型,如感知纳米机器、中继纳米机器、网关纳米机器等[27],下面分别介绍这些组件.
1) 感知纳米机器
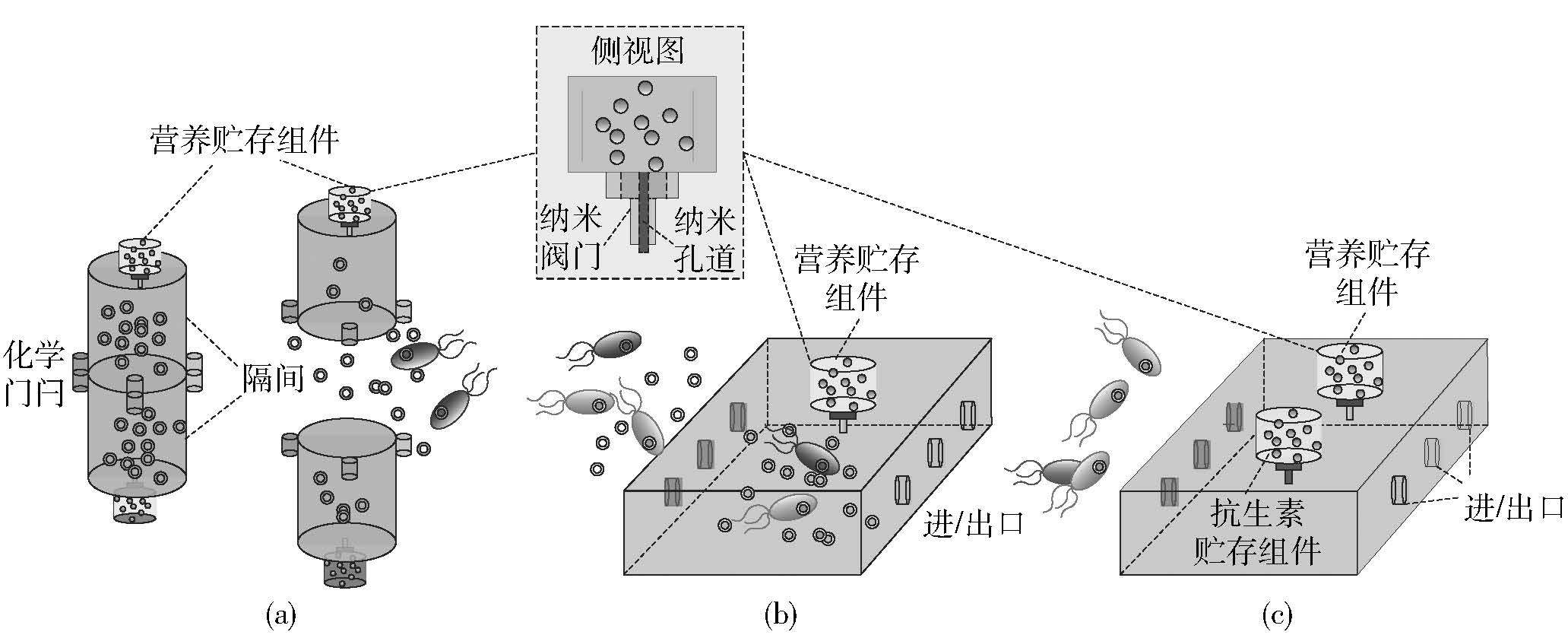
在身体域纳米网络中,可以通过感知纳米机器来感知人体内的有害物质. 为了方便起见,信息的编码过程在体外进行,如图 10(a)所示,感知纳米机器中分隔出多个线性排列的隔间来存储预先编码的信息质粒,隔间之间通过化学门闩进行连接. 当感知纳米机器检测到由癌细胞产生的特定酶时,连接各个隔间的化学门闩将打开,预先编码的质粒和营养贮存组件内的TA将同时排放到外部空间中. 考虑到这些原件都需植入到人体内,因此均需选用生物兼容的材料. 另外,对于感知纳米机器的化学门闩有两点要求:其一是在没有感知到有害物质时,化学门闩能够紧密地锁住所有的隔间,以保证编码质粒中信息的纯净;其二是在感知到有害物质后,化学门闩能够及时打开各个隔间释放其中质粒,以实现相关信息的传递,这要求化学门闩对特定的有害物质(癌细胞所产生的酶)较为敏感. 与此同时,为了使细菌能够最大程度地接合质粒,即在化学门闩打开后尽可能充分地将质粒排放到外部空间,需要为感知纳米机器配置纳米管道和动力设备,这是未来的改进方向之一.
2) 中继纳米机器
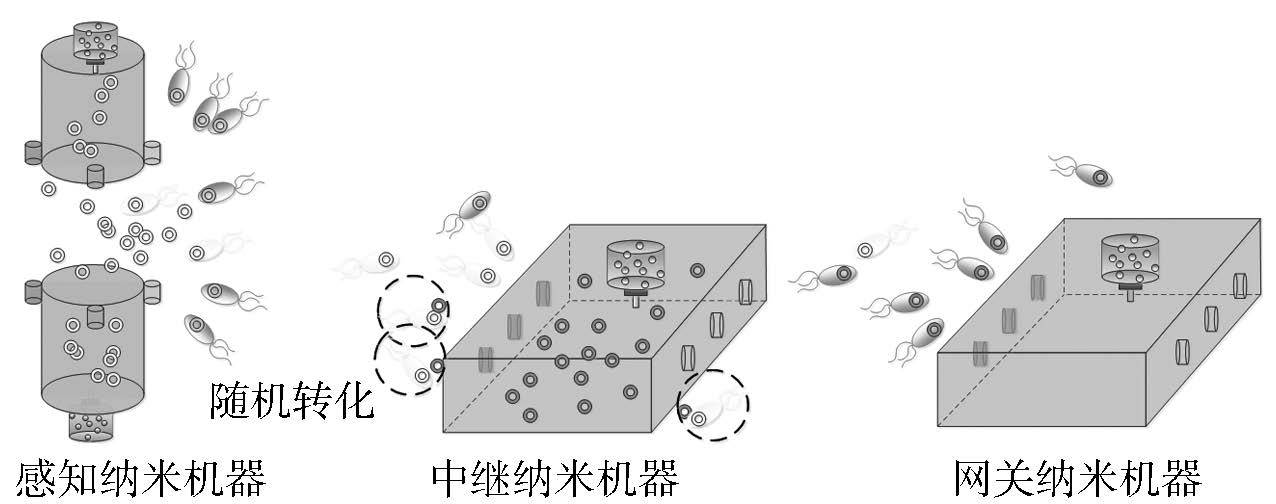
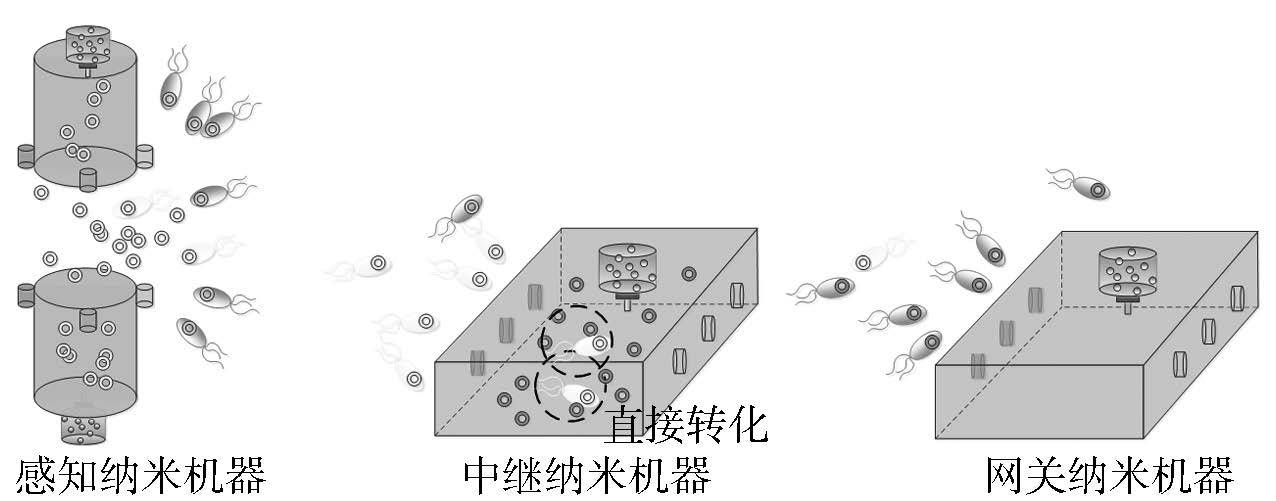
形象地说,中继纳米机器是细菌传输过程中的灯塔和加油站,其所存储的营养物质在为细菌指明前进方向的同时,还可以提高细菌的存活以及繁殖数量,从而确保信息被正确地传递到网关纳米机器处. 如图 10(b)所示,中继纳米机器具有多个纳米进出口,这里有两种设定:①营养贮存组件仅向外部环境排放RA以吸引载体细菌,中继纳米机器仅出口打开以排放其中的转移质粒,使得细菌在中继纳米机器附近与质粒进行随机接合;②营养贮存组件同时向中继纳米机器内外释放RA,且纳米机器进出口的门闩将会周期性打开,细菌可进入中继纳米机器内部与其中的质粒进行直接接合,当一个周期时间结束后,中继纳米机器内的细菌将会被排出,新的细菌将进入到纳米机器内部以进行下一轮的接合. 因此,通过中继纳米机器的表述,可以得到两种通信的中继方式,分别为随机接合方式和直接接合方式.
3) 网关纳米机器
在身体域纳米网络中,网关纳米机器用来接收细菌,将所得到的信息无线传输给体外设备. 如图 10(c)所示,与前两种纳米机器相同,网关纳米机器也配有营养贮存组件,从而排放相应TA以吸引载体细菌. 不同的是,网关纳米机器具有一个特殊的组件,即抗生素贮存组件,可将非法细菌(不携带相关信息的细菌)消除,以减轻噪声的干扰. 此外,抗生素的引用还有助于防止细菌分子通信的遗传搭车现象,即基因变化频率加快并在细菌间进行传递的现象. 在基于细菌分子通信的身体域纳米网络中,有用信息与细菌本身的基因信息一起进行传输,这会导致遗传搭车现象的产生. 因此,抗生素有助于控制细菌的行为,以避免由遗传搭车所导致的不理想行为.
2.1 基于接合机制的多跳通信方式正如前文所述,通过接合通信机制,细菌间可生成一个物理连接来进行质粒交换,这为基于细菌的多跳分子通信提供了基础. 下面将介绍两种基于细菌接合的多跳分子通信方法:多跳随机接合和多跳直接接合[27].
随机接合的多跳分子通信依赖于载体细菌与中继纳米机器排放到外部空间的质粒的随机接合. 当载体细菌与游离质粒相遇后,载体细菌有一定几率会吸收该质粒. 这时,通过细菌的转化过程,可改变细菌的RA信息,以改变其所吸引的引诱物,从而使其可进行下一跳的信息传递. 因此,通过对细菌质粒中RA信息的改变,可以最终将信息传递给网关纳米机器并进行相应分析,进而将信息传递给体外接收机. 如图 11所示,在感知纳米机器所吸引的空白细菌中,将有一部分吸收了感知纳米机器排放质粒的细菌成为载体细菌. 载体细菌由于受到中继纳米机器RA的吸引,将会在中继纳米机器周围随机地与其排放的质粒相遇、接合,进而改变细菌质粒中的RA信息,并向下一跳节点进行传递. 图 11中简化为2跳网络,即仅有一个中继节点,因此,细菌信息的传输在中继纳米机器处完成接力,通过RA信息的改变实现下一跳节点的定位和信息的多跳传输.
直接接合的多跳方式相对要更加保守,如图 12所示,这种方式中细菌必须直接游入到中继纳米机器中,才能和其中的质粒完成转化过程. 为了保证细菌的转化率,以确保信息在多跳节点间的正确传输,中继纳米机器只有在检测到特定浓度的转化细菌时,才会将体内的细菌全部排放到外部空间中. 需要注意的是,虽然中继纳米机器体内空间相对狭小,可以加速细菌与质粒的转化过程,但是也会引入较高的复杂度以实现转化细菌浓度的精确检测,以及纳米机器门闩的准确开关.
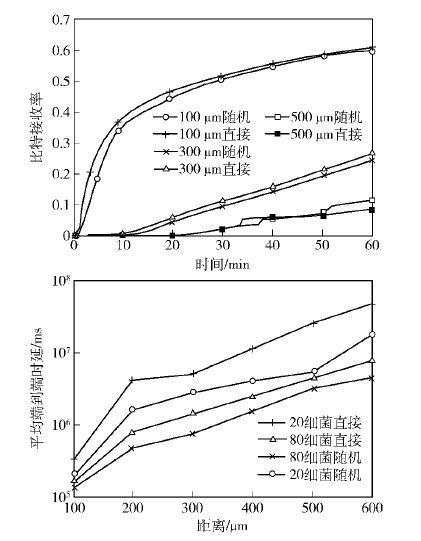
如果不考虑复杂度影响,两种方法的性能比较如图 13所示. 随机接合方式可以获得较低的时延,但是相应的比特接收率也较低;与此相反,直接接合方式在以时延为代价的情况下,可以获得较高的比特接收率. 因此,为了获得满意的通信效果,针对不同的通信环境,需要对这两种方法的使用进行权衡. 当通信环境中的营养物质充足时,细菌可以保证相对的存活量来进行信息的传输,此时比特到达率已不是考量重点,因此,为了获得最小时延收益,随机接合是相对理想的多跳方式. 然而,当通信环境中的营养物质短缺时,细菌的存活问题是首要考量因素,直接接合方式可在中继纳米机器体内为细菌提供相对充足的营养以进行细菌的转化过程,从而得到较高的比特到达率. 此外,可以考虑这两种方式的折衷使用,即通过检测环境中营养的浓度指标以决定中继纳米机器释放其中细菌的间隔时间.
由于中继纳米机器没有检测信息目的地网络地址的能力,且没有相应的转发路由表,因此随机接合和直接接合的多跳方式均只适用于简单的,甚至是2跳的身体域纳米网络. 若中继纳米机器具有这两项能力,则可根据信息解析后的目的地网络地址和本地路由表,在全网内为其选择最优的多跳路径.具体步骤:在为每个节点分配RA时,中继纳米机器选用以高速率排放的引诱剂,以获得较大范围的细菌吸引力;而网关节点的引诱剂则无需太高的排放速率,即不需太大的影响范围. 由于TA用来吸引空白细菌,因此节点间可选用相同的TA,并且TA的排放速率不需太高. 如图 14所示,每个中继纳米机器(图中由圆形表示)有其所服务的范围,在该范围内的感知纳米机器(图中由正方形表示)可配置相同的RA,并且这些感知纳米机器无需维持路由表. 与此相对,这些中继纳米机器均需维持复杂的路由表,以此来为服务区域的感知纳米机器选定下一跳中继节点所需的RA,并通过细菌的转化过程,改变细菌的RA信息,以使其可沿选好的路径传递,最终传递到网关纳米机器(图 14中用三角形表示)处. 在此期间,服务区域无交叠的中继纳米机器可使用相同的RA以提高其复用率. 需要说明的是,目前研究尚没有给出中继纳米机器内路由表实现的具体方法,因此,适合细菌分子通信的路由设计有待进一步研究和实现.
2.2 基于分泌机制的多跳通信方式不同于基于细菌接合机制的多跳通信,基于分泌机制的分子通信依靠分子的交换来实现信息的传递,因此,相应的多跳通信需要多种类别的分子共同协作完成,在整个网络中形成了两种模式的通信,即节点内部通信及节点间通信. 节点内部通信依靠细菌间的协作感知,正如上面所提到的,细菌间通过分泌分子(类型1)来实现信息共享,而节点间则使用与之不同的分子(类型2)来进行信息的传递[14],如图 15所示.
节点内部的协作感知主要依靠细菌的群体感知. 在每个节点内,细菌会独立感知某个参数或接收信号的浓度,并形成本地的自我认知,通过群体感知,相关参数的信息将在节点内所有细菌间进行传播,从而节点内的所有细菌将同时对这个信息达成一致的评估.
节点内部信息生成过程的结束将引发节点间的通信,这可通过触发相关基因以产生和分泌类型2分子的细菌工程化来实现. 这里,每个节点都可看作是独立的实体,可以感知不同种类的分子,处理信息并释放自身的分子. 为了使每个节点可以以任意的速率排放分子,每个节点应该产生一个刺激来唤醒相应数量的细菌,这样,由于每个细菌的分子排放速率是相同且恒定的,可以获得准确且多变的分子排放速率. 假设每个节点的细菌有两种类型2的分子,分别为类型 2- A和类型 2- B. 一个节点可以接收编码在类型 2- A上的信号,并传输信号通过类型 2- B. 多径路径上的节点位置必须保证一个节点排放的分子类型与下一个节点所能接收的分子类型是相匹配的.
由于细菌的分子排放是二进制的,即按固定速率排放或因休眠而不排放分子,对于有n个细菌的节点来说,节点内分子的浓度可以有n+1个等级,即可以具有lb(n+1)bit的信息量. 当前节点将根据前一跳所传信息的浓度来产生一定等级的刺激,以唤醒相应数量的细菌,从而产生类型2的分子并传递给下一跳节点. 由于细菌信息接收的概率特性,信息在多跳传输的每一跳都有可能产生错误信息. 这里有两个因素会导致信息的误传,其一是节点内细菌的数量,其二是每个细菌受体的数量. 节点内细菌的数量决定了该节点可检测的输入范围大小,一个含有n个细菌的节点可以接收并解码n+1个等级的信息. 另一方面,每个细菌受体的数量决定其感知相关参数浓度的准确性.
3 身体域纳米网络的互联身体域纳米网络的互联包括两方面,一是身体域纳米网络间的互联;二是基于生物启发的身体域纳米网络与传统的电磁波无线网络的互联[2]. 在这里,生物兼容性是需要保证的第一要素,而传统纳米传感器的电磁波发射设备不能满足要求.
对于人体来说,可以视为有多个身体域纳米网络. 这些不同身体域纳米网络间的互联,由于身体内位置的不同,每个身体域纳米网络基于不同的传输机制,它们之间的互联需要进行传输机制的转换,所以可以制造人工细胞,内部嵌入特定的生物基因电路,当一种传输机制的信息被人工细胞的受体所检测时,基于其内生物基因电路的表达,可以产生另一种传输机制内相同的信息进行传输,从而完成不同身体域纳米网络间的互联.
相比于基于生物启发的身体域纳米网络间的互联,身体域纳米网络与体外的物联网互联即是分子通信传输机制与电磁波传输机制的转换. 这时,在人工细胞内需要嵌入特定的电磁波纳米发射器,人工细胞外的受体会将接收到的信息由生化域转换为电磁域,并传递给体内的电磁波纳米发射器,从而通过无线电磁波与体外的电磁波接收设备取得连接.
取得互联作用的网关节点均为嵌入特定组件的人造细胞,因此可以满足体域网互联所需要的生物兼容性要求. 然而需要注意的是,不同传输机制间信息转换的精度问题,以及电磁波纳米发射器的功率问题. 发射功率过小会导致信息无法被体外设备所接收,而发射功率过大则有可能损害人体的健康,这些都是未来亟需解决的问题.
身体域纳米网络与传统通信网络的性能指标有显著差异,身体域纳米网络的理论和技术挑战及对应的可能解决方案如下[28].
1) 传输延时大限制信息的重传、节点的载波监听以及同步. 因此,身体域纳米网络应着重保证信息传输的准确性以减少重传,同时采用以分子类别为划分的多址接入技术替代传统无线局域网采用的载波监 听- 冲突避免或者蜂窝移动通信系统采用的多址接入方式. 另外,细菌的群体感知行为是分子通信特有的特征,也是身体域纳米网络同步的可行解决方案.
2) 分子通信经历的信道快速衰减限制单跳的传输距离. 因此,对于身体域纳米网络来说,需要通过协作传输或者多跳中继传输来扩展传输距离.
3) 和传统无线网络不同,身体域纳米网络的信道易畸变,这会产生严重的符号间干扰. 不同于传统的均衡和多用户检测技术,身体域纳米网络可以利用接收机吸收到达的分子和使用生存时间机制来抑制符号间干扰.
4) 纳米机器非常有限的能力不允许采用无线网络类似的复杂调制编码技术以及相关协议,目前身体域纳米网络倾向于采用重复的纠错编码以及脉冲调制等易实现的技术.
5) 纳米机器节点的移动粒度非常小,从微观来看其复杂的移动特性急需先进的动态组网机制,确保身体域纳米网络能够自适应动态智能组网.
6) 和传统无线网络不同,身体域纳米网络的纳米机器节点的密集分布使得单独寻址不再高效,以节点类别寻址是一种更好的解决方案.
4 结束语基于生物启发的分子通信技术使得身体域纳米网络的组建成为可能,相比于自由扩散传输机制,细菌的自由移动以及群体感知特性使得基于细菌的分子通信传输机制具有更加广阔的研究和应用前景. 笔者针对细菌分子通信,就细菌特性、相关传输机制,以及基于多跳技术的身体域纳米网络的基本原理、系统结构组成、关键技术和未来挑战等进行了系统阐述和介绍.
已有研究均假设分子通信限基于固定路由表,并不适合于身体域纳米网络中纳米机器的动态位置和网络状态. 因此,基于身体域纳米网络的动态路由亟需解决. 另外,身体域纳米网络中众多纳米机器密集分布,可以通过纳米机器间的协作信号处理来提高系统的整体性能与鲁棒性. 例如,可以通过多个感知纳米机器同时测量外界的有害物质浓度,并通过所测量值的加权平均结果进行系统决策,这方面有待进一步研究. 其他问题和挑战还包括拥塞控制和拓扑管理等,这些问题的顺利突破和解决才能引导身体域纳米网络实现自动形成、自动配置、自动优化和自动愈合.
| [1] | Atakan B, Akan O B, Balasubramaniam S. Body area nanonetworks with molecular communications in nanomedicine[J]. IEEE Communications Magazine, 2012, 50(1):28-34.[引用本文:1] |
| [2] | Akyildiz I, Pierobon M, Balasubramaniam S, et al. The internet of bio-nano things[J]. IEEE Communications Magazine, 2015, 53(3):32-40.[引用本文:2] |
| [3] | Movassaghi S, Abolhasan M, Lipman J, et al. Wireless body area networks:a survey[J]. IEEE Communications Survey & Tutorials, 2014, 16(3):1658-1686.[引用本文:1] |
| [4] | Akyildiz I, Brunetti F, Blazquez C. Nanonetworks:a new communication paradigm[J]. Computer Networks, 2008, 52(12):2260-2279.[引用本文:1] |
| [5] | Chahibi Y, Pierobon M, Sang Ok Song, et al. A molecular communication system model for particulate drug delivery systems[J]. IEEE Transactions on Biomedical Engineering, 2013, 60(12):3468-3483.[引用本文:1] |
| [6] | Freitas R. Nanotechnology, nanomedicine and nanosurgery[J]. International Journal of Surgery, 2005, 3(4):243-246.[引用本文:1] |
| [7] | 黎作鹏, 张菁, 蔡绍滨, 等. 分子通信研究综述[J]. 通信学报, 2013, 34(5):152-167. Li Zuopeng, Zhang Jing, Cai Shaobin, et al. Review on molecular communication[J]. Journal on Communications, 2013, 34(5):152-167.[引用本文:1] |
| [8] | Gregori M, Akyildiz I. A new nanonetwork architecture using flagellated bacteria and catalytic nanomotors[J]. IEEE Journal on Selected Areas in Communications, 2010, 28(4):612-619.[引用本文:1] |
| [9] | Cobo L, Akyildiz I. Bacteria-based communication in nanonetworks[J]. Nano Communication Networks, 2010, 1(4):244-256.[引用本文:6] |
| [10] | Gao Yunlong, Lakshmanan S, Sivakumar R. On attractant scheduling in networks based on bacterial communication[C]//IEEE Conference on Computer Communications Workshops (INFOCOM WKSHPS). Shanghai:[s.n.], 2011:419-424.[引用本文:1] |
| [11] | Lio P, Balasubramaniamb S. Opportunistic routing through conjugation in bacteria communication nanonetwork[J]. Nano Communication Networks, 2012, 3(1):36-45.[引用本文:1] |
| [12] | Petrov V, Balasubramaniam S, Moltchanov D, et al. Forward and reverse coding for chromosome transfer in bacterial nanonetworks[J]. Nano Communication Networks, 2014, 5(1-2):15-24.[引用本文:1] |
| [13] | Islam N, Misra S. Collision bottleneck throughput in bacterial conjugation-based nanonetworks[J]. IEEE Transactions on Nanobioscience, 2015, 14(1):112-120.[引用本文:2] |
| [14] | Einolghozati A, Sardari M, Beirami A, et al. Data gathering in networks of bacteria colonies:collective sensing and relaying using molecular communication[C]//IEEE Conference on Computer Communications Workshops (INFOCOM WKSHPS). Orlando, FL:[s.n.], 2010:256-261.[引用本文:2] |
| [15] | Wang Zhiyu, Kim M, Rosen G. Validating models of bacterial chemotaxis by simulating the random motility coefficient[C]//IEEE 8th International Conference on BioInformatics and Bio Engineering. Athens, Greece:[s.n.], 2008:1-5.[引用本文:1] |
| [16] | Hasan M, Hossain H, Balasubramaniam S, et al. Social behavior in bacterial nanonetworks:challenges and opportunities[J]. IEEE Network, 2015, 29(1):26-34.[引用本文:1] |
| [17] | Petrov V, Moltchanov D, Balasubramaniam S, et al. Incorporating bacterial properties for plasmid delivery in nano sensor networks[J]. IEEE Transactions on Nanotechnology, 2015, 14(4):751-760.[引用本文:1] |
| [18] | Dubey G, Ben-Yehuda S. Intercellular nanotubes mediate bacterial communication[J]. Cell, 2011, 144(4):590-600.[引用本文:1] |
| [19] | Ortiz M, Endy D. Engineered cell-cell communication via DNA messaging[J]. Journal of Biological Engineering, 2012, 6(1):1-12.[引用本文:1] |
| [20] | Hanahan D. Studies on transformation of escherichia coli with plasmids[J]. Journal of molecular biology, 1983, 166(4):557-580.[引用本文:1] |
| [21] | Blattner F, Plunkett III G, Perna N. The complete genome sequence of escherichia coli K-12[J]. Science, 1997, 277(5331):1453-1462.[引用本文:1] |
| [22] | Hazelbauer G, Mesibov R, Adler J. Escherichia coli mutants defective in chemotaxis toward specific chemicals[J]. Proceedings of the National Academy of Science, 1969, 64(4):1300-1307.[引用本文:1] |
| [23] | Fernandes R, Luo Xiaolong, Tsao C, et al. Biological nanofactories facilitate spatially selective capture and manipulation of quorum-sensing bacteria in a biomems device[J]. Lab on a Chip, 2010, 10(9):1128-1134.[引用本文:1] |
| [24] | Akyildiz I, Fekri F, Sivakumar R, et al. Monaco:Fundamentals of molecular nano-communication networks[J]. IEEE Wireless Communications, 2012, 19(5):12-18.[引用本文:1] |
| [25] | Sneddon M, Faeder J, Emonet T. Efficient modeling, simulation and coarse-graining of biological complexity with NFSim[J]. Nature Methods, 2010, 8(2):177-183.[引用本文:1] |
| [26] | Wei Guopeng, Bogdan P, Marculescu R. Efficient modeling and simulation of bacteria-based nanonetworks with BNSim[J]. IEEE Journal on Selected Areas in Communications, 2013, 31(12):868-878.[引用本文:1] |
| [27] | Balasubramaniam S, Lyamin N, Kleyko D, et al. Exploiting bacterial properties for multi-hop nanonetworks[J]. IEEE Communications Magazine, 2014, 52(7):184-191.[引用本文:2] |
| [28] | Llatser I, Cabellos-Aparicio A, Alarcon E. Networking challenges and principles in diffusion-based molecular communication[J]. IEEE Wireless Communications, 2012, 19(5):36-41.[引用本文:1] |